Cincias da Natureza e suas Tecnologias Qumica Ensino































- Slides: 33

Ciências da Natureza e suas Tecnologias - Química Ensino Médio, 2ª Série Mistura de gases

q. Materiais • • detergente; água; canudo ou arco para fazer as bolhas; glicerina (vendida em farmácias). Imagens: (a)Autor desconhecido/Disponibilizado por Xanthine Complex/Domínio Público; (b) Martin Meise/GNU Free Documentation License; (c) : Kristian Ovaska/Creative Commons - Atribuição - Partilha nos Mesmos Termos 2. 5 Genérica. QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Experimento: Bolhas de Sabão

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Experimento: Bolhas de Sabão q. Procedimento: Imagem : Andreas Hendrik/Public Domain. • misture bem a água com o detergente e a glicerina; • num local com pouca ventilação, faça a maior bolha de sabão que puder. A bolha formada contém gás carbônico (CO 2), cuja massa molar é 44 g/mol. Como a massa molar aparente do ar atmosférico é de 28, 96 g/mol, a bolha desce ao invés de subir.

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Imagem : Peter Southwood/ Creative Commons Atribuição. Partilha nos Termos da Mesma Licença 3. 0 Unported. Nos cilindros de ar que os mergulhadores carregam, o gás oxigênio (O 2) é misturado com gás hélio (He). O ar atmosférico é uma mistura dos gases nitrogênio, N 2 (78%), oxigênio, O 2 (21%), e outros gases (1%), com predominância do argônio, Ar. Imagem : Omniii/GNU Free Documentation License. Misturas Gasosas

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Uma Mistura Gasosa p. A Os cilindros VA Gás A Contendo. . . p. B p. C VC VB Gás B TA Gás C TB n. A TC n. C Após serem misturados, submetidos a uma pressão, V ocupando um volume, numa temperatura, contendo um número de mols (quantidade de matéria), T Gás A Gás B Gás C num recipiente de volume V. . . e atingirem o equilíbrio térmico numa temperatura T, com quantidade de matéria nt = n A + n B + n C , possuem pressão final Pt, dada por Pt = p A + p B + p C

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Fique Atento! • Como os gases ideais não reagem entre si, a mistura irá se comportar como um gás único e obedecerá às mesmas leis que os gases isolados; • para uma mistura gasosa do tipo A + B + C; • poderemos aplicar a equação dos gases ideais: Pt. V = nt. R. T

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Fração Molar de um Gás A (x. A) • é a relação entre a quantidade de matéria de um gás A (n. A), por exemplo, e a quantidade de matéria total da mistura gasosa (nt): FIQUE ATENTO!! • a soma das frações molares numa mistura deve ser sempre igual a 1: x. A + x B + x C = 1 • atualmente, utilizamos o termo fração em quantidade de matéria em vez de fração molar.

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Pressão Parcial • é a pressão que um gás exerceria se estivesse sozinho, ocupando o volume total da mistura e na mesma temperatura em que essa mistura se encontra; • lei das pressões parciais de Dalton: “a pressão total de uma mistura é a soma das pressões parciais dos gases”: Pt = p A + p B + p C • enunciando a Lei de Dalton de outra forma, podemos afirmar que “a pressão parcial de cada componente de uma mistura gasosa é proporcional à quantidade de matéria desse componente na mistura”: p. A = x. A. Pt

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Lei de Dalton, matematicamente • após a mistura dos gases e utilizando a equação dos gases ideais, temos Ø para um gás A: p. A. V = n. A. R. T Ø para a mistura: Pt. V = nt. R. T • dividindo as equações (Gás A/Mistura), temos: multiplicando meios pelos extremos obtemos A pressão parcial do gás A é proporcional à quantidade de matéria.

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Imagem : Charles Turner/United States Public Domain John Dalton Nasceu em Eaglesfield (1766) e faleceu em Manchester (1844). §começou a ensinar aos 12 anos numa escola da seita Quaker; §em 1773, começou a lecionar Ciências em Manchester, num colégio presbiteriano; §estudando as condições climáticas, coletou cerca de 200 mil observações do tempo ao longo de sua vida; §concluiu que o magnetismo da Terra influenciava a formação das auroras boreais; §em 1794, Dalton descreveu cientificamente sua dificuldade para distinguir as cores – hoje chamada de daltonismo em sua homenagem; §elaborou a lei das pressões parciais estudando a atmosfera; §foi o primeiro a expressar claramente a chamada Lei das proporções definidas; §elaborou a Teoria Atômica em 1804; §recebeu o título de Doutor em 1832; §foi professor particular e de escolas por toda sua vida.

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Imagem : Ackbahr/GNU Free Documentation License Pressões Parciais no Mergulho As pressões parciais dos gases oxigênio e nitrogênio devem ser controladas durante o mergulho. O sangue apresenta os gases oxigênio e nitrogênio dissolvidos, provenientes da respiração, principalmente. Uma pressão parcial do nitrogênio elevada provoca sintomas semelhantes a uma embriaguez, fazendo o mergulhador perder a noção da realidade. Uma pressão parcial do oxigênio acima de 1, 6 atm acelera o metabolismo a níveis perigosos. Por isso, utiliza-se uma mistura de oxigênio com gás hélio nos cilindros. Para saber mais sobre os efeitos da pressão durante o mergulho: http: //www. biofisica. xpg. com. br/Capitulo%201/efeitos%20 da%20 pressao%20 durante%20 o%20 mergulho. htm acesso em 02/07/2012.

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Pressões Parciais e a calibragem dos Pneus Imagem : A. Viazemsky/Public Domain Supondo que os pneus do automóvel da figura sejam calibrados com uma pressão de 3, 0 atm, em Recife (cuja pressão atmosférica é 1, 0 atm) e que o ar seja formado por 79% de nitrogênio (N 2) e 21% de oxigênio (O 2), as pressões parciais dos gases serão: Gás nitrogênio (A): 79%. 3, 0 atm = 2, 19 atm Gás oxigênio (B): 21%. 3, 0 atm = 0, 63 atm Observe que, somando-se as pressões parciais dos gases, obtemos a pressão total no interior dos pneus: 2, 19 atm + 0, 63 atm = 3, 0 atm Confirmando-se, assim, a Lei de Dalton das pressões parciais: Pt = p A + p B Calibrar os pneus é importante para a segurança do automóvel e deve ser feito no horário da manhã! Lembremos que o ar inserido nos pneus também é uma mistura gasosa.

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Seleção Brasileira e as Pressões Parciais Quando a Seleção Brasileira vai jogar em La Paz (Bolívia), cerca de 3. 700 m acima do nível do mar, os jogadores sentem muito o efeito da altitude. Estádio de futebol em La Paz, Bolívia Quanto maior a altitude, menor será a pressão atmosférica. Ao nível do mar (como em Recife), a pressão parcial do gás oxigênio dissolvido no sangue é de 0, 20 atm. Em La Paz, essa pressão parcial cai para 0, 12 atm. O corpo demora um tempo para se adaptar a essa nova pressão. Imagem : Henrry 104 1/Creative Commons Attribution. Share Alike 3. 0 Unported

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Volume Parcial • numa mistura gasosa, volume parcial de um gás é o volume ocupado por ele estando sozinho e submetido à pressão total e à temperatura da mistura; • lei de Amagat: O volume total de uma mistura gasosa é a soma dos volumes parciais de todos os gases componentes da mistura. V = V A + VB + VC Obs. : Emile Hilaire Amagat (1841 – 1915) , um físico francês: üinventou o manômetro hidráulico, que foi capaz de suportar até 3. 200 atmosferas; üem 1880 ele publicou sua Lei de Volumes Parciais; üfoi eleito membro da Academia Francesa de Ciências em 09 de junho de 1902; üAmagat é o nome da unidade de densidade numérica em sua homenagem.

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas • • a Região Metropolitana do Recife atingiu a marca de 1 milhão de veículos em setembro de 2011. No início do mês, a frota de Pernambuco já tinha chegado a 2 milhões. Atualmente, o Estado tem emplacado entre 1. 000 e 1. 300 veículos por dia; uma das principais preocupações dos ambientalistas é a quantidade de gases poluentes emitida diariamente para a atmosfera; como o volume de ar na atmosfera é muito grande, costumam-se expressar as quantidades dos poluentes em ppm (partes por milhão) e ppb (partes por bilhão). Imagem: EPA / Public Domain. • Poluição do Ar FONTE: Adaptado de http: //jconlineblogs. ne 10. uol. com. br/deolhonotransito/2011/09/20/frota-da-regiao-metropolitana-do-recife-chega-a-1 -milhao-de-veiculos/ acesso em 05/07/2012. Concentrações de monóxido de carbono (CO) acima de 400 ppm no ar (400 partes de CO em 1 milhão de partes de ar, em L, por exemplo) são potencialmente mortais. Isso significa que, num ambiente de 1. 000 L, 400 m. L de CO serão suficientes para causar a morte.

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Massa Molar Aparente de uma Mistura Gasosa • Sabemos que a massa total de uma mistura gasosa (mt) é igual à soma das massas de cada gás: mt = m. A + m. B + m. C; • e a quantidade de matéria total na mistura (nt) é a soma das quantidades de matéria de cada gás: nt = n. A + n. B + n. C ; • sendo temos que alternando as variáveis para um único gás • para uma mistura, temos Map = Massa aparente da mistura (em g/mol)

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Fique Atento! • Podemos calcular a massa molar aparente (Map. ) da mistura como a média ponderada das massas molares dos gases que compõem a mistura; • os “pesos” serão as frações molares dos gases (ou seus percentuais em volume); • ou ainda:

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Qual a massa molar aparente do ar atmosférico? q Como vimos anteriormente, o ar atmosférico é composto por uma mistura de 78% de gás nitrogênio (N 2), 21% de gás oxigênio (O 2) e 1% de gás argônio (Ar); q temos, então: • M(N 2) = 28 g/mol • M(O 2) = 32 g/mol • M(Ar) = 40 g/mol

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Os antigos dirigíveis eram inflados com gás hidrogênio (H 2), um gás muito inflamável. Atualmente usase o gás hélio (He). O princípio básico para fazer um dirigível voar é baseado no fato de o hidrogênio, 2 g/mol (ou hélio, 4 g/mol), ser mais leve que o ar. Última torre do Zeppelin do mundo, localizada em Recife. Os balões sobem porque a densidade do ar quente em seu interior é menor que a do ar atmosférico. Imagem : (A) NASA Ames Resarch Center (NASA-ARC)/Public Domain; (B) Lsouza 7 / Public Domain; (C) Björn Appel/GNU Free Documentation License; (D)Jdlong 0624/ Creative Commons Atribuição-Partilha nos Termos da Mesma Licença 3. 0 Unported.

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Densidade gasosa • é a relação entre a massa molar aparente (Map. ) e o volume molar (Vm) da mistura gasosa: CNTP são as condições normais de temperatura e pressão (0°C e 1 atm). A unidade do volume molar é L/mol. Volume de 1 mol da mistura medido nas CNTP. • para condições diferentes das CNTP, deveremos utilizar a equação de Clapeyron: Para um único gás: Benoit Paul Émile Clapeyron (1799 — 1864) foi um engenheiro e físico francês. Imagem : AAAAA/Public Domain A unidade da densidade (d) é g/L.

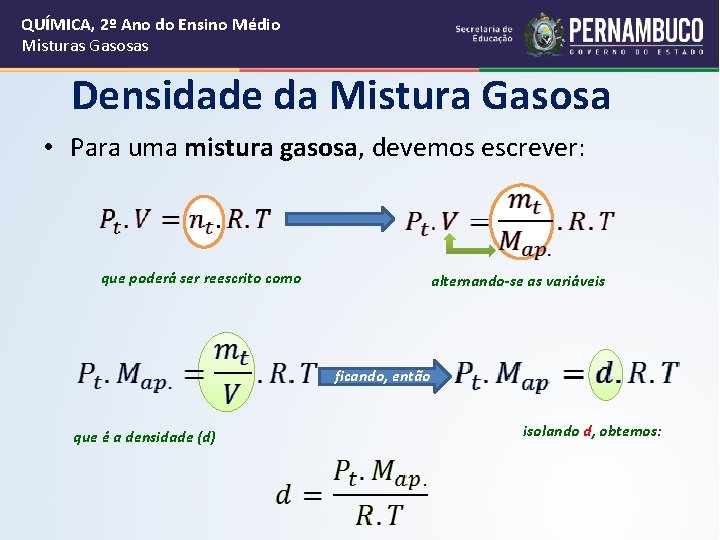
QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Densidade da Mistura Gasosa • Para uma mistura gasosa, devemos escrever: que poderá ser reescrito como alternando-se as variáveis ficando, então que é a densidade (d) isolando d, obtemos:

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Densidade Relativa • Considerando condições idênticas de temperatura e pressão, podemos dizer que a densidade relativa do gás A em relação ao gás B é o quociente entre as densidades absolutas de A e de B: Quanto maior a massa molar, maior será a densidade. Mas. . . obtemos

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Fique Ligado! • A densidade relativa (DA, B) não possui unidade; • a densidade relativa indica quantas vezes um gás é mais (ou menos) denso que outro gás; • as densidades dos gases são proporcionais às suas massas molares; • assim, reforçando: quanto maior a massa molar, mais denso será o gás.

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Sentimos o cheiro de um perfume porque algumas moléculas passam para o estado gasoso, difundindo-se pelo ar. É a difusão do gás! Por que os balões de aniversário ficam murchos no dia seguinte? Embora o balão esteja bem amarrado, o gás acaba escapando pelos minúsculos orifícios existentes na borracha. É a efusão do gás! Imagem : Esther Simin/GNU Free Documentation License Imagem : shakko/Creative Commons Attribution. Share Alike 3. 0 Unported Efusão e Difusão

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Difusão Gasosa • Os gases se movimentam continuamente e com altas velocidades; • assim, os gases se misturam rapidamente, originando SEMPRE uma mistura homogênea; • difusão gasosa é o movimento espontâneo da dispersão de um gás sobre outro numa mistura gasosa; • em outras palavras, é a mistura espontânea dos gases entre si.

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Fique Ligado! • Efusão gasosa ocorre quando um gás escapa através de um orifício; • percebemos a efusão gasosa quando balões de aniversário murcham no dia seguinte; • Lei de Graham das efusões gasosas: A velocidade de efusão é dada em L/min geralmente! • como velocidade de efusão de um gás e sua massa molar são inversamente proporcionais, concluímos que quanto maior for a massa molar, mais devagar o gás deverá escapar, demorando a difundir-se.

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas • nasceu em Glasgow (Escócia), em 1805, e faleceu em Londres (Inglaterra), em 1869; • estudou nas universidades de Edimburgo (Escócia) e de Glasgow. Ensinou Química em Glasgow e no University College London; • desde 1855 até sua morte, foi diretor da Real Fábrica de Moeda; • descobriu o método da diálise para separar os coloides das soluções. A hemodiálise é uma diálise que ocorre no sangue, utilizando-se uma membrana semipermeável artificial (filtro) no tratamento de pacientes com deficiências renais. Imagem : Autor desconhecido/Disponibilizado por Stanmar / Domínio Público Thomas Graham

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Aplicação no vestibular 1 q (UFSE) Dentre os gases abaixo, nas mesmas condições, o que se difunde mais rapidamente é: a) o monóxido de carbono. b) a amônia. c) o ozônio. d) o nitrogênio. e) o hidrogênio. • Dados: H = 1; C = 12; = 14; O = 16 Pela Lei de Graham, o gás que mais rapidamente irá se difundir será o que possuir menor massa molar!

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Cálculo das massas molares: q Monóxido de carbono (CO): M(CO) = 1. 12 + 1. 16 = 28 g/mol q Amônia (NH 3): M(NH 3) = 1. 14 + 3. 1 = 17 g/mol q Ozônio (O 3): M(O 3) = 3. 16 = 48 g/mol q Nitrogênio (N 2): M(N 2) = 2. 14 = 28 g/mol q Hidrogênio (H 2): M(H 2) = 2. 1 = 2 g/mol Como o gás hidrogênio possui a menor massa molar, concluímos que este irá se difundir mais rapidamente. A alternativa correta é LETRA E!

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Aplicação no vestibular 2 q (Covest) O ar é uma solução gasosa contendo 20%, aproximadamente, de oxigênio. Em um recipiente com 5 atmosferas de ar, qual a pressão parcial do oxigênio? a) 0, 2 ØDe acordo com a Lei de Dalton, temos: b) 0, 8 c) 1 d) 2 ü 20% representa a fração molar do gás oxigênio: x = 20% = 0, 20 e) 5 ü 5 atm é a pressão da mistura (pressão total): Pt = 5 atm üa pressão parcial do oxigênio será: p = 0, 20. 5 = 1 atm

QUÍMICA, 2º Ano do Ensino Médio Misturas Gasosas Curiosidade Seria possível alguém se amarrar em balões cheios com hélio e voar? O sacerdote brasileiro Adelir de Carli era conhecido por voar amarrado a balões de gás hélio e planejava bater o recorde de permanência no ar, mas saiu de sua rota por causa de condições climáticas adversas e acabou desaparecendo, sendo encontrado morto após mais de 2 meses de buscas. Leia mais em ühttp: //pt. wikipedia. org/wiki/Adelir_Ant%C 3%B 4 nio_de_Carli, acesso em 05/07/2012. ühttp: //www. iparaiba. com. br/noticias, 123764, 1, buscas+por+padre+que+sumi u+com+baloes+sao+encerradas. html, acesso em 03/07/2012.

Tabela de Imagens n° do direito da imagem como está ao lado da link do site onde se consegiu a informação Data do Acesso slide foto 2 A Autor desconhecido / Disponibilizado por http: //pt. wikipedia. org/wiki/Ficheiro: Drinking. Stra 24/08/2012 Xanthine Complex/Domínio Público ws. jpg 2 B Martin Meise / GNU Free Documentation http: //commons. wikimedia. org/wiki/File: Stirring_i 24/08/2012 License n_a_glass_of_Water. jpg? uselang=pt-br 2 C Kristian Ovaska / Creative Commons - http: //pt. wikipedia. org/wiki/Ficheiro: Fairy. Bottles. 24/08/2012 Atribuição - Partilha nos Mesmos Termos 2. 5 jpg Genérica 3 Andreas Hendrik / Public Domain http: //commons. wikimedia. org/wiki/File: Seifenbl 24/08/2012 asen. jpg 4 A Peter Southwood / Creative Commons http: //commons. wikimedia. org/wiki/File: Charging 24/08/2012 Atribuição-Partilha nos Termos da Mesma _a_spare_air_cylinder_PB 048172. jpg? uselang=pt. Licença 3. 0 Unported br 4 B Omniii / GNU Free Documentation License. http: //pt. wikipedia. org/wiki/Ficheiro: Skyshot. jpg 24/08/2012 10 Charles Turner / United States Public Domainhttp: //commons. wikimedia. org/wiki/File: John_Da 24/08/2012 lton_by_Charles_Turner. jpg 11 Ackbahr / GNU Free Documentation License http: //commons. wikimedia. org/wiki/File: Typical_ 24/08/2012 diver. jpg 12 A. Viazemsky / Public Domain http: //commons. wikimedia. org/wiki/File: Kwik 24/08/2012 Fit_3. jpg 13 Henrry 104 1/ Creative Commons Attribution http: //commons. wikimedia. org/wiki/File: Estadio. B 24/08/2012 -Share Alike 3. 0 Unported olivia. jpg

Tabela de Imagens n° do direito da imagem como está ao lado da link do site onde se consegiu a informação Data do Acesso slide foto 15 EPA / U. S. Environmental Protection Agency https: //commons. wikimedia. org/wiki/File: Diesel- 29/10/2012 /Public Domain smoke. jpg 19 A NASA Ames Resarch Center (NASA-ARC) / http: //commons. wikimedia. org/wiki/File: Zeppelin. 24/08/2012 Public Domain jpg? uselang=pt-br 19 B Lsouza 7 / Public Domain http: //commons. wikimedia. org/wiki/File: Torre_d 24/08/2012 o_Zeppelin_-_Jiquia_-_Recife. JPG? uselang=pt-br 19 C Björn Appel / GNU Free Documentation http: //commons. wikimedia. org/wiki/File: Ballon 24/08/2012 License flame 02. jpg? uselang=pt-br 19 D Jdlong 0624 / Creative Commons Atribuição- http: //commons. wikimedia. org/wiki/File: Ballon_G 24/08/2012 Partilha nos Termos da Mesma Licença 3. 0 low. jpg? uselang=pt-br Unported 20 AAAAA / Public Domain http: //commons. wikimedia. org/wiki/File: Benoit_C 24/08/2012 lapeyron. png 24 A shakko / Creative Commons Attributionhttp: //commons. wikimedia. org/wiki/File: Guerlain 24/08/2012 Share Alike 3. 0 Unported _-_Le_parfum_de_Champs. Elysees_(1904)_Tortue. jpg 24 B Esther Simin / GNU Free Documentation http: //commons. wikimedia. org/wiki/File: Baloon. j 24/08/2012 License pg 27 Autor desconhecido / Disponibilizado por http: //commons. wikimedia. org/wiki/File: Thomas_ 24/08/2012 Stanmar/Domínio Público Graham. jpg? uselang=pt-br