cidos y steres Tema 9 Introduccin Prostaglandina cido









- Slides: 14

Ácidos y ésteres Tema 9

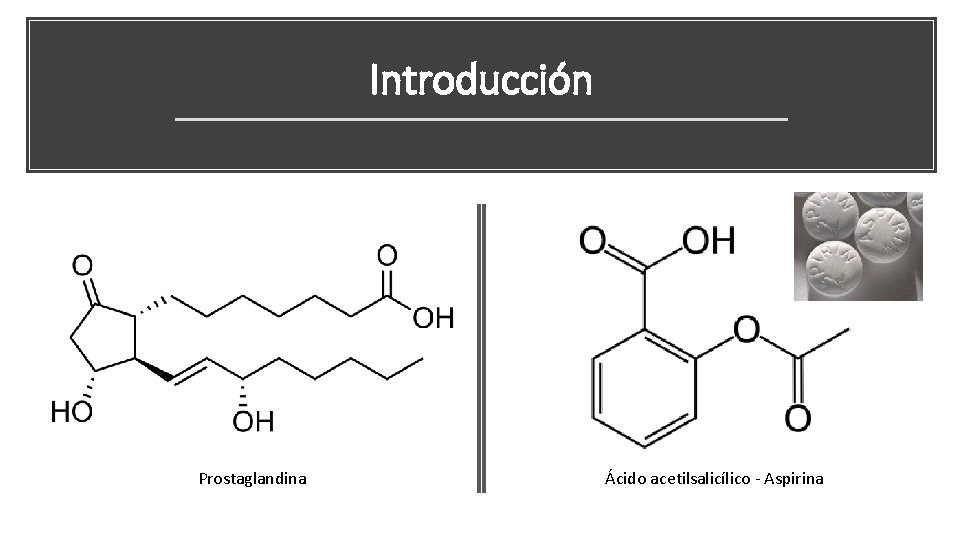
Introducción Prostaglandina Ácido acetilsalicílico - Aspirina

9. 1 Ácidos carboxílicos • Los ácidos carboxílicos son el resultado de la oxidación de los aldehídos, y se originan por el desplazamiento del hidrógeno del grupo funcional aldehído (-CH=O) por el grupo funcional hidroxilo (OH). • El grupo funcional ácido recibe el nombre de carboxilo y se representa de la siguiente forma (–COOH). • Son De gran importancia en la industria farmacéutica

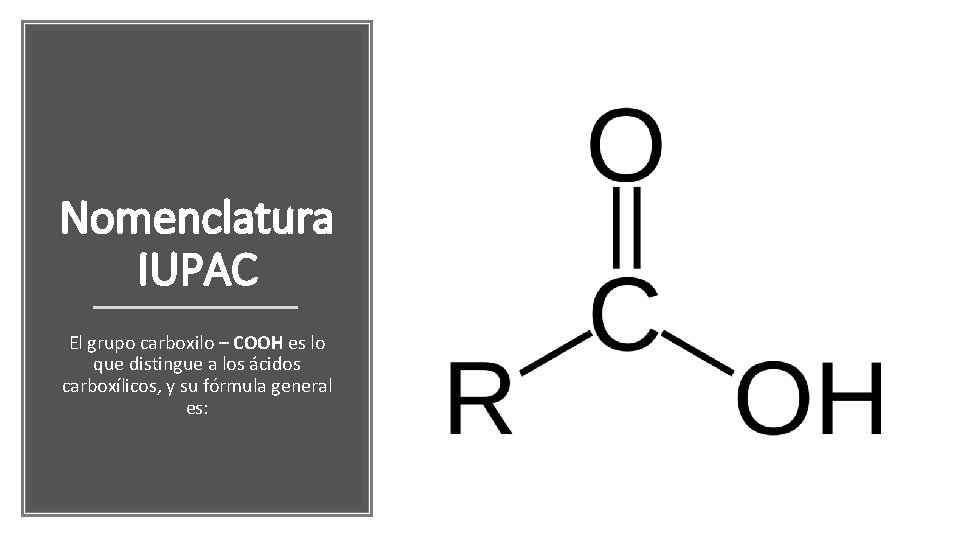
Nomenclatura IUPAC El grupo carboxilo – COOH es lo que distingue a los ácidos carboxílicos, y su fórmula general es:

Para darles su nombre: 1. Escoge la cadena que posea la mayor cantidad de carbonos y que incluya a todos los grupos carboxilos que se encuentren en la molécula. 2. El nombre de la cadena es igual al nombre del alcano, alqueno, alquino, o hidrocarburo cíclico del cual deriva con la terminación –oico o –dioico, según el número de carboxilos. 3. Numera la cadena principal empezando por el carboxilo; si hay dos carboxilos, se numera de tal forma que el grupo que sigue en prioridad tenga la mínima posición. 4. Denomina y organiza las ramificaciones igual que en los grupos funcionales revisados antes. 5. Escribe el nombre del ácido con el nombre base de la estructura, anteponiendo al principio la palabra ácido.

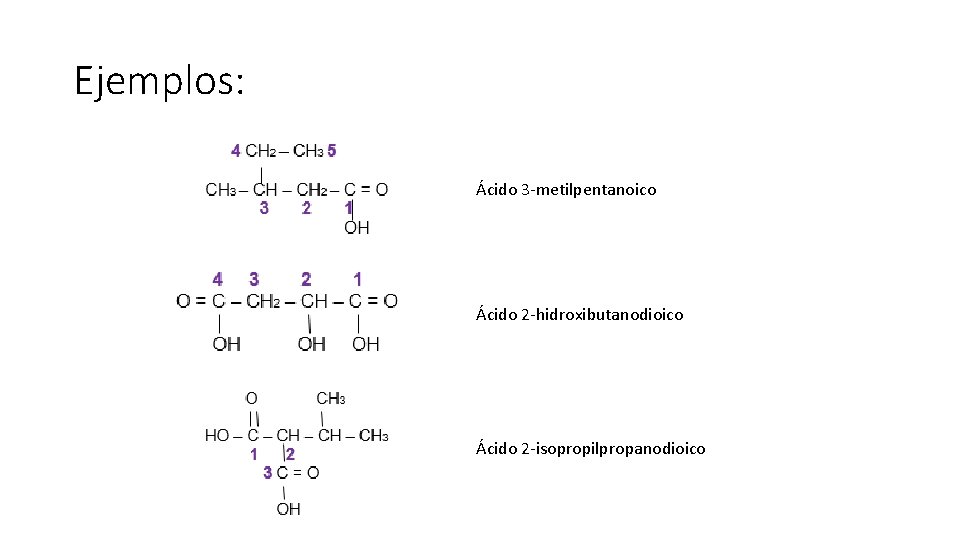
Ejemplos: Ácido 3 -metilpentanoico Ácido 2 -hidroxibutanodioico Ácido 2 -isopropilpropanodioico

Propiedades físicas • Olor: los tres primeros presentan un olor desagradable y picante. • Solubilidad: son compuestos polares por el –OH que tiene el carboxilo, por lo tanto son solubles en agua y solventes polares, al aumentar los grupos alquilo en la cadena principal disminuye la polaridad y por consiguiente la solubilidad en agua. • Puntos de ebullición: forman puentes de hidrógeno, entonces tienen altos puntos de ebullición. Los compuestos con dos grupos carboxilos (dicarboxílicos) son sólidos con puntos de ebullición muy altos por la cantidad de puentes de hidrógeno que forman. Grupos funcionales Ácido carboxílico Alcohol Éter Ejemplo Ácido propanoico Propanol Oxapropano Punto de ebullición 141°C 97°C 7. 9°C Ejemplo Ácido butanoico Butanol Oxabutano Punto de ebullición 163°C 117°C 39°C

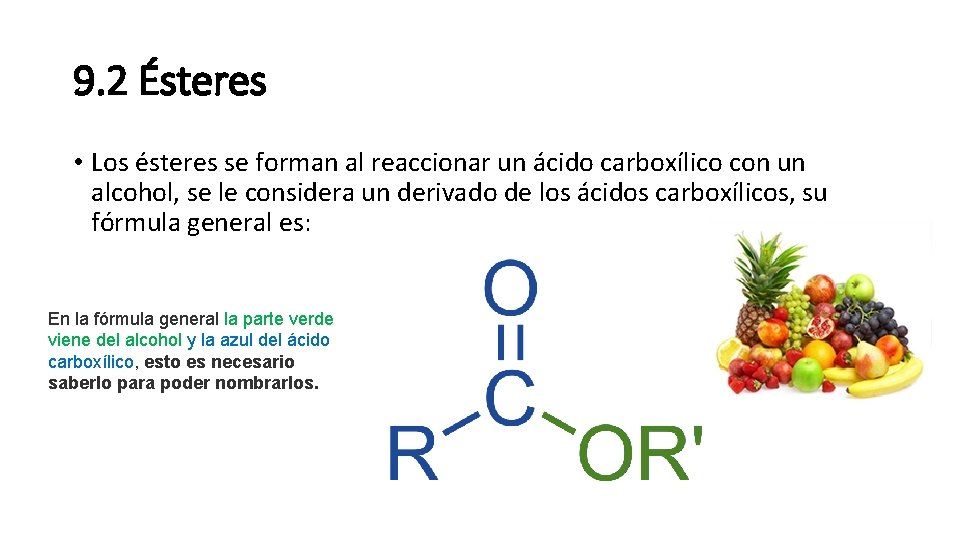
9. 2 Ésteres • Los ésteres se forman al reaccionar un ácido carboxílico con un alcohol, se le considera un derivado de los ácidos carboxílicos, su fórmula general es: En la fórmula general la parte verde viene del alcohol y la azul del ácido carboxílico, esto es necesario saberlo para poder nombrarlos.

Nomenclatura IUPAC Para nombrarlo: 1. Se escribe por separado la parte del ácido y la parte del alcohol, se numera empezando por el grupo éster. 2. A la parte del ácido se le da el sufijo oato; a la parte del alcohol ilo. 3. Luego se articula el nombre como parte del ácido de parte del alcohol.

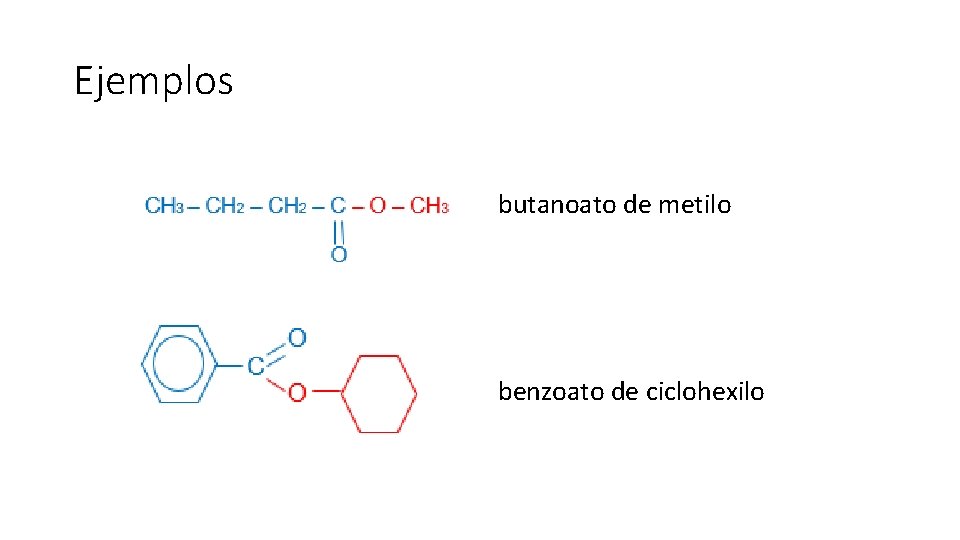
Ejemplos butanoato de metilo benzoato de ciclohexilo

Propiedades físicas • Solubilidad: son polares, solubles en agua y en solventes polares, e igual que los anteriores grupos funcionales, disminuye la polaridad al aumentar los carbonos de la cadena principal y por lo tanto la solubilidad en el agua. • Puntos de ebullición: son parecidos a las cetonas correspondientes. Los puntos de ebullición de los ésteres son inferiores en comparación con los puntos de ebullición de los ácidos carboxílicos con masas moleculares semejantes.

9. 3 Usos de ácidos carboxílicos y ésteres • Ácido metanoico/Ácido fórmico: Se utiliza en el área textil como secante de teñido, para tratar cuero, en fumigantes, insecticidas, lacas, electroplateado en espejos, electrocromado. • Ácido etanoico. Otro nombre es el ácido acético, es el principal componente del vinagre. • Ácido 2 -hidroxi-propanoico. Ácido láctico principal componente de la leche que se usa para elaborar quesos y otros derivados lácteos, acidulantes para bebidas. • Ácido propenoico. Usado en la síntesis del hule sintético y en la elaboración de algunas vitaminas.

Usos de ésteres • Los de bajo peso molecular se usan como solventes, como esencias artificiales, dan olor a plátano, ron, piña, manzana, durazno, naranja. • Utilizados en perfumes y en forma de aditivos alimenticios por el olor. • Muchos analgésicos se elaboran a partir de ellos • Se utilizan también como repelentes de insectos y en la síntesis de muchas resinas poliméricas de las cuales salen muchos plásticos.
