CIDOS Y BASES Metodologa cientfica y Aprendizaje de

ÁCIDOS Y BASES Metodología científica y Aprendizaje de la Física y Química Irene Moreno Horrillo

Objetivos � Conocer las características experimentales de ácidos y bases. � Estudiar las teorías que permiten explicar el comportamiento de los ácidos y de las bases. � Comprender que no todos los ácidos ni todas las bases son igual de fuertes, y que puede haber ácidos y bases fuertes y débiles. � Aprender la importancia de la escala p. H para indicar la concentración de protones o de hidróxidos de una disolución. � Calcular y medir el p. H de una disolución. � Aprender a realizar volumetrías ácido-base. � Entender que una disolución de una sal puede ser ácida o básica en función de la procedencia de la sal. � Conocer el funcionamiento de las disoluciones reguladoras. Ácidos y Bases

Contenidos 1. 2. 3. 4. 5. 6. 7. 8. Introducción Propiedades generales Teorías de ácidos y bases Fuerza relativa de ácidos y bases Autoionización del agua Concepto de p. H y p. OH Indicadores de ácido-base Valoraciones ácido-base (Volumetrías) Ácidos y Bases
1. INTRODUCCIÓN Lavoisier Los ácidos se formaban al quemar no metales (C, P, S…) en atmósfera de O 2 y posterior disolución en H 2 O El O 2 es el causante de las propiedades ácidas Lavoisier y su esposa Davy (1810) Uebig Ácidos y Bases HCl, (H y Cl) El H es el causante de la acidez características del ataque de los ácidos sobre los metales los ácidos son aquellas sustancias que contienen por lo menos un átomo de hidrógeno sustituible por un metal.

2. PROPIEDADES GENERALES �Ácidos � Tienen sabor agrio. � Son corrosivos para la piel. � Enrojecen ciertos colorantes vegetales. � Disuelven sustancias. � Atacan a los metales desprendiendo H 2 � Pierden sus propiedades al reaccionar con bases. Ácidos y Bases

2. PROPIEDADES GENERALES �Bases � Tienen sabor amargo. � Suaves al tacto pero corrosivos con la piel. � Dan color azul a ciertos colorantes vegetales. � Precipitan sustancias disueltas por ácidos. � Disuelven grasas. � Pierden sus propiedades al reaccionar con ácidos. Ácidos y Bases

3. TEORIAS ÁCIDO-BASE � Teoría Arrhenius v Ácido: sustancia que en disolución acuosa produce iones H+1 Ejemplo: HCl(aq) H+1(aq) + Cl-1(aq) v Base: sustancia que en disolución acuosa produce iones OH-1 Ejemplo: Na. OH(aq) Na+1(aq) + OH-1(aq) NOTA: la teoría de Arrhenius no incluía las bases que no contienen OH como el NH 3. Ácidos y Bases Arrhenius

3. TEORIAS ÁCIDO-BASE � Teoría Bronsted-Lowry v Ácido: especie química que dona un protón. Ejemplo: HCl + H 2 O Ácido Base Cl. Base conjugada + H 3 O+ Ácido conjugado Johannes Bronsted v Base: especie química que acepta un protón. Ejemplo: NH 3 + H 2 O Base Ácido NH 4+1 Ácido conjugado + OH- Base conjugada Thomas Lowry Ácidos y Bases

3. TEORIAS ÁCIDO-BASE � Teoría de Lewis v Ácido de Lewis: sustancia que acepta un par de electrones (no enlazantes) Ejemplo: H+ v Base de Lewis: sustancia que cede un par de electrones (no enlazantes) y que forma enlace covalente coordinado. Ejemplo: : NH 3 Ácidos y Bases Gilbert N. Lewis

3. TEORIAS ÁCIDO-BASE Hay compuestos que pueden comportarse como ácidos y como bases, según se enfrenten a una sustancia que sea más o menos ácida que ella. A estas sustancias se las denomina anfóteras, anfipróticas o anfolíticas. La sustancia anfótera, por excelencia, es el agua (H 2 O). Ejemplo: HCl + H 2 O NH 3 + H 2 O Ácidos y Bases Cl. NH 4+ + + H 3 O+ OH-

4. FUERZA RELATIVA DE ÁCIDOS Y BASES La fuerza de un ácido y de una base está determinado por la capacidad que tienen de donar o aceptar un protón. Cuanto más fuerte sea un ácido, tanto más débil será su base conjugada; y viceversa. Ejemplo de reacción ácido-base general: AH + Ácidos y Bases B Base ABase conjugada + BH+ Ácido conjugado

Ácido fuerte � Son sustancias químicas que se disocian totalmente al ser disueltas en H 2 O, dando lugar a un proceso irreversible. � Pueden ser buenos conductores. � Entre los ácidos fuertes tenemos: HCl. O 4, HI, HBr, HCl, H 2 SO 4, HNO 3 Ejemplo: HCl 2 M H 2 SO 4 3 M Ácidos y Bases H+ 2 M 2 H+ 6 M + Cl 2 M + SO 4 -2 3 M

Base fuerte � Son sustancias químicas que se disocian totalmente (100%) debido a que la reacción de disociación transcurre en un solo sentido ( � Entre las bases fuertes tenemos: Li. OH, Na. OH, KOH, Ca(OH)2 Ejemplo: Na. OH 0, 5 M Ácidos y Bases Na+ 0, 5 M + OH 0, 5 M ).

Ácido débil � Son sustancias químicas que se disocian parcialmente (ceden con dificultad su protón). � Es un proceso reversible que presenta un equilibrio iónico. � Entre los ácidos débiles tenemos: Ácido acético H 3 COOH Ácido bórico H 3 BO 3 Ácido sulhídrico H 2 S entre otros. Ácidos y Bases

Base débil � Son sustancias químicas que se disocian parcialmente (ceden con dificultad su protón. � Es un proceso reversible que presenta un equilibrio iónico. � Entre los ácidos débiles tenemos: NH 3, Na. Cl. O, NH 4 OH NOTA: La fuerza de un ácido y de una base depende de su constante de acidez o basicidad. A mayor valor de la constante, mayor facilidad del ácido o base para disociarse (mayor fuerza ácida o básica). Ácidos y Bases
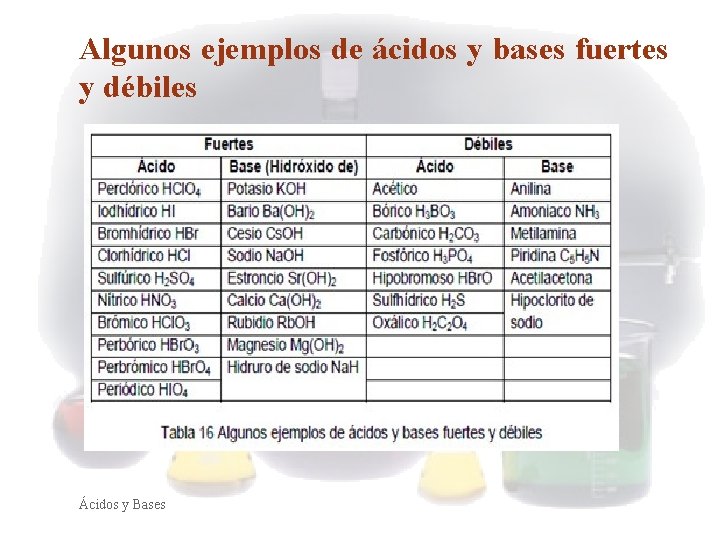
Algunos ejemplos de ácidos y bases fuertes y débiles Ácidos y Bases

¿Valor de K? � Resulta de aplicar la Ley de acción de masas a la reacción. � Ka: AH + H 2 O A- + H 3 O+ Ka La Ka, llamada constante de acidez, mide cuantitativamente la fuerza del ácido. A mayor Ka, más fuerte será el ácido y, por tanto, más débil su base conjugada. Ácidos y Bases

Actividad 1 � En una disolución 0, 050 M de un ácido HA monoprótico se determina que la concentración de H 3 O+en la disolución es 4· 10− 5 M. Calcula el valor de la constante de ionización del ácido. Ácidos y Bases

¿Valor de K? � Resulta de aplicar la Ley de acción de masas a la reacción. � Kb: B + H 2 O BH+ + OH- Kb La Kb, llamada constante de basicidad, mide cuantitativamente la fuerza de una base. A mayor Kb, más desplazado estará el equilibrio hacia la derecha. Ácidos y Bases

5. AUTOIONIZACIÓN DEL AGUA � Es el disolvente común de ácidos y bases y se autoioniza de la siguiente manera: H 2 O + H 2 O H 3 O+ + OH- =10 -14 mol/L Kw Ácidos y Bases Producto iónico del agua

5. AUTOIONIZACIÓN DEL AGUA � ¿Qué relación tienen Kw con Ka y Kb? Ácidos y Bases

5. AUTOIONIZACIÓN DEL AGUA Así, podemos distinguir tres tipos de disoluciones según las proporciones de los iones procedentes de la ionización del agua: Neutras: [H 3 O+]=[OH-]= 10 -7 Nota: : [H 3 O+]=[H+] Ácidos y Bases Ácidas: [H 3 O+]>[OH-] [H 3 O+]>10 -7 Básicas: [H 3 O+]<[OH-] [H 3 O+]< 10 -7

6. CONCEPTO p. H Y p. OH � Propuesto por Sorensen en 1909. � El p. H es el logaritmo decimal del inverso de [H 3 O+] (o menos el logaritmo decimal de [H 3 O+]). p. H-metro Ácidos y Bases

6. CONCEPTO p. H Y p. OH De la aplicación de las propiedades de los logaritmos, y del conocimiento de los valores posibles de [H 3 O+] , obtendremos que el p. H puede variar entre 0 y 14, de modo que los tipos de disoluciones se caracterizarán: • Si p. H<7 • Si p. H = 7 • Si p. H> 7 Ácidos y Bases Dis. Ácida Dis. Neutra Dis. Básica

6. CONCEPTO p. H Y p. OH De la misma manera puede definirse el p. OH. Es el logaritmo negativo de [OH-]. Se cumple que p. H+p. OH=14 Escala de p. H: Ácidos y Bases
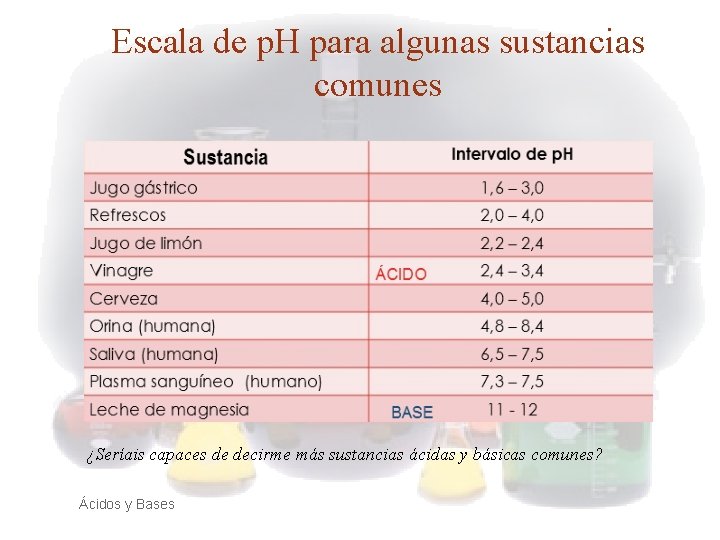
Escala de p. H para algunas sustancias comunes ¿Seríais capaces de decirme más sustancias ácidas y básicas comunes? Ácidos y Bases

Actividad 2 � Calcula el p. H de una disolución 3, 0· 10 -3 M de Ba(OH)2 Los hidróxidos se disocian totalmente a no ser que nos indiquen lo contrario. Ácidos y Bases
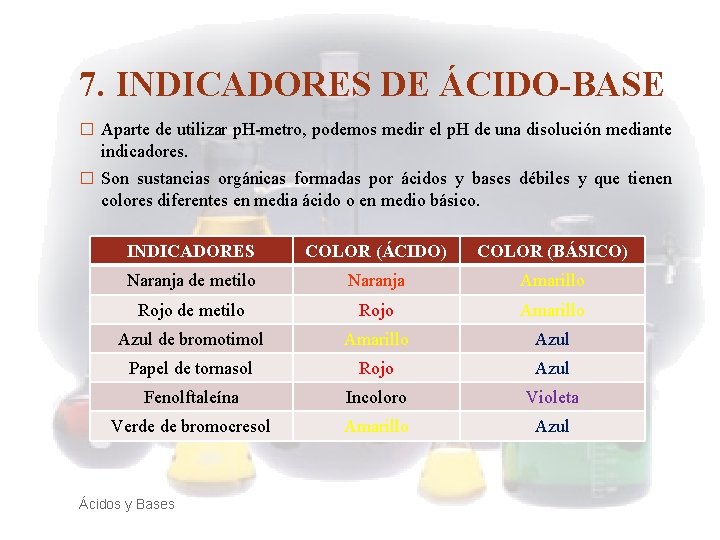
7. INDICADORES DE ÁCIDO-BASE � Aparte de utilizar p. H-metro, podemos medir el p. H de una disolución mediante indicadores. � Son sustancias orgánicas formadas por ácidos y bases débiles y que tienen colores diferentes en media ácido o en medio básico. INDICADORES COLOR (ÁCIDO) COLOR (BÁSICO) Naranja de metilo Naranja Amarillo Rojo de metilo Rojo Amarillo Azul de bromotimol Amarillo Azul Papel de tornasol Rojo Azul Fenolftaleína Incoloro Violeta Verde de bromocresol Amarillo Azul Ácidos y Bases
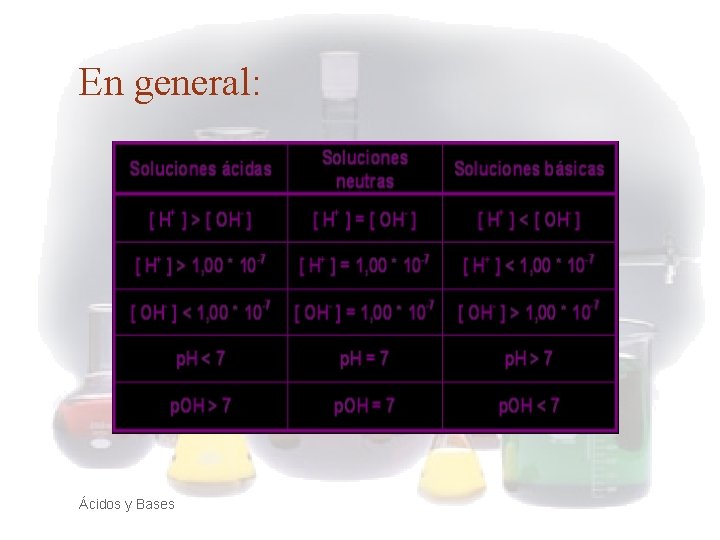
En general: Ácidos y Bases

8. VOLUMETRÍAS ÁCIDO-BASE Son reacciones que neutralizan, y tiene lugar entre un ácido y una base dando como productos el agua y la sal correspondiente. Ácido + Base Sal + Agua Se utilizan para determinar la concentración de una disolución. Al final de cualquier neutralización siempre se cumple que: Nº de H+ del ácido = Nº de OH- de la base Na · V a = N b · V b Ácidos y Bases
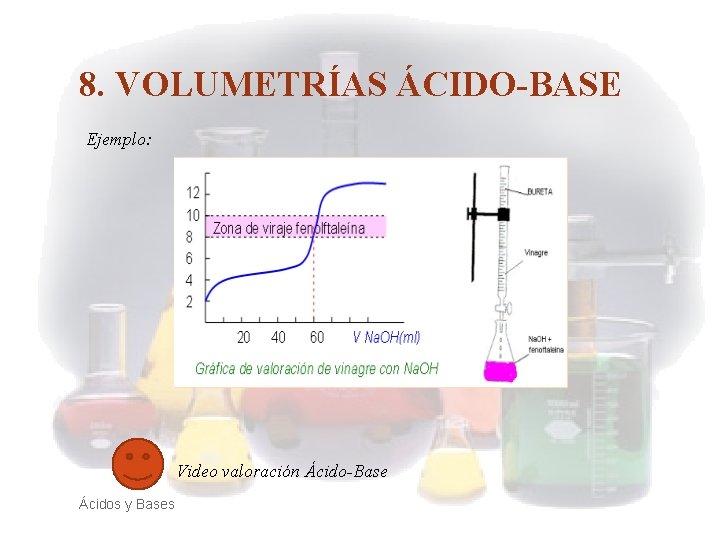
8. VOLUMETRÍAS ÁCIDO-BASE Ejemplo: Video valoración Ácido-Base Ácidos y Bases
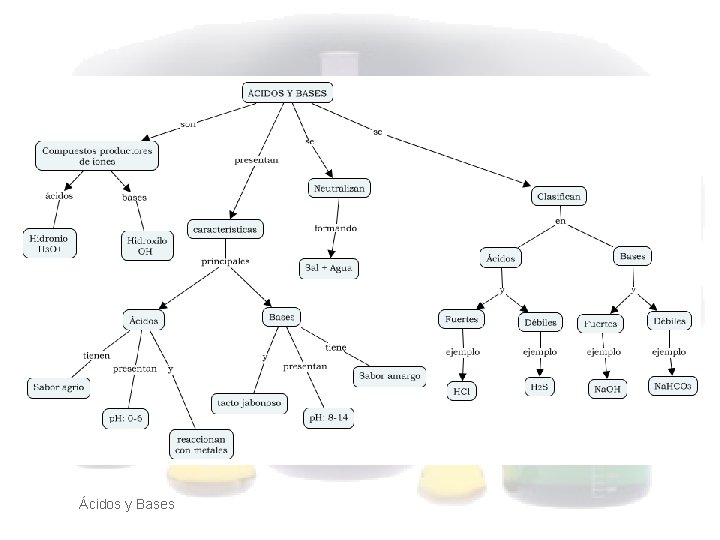
Ácidos y Bases

Actividades Ácidos y Bases

BIBLIOGRAFÍA � http: //recursostic. educacion. es/newton/web/materiales_didacticos/acidosbases/h istoria. html? 0&0 � http: //fresno. pntic. mec. es/~fgutie 6/quimica 2/Archivos. PDF/04 Acido. Base. pdf � http: //www. alonsoformula. com/inorganica/_private/Quimica 2 bach 06 cast. pdf � Química 2º Bachillerato. Edelvives. Ed 2009 Ácidos y Bases

Gracias por la atención Ácidos y Bases
- Slides: 35