Ciclo do cido Ctrico Ciclo do Citrato Ciclo











- Slides: 26

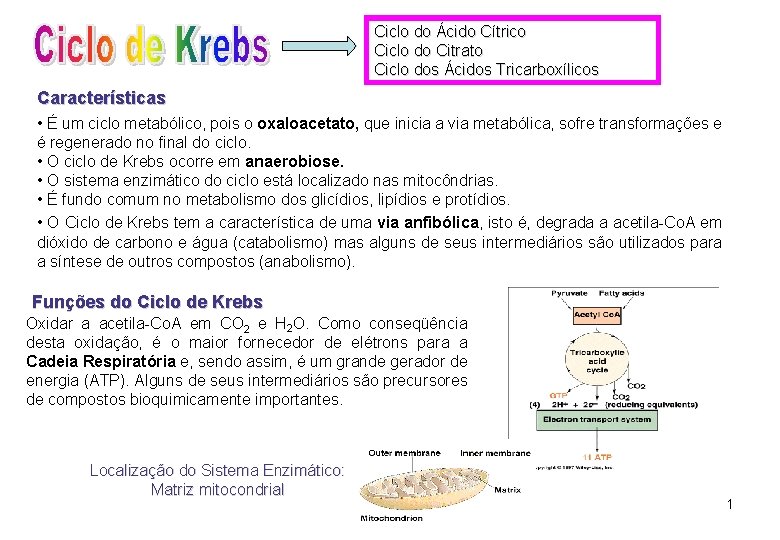
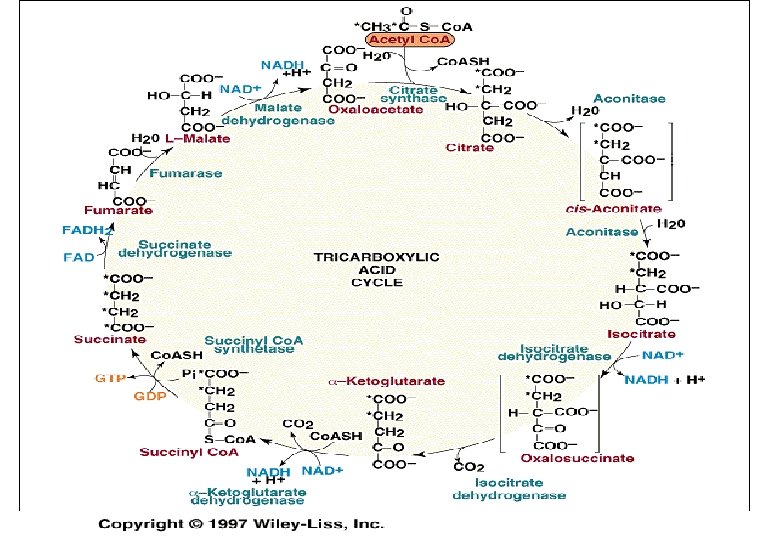
Ciclo do Ácido Cítrico Ciclo do Citrato Ciclo dos Ácidos Tricarboxílicos Características • É um ciclo metabólico, pois o oxaloacetato, que inicia a via metabólica, sofre transformações e é regenerado no final do ciclo. • O ciclo de Krebs ocorre em anaerobiose. • O sistema enzimático do ciclo está localizado nas mitocôndrias. • É fundo comum no metabolismo dos glicídios, lipídios e protídios. • O Ciclo de Krebs tem a característica de uma via anfibólica, isto é, degrada a acetila-Co. A em dióxido de carbono e água (catabolismo) mas alguns de seus intermediários são utilizados para a síntese de outros compostos (anabolismo). Funções do Ciclo de Krebs Oxidar a acetila-Co. A em CO 2 e H 2 O. Como conseqüência desta oxidação, é o maior fornecedor de elétrons para a Cadeia Respiratória e, sendo assim, é um grande gerador de energia (ATP). Alguns de seus intermediários são precursores de compostos bioquimicamente importantes. Localização do Sistema Enzimático: Matriz mitocondrial 1

2

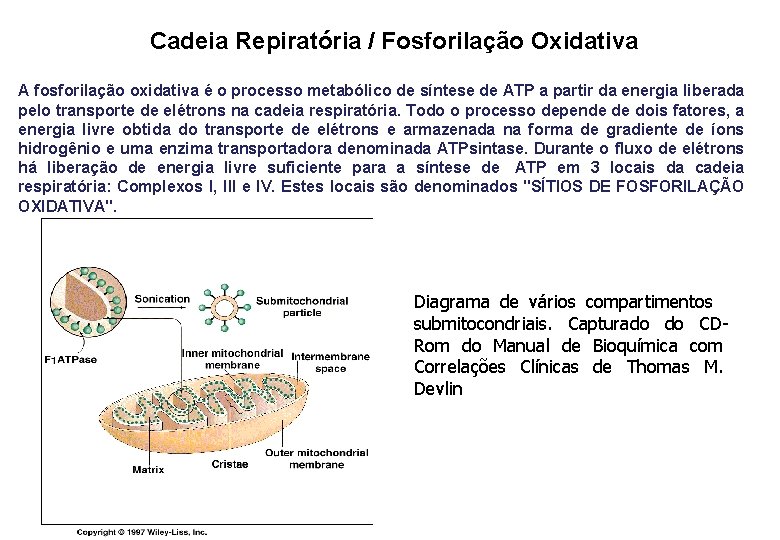
Cadeia Repiratória / Fosforilação Oxidativa A fosforilação oxidativa é o processo metabólico de síntese de ATP a partir da energia liberada pelo transporte de elétrons na cadeia respiratória. Todo o processo depende de dois fatores, a energia livre obtida do transporte de elétrons e armazenada na forma de gradiente de íons hidrogênio e uma enzima transportadora denominada ATPsintase. Durante o fluxo de elétrons há liberação de energia livre suficiente para a síntese de ATP em 3 locais da cadeia respiratória: Complexos I, III e IV. Estes locais são denominados "SÍTIOS DE FOSFORILAÇÃO OXIDATIVA". Diagrama de vários compartimentos submitocondriais. Capturado do CDRom do Manual de Bioquímica com Correlações Clínicas de Thomas M. Devlin

UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ Campus Londrina Micrografia eletrônica de mitocôndrias de hepatócito de fígado de rato (x 39600). Capturado do CD-Rom do Manual de Bioquímica com Correlações Clínicas de Thomas M. Devlin Micrografia eletrônica de mitocôndrias de fibras musculares de coelho (x 39600). Capturado do CD-Rom do Manual de Bioquímica com Correlações Clínicas de Thomas M. Devlin

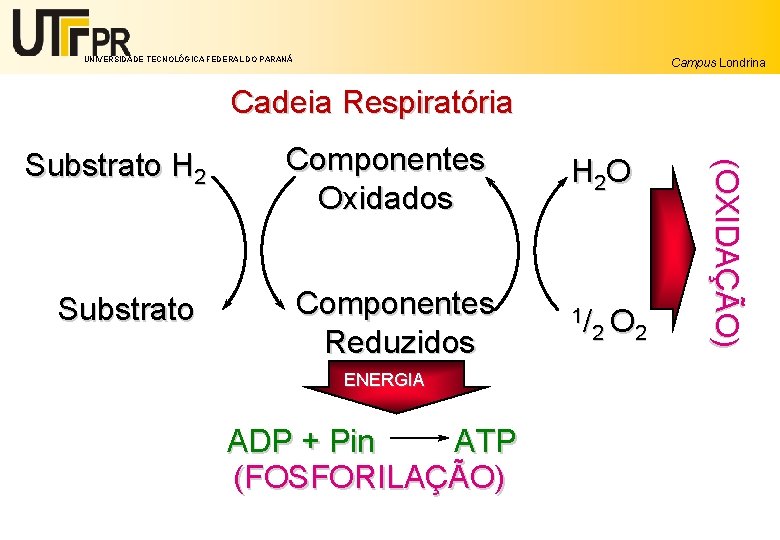
UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ Campus Londrina Cadeia Respiratória Substrato Componentes Oxidados Componentes Reduzidos ENERGIA ADP + Pin ATP (FOSFORILAÇÃO) H 2 O 1/ O 2 2 (OXIDAÇÃO) Substrato H 2

UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ Campus Londrina Elementos da Cadeia Respiratória 1 - Nucleotídeos - NAD • Nicotinamida Adenina Dinucleotídio. Coenzima que possui vit. PP (B 5) em sua estrutura. • Apresenta a capacidade de transportar dois elétrons e um próton em sua estrutura, conforme a reação: Substrato-H 2+NADoxi (Reduzido) Substrato+NADH+H+ (Oxidado) NAD desidrogenases (DSH) • Alcool Desidrogenase • Malato Desidrogenase • Lactato Desidrogenase • Hidroxiacil-Co. A Desidrogenase • Gliceraldeído 3 fosfato Desidrogenase

UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ 2 - Nucleotídios - FMN Flavina Mononucleotídio. O FMN transfere dois elétrons e dois prótons e possui vitamina (riboflavina) B 2 em sua molécula Campus Londrina

UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ Campus Londrina 3 - Nucleotídios - FAD O FAD constitui o complexo II, transfere dois elétrons e dois prótons para Co. Q. Possui vitamina (riboflavina) B 2 em sua molécula

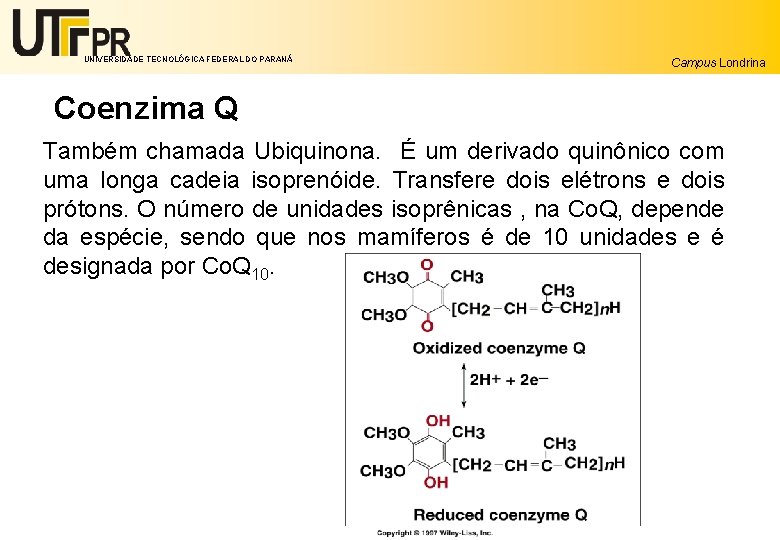
UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ Campus Londrina Coenzima Q Também chamada Ubiquinona. É um derivado quinônico com uma longa cadeia isoprenóide. Transfere dois elétrons e dois prótons. O número de unidades isoprênicas , na Co. Q, depende da espécie, sendo que nos mamíferos é de 10 unidades e é designada por Co. Q 10.

UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ Campus Londrina Citocromos São proteínas transportadoras de elétrons. Apresentam um grupo prostético, com Fe, semelhante ao Heme. Os radicais ligados aos núcleos pirrólicos são diferentes entre os diversos citocromos, mas específicos para cada um deles. Os citocromos têm estruturas e propriedades distintas. Distinguidos por diferenças nos seus espectros de absorção • • • Cit b Cit c 1 Cit c Cit a 3 560 nm 550 nm 600 nm

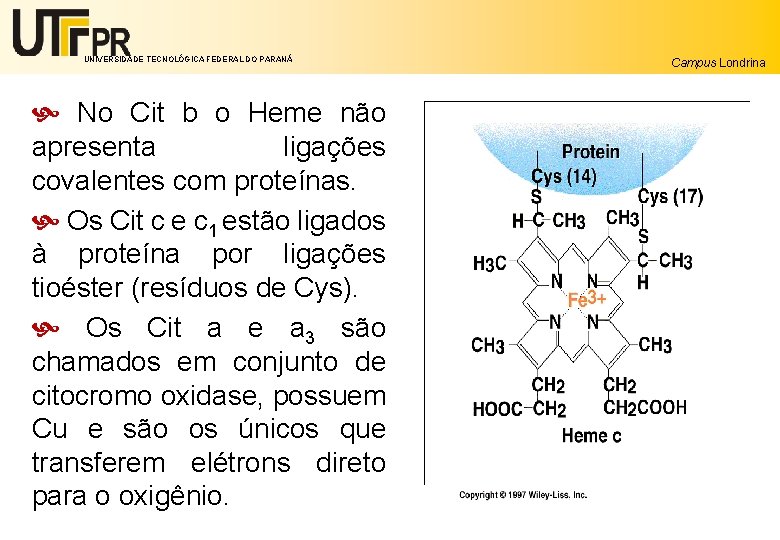
UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ No Cit b o Heme não apresenta ligações covalentes com proteínas. Os Cit c e c 1 estão ligados à proteína por ligações tioéster (resíduos de Cys). Os Cit a e a 3 são chamados em conjunto de citocromo oxidase, possuem Cu e são os únicos que transferem elétrons direto para o oxigênio. Campus Londrina

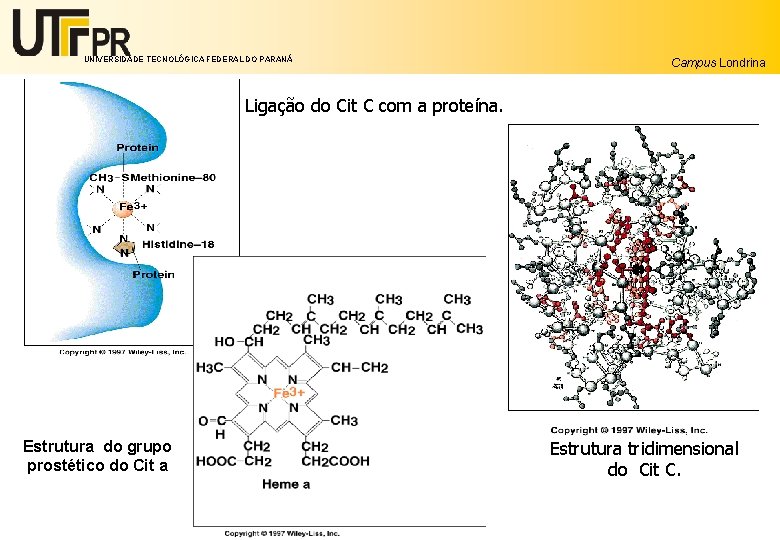
UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ Campus Londrina Ligação do Cit C com a proteína. Estrutura do grupo prostético do Cit a Estrutura tridimensional do Cit C.

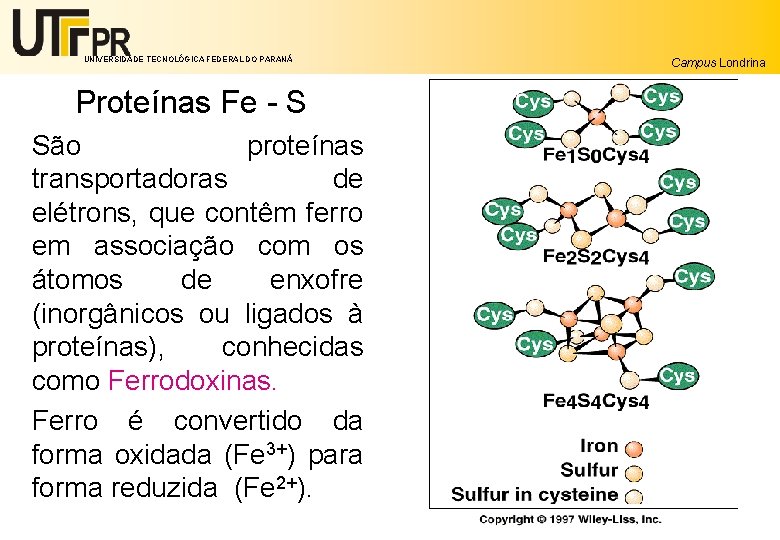
UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ Campus Londrina Proteínas Fe - S São proteínas transportadoras de elétrons, que contêm ferro em associação com os átomos de enxofre (inorgânicos ou ligados à proteínas), conhecidas como Ferrodoxinas. Ferro é convertido da forma oxidada (Fe 3+) para forma reduzida (Fe 2+).

UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ Campus Londrina Ordem dos Componentes Os componentes da C. R. estão ordenados segundo suas afinidades eletrônicas (potencial redox E’). NAD FMN Co. Q Citb Citc 1 Citc Citaa 3 Transporte de Elétrons O transporte de elétrons da C. R. inicia quando o substrato entrega 2 elétrons e 2 prótons para o NAD e termina quando estas partículas são entregues ao oxigênio formando água.

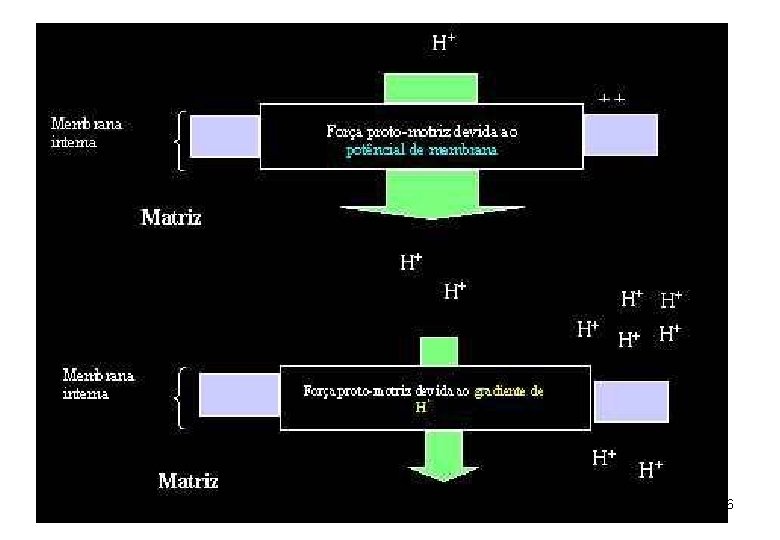
Hipótese Quimiosmótica para transferência de elétrons ( Mitchell) A C. R. , ao transportar os elétrons, bombeia prótons da matriz para o citosol; a MMI, por ser impermeável a prótons, impede o retorno destes à matriz; cria-se um GRADIENTE DUPLO (p. H e eletrostático) através da MMI (situação de instabilidade) e atrai os prótons de volta (força próton-motriz), dirige o refluxo de prótons à matriz mitocondrial através dos canais de prótons da enzima ATPase; a passagem dos prótons pela ATPase determina a síntese do ATP. 15

16

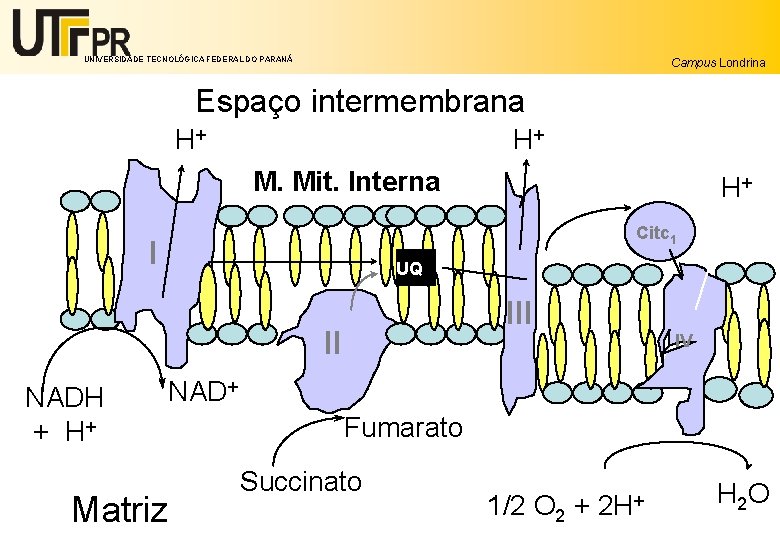
UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ Campus Londrina Espaço intermembrana H+ H+ M. Mit. Interna Citc 1 I UQ III II NADH + H+ H+ IV NAD+ Matriz Fumarato Succinato 1/2 O 2 + 2 H+ H 2 O

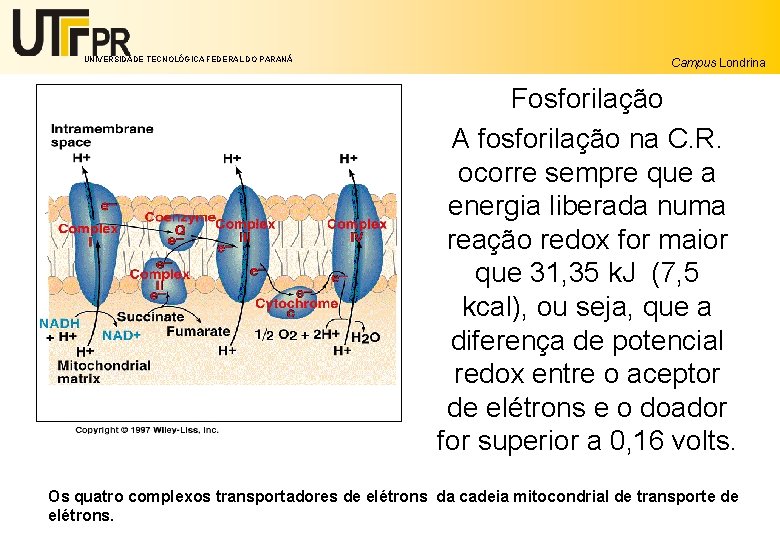
UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ Campus Londrina Fosforilação A fosforilação na C. R. ocorre sempre que a energia liberada numa reação redox for maior que 31, 35 k. J (7, 5 kcal), ou seja, que a diferença de potencial redox entre o aceptor de elétrons e o doador for superior a 0, 16 volts. Os quatro complexos transportadores de elétrons da cadeia mitocondrial de transporte de elétrons.

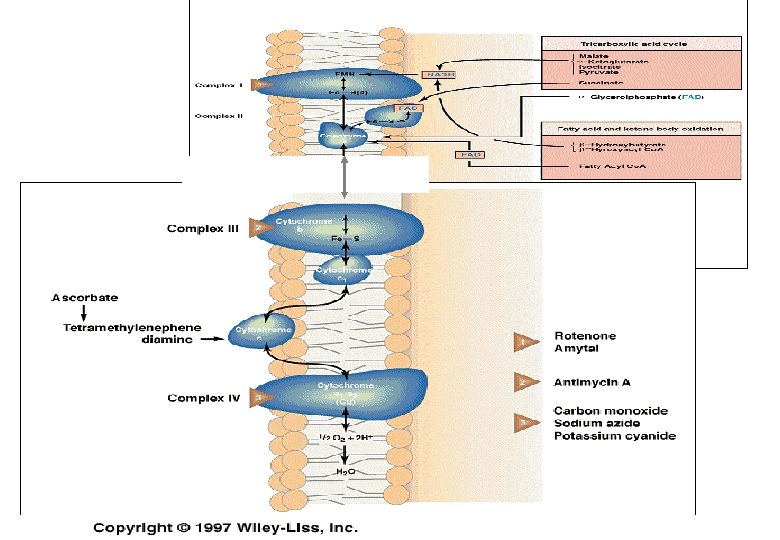
UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ Campus Londrina Substratos que cedem elétrons para o NAD 3 -Hidroxiacil-Co. A Piruvato -Cetoglutarato Isocitrato Malato Substratos que cedem elétrons para o FAD Succinato Acil Co. A graxo


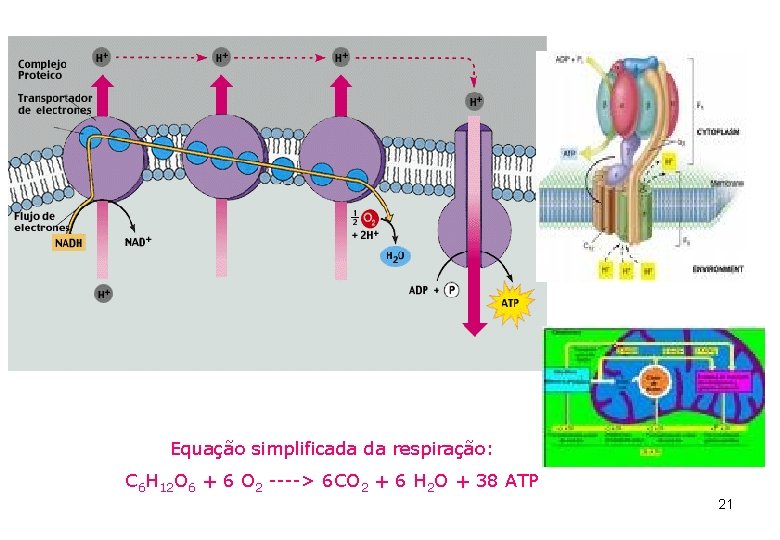
Equação simplificada da respiração: C 6 H 12 O 6 + 6 O 2 ----> 6 CO 2 + 6 H 2 O + 38 ATP 21

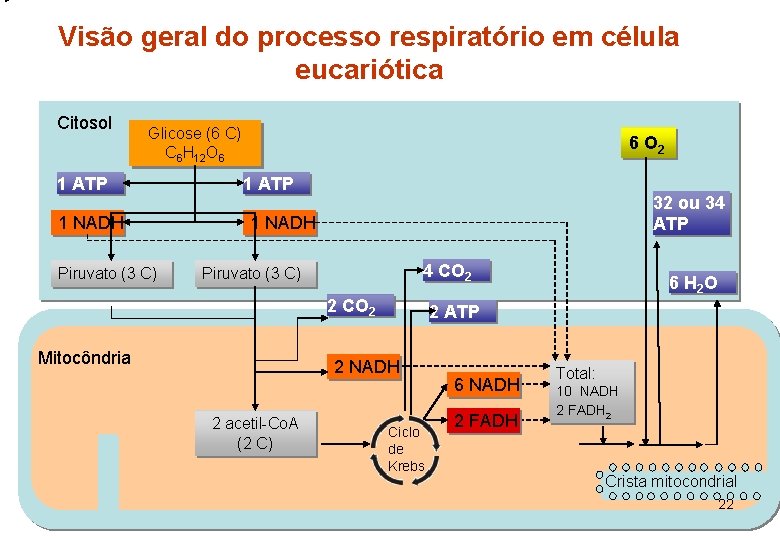
Visão geral do processo respiratório em célula eucariótica Citosol Glicose (6 C) C 6 H 12 O 6 1 ATP 1 NADH Piruvato (3 C) 6 O 2 1 ATP 32 ou 34 ATP 1 NADH 4 CO 2 Piruvato (3 C) 2 CO 2 Mitocôndria 2 ATP 2 NADH 2 acetil-Co. A (2 C) 6 H 2 O Ciclo de Krebs 6 NADH 2 FADH Total: 10 NADH 2 FADH 2 Crista mitocondrial 22

UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ Campus Londrina Formação de Água Metabólica: É a água formada no final da C. R. pela combinação dos prótons liberados pela Co. Q, pelos dois elétrons transportados e pelo átomo de oxigênio de uma hidroxila ativa. Controle da Velocidade A C. R. pode ser controlada indiretamente ao nível das rotas metabólicas. Na ausência de substrato reduzido todos os componentes da C. R. ficam oxidados. Diretamente quem controla a C. R. é a disponibilidade de ADP.

UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ Campus Londrina Controle de Velocidade Condição: Ausência de Substrato Ausência de Oxigênio Aumento de ADP Aumento de ATP Velocidade zero Aumentada Diminuída Componentes Oxidados Reduzidos Oxid. e Red. Intercâmbio de ATP e ADP entre Mitocôndria e o Citosol - O ATP sintetizado na Mitocôndria é utilizado pela célula. A saída de ATP através da membrana mitocondrial interna não se dá por simples difusão, mas sim por um carregador e acoplada à entrada de ADP.

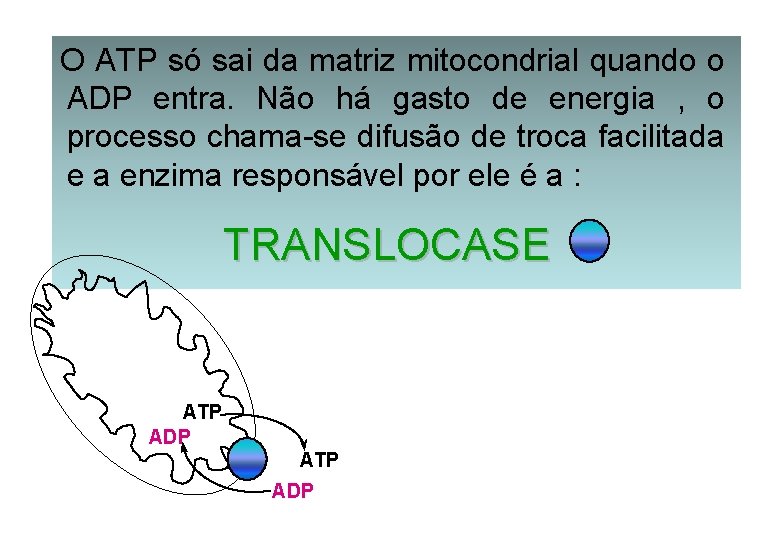
O ATP só sai da matriz mitocondrial quando o ADP entra. Não há gasto de energia , o processo chama-se difusão de troca facilitada e a enzima responsável por ele é a : TRANSLOCASE ATP ADP

Balanço Final da respiração Celular Ao calcular o rendimento em ATPs da oxidação total de uma molécula de glicose, e considerando que cada par de elétrons do NADH rende 3 ATPs, e cada par de elétrons do FADH 2 rende 2 ATPs na fosforilação oxidativa, tem-se: 10 NADH 30 ATPs 2 FADH 2 4 ATPs 2 ATPs + 2 GTPs 4 ATPs Total: 38 ATPs Este número pressupõe gasto de ATP zero em processos paralelos, o que não ocorre na prática; considerando-se o gasto de ATP utilizado no início da respiração, o balanço final gira em torno de 36 ATPs. 26