CHUYN MT S PHNG PHP GII NHANH BI



CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Phần mở đầu - Hiện nay trên thế giới nói chung và Việt Nam ta nói riêng việc đưa loại bài tập trắc nghiệm có nhiều lựa chọn vào các kì thi ngày càng phổ biến vì nó có nhiều ưu điểm. + Kiểm tra đánh giá được nhiều kiến thức, tránh học tủ, học lệch ở HS + Xác suất đúng ngẫu nhiên thấp + Gây được hứng thú học tập của học sinh + Tiết kiệm thời gian chấm bài + Học sinh có thể tự kiểm tra đánh giá kết quả học tập của mình một cách nhanh chóng qua các bài kiểm tra trên lớp, trong sách, hay trên mạng internet. Đồng thời tự đề ra phương pháp học tập để bổ sung kiến thức một cách hợp lý. - Tuy nhiên đối với những loại bài tập trắc nghiệm các em cần phải trả lời nhanh và chính xác cao vì thời gian dành cho mỗi câu trung bình chỉ là 1, 5 phút. Do đó các em phải trang bị cho mình ngoài những cách giải thông thường, cần có những phương pháp giải nhanh, chọn đúng

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Phần mở đầu Qua những năm giảng dạy trực tiếp bộ môn Hóa học 9, tôi nhận thấy các em học sinh thường rất yếu khi giải bài tập đặc biệt là bài tập trắc nghiệm khách quan. Hiện nay theo hướng kiểm tra đánh giá trắc nghiệm khách quan thì trong một bài kiểm tra thường có rất nhiều dạng toán, mà thời gian chia đều cho mỗi câu lại rất hạn chế. Nếu các em vẫn giải bài tập theo hướng tự luận như trước đây thì thường không đủ thời gian để hoàn thành một bài kiểm tra đánh giá dẫn đến chất lượng bộ môn thấp. Từ thực tế trên, tôi đã sưu tầm các tài liệu, tìm tòi, nghiên cứu và đã tích lũy được một số kinh nghiệm giúp HS giải các bài toán Hóa học một cách nhanh chóng và hiệu quả. Với những lý do trên tôi mạnh dạn thực hiện chuyên đề “ Một số phương pháp giải nhanh bài toán môn Hóa học 9” nhằm giúp cho các em học sinh có kinh nghiệm giải các bài tập một cách tự tin, nhanh chóng và có hiệu quả.

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 1: PHƯƠNG PHÁP ÁP DỤNG ĐỊNH LUẬT BẢO TOÀN NGUYÊN TỐ VÀ KHỐI LƯỢNG I. Cơ sở kiến thức 1. Trong phản ứng hóa học, các nguyên tố và khối lượng của chúng được bảo toàn. Từ đó suy ra 2 định luật: + Tổng khối lượng các chất trước phản ứng luôn bằng tổng khối lượng các chất sau phản ứng. (ĐLBTKL) + Tổng số mol nguyên tử của nguyên tố A trước phản ứng luôn bằng tổng số mol nguyên tử của nguyên tố A sau phản ứng. (ĐLBTNT) 2. Áp dụng + Trong phản ứng có n chất tham gia và sản phẩm, nếu biết khối lượng của (n-1) chất thì ta dễ dàng tính được khối lượng của chất còn lại + Bài toán: Kim loại + axit Muối + Khí + Bài toán hỗn hợp oxit kim loại + H 2, CO…. + Bài toán có chuỗi các PTHH

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 1: PHƯƠNG PHÁP ÁP DỤNG ĐỊNH LUẬT BẢO TOÀN NGUYÊN TỐ VÀ KHỐI LƯỢNG Lưu ý: Đối với phản ứng (kim loại + axit) kim loại đó phải phản ứng hoàn toàn Giả sử kim loại R 2 R + 2 HCl 2 R + 6 HCl Ta có: n. Cl = 2 RCl + H 2 RCl 2 + H 2 2 RCl 3 + 3 H 2 2 R + H 2 SO 4 2 R + 3 H 2 SO 4 Ta có: R 2 SO 4 + H 2 R 2(SO 4)3 + 3 H 2

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 1: PHƯƠNG PHÁP ÁP DỤNG ĐỊNH LUẬT BẢO TOÀN NGUYÊN TỐ VÀ KHỐI LƯỢNG Lưu ý: * Đối với phản ứng (kim loại + axit) kim loại đó phải phản ứng hoàn toàn * Ta có: + n. Cl = ; + Muối Gốc axit *m mkim loại muối = Kim loại ++m gốc axit *m = m loại + moxi Oxit = kim loại + oxit kim loại II. Phương pháp giải - Tính n theo đề ra - Tính ngốc axit: Hoặc - Tính theo yêu cầu của đề: moxit = m. Kim loại + m. O; mmuối = mkim loại + mgốc axit

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 1: PHƯƠNG PHÁP ÁP DỤNG ĐỊNH LUẬT BẢO TOÀN NGUYÊN TỐ VÀ KHỐI LƯỢNG II. Phương pháp giải - Tính n theo đề ra - Tính ngốc axit: ; Hoặc - Tính theo yêu cầu của đề: moxit = m. Kim loại + m. O; mmuối = mkim loại + mgốc axit III. Ví dụ minh họa Ví dụ 1: (Hỗn hợp 2 kim loại + HCl) Cho 7, 8 gam hỗn hợp kim loại Al và Mg tác dụng với HCl thu được 8, 96 lit H 2(đktc). Hỏi khi cô cạn thu được bao nhiêu gam muối khan? A. 36, 2 g B. 36 g C. 34, 6 g D. 30, 2 g Tóm tắt: m 2 kim loại = 7, 8 g mmuối =? g Lời giải: 8, 96 = 0, 4 mol n. H = 22, 4 2 mmuối = mkim loại + mgốc axit = 7, 8 + 0, 8 x 35, 5 = 36, 2 (g)

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 1: PHƯƠNG PHÁP ÁP DỤNG ĐỊNH LUẬT BẢO TOÀN NGUYÊN TỐ VÀ KHỐI LƯỢNG II. Phương pháp giải - Tính n theo đề ra - Tính ngốc axit: ; Hoặc - Tính theo yêu cầu của đề: moxit = m. Kim loại + m. O; mmuối = mkim loại + mgốc axit III. Ví dụ minh họa VD 2: Hòa tan hoàn toàn 3, 22 gam hỗn hợp kim loại X gồm Fe, Zn và Mg bằng một lượng vừa đủ H 2 SO 4 loãng, thu được 1, 344 lít H 2(đktc). Khối lượng muối thu được là: A. 8, 9 g B. 8, 98 g C. 9, 8 g D. 9, 88 g VD 3: Hòa tan hoàn toàn 14, 7 g hỗn hợp Mg, Zn, Ni bằng HCl, thu được 6, 72 lít khí (đktc). Tính khối lượng muối thu được? VD 4: Cho 29 g hỗn hợp Mg, Fe, Zn tác dụng hoàn toàn với H 2 SO 4 loãng, Thu được V lít khí (đktc) và 86, 6 g muối. Tính V

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 1: PHƯƠNG PHÁP ÁP DỤNG ĐỊNH LUẬT BẢO TOÀN NGUYÊN TỐ VÀ KHỐI LƯỢNG II. Phương pháp giải - Tính n theo đề ra - Tính ngốc axit: ; Hoặc - Tính theo yêu cầu của đề: moxit = m. Kim loại + m. O; mmuối = mkim loại + mgốc axit III. Ví dụ minh họa Ví dụ 5: (Hỗn hợp 2 oxit kim loại + H 2) Khử hoàn toàn 32 g hỗn hợp A gồm Cu. O và Fe 2 O 3 bằng khí H 2, thấy tạo ra 9 g H 2 O. Khối lượng hỗn hợp kim loại thu được là: A. 12 g B. 24 g C. 23 g D. 41 g Tóm tắt: m 2 oxit = 32 g mkim loại =? g Hướng dẫn n. O moxit = m. Kim loại + m. O

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 1: PHƯƠNG PHÁP ÁP DỤNG ĐỊNH LUẬT BẢO TOÀN NGUYÊN TỐ VÀ KHỐI LƯỢNG II. Phương pháp giải - Tính n theo đề ra - Tính ngốc axit: ; Hoặc - Tính theo yêu cầu của đề: moxit = m. Kim loại + m. O; mmuối = mkim loại + mgốc axit III. Ví dụ minh họa Bài toán có nhiều PTHH xảy ra liên tiếp

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 2: DỰA VÀO KHỐI LƯỢNG MOL TRUNG BÌNH I. Cơ sở kiến thức 1. Kiến thức MA < M B 2. Áp dụng - Áp dụng khi giải bài toán gồm 2 kim loại, 2 oxit, 2 muối…. của 2 kim loại liên tiếp trong cùng một nhóm. - Áp dụng khi cho hỗn hợp 2 chất hữu cơ liên tiếp cùng dãy đồng đẳng II. Phương pháp giải + Tính n theo đề ra + Viết pt tổng quát, rồi lập tỉ lệ mol + Áp dụng + Tìm MA và MB

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 2: DỰA VÀO KHỐI LƯỢNG MOL TRUNG BÌNH II. Phương pháp giải + Tính n theo đề ra + Viết pt tổng quát, rồi lập tỉ lệ mol + Áp dụng Tìm MA và MB III. Ví dụ minh họa Ví dụ 1: Cho 17 g hỗn hợp X gồm 2 kim loại kiềm kế tiếp nhau trong nhóm IA, tác dụng hết với nước thu được 6, 72 lít khí H 2 (đktc) và dung dịch Y. X gồm những kim loại : A. Li, Na B. Na, K C. K, Rb D. Rb, Cs Bài giải: 2 M + 2 H 2 O 2 MOH + H 2 Vậy X gồm: Na = 23 và K = 39

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 2: DỰA VÀO KHỐI LƯỢNG MOL TRUNG BÌNH II. Phương pháp giải + Tính n theo đề ra + Viết pt tổng quát, rồi lập tỉ lệ mol + Áp dụng Tìm MA và MB III. Ví dụ minh họa Ví dụ 2: Hòa tan hoàn toàn 19, 3 g hỗn hợp X gồm 2 kim loại A và B (chỉ có A tan, MA>MB) cùng hóa trị II, bằng Dd HCl dư. Sau phản ứng thu được 2, 24 lit khí H 2 (đktc). Xác định 2 kim loại nói trên. Biết n. A bằng nửa n. B. A. Fe và Cu B. Fe và Zn C. Zn và Cu D. Ca và Mg Hướng dẫn MA, MB (MA>MB) n. A ; n. B (n. B = 2 n. A) (Chỉ có A + HCl)

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 3: XÁC ĐỊNH NGUYÊN TỐ DỰA VÀO CÔNG THỨC OXIT CAO NHẤT I. Cơ sở kiến thức 1. Kiến thức + Oxit cao nhất của nguyên tố R hóa tri y là: Rx. Oy, thì hợp chất của nó với Hidro là: RH 8 -y + Ngược lại khi cho hợp chất khí với hidro của một nguyên tố là RHy, thì oxit cao nhất của nó là Rx. O 8 -y + Vận dụng tính theo công thức hóa học: 2. Áp dụng + Các bài toán tìm tên nguyên tố (liên quan đến hợp chất của nó với H, O)

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 3: XÁC ĐỊNH NGUYÊN TỐ DỰA VÀO CÔNG THỨC OXIT CAO NHẤT II. Phương pháp giải + Từ Rx. Oy RH 8 -y Hoặc từ RHy Rx. O 8 -y (x, y là hóa trị của O, R) + Vận dụng công thức: + Tìm MR suy ra tên nguyên tố III. Ví dụ minh họa Ví dụ 1: Nguyên tố R tạo thành hợp chất khí với hidro có công thức RH 3. Trong hợp chất oxit cao nhất có 25, 93% R về khối lượng. Nguyên tố R là: A. Lưu huỳnh B. Nito C. Photpho D. Cacbon Hướng dẫn: RH Rx. O 8 -y y Hợp chất của nó với hidro là RH 3 MR = 14. Vậy R là Nito Oxit cao nhất của nguyên tố là R 2 O 5

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 3: XÁC ĐỊNH NGUYÊN TỐ DỰA VÀO CÔNG THỨC OXIT CAO NHẤT II. Phương pháp giải + Từ Rx. Oy RH 8 -y Hoặc từ RHy Rx. O 8 -y (x, y là hóa trị của O, R) + Vận dụng công thức: + Tìm MR suy ra tên nguyên tố III. Ví dụ minh họa Ví dụ 2: Oxit cao nhất của một nguyên tố là RO 3. Trong hợp chất của nó với Hidro có 5, 88% H về khối lượng. Nguyên tố đó là. A. Lưu huỳnh B. Nito C. Photpho D. Cacbon RH 8 -y Hướng dẫn: Rx. Oy Oxit cao nhất của nguyên tố là RO 3 Vậy R là S hợp chất của nó với H là RH 2

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 4: PHƯƠNG PHÁP TĂNG GIẢM KHỐI LƯỢNG I. Cơ sở kiến thức 1. Kiến thức + Vận dụng Định luật bảo toàn khối lượng + Kim loại 1 + Muối 1 Muối 2 + Kim loại 2 2. Áp dụng - Các bài toán tăng giảm khối lượng sau phản ứng II. Phương pháp giải + Viết PTPU. Gọi số mol kim loại 1 là x + Lập PT đại số mkim loại 1 – mkim loại 2 + Tìm x, rồi tính theo yêu cầu của đề. = Độ tăng (giảm)

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 4: PHƯƠNG PHÁP TĂNG GIẢM KHỐI LƯỢNG II. Phương pháp giải + Viết PTPU. Gọi số mol kim loại 1 là x + Lập PT đại số mkim loại 1 – mkim loại 2 = Độ tăng (giảm) + Tìm x, rồi tính theo yêu cầu của đề. III. Ví dụ minh họa Ví dụ 1: Nhúng 37, 5 g kim loại Zn vào dd Cu. SO 4 đến phản ứng hoàn toàn. Sau phản ứng lấy thanh Zn ra rửa nhẹ, lau khô cân nặng 37, 44 g. Coi toàn bộ lượng Cu sinh ra đều bám vào thanh Zn. m. Zn phản ứng là: A. 3, 9 g B. 6, 4 g C. 3, 2 g D. 5, 2 g Bài giải: Zn + Cu. SO 4 x(mol) Zn. SO 4 + Cu x(mol) Ta có : 65 x – 64 x = 37, 5 – 37, 44. Vậy x = 0, 06 mol Vậy m. Zn = 0, 06. 65 = 3, 9 g

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 4: PHƯƠNG PHÁP TĂNG GIẢM KHỐI LƯỢNG III. Ví dụ minh họa Ví dụ 2: Nhúng thanh Mg vào dd Cu. SO 4 Sau một thời gian lấy thanh kim loại ra, rửa nhẹ làm khô, cân lại thấy khối lượng kim loại tăng 1, 2 g. Tính khối lượng Mg phản ứng? VD 3: Cho Pb + Cu. Cl 2 Sau một thời gian phản ứng thấy khối lượng kim loại giảm 1, 43 g. Tính khối lượng Pb phản ứng?

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 5: PHƯƠNG PHÁP XÁC ĐỊNH CÔNG THỨC PH N TỬ HỢP CHẤT HỮU CƠ II. Phương pháp giải - Tính số mol của chất đề cho (CO 2, H 2 O, Br 2, …) - So sánh số mol của pư cháy hoặc pư cộng Br 2 nếu: Cn. H 2 n+2 (Ankan) Hoặc Cn. H 2 n (Anken) Cn. H 2 n-2 (Ankin) III. Ví dụ minh họa Ví dụ 1: Đốt cháy hoàn toàn một Hidrocacbon X thu được 17, 6 g CO 2 và 7, 2 g H 2 O. Công thức hóa học của X là: A. C 2 H 2 B. C 2 H 4 C. C 3 H 4 D. CH 4 Lời giải: X là C 2 H 4

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 5: PHƯƠNG PHÁP XÁC ĐỊNH CÔNG THỨC PH N TỬ HỢP CHẤT HỮU CƠ II. Phương pháp giải - Tính số mol của chất đề cho (CO 2, H 2 O, Br 2, …) - So sánh số mol cháy hoặc pư cộng Br 2 nếu: Cn. H 2 n+2 (Ankan) Hoặc Cn. H 2 n (Anken) Cn. H 2 n-2 (Ankin) III. Ví dụ minh họa Ví dụ 2: Biết 0, 01 mol một Hidrocacbon X có thể tác dụng tối đa với 200 ml dung dịch Brom 0, 1 M. Công thức hóa học của X là: A. C 2 H 2 B. C 2 H 4 C. C 6 H 6 D. CH 4 Giải: n. X = 0, 01 mol X là C 2 H 2

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 5: PHƯƠNG PHÁP XÁC ĐỊNH CÔNG THỨC PH N TỬ HỢP CHẤT HỮU CƠ II. Phương pháp giải - Tính số mol của chất đề cho (CO 2, H 2 O, Br 2, …) - So sánh số mol cháy hoặc pư cộng Br 2 nếu: Cn. H 2 n+2 (Ankan) Hoặc Cn. H 2 n (Anken) Cn. H 2 n-2 (Ankin) III. Ví dụ minh họa Ví dụ 3: Khi đốt cháy hoàn toàn 2 hidrocacbon liên tiếp trong dãy đồng đẳng thu được 16, 8 lít CO 2 (đktc) và 13, 5 g H 2 O. Hai hidrocacbon đó thuộc dãy đồng đẳng nào? A. Ankan B. Ankin C. Anken D. Aren Giải: Anken

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Bài tập 1: Đốt cháy một hidrocacbon X thu được CO 2 và H 2 O có tỉ lệ số mol tương ứng là 1: 2. Công thức phân tử của X là. A. CH 4 B. C 2 H 4 C. C 2 H 2 D. C 2 H 6 Hướng dẫn: Theo ĐLBTNT ta có: Suy ra nc : n. H = 1 : 4


CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 1: PHƯƠNG PHÁP ÁP DỤNG ĐỊNH LUẬT BẢO TOÀN NGUYÊN TỐ VÀ KHỐI LƯỢNG II. Phương pháp giải - Tính n theo đề ra - Tính ngốc axit: ; Hoặc - Tính theo yêu cầu của đề: moxit = m. Kim loại + m. O; mmuối = mkim loại + mgốc axit III. Ví dụ minh họa Ví dụ 2: (Hỗn hợp 3 kim loại + H 2 SO 4) Hòa tan hoàn toàn 3, 22 gam hỗn hợp kim loại X gồm Fe, Zn và Mg bằng một lượng vừa đủ H 2 SO 4 loãng, thu được 1, 344 lit H 2(đktc). Khối lượng muối thu được là: A. 8, 9 g B. 8, 98 g C. 9, 8 g D. 9, 88 g Bài giải PTHH chung: M + H 2 SO 4 MSO 4 + H 2 Cách 1: Áp dụng ĐLBTNT ta có: Cách 2: Áp dụng ĐLBTKL ta có: mmuối = mkim loại + mgốc axit = 3, 22 + 0, 06 x 96 = 8, 98 (g) = 3, 22 + 98. 0, 06 – 2. 0, 06 = 8, 98 (g)
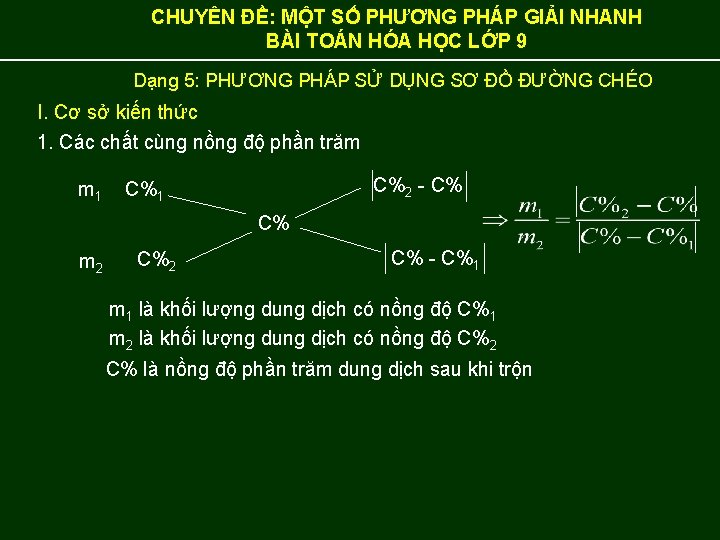
CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 5: PHƯƠNG PHÁP SỬ DỤNG SƠ ĐỒ ĐƯỜNG CHÉO I. Cơ sở kiến thức 1. Các chất cùng nồng độ phần trăm m 1 C%2 - C% C%1 C% m 2 C% - C%1 m 1 là khối lượng dung dịch có nồng độ C%1 m 2 là khối lượng dung dịch có nồng độ C%2 C% là nồng độ phần trăm dung dịch sau khi trộn
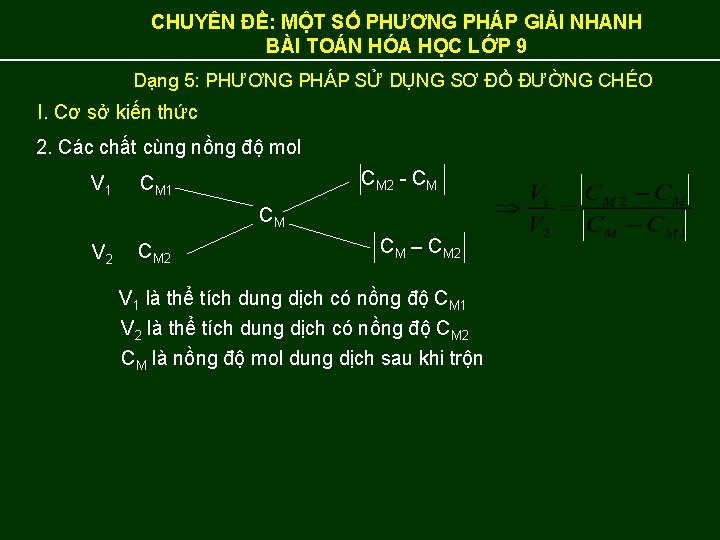
CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 5: PHƯƠNG PHÁP SỬ DỤNG SƠ ĐỒ ĐƯỜNG CHÉO I. Cơ sở kiến thức 2. Các chất cùng nồng độ mol V 1 CM 2 - CM CM 1 CM V 2 CM – CM 2 V 1 là thể tích dung dịch có nồng độ CM 1 V 2 là thể tích dung dịch có nồng độ CM 2 CM là nồng độ mol dung dịch sau khi trộn
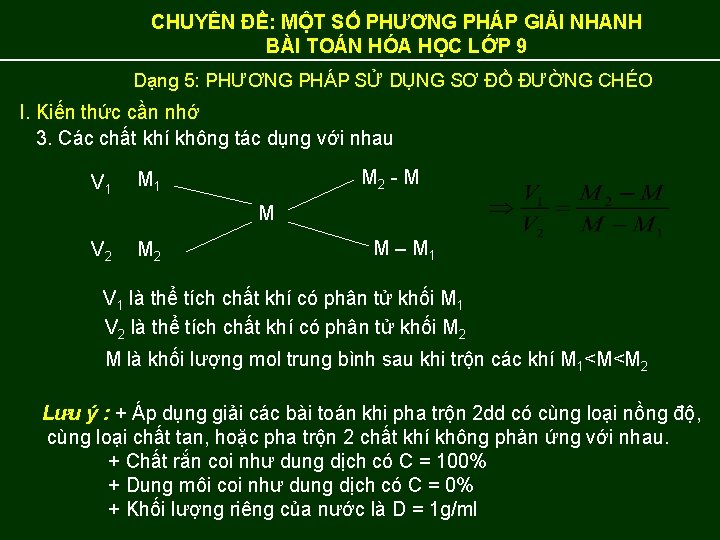
CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 5: PHƯƠNG PHÁP SỬ DỤNG SƠ ĐỒ ĐƯỜNG CHÉO I. Kiến thức cần nhớ 3. Các chất khí không tác dụng với nhau V 1 M 2 - M M 1 M V 2 M – M 1 V 1 là thể tích chất khí có phân tử khối M 1 V 2 là thể tích chất khí có phân tử khối M 2 M là khối lượng mol trung bình sau khi trộn các khí M 1<M<M 2 Lưu ý : + Áp dụng giải các bài toán khi pha trộn 2 dd có cùng loại nồng độ, cùng loại chất tan, hoặc pha trộn 2 chất khí không phản ứng với nhau. + Chất rắn coi như dung dịch có C = 100% + Dung môi coi như dung dịch có C = 0% + Khối lượng riêng của nước là D = 1 g/ml

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 5: PHƯƠNG PHÁP SỬ DỤNG SƠ ĐỒ ĐƯỜNG CHÉO II. Phương pháp giải 1. Các chất cùng nồng độ phần trăm 2. Các chất cùng nồng độ mol 3. Các chất khí không tác dụng với nhau III. Ví dụ minh họa Ví dụ 1: Trộn dung dịch HCl 45% với dung dịch HCl 15% để có dung dịch HCl 20% thì cần pha chế khối lượng giữa 2 dung dịch HCl ban đầu theo tỉ lệ là: A. 1: 3 B. 1: 5 C. 3: 1 D. 5: 1 Tóm tắt Lời giải: C%1 = 45% Áp dụng phương pháp đường chéo ta có C%2 = 15% C% = 20%

CHUYÊN ĐỀ: MỘT SỐ PHƯƠNG PHÁP GIẢI NHANH BÀI TOÁN HÓA HỌC LỚP 9 Dạng 5: PHƯƠNG PHÁP SỬ DỤNG SƠ ĐỒ ĐƯỜNG CHÉO II. Phương pháp giải 1. Các chất cùng nồng độ phần trăm 2. Các chất cùng nồng độ mol 3. Các chất khí không tác dụng với nhau III. Ví dụ minh họa Ví dụ 2: Thể tích nước và dung dịch Mg. SO 4 2 M cần để pha chế được 100 ml Dung dịch Mg. SO 4 0, 4 M lần lượt là: A. 50 ml và 50 ml C. 40 ml và 60 ml C. 80 ml và 20 ml Lời giải: Gọi V là thể tích nước thể tích dd Mg. SO 4 = 100 - V Áp dụng phương pháp đường chéo ta có; Vậy
- Slides: 31