Chromatographie 2 Einfhrung GC und HPLC Gaschromatographie GC















- Slides: 32

Chromatographie 2 Einführung: GC und HPLC

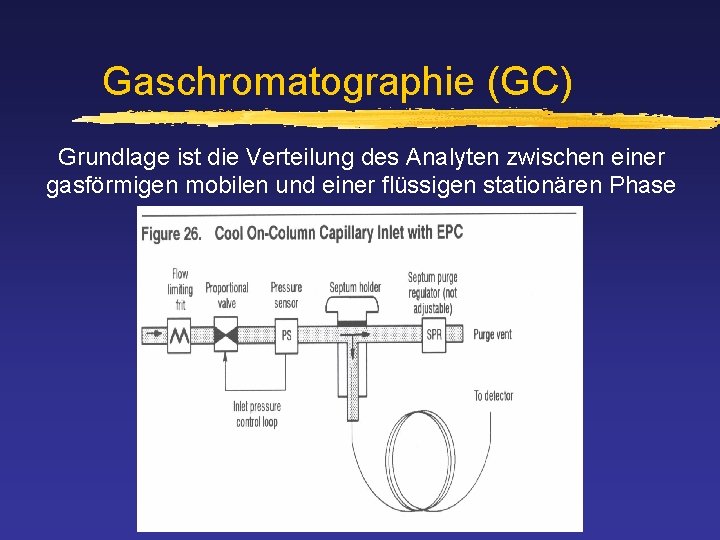
Gaschromatographie (GC) Grundlage ist die Verteilung des Analyten zwischen einer gasförmigen mobilen und einer flüssigen stationären Phase

GC Stationäre Phase z Eigenschaften - Geringe Flüchtigkeit (hoher Siedepunkt >400 °C) - Thermische Stabilität - Chemische Inertheit z Immobilisierte Flüßigkeiten Polarität ausschlaggebend; meist hochsiedende Silikonöle DB-1, HP-1, CP-1 = Polydimethylsiloxan (unpolar) DB-5= Poly(phenylmethyl)dimethylsiloxan (5% Phenyl) Carbowax = Polyethylenglycol (polarer)

GC Trennsäulen z Gepackte Säulen ca. 2 m lange Glassäulen; Innen-Ø 2 mm Trägermaterial (z. B. Kieselgur, Ø 150 -250 µm) Stationäre Phase als Film auf Träger (0. 05 - 1 µm) z Kapillarsäulen Quarzsäulen mit Polyimidbeschichtung (flexibel!) 10 - 100 m lang; Innen-Ø von 0. 1 - 0. 5 mm Stationäre Phase als Film an der Kapillare (FSOT) Filmdicke 0. 01 - 5 µm

GC Mobile Phase tritt nicht mit dem Analyten in Wechselwirkung, sondern sorgt nur für den Transport des Analyten durch die Säule ! z Eigenschaften Inertes Gas (H 2, He, N 2); sauerstofffrei z Flußraten (Kapillarsäulen) Massefluß: 0. 5 - 2. 0 m. L min-1 Lineare Strömungsgeschwindigkeit (µ) 5 - 40 cm s-1

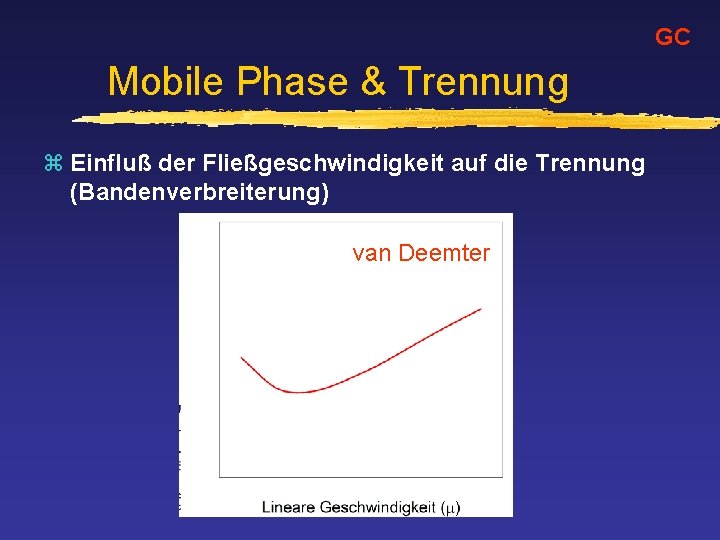
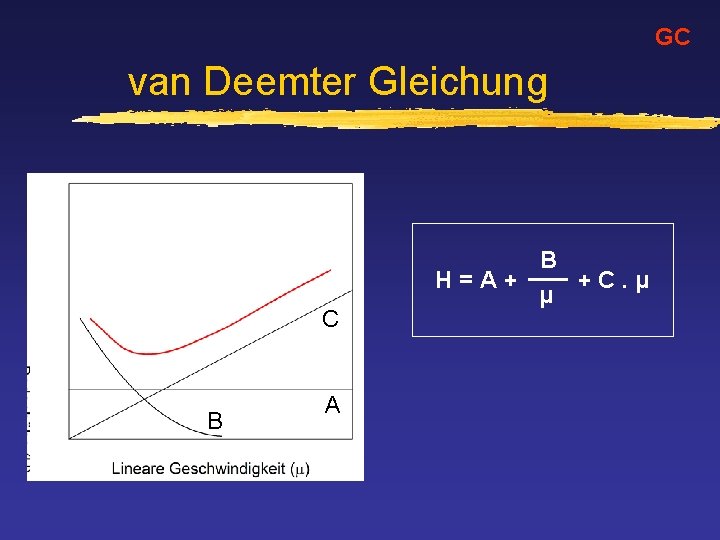
GC Mobile Phase & Trennung z Einfluß der Fließgeschwindigkeit auf die Trennung (Bandenverbreiterung) van Deemter

GC van Deemter Gleichung Massentransferkoeffizient (C) Diffusionskontrolierter Massetransfer zwischen stationären und mobiler Phase. Linear von der Geschwindigkeit abhängig Die in der mobilen Phase befindlichen Moleküle wandern weiter, während sich jene die aus der stationären Phase zurückkehren nur verzögert in die Bande eingleidern können Bandenverbreiterung

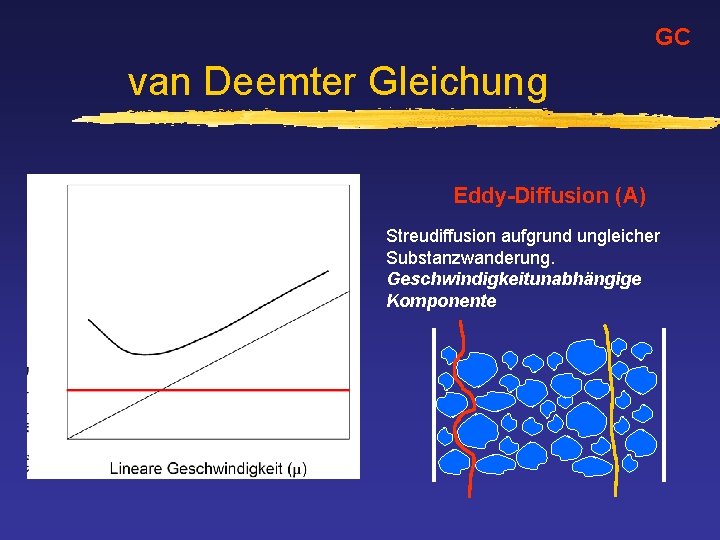
GC van Deemter Gleichung Eddy-Diffusion (A) Streudiffusion aufgrund ungleicher Substanzwanderung. Geschwindigkeitunabhängige Komponente

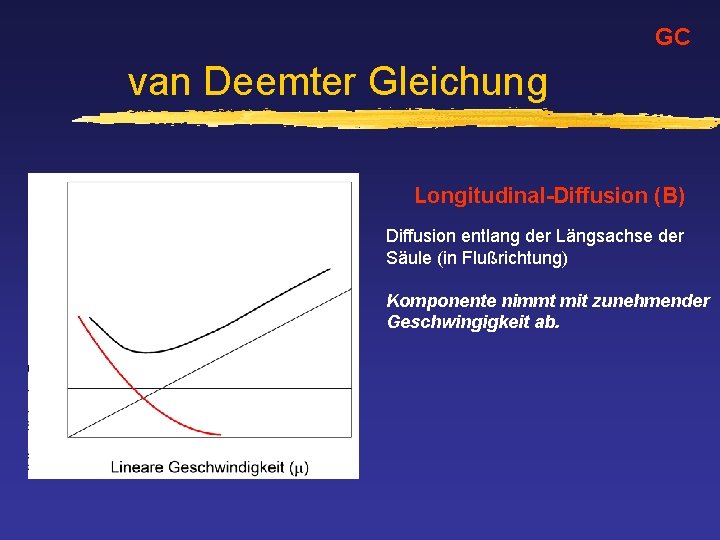
GC van Deemter Gleichung Longitudinal-Diffusion (B) Diffusion entlang der Längsachse der Säule (in Flußrichtung) Komponente nimmt mit zunehmender Geschwingigkeit ab.

GC van Deemter Gleichung C B A B H=A+ +C. µ µ

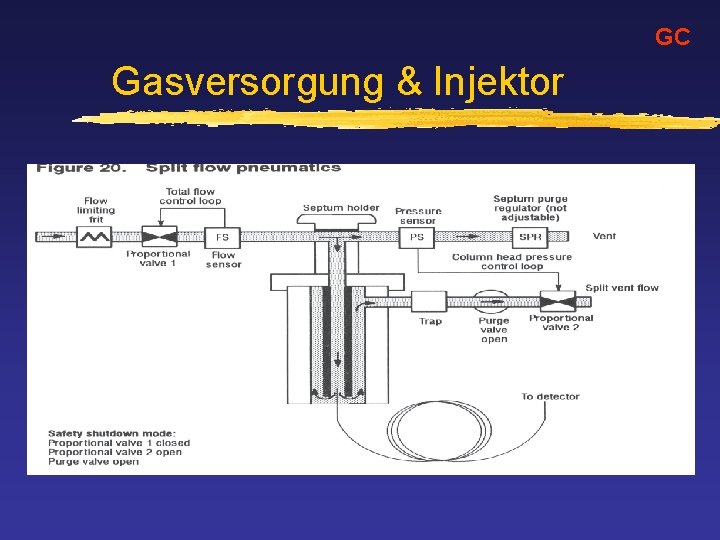
GC Trägergasversorgung Druckregelung Trägergasflüsse z Säulenvordruck wird eingestellt (column head pressure) ca. 20 -150 h. Pa Wenn Temperatur gesteigert wird, fällt bei gleichbleiben-den Druck die lineare Geschwindigkeit! z Durchflußmessung mittels Blasenzähler am Ende der Säule Abhilfe schafft eine elektronische Druckregelung, die lineare Geschwindigkeit konstant hält.

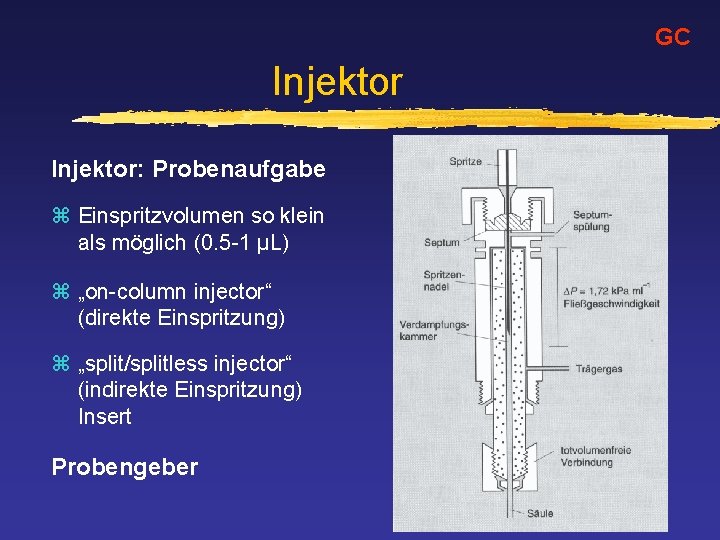
GC Injektor: Probenaufgabe z Einspritzvolumen so klein als möglich (0. 5 -1 µL) z „on-column injector“ (direkte Einspritzung) z „split/splitless injector“ (indirekte Einspritzung) Insert Probengeber

GC Gasversorgung & Injektor

GC Split/Splitless-Injektor

GC Temperatur & Säulenofen Säulentemperatur z Wichtige Variable! Elutionstemperatur muß höher sein als die Siede-temperatur des Analyten z Proben unterschiedlicher Siedetemperatur werden mit einem Temperaturprogramm aufgetrennt z Säulenofen zur Thermostatierung (kontinuierliche T-Erhöhung) 45° 145° 35 -180°

GC Detektoren Eigenschaften Arten von Detektoren z Ausreichende Empfindlichkeit z Gute Stabilität z Gute Reproduzierbarkeit z Großer linarer Bereich z Schnelle Ansprechzeiten z Selektivität z Hoher Temperaturbereich FID (Flammenionisationsdetektor) TCD (Wärmeleitfähigkeitsdetektor) ECD (Elktroneneinfangdetektor) AED (Atomemissionsdetektor) GC-MS (Kopplung zu einem Massenspektrometer)

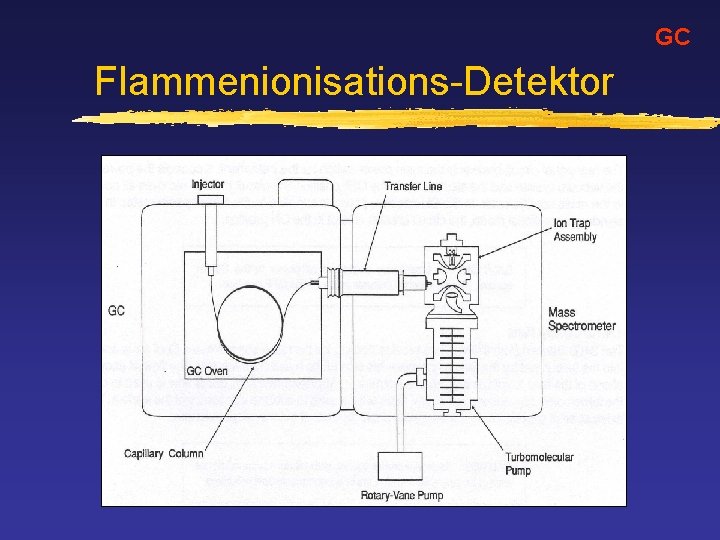
GC Flammenionisations-Detektor

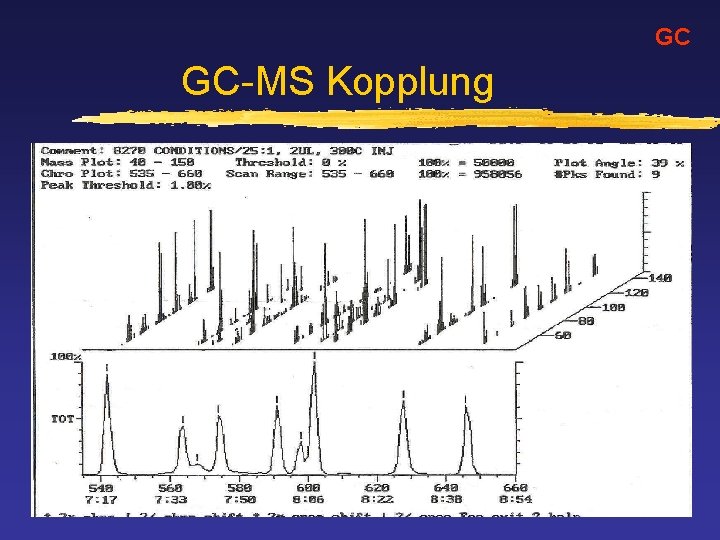
GC GC-MS Kopplung

GC GC-MS Chromatogram

GC Derivatisierung z Viele polare organische Moleküle sind nicht verflüchtigbar! z Derivatisierung: chemische Modifizierung, die Analyte flüchtig(er) macht und gleichzeitig bei hohen Temperaturen stabilisiert z Häufig Methylierungen (z. B. Trimethylsilyl-Derivate) z Silylierung Übertragung einer TMSi. Gruppe [-Si(CH 3) 3] auf funktionelle Gruppen: - OH - COOH - NH 2 - SH z Silylierung muß im wasserfreien Milleu erfolgen! z Pyridin + BSTFA + TMCS

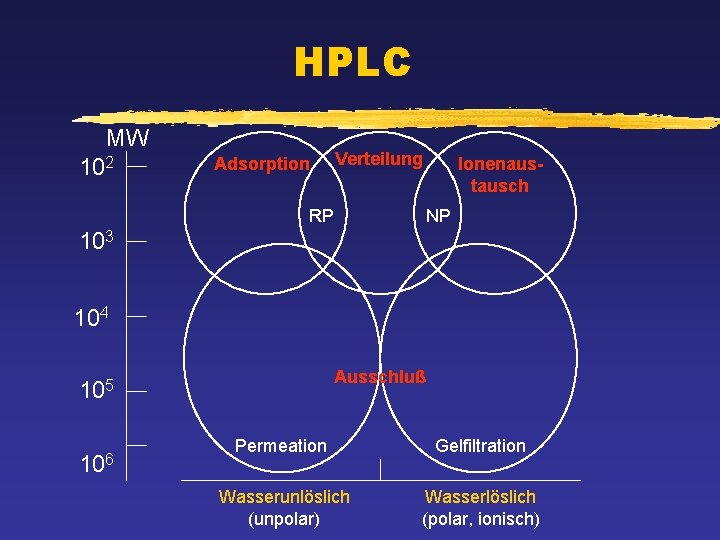
HPLC MW 102 Adsorption Verteilung RP Ionenaustausch NP 103 104 Ausschluß 105 106 Permeation Gelfiltration Wasserunlöslich (unpolar) Wasserlöslich (polar, ionisch)

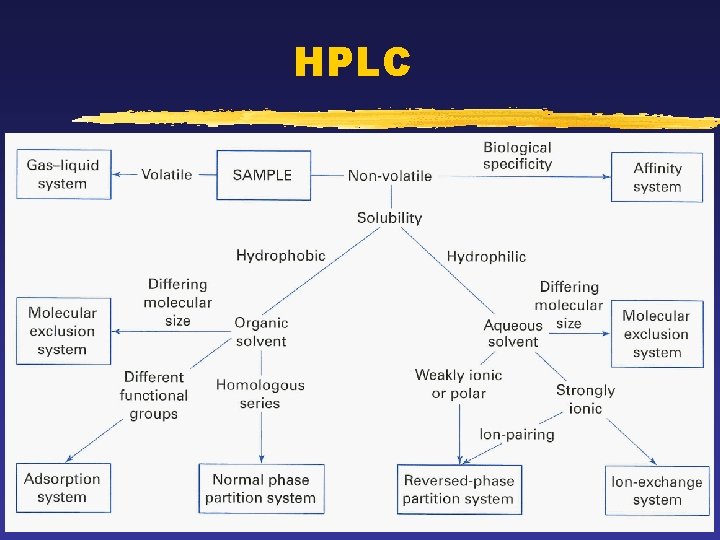
HPLC

HPLC Verteilungschromatographie z Trennung nach POLARITÄT! z (Flüßig-Chromatographie oder) Chromatographie an chemisch gebundenen Phasen Stationäre Phasen: Silikagele (3 -10 µm) modifiziert mit z. B. C 18 (ODS), C 4 -, Aminogruppen Silikagel R ODS

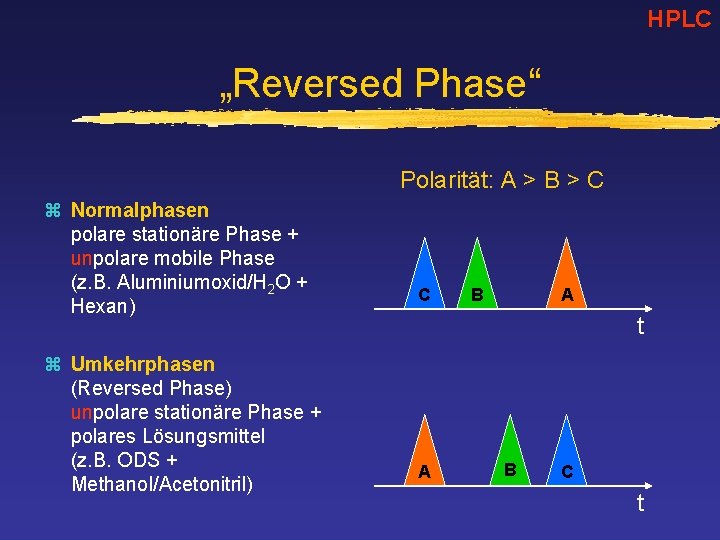
HPLC „Reversed Phase“ Polarität: A > B > C z Normalphasen polare stationäre Phase + unpolare mobile Phase (z. B. Aluminiumoxid/H 2 O + Hexan) z Umkehrphasen (Reversed Phase) unpolare stationäre Phase + polares Lösungsmittel (z. B. ODS + Methanol/Acetonitril) C B A t A B C t

HPLC Adsorptionschromatographie z Kieselgele oder Aluminiumoxide als stationäre Phasen z Zur Trennung kann nur die Polarität der mobilen Phase geändert werden z Als Ergänzung zur Verteilungschromatographie, wenn Substanzen stark unpolar sind (in polaren Lösungsmitteln schwer löslich sind) z Sehr gut für Isomeren-Trennung geeignet

HPLC Ionenchromatographie z Stationäre Phasen sind Ionenaustauscher (meist Kunstharze auf Polystyrenbasis) mit immobilisierten geladenen funktionellen Gruppen: Anionenaustauscher: [ — N(CH 3)3+ OH-] Kationenaustauscher: [ — SO 3 - H+] z Mobile Phasen sind Elektrolyte Niedrigkonzentrierte Salzlösungen, Säuren oder Basen Elution erfolgt entweder durch Erhöhung der Ionenstärke oder durch p. H-Änderung!

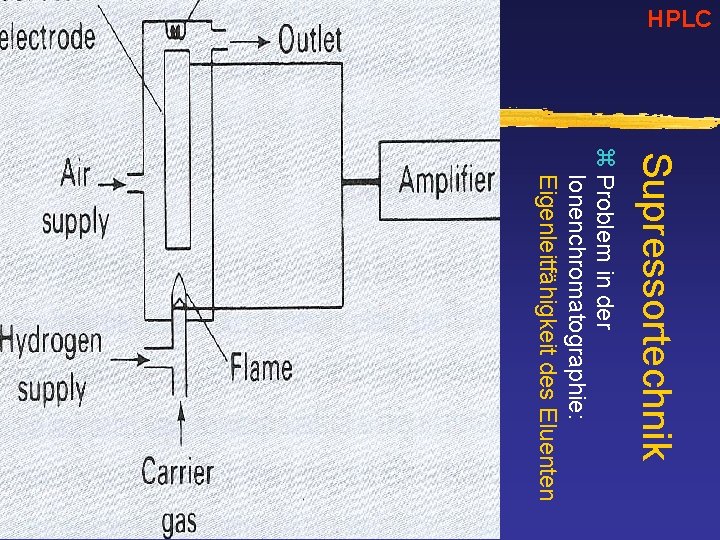
HPLC Supressortechnik z Problem in der Ionenchromatographie: Eigenleitfähigkeit des Eluenten

Anwendungen der Ionenchromatographie HPLC z Auftrennung von organischen und anorganische Ionen (insbesondere von Anionen, für die nur wenige verläßliche Trennmethoden existieren) z Bestimmung von Kohlenhydraten an Anionentauschern (KH sind im alkalischen Millieu geladen!) z Bestimmung von Aminosäuren an Kationentauschern (Aminosäuren sind amphotere Substanzen und im liegen unterhalb von p. H=6 vollständig als Kationen vor) z Wichtige Methode bei der Trennung von Proteinen (AEC an schwachen Anionenaustauschern)

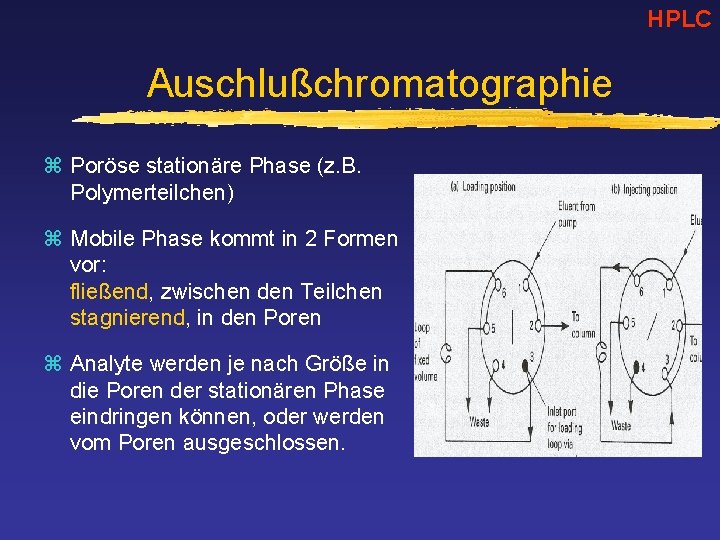
HPLC Auschlußchromatographie z Poröse stationäre Phase (z. B. Polymerteilchen) z Mobile Phase kommt in 2 Formen vor: fließend, zwischen den Teilchen stagnierend, in den Poren z Analyte werden je nach Größe in die Poren der stationären Phase eindringen können, oder werden vom Poren ausgeschlossen.

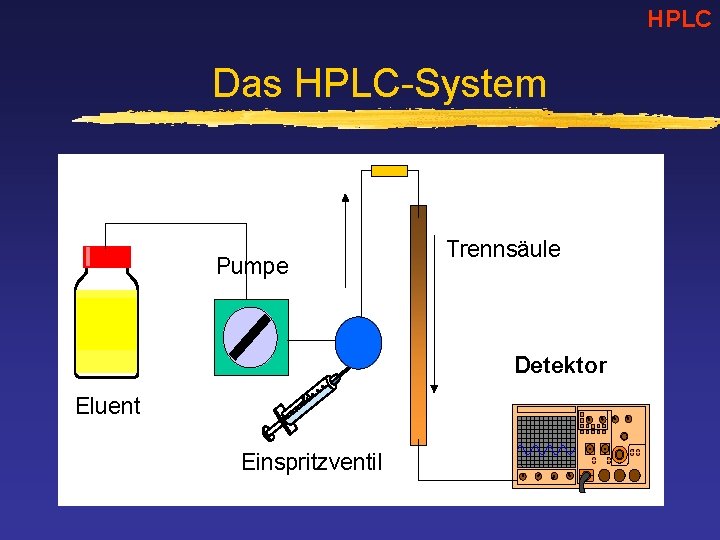
HPLC Das HPLC-System Pumpe Trennsäule Detektor Eluent Einspritzventil

HPLC Injektoren Rheodyne

HPLC Detektoren Nachweisgrenzen z UV-Vis Detektor z Diodenarray-Detektoren z Brechungsindex-Detektor (RI) z Elektrochemischer Detektor (AD, PAD) z Leitfähigkeitsdetektor (CD) z Fluoreszenz-Detektoren z Lichtstreu-Detektor z HPLC-MS Kopplung 1 µg 10 pg 1 ng 10 pg 10 µg 1 ng