Chrom und seine Verbindungen Chrmchen und seine Shnchen

Chrom und seine Verbindungen Chrömchen und seine Söhnchen
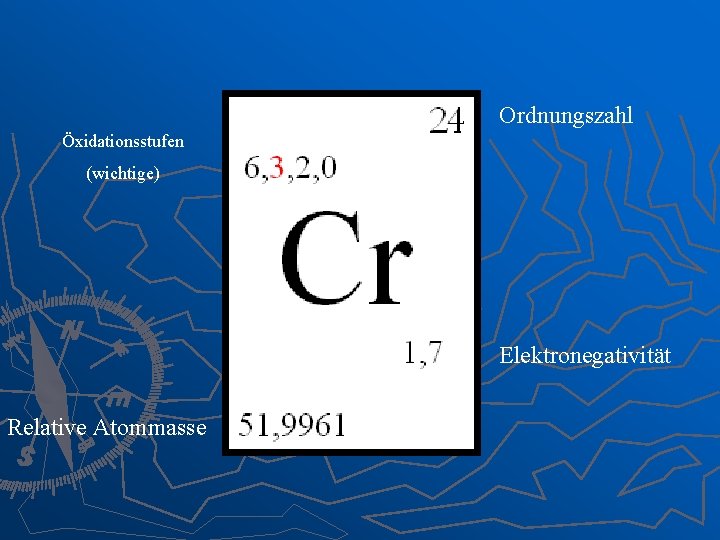
Ordnungszahl Öxidationsstufen (wichtige) Elektronegativität Relative Atommasse

Geschichtliches Das Wort Chrom leitet sich vom griechischen Wort chroma (= Farbe) ab ► 1761 entdeckte Johann Gottlob Lehmann ein orange-rotes Bleichromat-Mineral (Pb. Cr. O 4) im Ural, das er Rotbleierz nannte ► 1770 fand Peter Simon Pallas an gleicher Stelle ein rotes Bleimineral, das wegen seiner Rotfärbung Krokoit (von griech. krokos = safranfarben) genannt wurde ► 1797 entdeckten Martin Heinrich Klaproth und Louis-Nicolas Vauquelin Chrom(III)oxid (Cr 2 O 3) im Krokoit ► 1798 gewann Louis-Nicolas Vauquelin elementares Chrom aus Chrom(III)oxid; dies war jedoch stark mit Carbiden verunreinigt ► 1894 gelang es Hans Goldschmidt reines Chrom zu gewinnen (Goldschmidtverfahren) ►

Peter Simon Pallas Rotbleierz Martin Heinrich Klaproth Louis-Nicolas Vauquelin Hans Goldschmidt

Allgemeines ► Chrom tritt in der Lithosphäre nur in gebundener Form, meist als Chromeisenstein / Chromit (Fe. Cr 2 O 4) ► Physiologisch ist Chrom essentiell für den Menschen (Glucose- und Lipidabbau) ► 3/4 des Weltjahresumsatzes werden für die Herstellung von Ferrochrom verwendet, 1/8 für Feuerwerkskörper und 1/8 für reines Chrom und Verbindungen ► Nuklid, ein künstliches Chromisotop, wird als Tracer in der Medizin verwendet ► Chrom(VI)-Verbindungen sind führen zur Ödemen und gelten als cancerogen sowie mutagen

Vorkommen ► Chrom stellt 0, 02 % der Erdkruste und ist somit sehr häufig ► Dennoch gibt es Lagerstätten und wird hauptsächlich in Südafrika (78%) und Simbawe (19%) abbgebaut ► Neben Chromit und Rotbleierz findet man Chrom als Chrom(III)-oxid oder Chromocker (Cr 2 O 3) Chromit Chromocker
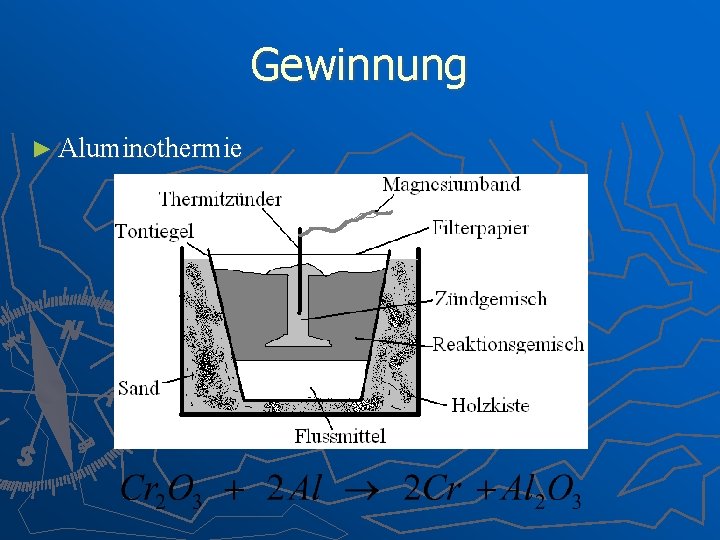
Gewinnung ► Aluminothermie
![Chemische Eigenschaften ► Übergangsmetall ► Elektrische Leitfähigkeit ► Elektronenkonfiguration [Ar] 3 d 5 4 Chemische Eigenschaften ► Übergangsmetall ► Elektrische Leitfähigkeit ► Elektronenkonfiguration [Ar] 3 d 5 4](http://slidetodoc.com/presentation_image_h2/e1c995d318f4fd30f9e78b46a8a73c49/image-8.jpg)
Chemische Eigenschaften ► Übergangsmetall ► Elektrische Leitfähigkeit ► Elektronenkonfiguration [Ar] 3 d 5 4 s 1 (eigentlich: [Ar] 3 d 5 4 s 1 ► Atomradius 129 pm ► Chrom(IV) und (V) – Verbindungen disproportionieren in wässriger Lösung sofort wieder

Physikalische Eigenschaften ► Zwei Modifikationen § α – Chrom: kubisch raumzentriet § β – Chrom: hexagonal dichteste KP ► Silberglänzendes Metall ► rein: gut schmiede- und dehnbar ► mit Sauer- oder Wasserstoff verunreinigt: spröde ► Smp: 1903°C; Sdp: 2640°C ► Bei RT außerordentlich widerstandfähig (oxidiert an feuchter Luft kaum; reagiert nicht mit Halogenen, …) ► Läßt sich „passivieren“
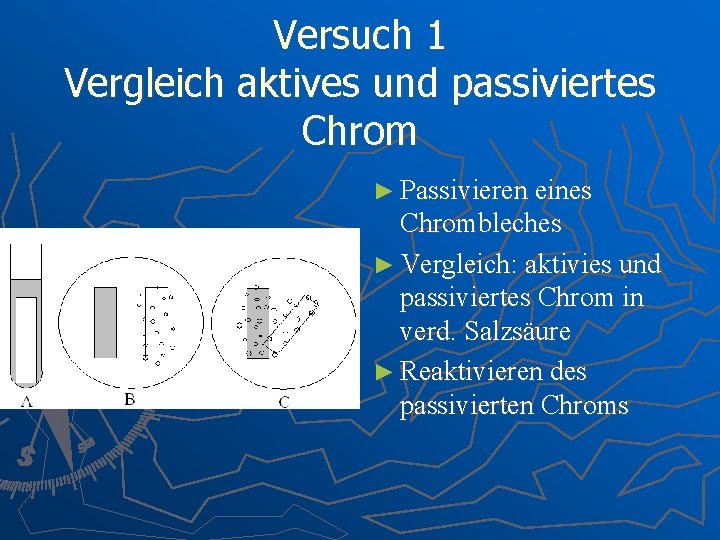
Versuch 1 Vergleich aktives und passiviertes Chrom ► Passivieren eines Chrombleches ► Vergleich: aktivies und passiviertes Chrom in verd. Salzsäure ► Reaktivieren des passivierten Chroms

Reaktionsgleichungen Versuch 1 ► Passivieren Cr + HNO 3 Cr 2 O 3 + ► Reaktion in verd. Sallzsäure ► Reaktivieren des passivierten Chroms Und weiter wie oben!

Auswertung Versuch 1 Die Reaktion des Chroms mit der Salpetersäure führt zu einer sehr dichten Oxidationsschicht die das Chrom innert gegenüber der Säure macht (Passivierung) ► Das unedlere aktive Chrom reagiert mit der verd. Salsäure und wird aufgelöst ► Normalpotentiale ► § Chrom: E° = - 0, 74 V Zwischen Eisen (-0, 44 V) und Zink (-0, 76 V) § Chrom(III)-oxid: E° = + 1, 33 V Zwischen Quecksilber (+0, 86 V) und Gold (+1, 51 V) ► Durch den Elektronenfluß von aktivierten zum passivierten Chrom wird die Oxidationsschicht aufgelöst und somit das Chrom reaktiviert

Verwendung ► Chrom-Eisen-Legierungen werden zur Herstellung von nichtrostenden Stählen verwandt ► Das Chrom hebt des Weiteren die Wärmebeständigkeit des Stahls ► Chromatieren: Korrosionsschutz und Verbesserung der Hafteigenschaften für Lacke aus sauren Chrom(VI)Lösungen (auch mit Chrom(III)-Verbindungen möglich; Lebensmittelindustrie) ► Galvanisches Verchromen

Industrielle Verarbeitung ► Wichtigste Verwendung von Chrom ist der Einsatz als Legierung, dazu benutzt man in der Regel Ferrochrom ► Dieses wir aus Chromit und Eisen(II)-oxid unter Zugabe von Kohle in Siemens-Martin-Öfen durch Reduktion hergestellt ► Der Chromgehalt beträgt normalerweise 52 -75 %

Chrom im Alltag

Toxikologisches ► Ein Mensch sollte jeden Tag 0, 05 -0, 5 mg Chrom aufnehmen und kann bis zu einer Menge von 10 mg an einem Tag ohne bleibende Schäden vertragen (Höchstgrenze) ► Besonders Chrom(VI)-Verbindungen sind gefährlich für den Menschen § Sie verätzen Haut und besonders Schleimhäute und führen dort zu schlecht heilenden Geschwüren § Bei Vergiftungen kommt es zu Magen-Darm-Erkrankungen, Leber- und Nierenschäden § Die roten Blutkörperchen reduzieren diese Verbindungen zu Chrom(III)-Verbindungen, die in den Erythrozyten erhalten bleiben und dort als cancerogen eingestuft werden § Folge: Leukemie

Versuch 2 anodische Oxidation von Chrom ► Ein Chromblech wird in verd. Salpetersäure als Anode einer Elektrolyse geschaltet ► Gegenelektrode ist ein Eisenblech

Auswertung und Reaktionsgleichungen von Versuch 2 ► Die Elektrolyse des Chroms führt zur Bildung einer Chrom(VI)-Verbindung, die sich in dünnen Schlieren von der Anode aus in Lösung geht ► Diese gelbe Chrom(VI)-Verbindung ist das Chromat ► Eine Elektrolyse in Anderer Richtung entspricht einer galvanischen Verchromung 2 - Cr + 4 H 2 O Cr. O 4 + 4 H 2

Versuch 3 Gleichgewicht zwischen Chromat und Dichromat ► Eine Chromatlösung wird verschieden stark angesäuert ► Die schwächer angesäuerte Lösung wird wieder neutralisiert ► Die neutrale Lösung wird basisch gemacht ► In die stark angesäuerte Lösung wird ein Impfkristall gegeben

Auswertung und Reaktionsgleichungen von Versuch 3 ► Das Chromat-Ion ist gelb ► Das Dichromat-Ion ist orange-rot ► Die Reaktion zwischen Chromat und Dichromat ist eine protonenabhängige Gleichgewichtsreaktion ► Schon ab p. H 6 (und höher) liegt das Gleichgewicht vollständig beim Chromat 22 Cr. O 4 + 2 H 3 O+ ↔ 2 Cr 2 O 7 + 3 H 2 O

Auswertung Versuch 3 Teil 2 ► Ab p. H 2 (und darunter) liegt das Gleichgewicht vollständig beim Dichromat ► Die Reaktion verläuft in zwei Schritten 2 - + - 2 - 2 Cr. O 4 + 2 H 3 O ↔ 2 HCr. O 4 + 2 H 2 O ↔ Cr 2 O 7 + 3 H 2 O ► Die Hydrogenchromate lassen sich nicht ungelöst nachweisen ► Sie sind schwach sauer und bilden das eigentliche Gleichgewicht zu den Chromaten und Dichromaten ► Unter Wasserabspaltung bildet sich aus Hydrogenchromaten ein Dichromat
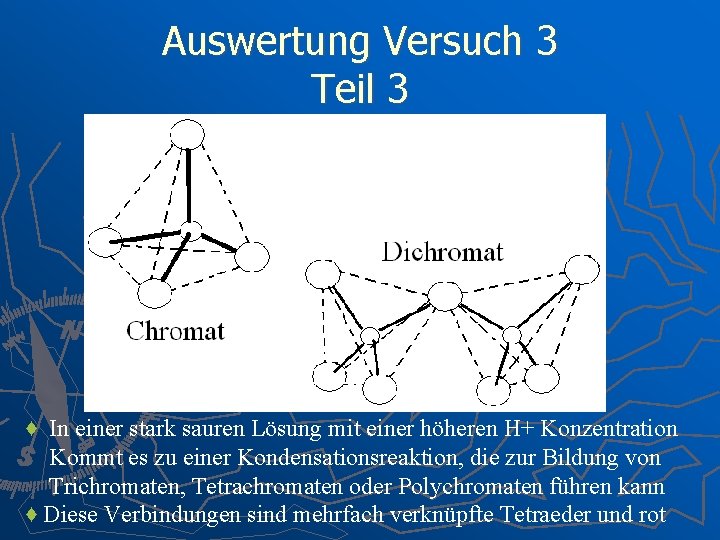
Auswertung Versuch 3 Teil 3 ♦ In einer stark sauren Lösung mit einer höheren H+ Konzentration Kommt es zu einer Kondensationsreaktion, die zur Bildung von Trichromaten, Tetrachromaten oder Polychromaten führen kann ♦ Diese Verbindungen sind mehrfach verknüpfte Tetraeder und rot
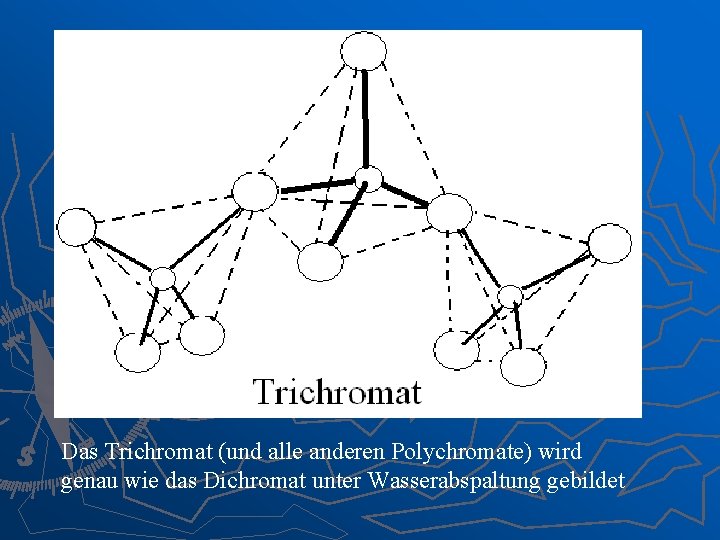
Das Trichromat (und alle anderen Polychromate) wird genau wie das Dichromat unter Wasserabspaltung gebildet

Versuch 4 Reduktion von Chromat

Auswertung Versuch 4 ► Das Ethanol wirkt reduzierend auf das starke Reduktionsmittel Dichromat ► Das Dichromat (Cr(VI)) wird hierbei zu einem Cr(III)Ion reduziert Farbänderung ► Das Ethanol wird zu einem Aldehyd und weiter zur Essigsäure oxidiert ► Bei der Zugabe von Na. OH bildet sich Chromhydroxid und Acetat-Ionen ► Die Acetat-Ionen lassen sich mit Eisen(II)-Ionen nachweisen

Versuch 4 Reaktionsgleichungen I ► Reduktion des Dichromat-Ions in saurer Lösung

Versuch 4 Reaktionsgleichungen II ► Bildung des Chromtrihydroxids grün ► Chromtrihydroxids ist amphoter und bleibt in Lösung tiefgrün

Versuch 4 Reaktionsgleichungen III ► Fällung des Acetat-Ions als Eisen(III)-triacetat rot

Versuch 4 b Reduktion durch thermische Zersetzung Der chemische (oder rauschende) Vulkan

Auswertung Versuch 4 b ► Ammoniumdichromat zersetzt sich zu Chrom(III)-oxid, Stickstoff und Wasser ► Das voluminöse Chromoxid wird durch die entstehenden Gase aufgewirbelt

Farben der Oxidationsstufen Quelle: Hollemann-Wieberg Auswirkungen auf Färbungen in Edelsteinen Smaragd (grün): Cr(III), V(III) Rubin (rot): Cr(III) Amethyst (violett): Cr(III), Ti(IV)

Chrom als Farbstoff ► Chrom diente seid seiner Entdeckung (und schon davor) als Farbpigment ► Viele Chromfarben sind ausschließlich Künstlerfarben ► Die Automobilindustrie verwendet einige Chromlacke ► Grüne und gelbliche Kosmetikprodukte beinhalten häufig Chrom (-Verbindungen)

Evt Versuch 5 Cr-Nachweis in Lidschatten ► Als Oxidationsschmelze ► + Nachweis als Phosphorsalzperle (nur erwähnen und rumgeben)

Versuch 5 Hydratisomerie von Cr(III)

Versuch 5 Auswertung ► Die Hydrationsisomerie ist ein Spezialfall der Ionisations. Isomerie bei Komplexen, bei dem Wasser einmal komplexgebunden und einmal im Kristallwasser vorliegt violett grün Ab einer Temperatur von 43°C bildet sich der grüne Tetraaqua. Komplex aus dem violetten Hexaquakomplex ► Über 70°C liegt das Gleichgewicht vollständig auf der rechten Seite ► Beim Abkühlen bildet sich wieder Hexaquakomplex; die vollständige Umsetzung erfolgt jedoch erst nach einigen Tagen ►

Versuch 6 Lösen vonn Chrom(III)-chlorid

Auswertung Versuch 6 ► Das Chrom(III)-chlorid ist in Wasser unlößlich ► Spuren von Cr(II)-Ionen oder wie im Versuch dargestellten Reduktionsmitteln übertragen Elektronen auf das Cr(III) im Kristallgitter wodurch dieses in Lösung geht und wiederum zu Cr(III) oxidiert da dieses stabiler ist ► Das Zink und HCl Gemisch ist ein starkes Reduktionsmittel (über naszierenden Wasserstoff) und somit für eine schnellere Reaktion geeignet als Cr(II)Ionen

Auswertung Versuch 6 Teil II ► Wird die Lösung länger bei Zimmertemperatur stehengelassen wird sie zunächst hellblaugrün und schließlich violett ► Dies ist wiederum eine Hydrat-Isomerie dunkelgrün hellblaugrün dunkelgrün violett ► Durch Erwärmen lässt sich diese Reaktion wieder umkehren

Schulrelevanz ► Klasse 9 § Elektrolyse & Ionenbegriff ► Klasse 11 § Redoxreaktionen § Kohlenstoffchemie (Alkoholtest) ► Klasse 13 § Chemische Analysen (z. B: Nachweis Chrom in Kosmetika) § Komplexchemie § Chemisches Gleichgewicht ► Fächerübergreifend § Biologie: Umweltschutz (Bsp. : Gärbung mit und ohne Chrom § Kunst: Was steckt in den Farben

Versuch 7 Alkoholteströhrchen ► Vor ca. 20 Jahren waren diese Röhrchen im gängigen Einsatz bei der Polizei

Auswertung Versuch 7 ► In den Alkoholteströhrchen ist schwefelsaures Chromat auf Kieselgel in mehreren Lagen eingeordnet und mit luftdurchlässigem Demmmaterial fixiert ► Befindet sich Alkohol im Atem der Testperson so oxidiert das Chromat und wechselt die Farbe von orange-gelb zu grün

Ledergerbung ► Cr(III)-Ionen haben eine große Tendenz kationische, neutrale und anionische Komplexe zu bilden ► Die meisten Komplexe sind hierbei oktaedrisch und kinetisch sehr stabil ► Bei der Chromgerbung nutzt man dieses um die Kollagene in der Haut zu verknüpfen und die Belastbarkeit des Leders zu erhöhen ► Kollagene besitzen –COOH – Gruppen welche leicht mit Chrom vernetzen lassen ► Dies erhöht die Temperaturunempfindlichkeit und verringert gleichermaßen die Quellbarkeit des Kollagens was zum aushärten des Leders führt
- Slides: 42