Chrom Poloha v periodick tabulce VI B skupina

Chrom
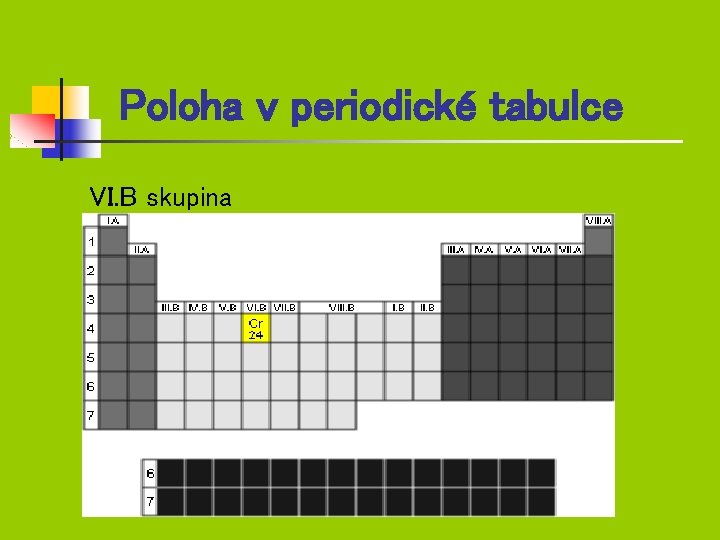
Poloha v periodické tabulce VI. B skupina
![Elektronová konfigurace a možná oxidační čísla n [Cr] Ar: 4 s 2 3 d Elektronová konfigurace a možná oxidační čísla n [Cr] Ar: 4 s 2 3 d](http://slidetodoc.com/presentation_image_h/b4570fdae28b96113c99446ae6b75d5f/image-3.jpg)
Elektronová konfigurace a možná oxidační čísla n [Cr] Ar: 4 s 2 3 d 4 n Oxidační čísla: 0, III, VI

Výskyt n n Zemská kůra, Vesmír V přírodě: současně s rudami Fe -> chromit (Cr 2 O 3. Fe. O) Minerál chromu -> ->krokoit Pb. Cr. O 4 n

Vlastnosti n n Tvrdý, stříbřitě lesklý kov Velmi stálý na vzduchu (na jeho povrchu se vytváří vrstva Cr 2 O 3 – brání další oxidaci) Rozpustný ve zředěných HCl, H 2 SO 4 je pasivován HNO 3

Výroba n a) čistý chrom se vyrábí aluminotermickou redukcí Cr 2 O 3 + 2 Al 2 Cr + Al 2 O 3 n b) redukce chromitu v elektrické peci při 1300°C ferrochrom (70% Cr, 30% Fe)

Využití n n n Metalurgie (výroba legovaných ocelí – korozevzdornost, zlepšení žáruvzdornosti) Výroba geologických vrtných strojů, výkonných nožů pro stříhání kovů Chirurgické nástroje, vodní stroje Potravinářský průmysl Přidává se do mosazi (zvětšuje se tak její tvrdost)

n V každodenním životě: materiál chránící kovové povrchy před korozí, chromování medicínských nástrojů, zlepšení vzhledu -> vybavení koupelen, části luxusních automobilových doplňků apod.

SLOUČENINY - chromnaté n velmi nestálé, snadno se oxidují

SLOUČENINY - chromité Cr 2 O 3 – „chromová zeleň“ n nerozpustný ve vodě, kyselinách ani zásadách n používal se při tisku bankovek § PŘÍPRAVA: 1) (NH 4)2 Cr 2 O 7 N 2 + Cr 2 O 3 + 4 H 2 O 2) Redukce dichromanu draselného sírou Na 2 Cr 2 O 7 + S Cr 2 O 3 + Na 2 SO 4

SLOUČENINY - chromité Cr(OH)3 n šedozelená sraženina n V kyselinách se rozpouští na soli chromité, se zásadami -> poskytuje chromitany § VÝROBA: srážení roztoků solí chromitých amoniakem nebo alkalickými hydroxidy 1) Cr(OH)3 + 3 HCl Cr. Cl 3 + 3 H 2 O 2) Cr(OH)3 + OH- [Cr(OH)4]-

SLOUČENINY - chromité Cr. Cl 3 n Z vodných roztoků krystalyzuje zelený Cr. Cl 3. 6 H 20 § VÝROBA: Cr(OH)3 + 3 HCl Cr. Cl 3 + 3 H 2 O Cr 2(SO 4)3. 18 H 2 O n Fialové krystalky § VÝROBA: Cr(OH)3 + H 2 SO 4

SLOUČENINY - chromité KCr(SO 4)2. 12 H 2 O n Kamenec draselnochromitý n Tmavě fialový § VÝROBA: K 2 Cr 2 O 7 + H 2 SO 4 + 3 SO 2 + 11 H 2 O 2 KCr(SO 4)2. 12 H 2 O Cr 2 S 3 § VÝROBA: suchou cestou – rce Cr a S, protože srážením S 2 - vzniká Cr(OH)3

SLOUČENINY - chromové Cr. O 3 n Červená krystalická látka, silně hygroskopická, vlastnostmi připomíná SO 3 n Silné oxidovadlo (zuhelňuje papír, zapaluje síru) 2 Cr. O 4 + 12 HCl 2 Cr. Cl 3 + 3 Cl 2 + 6 H 2 O § PŘÍPRAVA: K 2 Cr 2 O 7 + H 2 SO 4 konc. K 2 SO 4 + 2 Cr. O 3 + H 2 O

SLOUČENINY - chromové H 2 Cr. O 4 n známá pouze v roztoku, významné jejich soli – chromany (rozpustné, žluté Na 2 Cr. O 4, K 2 Cr. O 4, (NH 4)2 Cr. O 4); působením kyselin vznikají oranžové dichromany 2 Cr(O 2 -)4 + 2 H+ Cr 2(O 2 -)7 + H 2 O n působením alk. hydroxidů vznikají opět chromany Cr 2(O 2 -)7 + 2 OH- 2 Cr(O 2 -)4 + H 2 O

SLOUČENINY - chromové Na 2 Cr. O 4 – hygroskopická látka § PŘÍPRAVA (při 1000°C): 4 Fe. O. Cr 2 O 3 + 8 Na 2 CO 3 + 7 O 2 2 Fe 2 O 3 + 8 Na 2 Cr. O 4 + 8 CO 2 K 2 Cr. O 4 – není hygroskopický § VÝROBA: Na 2 Cr. O 4 + 2 KCl 2 Na. Cl + K 2 Cr. O 4 K 2 Cr 2 O 7 • Použití: odměrný roztok v analytické odměrné analýze (biochromátometrii) § VÝROBA: rce chromanů s kyselinami

Chromany a dichromany - - § jsou silná oxidační činidla: 2 Cr 2(OII-)7 + 16 H 2 O 4 Cr 3+ + 3 O 2 + 8 H 2 O Nerozpustné chromany (většinou žluté – užití: pigmenty) VÝROBA (srážením): Me. II + Cr(OII-)4 Me. Cr. O 4

Přehled barevných pigmentů Ba. Cr. O 4 žlutý ultramarín n Pb. Cr. O 4 chromová žluť n Zn. Cr. O 4 zinková žluť Další nerozpustné chromany n Ag 2 Cr. O 4 (červenohnědý) n Hg 2 Cr. O 4 (hnědý) Rozpustné chromany jsou jedovaté látky; použití: koželužství n

Zajímavosti n n trojmocný chrom je pokládán za převážně prospěšný a je nezbytnou součástí každodenní stravy (lesní plody, pivo…), ale šestimocný chrom působí negativně a je pokládán za potenciální karcinogen Dostatečný obsah chromu v organismu je důležitý pro metabolismus cukrů a tuků, pomáhá udržovat stabilitu krevního tuku, tlumí chuť na sladké potraviny (vhodný ke kontrole tělesné hmotnosti, vhodný ke sportovní stravě – růst svalové hmoty = kulturistika)
- Slides: 19