Chrom Klaudia Laks 1 b L Due Koo

Chrom Klaudia Laks, 1 b. L Duże Koło Chemiczne, Liceum Akademickie w ZS UMK w Toruniu (2012/2013)
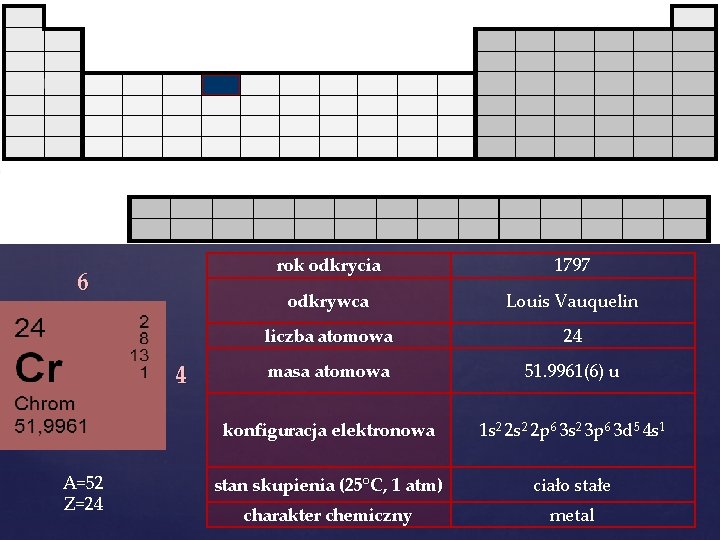
6 4 A=52 Z=24 rok odkrycia 1797 odkrywca Louis Vauquelin liczba atomowa 24 masa atomowa 51. 9961(6) u konfiguracja elektronowa 1 s 2 2 p 6 3 s 2 3 p 6 3 d 5 4 s 1 stan skupienia (25°C, 1 atm) ciało stałe charakter chemiczny metal

WŁAŚCIWOŚCI FIZYCZNE • srebrzystoszary metal (z błękitnym połyskiem w świetle) • właściwości antykorozyjne • znane są dwie odmiany alotropowe chromu. Najpospolitsza - trwała w temperaturze pokojowej - ma strukturę regularną, przestrzennie centrowaną. Druga odmiana, trwała w wysokiej temperaturze ma zwartą strukturę heksagonalną. Chrom stosowany jest jako dodatek do stali i stopów metali, a także do dodatek do stali i stopów metali wytwarzania powłok ochronnych zapobiegających korozji metali. Ma także wytwarzania powłok ochronnych zapobiegających korozji metali zastosowanie do wytwarzania barwników dodawanych do farb, szkła i porcelany. wytwarzania barwników Znaczenie praktyczne ma także stop złożony z chromu i niklu, tzw. chromonikiel, chromonikiel cechujący się dużym oporem elektrycznym (drut oporowy) – używany jest do budowy grzejników elektrycznych. Chrom jest pierwiastkiem występującym w organizmach żywych. Wchodzi w skład wielu enzymów. Jest niezbędny do organizmach żywych prawidłowej gospodarki węglowodanowej, gdyż ma wpływ na działanie insuliny

• chromicie Fe. Cr 2 O 4 • krokoicie Pb. Cr. O 4 • uwarowicie Ca 3 Cr 2(Si. O 4)3 • ochrze chromowej Cr 2 O 3 • chromitycie Fe 2 O 3× 2 Cr 2 O 3. Związki chromu(VI) są toksyczne i rakotwórcze.

• łatwo ulega pasywacji w stężonych kwasach utleniających. • reaguje z kwasem solnym lub tlenowymi rozcieńczonymi: • bez dostępu tlenu – daje sole w których jest dwuwartościowy • z dostępem powietrza daje sole w których jest trójwartościowy • chrom nie utlenia się na powietrzu, dopiero silnie ogrzany ulega utlenieniu. • w temperaturze pokojowej jest odporny na działanie wody, fluorowców, siarki, azotu • na powietrzu reaguje z tlenem - ulega pasywacji i powstaje tlenek chromu(III), który tworzy powłokę ochronną i zabezpiecza postępowaniu korozji na metalu

Właściwości magnetyczne 1 s 2 2 p 6 3 s 2 3 p 6 3 d 5 4 s 1 II stopień utlenienia III stopień utlenienia VI stopień utlenienia 1 s 2 2 p 6 3 s 2 3 p 6 3 d 4 1 s 2 2 p 6 3 s 2 3 p 6 3 d 3 1 s 2 2 p 6 3 s 2 3 p 6 diamagnetyk paramagnetyk diamagnetyk

Ze względu na swoja konfigurację elektronową może występować na stopniach utlenienia od I do VI. Głównie na: II III VI Związki chromu na stopniach utlenienia +1, +4 i +5 są trwałe tylko w stanie stałym, w roztworach wodnych chrom(IV) i (V) ulega dysproporcjonowaniu na chrom (III) i (VI). • • • Cr. O – charakter zasadowy Cr. O Cr 2 O 3 – charakter amfoteryczny Cr. O 3 – charakter kwasowy

II stopień utlenienia • Tlenek chromu (II) Czarny tlenek chromu (II) Cr. O powstaje w wyniku utleniania amalgamatu chromu tlenem atmosferycznym. Ogrzewany w obecności powietrza wiąże tlen i rozżarzając się przechodzi w tlenek chromu (III) Cr 2 O 3. Ma charakter zasadowy. 4 Cr. O +O 2 → 2 Cr 2 O 3 • Sole chromu (II) Są bardzo silnymi reduktorami. Jon Cr 2+ na zimno (w obecności jonów obcych metali jako katalizatorów), a także w czystym roztworze na gorąco, rozkłada wodę z wydzieleniem wodoru: Cr 2+ + H+ = Cr 3+ + 1/2 H 2 Roztwory soli mają najczęściej barwę niebieską. • Wodorotlenek chromu(II) Strąca się w postaci ciemno-brunatnego osadu z roztworu Cr 2+ po dodaniu do niego mocnej zasady. W czasie odwadniania odszczepia wodór i przechodzi w Cr 2 O 3.

III stopień utlenienia • Tlenek chromu(III) (zielony) Tlenek chromu(III) ma charakter amfoteryczny Tlenek chromu (III) • Reaguje z kwasami: • Reaguje z zasadami: • Wodorotlenek chromu(III) (charakter amfoteryczny) • Reakcja z kwasami: Osad Cr(OH)3 rozpuścił się dając zielony roztwór. • Reakcja z zasadami: Osad znika, a ciecz przyjmuje zielone zabarwienie.
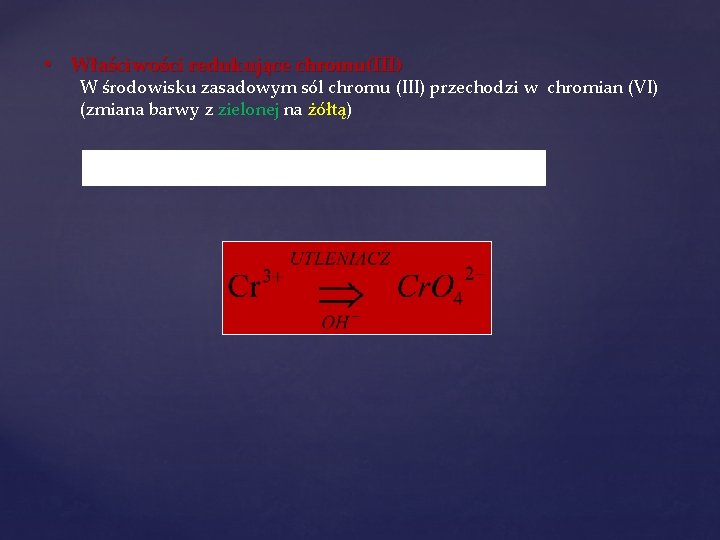
• Właściwości redukujące chromu(III) W środowisku zasadowym sól chromu (III) przechodzi w chromian (VI) (zmiana barwy z zielonej na żółtą)

VI stopień utlenienia Związki chromu(VI) są bardzo silnymi utleniaczami. • Tlenek chromu (VI) • Ma charakter kwasowy. • Dobrze rozpuszcza się w wodzie z wytworzeniem istniejącego tylko w roztworze żółtego kwasu chromowego H 2 Cr. O 4. • W temperaturze pokojowej występuje w postaci ciemnoczerwonych, higroskopijnych kryształów, płatków lub proszku. • Jest silnym utleniaczem np:

• Chromiany(VI) - sole kwasu chromowego(VI) Chromiany(VI) H 2 Cr. O 4. Jon Cr. O 42 - ma żółtą barwę i dlatego wszystkie chromiany są zabarwione na żółto. Rozpuszczalność chromianów jest zbliżona do rozpuszczalności analogicznych siarczanów (sole metali alkalicznych oraz magnezu, wapnia i strontu są łatwo rozpuszczalne w wodzie). Chromian(VI) potasu • Dichromiany(VI) - sole kwasu dichromowego(VI) Dichromiany(VI) H 2 Cr 2 O 7. Po dodaniu do roztworu chromianu jakiegokolwiek kwasu, nawet bardzo słabego, tworzy się dichromian. Charakteryzują się one barwą pomarańczową. Dichromian(VI) potasu Jony chromianowe (VI) powstają w środowisku lekko zasadowym, zaś jony dichromianowe w środowisku kwaśnym.
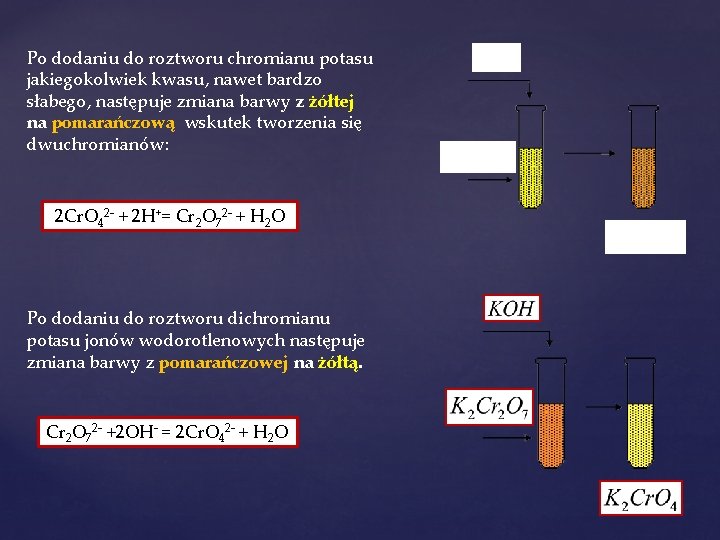
Po dodaniu do roztworu chromianu potasu jakiegokolwiek kwasu, nawet bardzo słabego, następuje zmiana barwy z żółtej na pomarańczową wskutek tworzenia się dwuchromianów: 2 Cr. O 42 - + 2 H+= Cr 2 O 72 - + H 2 O Po dodaniu do roztworu dichromianu potasu jonów wodorotlenowych następuje zmiana barwy z pomarańczowej na żółtą. Cr 2 O 72 - +2 OH- = 2 Cr. O 42 - + H 2 O

II stopień utlenienia III stopień utlenienia VI stopień utlenienia Cr. O czarny Cr 2 O 3 zielony H 2 Cr. O 4 żółty Cr 2+ niebieski Cr(OH)3 zielonoszary Cr. O 3 ciemnoczerwony ciemnobrunatny Cr 3+ zielony Cr. O 42 - żółty H 2 Cr 2 O 7 żołtopomarańczo wy zielony pomarańczo wy
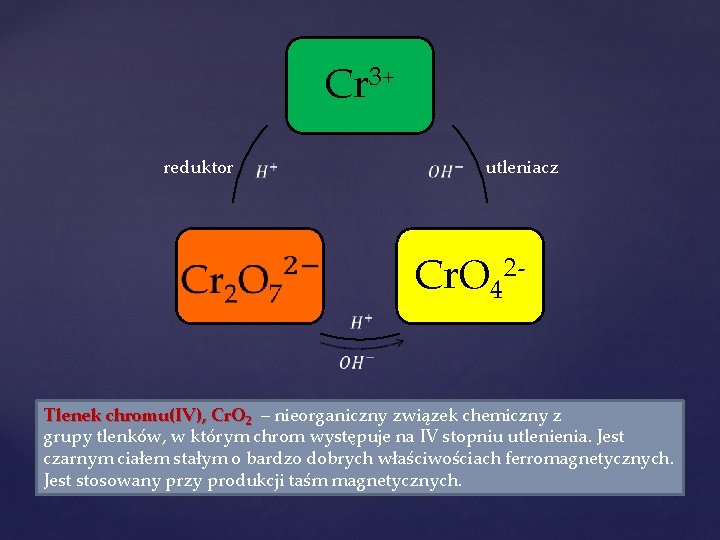
Cr 3+ reduktor utleniacz Cr. O 42 - Tlenek chromu(IV), Cr. O 2 – nieorganiczny związek chemiczny z grupy tlenków, w którym chrom występuje na IV stopniu utlenienia. Jest czarnym ciałem stałym o bardzo dobrych właściwościach ferromagnetycznych. Jest stosowany przy produkcji taśm magnetycznych.

Źródła • Materiały z Platformy Edukacyjnej Portalu www. szkolnictwo. pl – Chrom i jego związki (informacje, równania, schematy) • www. pl. wikipedia. org (zdjęcia)
- Slides: 16