CHO MNG CC EM N VI TIT HC











- Slides: 24

CHÀO MỪNG CÁC EM ĐÃ ĐẾN VỚI TIẾT HỌC HÔM NAY Môn: Hóa học 9 Tuần 22, tiết 42 Bài 29: AXIT CACBONIC VÀ MUỐI CACBONAT GV: Phan Thị Tư Em

Bài 29

I. Axit cacbonic(H 2 CO 3) 1. Tr¹ng th¸i tù nhiªn vµ tÝnh chÊt vËt lÝ: Dùa ho¸ vµohäc: th «ng tin SGK cho biÕt H 2 CO 3 cã ë ®©u? 2. TÝnh(? ) chÊt H 2 CO 3 cã trong n íc tù nhiªn vµ n íc m a Do CO 2 tan ® îc trong n íc t¹o thµnh dung dÞch H 2 CO 3 Tû lÖ VCO 2: VH 2 O = 90 : 1000

KÕt luËn nµo sau ®©y ®óng víi H 2 CO 3 ? A. Axit m¹nh, bÒn nhiÖt. B. Axit m¹nh, kh «ng bÒn. T¹i sao em chän ph ¬ng ¸n ®ã? C. C Axit yÕu, kh «ng bÒn. D. Axit yÕu, bÒn nhiÖt. H 2 CO 3 lµ axit yÕu, dung dÞch H 2 CO 3 lµm quú tÝm hãa ®á nh¹t. H 2 CO 3 kh «ng bÒn, dÔ bÞ ph©n hñy khi t¹o thµnh trong nh÷ng ph¶n øng hãa häc: H 2 CO 3 CO 2 + H 2 O §á nh¹t

I. Axit cacbonic(H 2 CO 3) 1. Tr¹ng th¸i tù nhiªn vµ tÝnh chÊt vËt lÝ: 2. TÝnh chÊt ho¸ häc: H 2 CO 3 lµ axit yÕu, dung dÞch H 2 CO 3 lµm quú tÝm hãa ®á nh¹t. H 2 CO 3 kh «ng bÒn, dÔ bÞ ph©n hñy khi t¹o thµnh trong nh÷ng ph¶n øng hãa häc: H 2 CO 3 CO 2 + II. Muèi cacbonat H 2 O

II. Muèi cacbonat VD: Ca. CO Na 2 CO , Mg. CO 3 1. Ph©n 3, lo¹i : 23 lo¹i Ca(HCO 3)2, Na. HCO 3 , KHCO 3 …. Cacbonat trung hßa VD: Ca. CO 3 , Na 2 CO 3 , Mg. CO 3, … Cacbonat axit lo¹i 3 , KHCO 3 VD: Ca(HCO 3)2 , 2 Na. HCO 2. TÝnh chÊt : Cacbonat trung hßa (Gäi lµ muèi cacbonat kh «ng cßn nguyªn tè H trongthµnh phÇn gèc axit) VD: Ca. CO 3 , Na 2 CO 3 , Mg. CO 3, … Nªu CTHH cña mét sè muèi cacbonat mµ em biÕt? … Cacbonat axit C¸c muèi ®ã ® îc ph©n thµnh (Gäi lµ muèi hi®rocacbonat, cã nguyªn tè H trong thµnh mÊy lo¹i? Dùa vµo ®©u ®Ó phÇn gèc axit) ph©n lo¹ic¸c muèi ®ã? VD: Ca(HCO 3)2 , Na. HCO 3 , KHCO 3 …

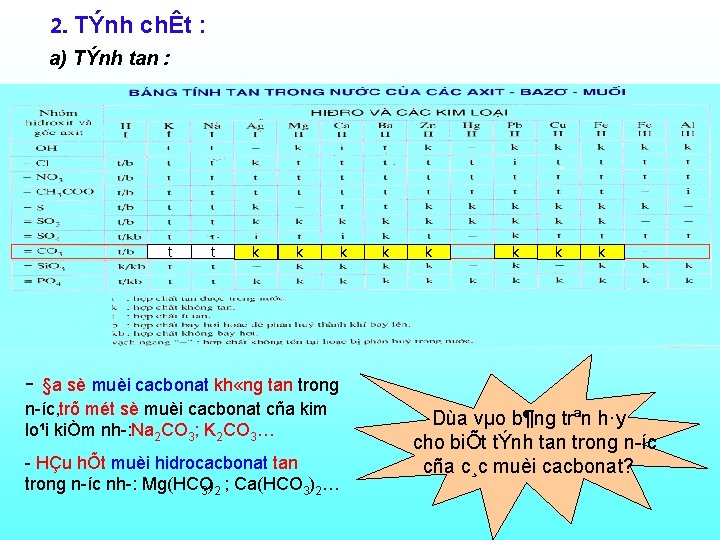
2. TÝnh chÊt : a) TÝnh tan : t t k k k k §a sè muèi cacbonat kh «ng tan trong n íc, trõ mét sè muèi cacbonat cña kim lo¹i kiÒm nh : Na 2 CO 3; K 2 CO 3… HÇu hÕt muèi hidrocacbonat tan trong n íc nh : Mg(HCO 3)2 ; Ca(HCO 3)2… Dùa vµo b¶ng trªn h·y cho biÕt tÝnh tan trong n íc cña c¸c muèi cacbonat?

II. Muèi cacbonat 1. Ph©n lo¹i : 2. TÝnh chÊt : a) TÝnh tan : §a sè muèi cacbonat kh «ng tan trong n íc, trõ mét sè muèi cacbonat cña kim lo¹i kiÒm nh : Na 2 CO 3; K 2 CO 3… HÇu hÕt muèi hidrocacbonat tan trong n íc nh : Mg(HCO 3)2 ; Ca(HCO 3)2…

Muèi cã c¸c tÝnh chÊt ho¸ häc lµ : Muèi + axit(m¹nh h¬n) muèi míi + axit míi §k: s¶n phÈm dd muèi + dd baz¬ muèi míi + baz¬ míi cã chÊt kh «ng tan dd muèi + dd muèi 2 Nªu muèitÝnh míi chÊt ho¸ häc hoÆc chung khÝ bay ra cña muèi ? dd muèi + kim lo¹i muèi míi + kim lo¹i míi ( §iÒu kiÖn: Kim lo¹i ph¶n øng ph¶i tõ Mg trë ®i vµ ho¹t ®éng ho¸ häc m¹nh h¬n kim lo¹i trong muèi) 1 sè muèi bÞ nhiÖt ph©n huû

Dùa vµo tÝnh chÊt ho¸ häc chung cña muèi, h·y dù ®o¸n c¸c tÝnh chÊt ho¸ häc cã thÓ cã cña muèi cacbonat? §Ó kiÓm tra dù ®o¸n cña b¹n chóng ta cïng lµm thÝ nghiÖm ?

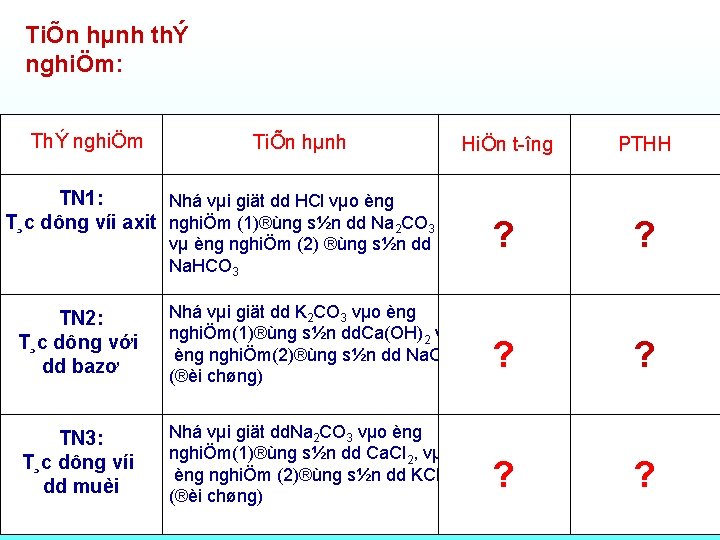
TiÕn hµnh thÝ nghiÖm: ThÝ nghiÖm TiÕn hµnh TN 1: Nhá vµi giät dd HCl vµo èng T¸c dông víi axit nghiÖm (1)®ùng s½n dd Na 2 CO 3 vµ èng nghiÖm (2) ®ùng s½n dd Na. HCO 3 TN 2: T¸c dông với dd bazơ Nhá vµi giät dd K 2 CO 3 vµo èng nghiÖm(1)®ùng s½n dd. Ca(OH)2 vµ èng nghiÖm(2)®ùng s½n dd Na. OH (®èi chøng) TN 3: T¸c dông víi dd muèi Nhá vµi giät dd. Na 2 CO 3 vµo èng nghiÖm(1)®ùng s½n dd Ca. Cl 2, vµ èng nghiÖm (2)®ùng s½n dd KCl (®èi chøng) HiÖn t îng PTHH ? ? ?

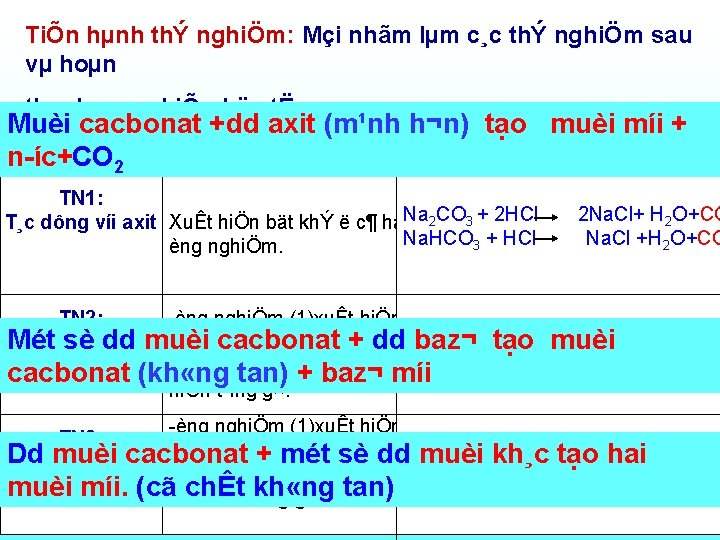
TiÕn hµnh thÝ nghiÖm: Mçi nhãm lµm c¸c thÝ nghiÖm sau vµ hoµn thµnh vµo phiÕu häc tËp: Muèi cacbonat +dd axit (m¹nh h¬n) tạo muèi míi + ThÝ nghiÖm HiÖn t îng PTHH n íc+CO 2 TN 1: T¸c dông víi axit XuÊt hiÖn bät khÝ ë c¶ hai. Na 2 CO 3 + 2 HCl Na. HCO 3 + HCl èng nghiÖm. 2 Na. Cl+ H 2 O+CO Na. Cl +H 2 O+CO TN 2: èng nghiÖm (1)xuÊt hiÖn Mét sè dd cacbonat + dd tạo muèi T¸c dông với muèi vÈn ®ôc hoÆc kÕt tña tr¾ng. Kbaz¬ Ca. CO 3 + 2 KO 2 CO 3 +Ca(OH)2 dd bazơ (kh «ng èng nghiÖm K 2 CO 3 + Na. OH kh «ng ph¶n øn cacbonat tan) (2) + kh «ng baz¬cãmíi hiÖn t îng g×. èng nghiÖm (1)xuÊt hiÖn TN 3: vÈn ®ôc hoÆckÕt tña tr¾ng. Na 2 CO 3 + kh¸c Ca. Cl 2 Dd T¸cmuèi dông víicacbonat + mét sè dd muèi èng nghiÖm (2) kh «ng Na 2 CO 3 + KCl dd muèi míi. (cãcãchÊt kh «ng hiÖn t îng g×. tan) tạo Ca. CO hai 3 + 2 Na kh «ng ph¶n øn

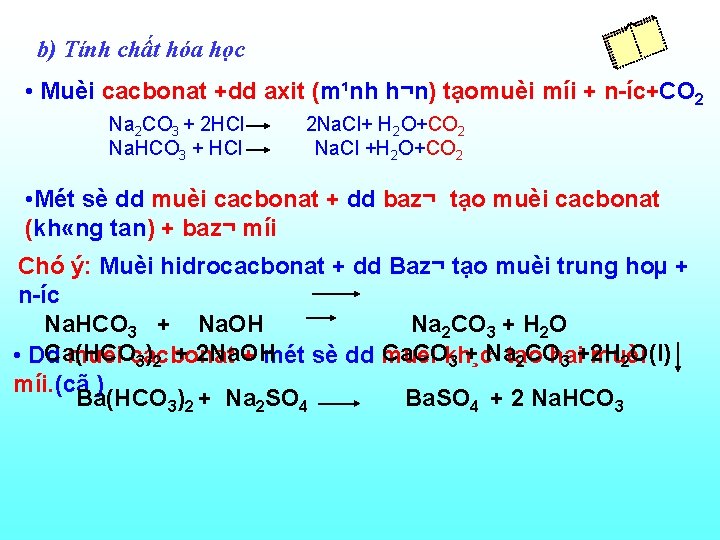
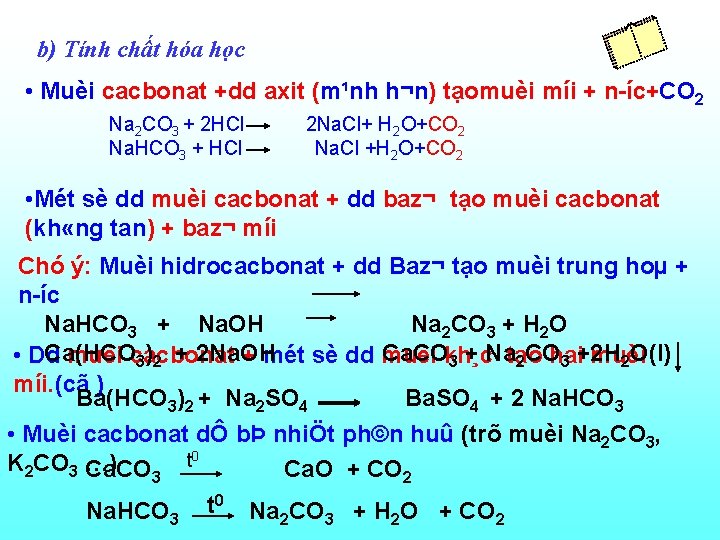
b) Tính chất hóa học • Muèi cacbonat +dd axit (m¹nh h¬n) tạomuèi míi + n íc+CO 2 Na 2 CO 3 + 2 HCl Na. HCO 3 + HCl 2 Na. Cl+ H 2 O+CO 2 Na. Cl +H 2 O+CO 2 • Mét sè dd muèi cacbonat + dd baz¬ tạo muèi cacbonat (kh «ng tan) + baz¬ míi Chó ý: Muèi hidrocacbonat + dd Baz¬ tạo muèi trung hoµ + n íc Na. HCO 3 + Na. OH Na 2 CO 3 + H 2 O Ca(HCO Ca. COkh¸c • Dd muèi cacbonat + mét sè dd muèi tạo hai muèi 3)2 + 2 Na. OH 3 + Na 2 CO 3 +2 H 2 O(l) míi. (cã ) Ba(HCO 3)2 + Na 2 SO 4 Ba. SO 4 + 2 Na. HCO 3

Muèi cacbonat cã t¸c dông ® îc víi kim lo¹i kh «ng ? T¹i sao ? Muèi cacbonat kh «ng t¸c dông ® îc víi kim lo¹i v× kh «ng tho¶ m·n ®iÒu kiÖn cña ph¶n øng.

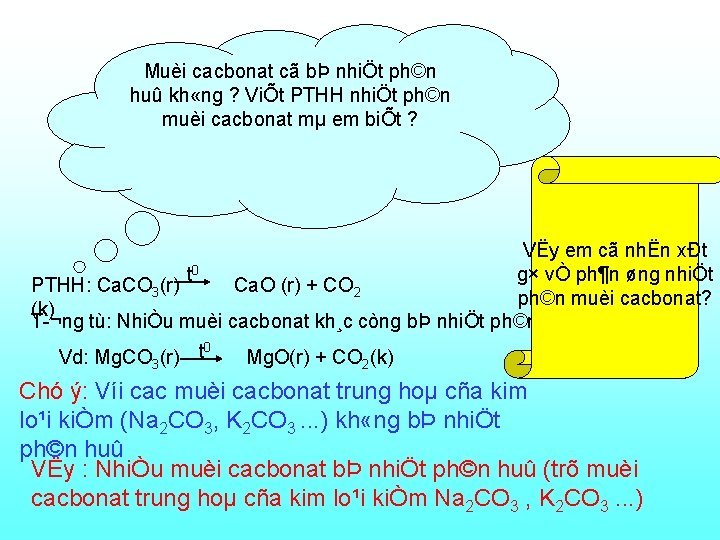
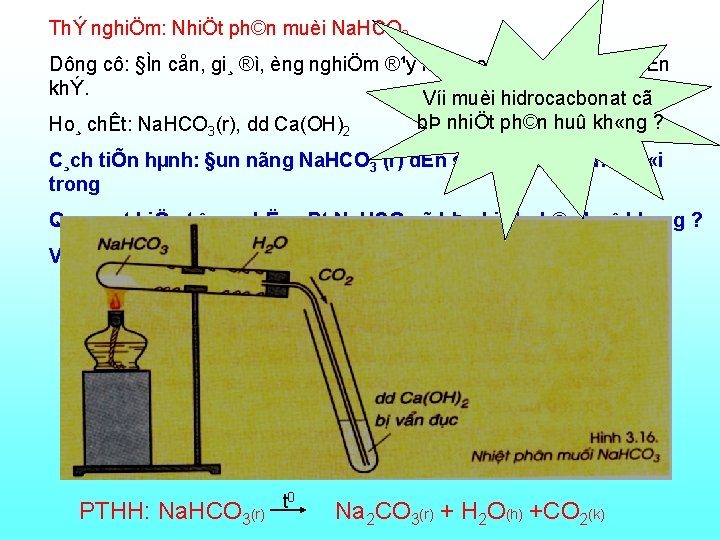
Muèi cacbonat cã bÞ nhiÖt ph©n huû kh «ng ? ViÕt PTHH nhiÖt ph©n muèi cacbonat mµ em biÕt ? VËy em cã nhËn xÐt t 0 g× vÒ ph¶n øng nhiÖt PTHH: Ca. CO 3(r) Ca. O (r) + CO 2 ph©n muèi cacbonat? (k) T ¬ng tù: NhiÒu muèi cacbonat kh¸c còng bÞ nhiÖt ph©n huû: 0 Vd: Mg. CO (r) t Mg. O(r) + CO (k) 3 2 Chó ý: Víi cac muèi cacbonat trung hoµ cña kim lo¹i kiÒm (Na 2 CO 3, K 2 CO 3. . . ) kh «ng bÞ nhiÖt ph©n huû VËy : NhiÒu muèi cacbonat bÞ nhiÖt ph©n huû (trõ muèi cacbonat trung hoµ cña kim lo¹i kiÒm Na 2 CO 3 , K 2 CO 3. . . )

ThÝ nghiÖm: NhiÖt ph©n muèi Na. HCO 3 Dông cô: §Ìn cån, gi¸ ®ì, èng nghiÖm ®¹y nót cao su cã chøa èng dÉn khÝ. Víi muèi hidrocacbonat cã Ho¸ chÊt: Na. HCO 3(r), dd Ca(OH)2 bÞ nhiÖt ph©n huû kh «ng ? C¸ch tiÕn hµnh: §un nãng Na. HCO 3 (r) dÉn s¶n phÈm qua n íc v «i trong Quan s¸t hiÖn t îng, nhËn xÐt Na. HCO 3 cã bÞ nhiÖt ph©n huû kh «ng ? ViÕt PTHH ? PTHH: Na. HCO 3(r) t 0 Na 2 CO 3(r) + H 2 O(h) +CO 2(k)

b) Tính chất hóa học • Muèi cacbonat +dd axit (m¹nh h¬n) tạomuèi míi + n íc+CO 2 Na 2 CO 3 + 2 HCl Na. HCO 3 + HCl 2 Na. Cl+ H 2 O+CO 2 Na. Cl +H 2 O+CO 2 • Mét sè dd muèi cacbonat + dd baz¬ tạo muèi cacbonat (kh «ng tan) + baz¬ míi Chó ý: Muèi hidrocacbonat + dd Baz¬ tạo muèi trung hoµ + n íc Na. HCO 3 + Na. OH Na 2 CO 3 + H 2 O Ca(HCO Ca. COkh¸c • Dd muèi cacbonat + mét sè dd muèi tạo hai muèi 3)2 + 2 Na. OH 3 + Na 2 CO 3 +2 H 2 O(l) míi. (cã ) Ba(HCO 3)2 + Na 2 SO 4 Ba. SO 4 + 2 Na. HCO 3 • Muèi cacbonat dÔ bÞ nhiÖt ph©n huû (trõ muèi Na 2 CO 3, 0 t K 2 CO 3 …) Ca. CO 3 Ca. O + CO 2 0 Na. HCO 3 t Na 2 CO 3 + H 2 O + CO 2

PTHH : Ca. CO 3 + H 2 O + CO 2 Ca(HCO 3)2 th¹ch nhò trong c¸c hang ®éng

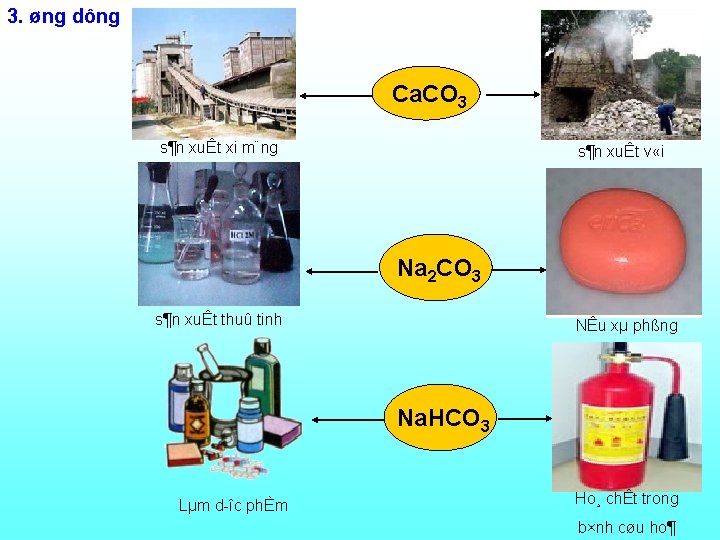
3. øng dông Ca. CO 3 s¶n xuÊt xi m¨ng s¶n xuÊt v «i Na 2 CO 3 s¶n xuÊt thuû tinh NÊu xµ phßng Na. HCO 3 Lµm d îc phÈm Ho¸ chÊt trong b×nh cøu ho¶

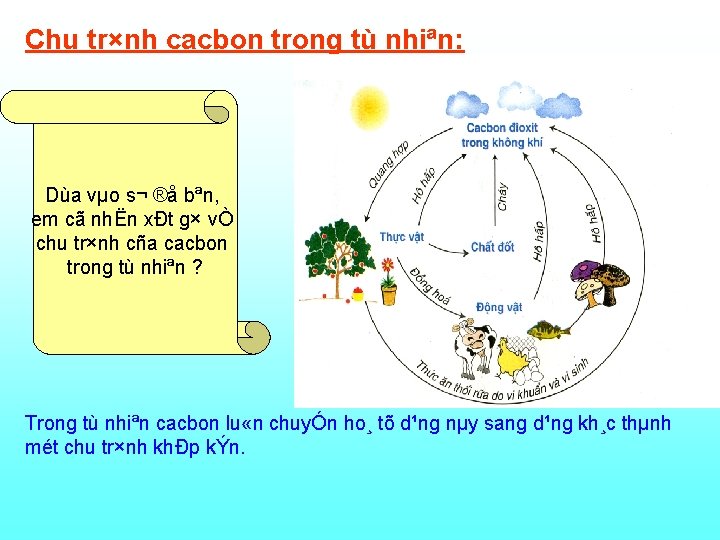
Chu tr×nh cacbon trong tù nhiªn: Dùa vµo s¬ ®å bªn, em cã nhËn xÐt g× vÒ chu tr×nh cña cacbon trong tù nhiªn ? Trong tù nhiªn cacbon lu «n chuyÓn ho¸ tõ d¹ng nµy sang d¹ng kh¸c thµnh mét chu tr×nh khÐp kÝn.

TiÕt 37: Axit cacbonic vµ muèi cacbonat I. Axit cacbonic (H 2 CO 3): 1. Tr¹ng th¸i tù nhiªn vµ tÝnh chÊt vËt lÝ: Axit yếu: 2. TÝnh chÊt ho¸ häc: H 2 CO 3 lµ Axit kém bền II. Muèi cacbonat: Muối cacbonat 1. Ph©n lo¹i: Cã 2 lo¹i Muối hiđrocacbonat 2. TÝnh chÊt : a) TÝnh tan: b) TÝnh chÊt ho¸ häc: 3. øng dông: (SGK trang 90) III: Chu tr×nh cacbon trong tù nhiªn: Trong tù nhiªn cacbon lu «n chuyÓn ho¸ tõ d¹ng nµy sang d¹ng kh¸c thµnh mé chu tr×nh khÐp kÝn.

Bµi tËp cñng cè H·y chän ph ¬ng ¸n ®óng Muèi nµo sau ®©y ®ù «c dïng lµm d îc phÈm lµ thuèc ch÷a bÖnh ®au d¹ dµy: C A. Ca. CO 3 B. Na 2 CO 3 C. Na. HCO 3 D. Bµi Na. Cl 4 (sgk/91) (Trß ch¬i ai nhanh h¬n ) H·y cho biÕt trong c¸c cÆp chÊt sau ®©y, cÆp nµo cã thÓ t¸c dông víi nhau? a) H 2 SO 4 vµ KHCO 3 ; d) Ca. Cl 2 vµ Na 2 CO 3 ; b) K 2 CO 3 vµ Na. Cl ; e) Ba(OH)2 vµ K 2 CO 3. c) Mg. CO 3 vµ HCl ; * C¸c cÆp chÊt cã thÓ t¸c dông víi nhau lµ: a, c, d, e. V× s¶n phÈm cña ph¶n øng cã chÊt khÝ hoÆc chÊt kh «ng tan. * Ph ¬ng tr×nh hãa häc: a) H 2 SO 4 + 2 KHCO 3 K 2 SO 4 + 2 CO 2 + 2 H 2 O c) Mg. CO 3 + 2 HCl Mg. Cl 2 + CO 2 + H 2 O d) Ca. Cl 2 + Na 2 CO 3 Ca. CO 3 + 2 Na. Cl e) Ba(OH)2 + K 2 CO 3 Ba. CO 3 + 2 KOH

H íng dÉn vÒ nhµ Bµi 5 (sgk/91) * ViÕt ph ¬ng tr×nh hãa häc: 2 Na. HCO 3 + H 2 SO 4 Na 2 SO 4 + 2 H 2 O + 2 CO 2 * Theo bµi ra: Sè mol cña dd H 2 SO 4 lµ: n = m/M = 980/98 = 10 (mol) mµ dd H 2 SO 4 ph¶n øng hÕt TÝnh theo sè mol H 2 SO 4. * Theo PTHH: n. CO 2 = 2 n. H 2 SO 4 = 2 x 10 = 20 (mol) ThÓ tÝch khÝ CO 2 t¹o thµnh (®ktc): V= 20 x 22, 4 = 448(l)

Cảm ơn các em đã theo dõi tiết học Chóc c¸c em häc tËp tèt