CHO MNG CC EM N VI BUI HC

CHÀO MỪNG CÁC EM ĐÃ ĐẾN VỚI BUỔI HỌC HÔM NAY

Tiết 48, 49, 50 CHỦ ĐỀ: HIĐRO (TÍNH CHẤT - ỨNG DỤNG - ĐIỀU CHẾ KHÍ HIĐRO PHẢN ỨNG THẾ)
CHỦ ĐỀ : HIĐRO TÍNH CHẤT ỨNG DỤNG ĐIỀU CHẾ PHẢN ỨNG THẾ

CHỦ ĐỀ: HIĐRO Kí hiệu hóa học: H Nguyên tử khối: 1 Công thức phân tử: H 2 Phân tử khối: 2 I. TÍNH CHẤT 1. Tính chất vật lí Khí hidro là chất khí, không màu, không mùi , không vị, tan rất ít trong nước, nhẹ nhất trong các chất khí. Quan sát lọ chứa hiđro cho biết trang thái , màu sắc. là chất khí, không màu không mùi, không vị Ở 15 o. C , 1 lít nước hoà tan được 20 ml khí Hiđro rất ít tan trong nước. So sánh khối lượng mol của khí H 2 so với khí N 2, CO 2, O 2 , không khí. nhẹ nhất trong các chất khí trên

So sánh TCVL của khí oxi và khí hiđro * Giống nhau: - Đều là chất khí không màu, không mùi, không vị. * Khác nhau: Khí Oxi - Ít tan trong nước - Nặng hơn không khí Khí Hiđro - Rất ít tan trong nước - Nhẹ hơn không khí và là khí nhẹ nhất.

CHỦ ĐỀ: HIĐRO Kí hiệu hóa học: H Nguyên tử khối: 1 Công thức phân tử: H 2 Phân tử khối: 2 I. TÍNH CHẤT 1. Tính chất vật lí Khí hidro là chất khí, không màu, không mùi , không vị, tan rất ít trong nước, nhẹ nhất trong các chất khí. 2. Tính chất hóa học a. Tác dụng với khí oxi 2 H 2 + O 2 2 H 2 O Hỗn hợp H 2 và O 2 là hỗn hợp nổ mạnh, nếu đúng tỉ lệ thể tích là 2: 1 Quan sát thí nghiệm: đốt cháy khí hiđro trong không khí Hiđro cháy trong không khí. (Hình 5. 1 b) - Sản phẩm tạo thành khi đốt cháy khí hiđro là gì? Nước có công thức hóa học là H 2 O

Trả lời câu hỏi: 1. Tại sao hỗn hợp khí H 2 và khí O 2 khi cháy lại gây tiếng nổ? Hỗn hợp khí hiđro và khí oxi là hỗn hợp nổ khí cháy vì hỗn hợp này cháy rất nhanh và tỏa ra rất nhiều nhiệt. Nhiệt này làm cho thể tích hơi nước tạo thành sau phản ứng tăng lên đột ngột nhiều lần do đó làm chấn động mạnh không khí, gây ra tiếng nổ. 2. Nếu đốt cháy dòng khí H 2 ngay ở đầu ống dẫn khí, dù ở trong lọ khí O 2 hay không khí sẽ không gây tiếng nổ mạnh. Vì sao? Vì khí hiđro được đốt cháy khi tiếp xúc với khí oxi mà không tạo thành hỗn hợp nổ hiđro và oxi. 3. Làm thế nào để biết dòng khí H 2 là tinh khiết để có thể đốt cháy dòng khí đó mà không gây ra tiếng nổ mạnh? Thử độ tinh khiết của khí hiđrô.


CHỦ ĐỀ: HIĐRO I. TÍNH CHẤT 1. Tính chất vật lí 2. Tính chất hóa học a. Tác dụng với khí oxi 2 H 2 + O 2 2 H 2 O Hỗn hợp H 2 và O 2 là hỗn hợp nổ mạnh, nếu đúng tỉ lệ thể tích là 2: 1 b. Tác dụng với đồng (II) oxit H 2 + Cu. O H 2 O + Cu (đen) (đỏ) H 2 + Oxit kim loại(Fe 2 O 3, Fe 3 O 4, Hg. O, Pb. O) Kim loai + H 2 O Kết luận: Hidro có tính khử, ở nhiệt độ thích hợp , hidro không những kết hợp được với đơn chất oxi mà còn có thể kết hợp với nguyên tố oxi trong 1 số oxit kim loại. Các phản ứng này đều tỏa nhiều nhiệt Quan sát thí nghiệm: Dẫn khí H 2 qua H 2 trong phản ứng này đóng vai trò là Cu. O đun nóng. Nêu hiện tựơng và viết chất khử, nó đã chiếm lấy O trong Cu. O PTHH để tạo ra nước. Ngoài ra H 2 còn có thể khử một số oxit kim loại khác, như là: Fe 2 O 3, Fe 3 O 4, Hg. O, Pb. O. Ta có thể viết phản ứng tổng quát như thế nào ? Cu. O từ màu đen chuyển thành đỏ (Cu) và nước động lại thành ống nghiệm (H 2 O)

Phương tiện giao thông gây ô nhiễm môi trường Ở Mỹ ô tô được chế tạo sử dụng nguyên liệu khí hiđro


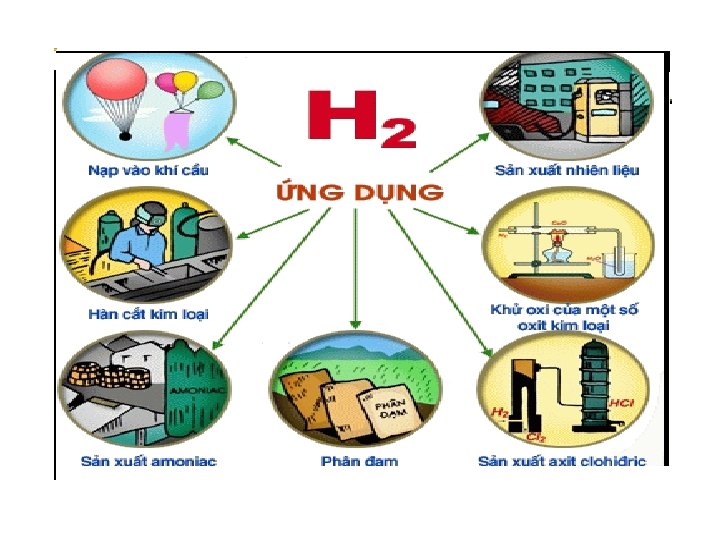
CHỦ ĐỀ: HIĐRO Kí hiệu hóa học: H Nguyên tử khối: 1 Công thức phân tử: H 2 Phân tử khối: 2 I. TÍNH CHẤT 1. Tính chất vật lí 2. Tính chất hóa học II. ỨNG DỤNG Khí hidro có nhiều ứng dụng, chủ yếu do tính chất rất nhẹ , do tính khử và khi cháy tỏa nhiều nhiệt

CHỦ ĐỀ: HIĐRO I. TÍNH CHẤT 1. Tính chất vật lí 2. Tính chất hóa học II. ỨNG DỤNG III. ĐIỀU CHẾ 1. Trong phòng thí nghiệm * Nguyên liệu: Một số kim loại: Zn, Al, Fe Dung dịch: HCl, H 2 SO 4 * Phương pháp: Cho kim loại tác dụng với axit * Phương trình hóa học: Zn + 2 HCl Zn. Cl 2 + H 2 Điều chế khí hiđro. Khí hiđro cháy trong không khí Nguyên liệu để điều chế khí hiđro trong phòng thí nghiệm. Phương pháp điều chế?
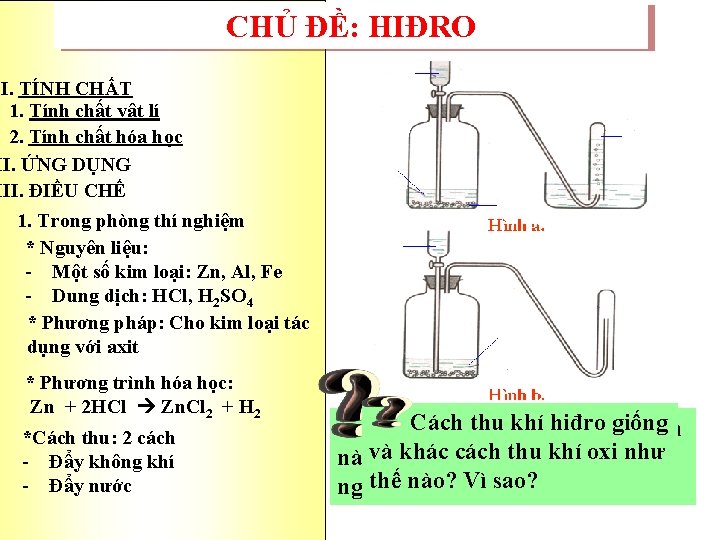
CHỦ ĐỀ: HIĐRO I. TÍNH CHẤT 1. Tính chất vật lí 2. Tính chất hóa học II. ỨNG DỤNG III. ĐIỀU CHẾ 1. Trong phòng thí nghiệm * Nguyên liệu: Một số kim loại: Zn, Al, Fe Dung dịch: HCl, H 2 SO 4 * Phương pháp: Cho kim loại tác dụng với axit * Phương trình hóa học: Zn + 2 HCl Zn. Cl 2 + H 2 *Cách thu: 2 cách Đẩy không khí Đẩy nước khíthu hiđro giống KhíCách hiđrothu được bằng cách khác khíphòng oxi như nàovà khi điềucách chế thu trong thí thế nào? Vì sao? nghiệm.
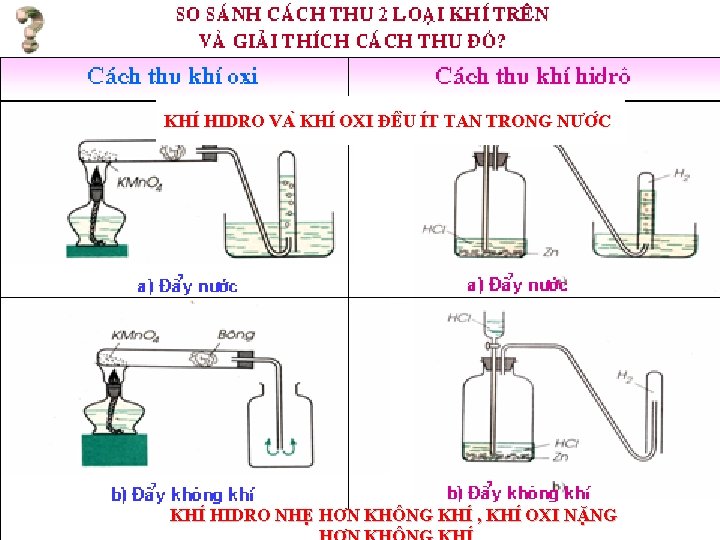
KHI HIDRO VA KHI OXI ĐÊ U I T TAN TRONG NƯƠ C KHI HIDRO NHE HƠN KHÔNG KHI , KHI OXI NĂ NG
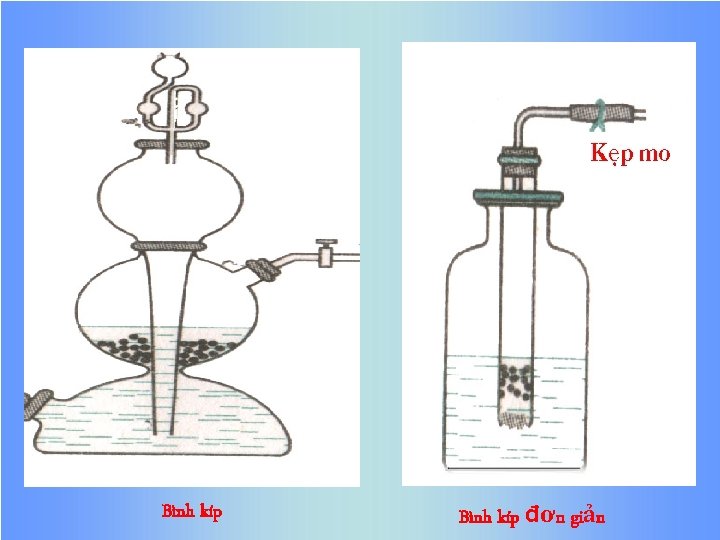
Bình kíp đơn giản

CHỦ ĐỀ: HIĐRO I. TÍNH CHẤT 1. Tính chất vật lí 2. Tính chất hóa học II. ỨNG DỤNG III. ĐIỀU CHẾ 1. Trong phòng thí nghiệm 2. Trong công nghiệp Điện phân nước Từ khí tự nhiên, Bằng điện Dùng than khử hơi nước phân nước Điều chế từ khí tự nhiên, khí dầu mỏ đp Vd: 2 H 2 O 2 H 2 + O 2 Bằng lò khí than Người ta điều chế khí hiđro trong công nghiệp bằng cách nào ?

CHỦ ĐỀ: HIĐRO I. TÍNH CHẤT 1. Tính chất vật lí 2. Tính chất hóa học II. ỨNG DỤNG III. ĐIỀU CHẾ IV. PHẢN ỨNG THẾ Phản ứng thế là phản ứng hóa học giữa đơn chất và hợp chất trong đó nguyên tử của đơn chất thay thế nguyên tử của 1 nguyên tố trong hợp chất VD : Zn + 2 HCl → Zn. Cl 2 + H 2↑ H 2 + Cu. O H 2 O + Cu Fe + Cu. SO 4 → Cu + Fe. SO 4 Trong các phản ứng sau, nguyên tử Zn, Fe đã thay thế nguyên tử nào của axit và Cu. SO 4? Các phản ứng dưới đây có điểm gì giống nhau? a) Zn + 2 HCl → Zn. Cl 2 + H 2 b) Fe + Cu. SO 4 → Fe. SO 4 + Cu Giống nhau: Đơn chất tác dụng hợp chất Nguyên tử đơn chất thay thế nguyên tử của một nguyên tố trong hợp chất

LUYỆN TẬP Câu 1: Viết PTHH cho các phản ứng sau Cho Zn, Fe (II), Al lần lượt tác dụng với axit HCl, H 2 SO 4 loãng Zn + 2 HCl → Zn. Cl 2 + H 2↑ Fe + 2 HCl → Fe. Cl 2 + H 2↑ 2 Al + 6 HCl → 2 Al. Cl 3 + 3 H 2↑ Câu 2: Viết PTHH cho các phản ứng sau Dẫn khí H 2 lần lượt qua các oxit bazo ở nhiệt độ cao như sau: Fe 2 O 3, Fe 3 O 4, Pb. O, Hg. O, Cu. O. 3 H 2 + Fe 2 O 3 2 Fe + 3 H 2 O 4 H 2 + Fe 3 O 4 3 Fe +4 H 2 O H 2 + Pb. O Pb + H 2 O H 2 + Hg. O Hg + H 2 O Câu 3: Cân bằng và cho biết các phản ứng sau thuộc loại phản ứng gì? Fe(OH)2 + H 2 O + O 2 Fe(OH)3 Al + Cu. SO 4 → Al 2(SO 4)3 + Cu KMn. O 4 K 2 Mn. O 4 + Mn. O 2 + O 2 4 Fe(OH)2 + 2 H 2 O + O 2 4 Fe(OH)3 Phản ứng hóa hợp 2 Al + 3 Cu. SO 4 → Al 2(SO 4)3 + 3 Cu Phản ứng thế 2 KMn. O 4 K 2 Mn. O 4 + Mn. O 2 + O 2 Phản ứng phân hủy

LUYỆN TẬP Câu 4: Dẫn 6, 72 lit khí H 2 qua Fe 2 O 3, đun nóng. Tính khối lượng Fe thu được. Giải 3 H 2 + Fe 2 O 3 2 Fe + 3 H 2 O 0, 3 mol 0, 1 mol 0, 2 mol 0, 3 mol Câu 5: Hòa tan 8, 1 gam Al vào dung dịch H 2 SO 4. Hãy tính: a) Khối lượng muối thu được b) Thể tích khí thu được ở đktc Giải 2 Al + 3 H 2 SO 4 → Al 2(SO 4)3 + 3 H 2 0, 3 mol 0, 45 mol 0, 15 mol 0, 45 mol

LUYỆN TẬP Câu 6: Hòa tan 19, 5 gam Zn vào dung dịch HCl thu muối và khí X. Dẫn khí X qua 16 gam Cu. O, đun nóng thu được a (gam) chất rắn. Hãy tính a) a(gam) chất rắn ? b)Xác định chất dư sau phản ứng. Giải Tóm tắt: 19, 5 g. Zn Muối + khí X Khí X + 16 (gam)Cu. O a(gam) rắn a) Tính a là m. Cu ? b) Tính chất dư ? Zn + 2 HCl → Zn. Cl 2 + H 2↑ 0, 3 0, 6 0, 3 H 2 + Cu. O H 2 O + Cu 0, 2 0, 2
- Slides: 22