Chng 7 HIROCACBON THM NGUN HIROCACBON THIN NHIN

Chương 7: HIĐROCACBON THƠM. NGUỒN HIĐROCACBON THIÊN NHIÊN. HỆ THỐNG HÓA VỀ HIĐROCACBON
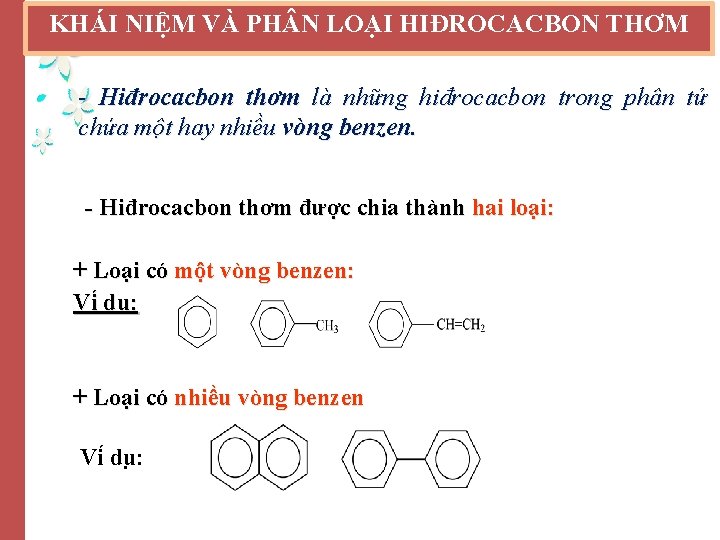
KHÁI NIỆM VÀ PH N LOẠI HIĐROCACBON THƠM - Hiđrocacbon thơm là những hiđrocacbon trong phân tử chứa một hay nhiều vòng benzen. - Hiđrocacbon thơm được chia thành hai loại: + Loại có một vòng benzen: Vi du : + Loại có nhiều vòng benzen Vi du :

TRƯỜNG THPT ĐÔNG HÀ QUẢNG TRỊ BENZEN VÀ ĐỒNG ĐẲNG. MỘT SỐ HIĐROCACBON THƠM KHÁC ( TIẾT 1)
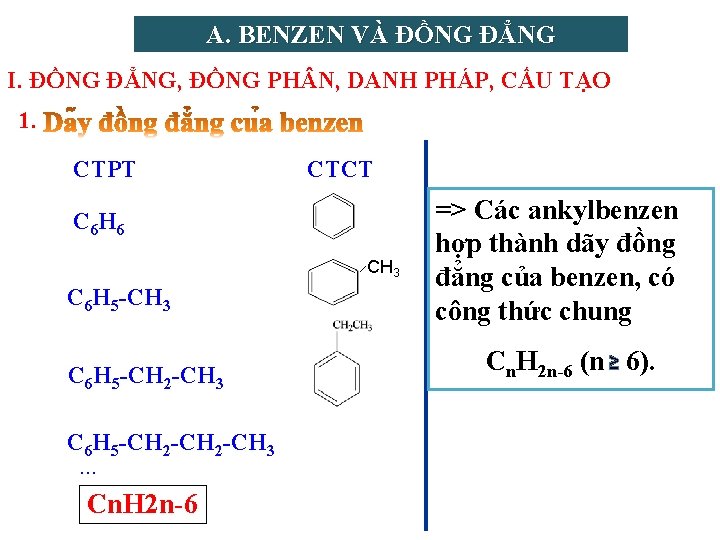
A. BENZEN VÀ ĐỒNG ĐẲNG I. ĐỒNG ĐẲNG, ĐỒNG PH N, DANH PHÁP, CẤU TẠO 1. CTPT CTCT C 6 H 6 CH 3 C 6 H 5 -CH 2 -CH 3 … Cn. H 2 n-6 => Các ankylbenzen hợp thành dãy đồng đẳng của benzen, có công thức chung Cn. H 2 n-6 (n ≥ 6).
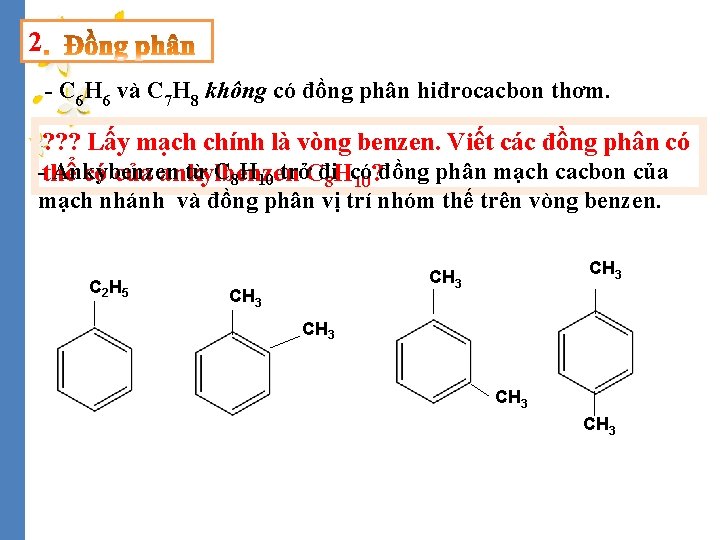
2 - C 6 H 6 và C 7 H 8 không có đồng phân hiđrocacbon thơm. ? ? ? Lấy mạch chính là vòng benzen. Viết các đồng phân có -thể Ankybenzen từ C 8 H 10 trởCđi có của ankylbenzen 8 Hcó 10? đồng phân mạch cacbon của mạch nhánh và đồng phân vị trí nhóm thế trên vòng benzen. C 2 H 5 CH 3 CH 3
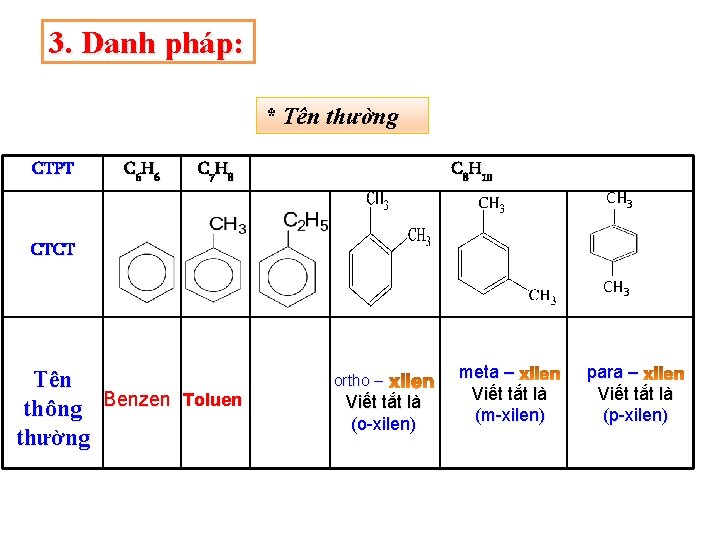
3. Danh pháp: * Tên thường CTPT C 6 H 6 C 7 H 8 C 8 H 10 CH 3 CTCT CH 3 Tên thông Benzen thường Toluen ortho – Viết tắt là (o-xilen) meta – Viết tắt là (m-xilen) para – Viết tắt là (p-xilen)
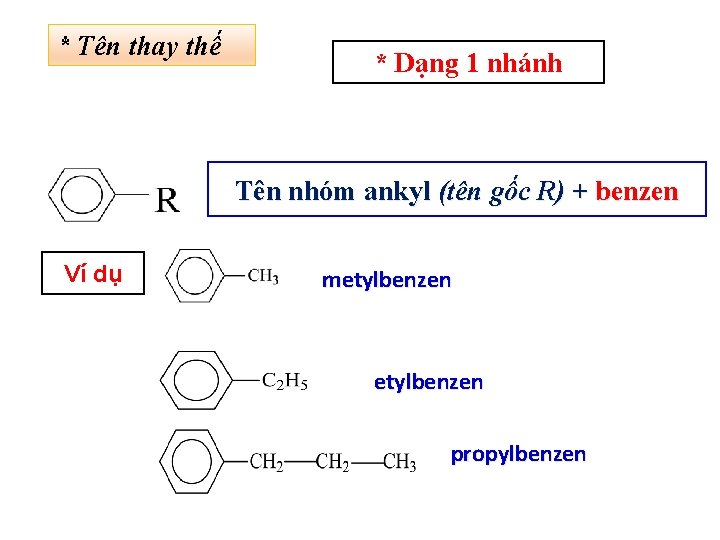
* Tên thay thế * Dạng 1 nhánh Tên nhóm ankyl (tên gốc R) + benzen Ví dụ metylbenzen propylbenzen
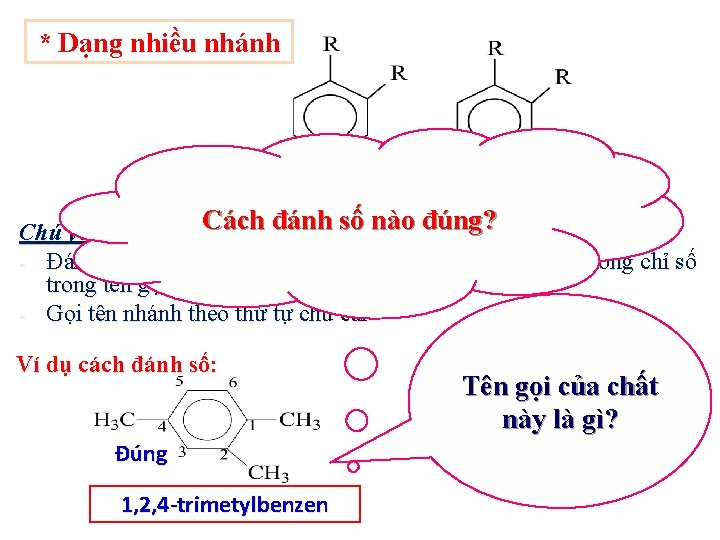
* Dạng nhiều nhánh Số chỉ vị trí nhánh + tên nhóm ankyl + benzen Cách đánh số nào đúng? Chú ý: - Đánh số các nguyên tử cacbon của vòng benzen sao cho tổng chỉ số trong tên gọi là nhỏ nhất. - Gọi tên nhánh theo thứ tự chữ cái Ví dụ cách đánh số: Đúng 1, 2, 4 -trimetylbenzen Tên gọi của chất này là gì? Sai
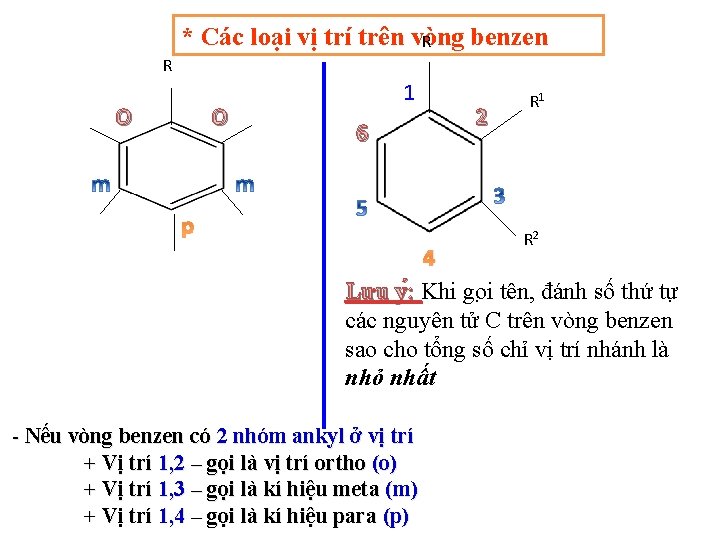
* Các loại vị trí trên vòng benzen R R O O 1 6 p 2 R 1 R 2 4 Lưu y : Khi go i tên, đánh số thứ tự các nguyên tử C trên vòng benzen sao cho tổng số chỉ vị trí nhánh là nhỏ nhất - Nếu vòng benzen có 2 nhóm ankyl ở vị trí + Vị trí 1, 2 – gọi là vị trí ortho (o) + Vị trí 1, 3 – gọi là kí hiệu meta (m) + Vị trí 1, 4 – gọi là kí hiệu para (p)
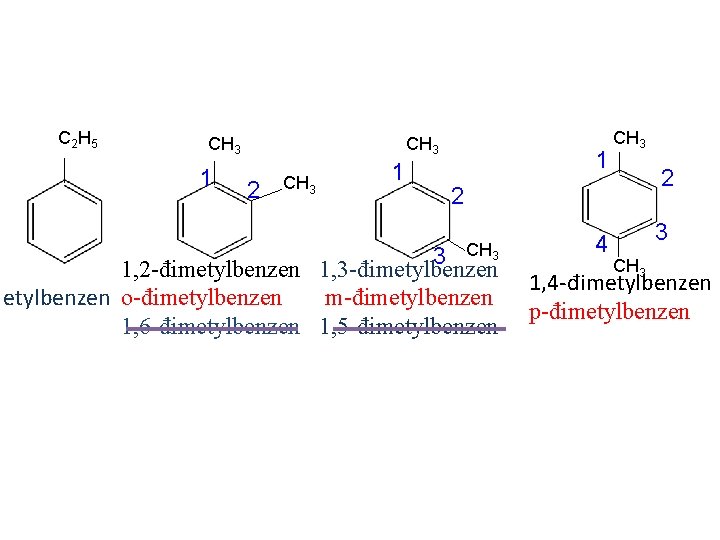
C 2 H 5 CH 3 1 2 CH 3 1 1 CH 3 2 2 3 CH 3 1, 2 -đimetylbenzen 1, 3 -đimetylbenzen o-đimetylbenzen m-đimetylbenzen 1, 6 -đimetylbenzen 1, 5 -đimetylbenzen 4 3 CH 3 1, 4 -đimetylbenzen p-đimetylbenzen
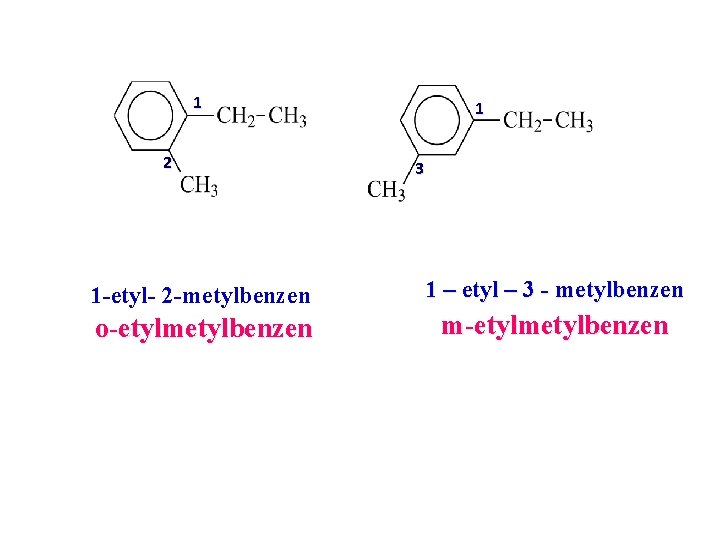
1 2 1 3 1 -etyl- 2 -metylbenzen 1 – etyl – 3 - metylbenzen o-etylmetylbenzen m-etylmetylbenzen
4. Cấu tạo Dạng đặc Dạng rỗng
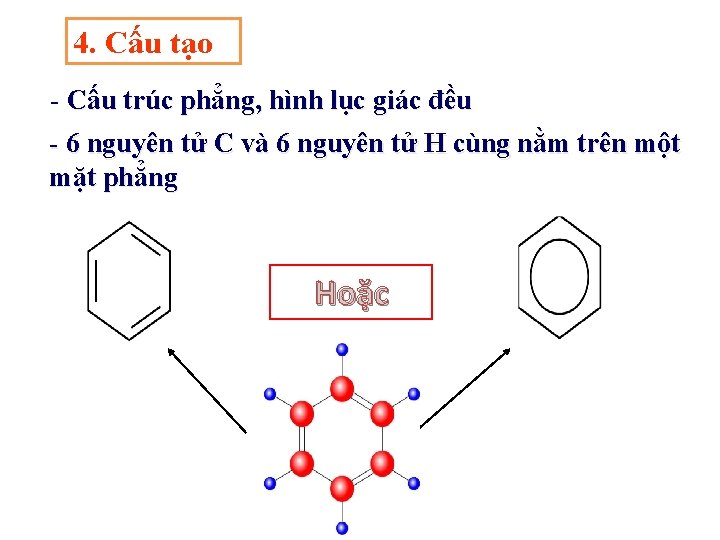
4. Cấu tạo - Cấu trúc phẳng, hình lục giác đều - 6 nguyên tử C và 6 nguyên tử H cùng nằm trên một mặt phẳng Hoặc
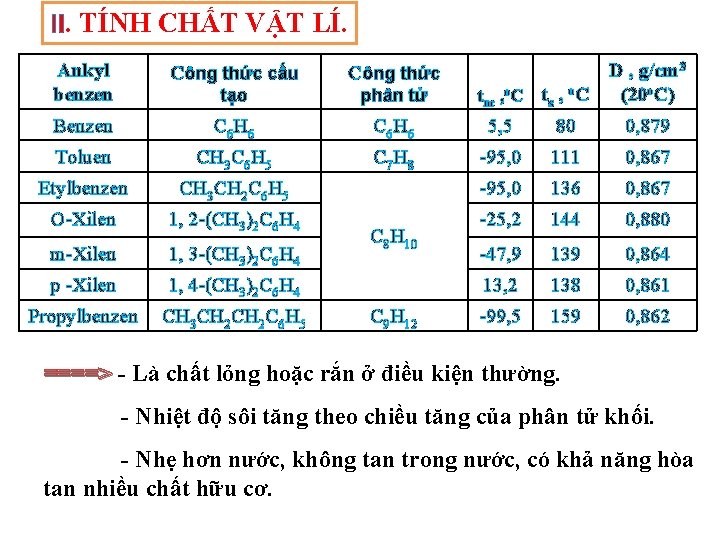
II. TÍNH CHẤT VẬT LÍ. Ankyl benzen Công thức cấu Công thức tạo phân tử Benzen C 6 H 6 5, 5 80 0, 879 Toluen CH 3 C 6 H 5 C 7 H 8 -95, 0 111 0, 867 Etylbenzen CH 3 CH 2 C 6 H 5 -95, 0 136 0, 867 O-Xilen 1, 2 -(CH 3)2 C 6 H 4 -25, 2 144 0, 880 m-Xilen 1, 3 -(CH 3)2 C 6 H 4 -47, 9 139 0, 864 p -Xilen 1, 4 -(CH 3)2 C 6 H 4 13, 2 138 0, 861 Propylbenzen CH 3 CH 2 C 6 H 5 -99, 5 159 0, 862 C 8 H 10 C 9 H 12 D , g/cm 3 (20 o. C) tnc , o. C ts , o. C ====> - Là chất lỏng hoặc rắn ở điều kiện thường. - Nhiệt độ sôi tăng theo chiều tăng của phân tử khối. - Nhẹ hơn nước, không tan trong nước, có khả năng hòa tan nhiều chất hữu cơ.
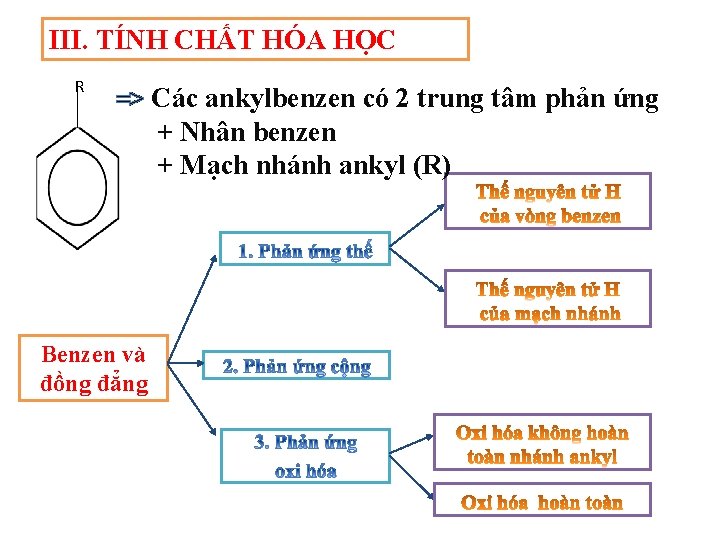
III. TÍNH CHẤT HÓA HỌC R => Các ankylbenzen có 2 trung tâm phản ứng + Nhân benzen + Mạch nhánh ankyl (R) Benzen và đồng đẳng
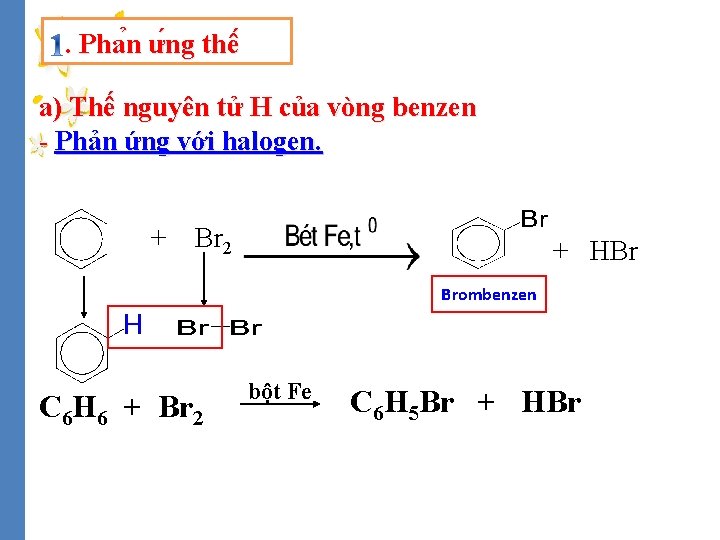
. Pha n ư ng thê a) Thế nguyên tử H của vòng benzen - Phản ứng với halogen. + Br 2 + HBr Brombenzen C 6 H 6 + Br 2 bột Fe C 6 H 5 Br + HBr
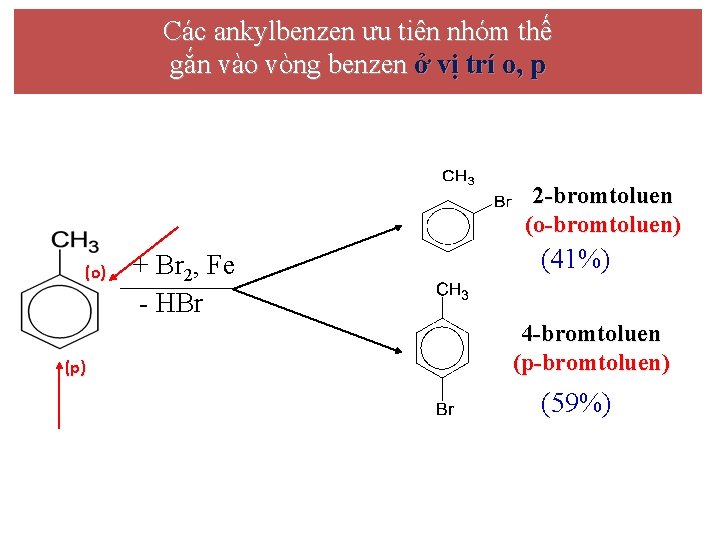
Các ankylbenzen ưu tiên nhóm thế gắn vào vòng benzen ở vị trí o, p 2 -bromtoluen (o-bromtoluen) (o) (p) + Br 2, Fe - HBr (41%) 4 -bromtoluen (p-bromtoluen) (59%)
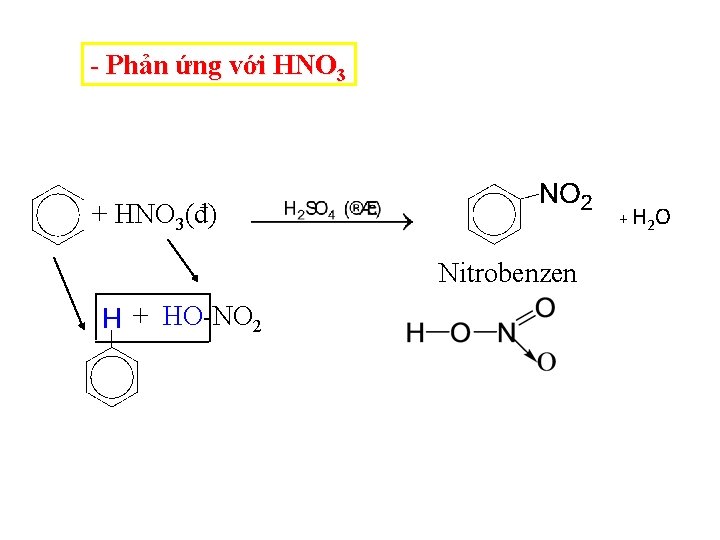
- Phản ứng với HNO 3 + HNO 3(đ) + H 2 O Nitrobenzen + HO-NO 2
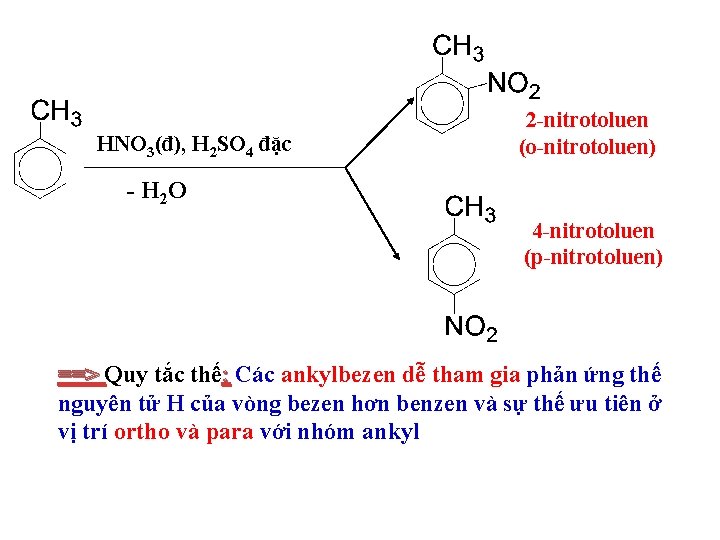
HNO 3(đ), H 2 SO 4 đặc 2 -nitrotoluen (o-nitrotoluen) - H 2 O 4 -nitrotoluen (p-nitrotoluen) ==> Quy tắc thế: Các ankylbezen dễ tham gia phản ứng thế nguyên tử H của vòng bezen hơn benzen và sự thế ưu tiên ở vị trí ortho và para với nhóm ankyl

BÀI TẬP CỦNG CỐ Câu 1: Dãy đồng đẳng của benzen có công thức chung là Câu 2: CH 3 C 6 H 4 C 2 H 5 có tên gọi là A. etylmetylbenzen. B. metylbenzen. C. p-etylmetylbenzen. D. p-metylbenzen. Câu 3: (CH 3)2 CHC 6 H 5 có tên gọi là A. propylbenzen. B. n-propylbenzen. C. iso-propylbenzen. D. đimetylbenzen.
- Slides: 20