Chng 11 C N BNG TRONG DUNG DCH

Chương 11 C N BẰNG TRONG DUNG DỊCH LỎNG Solutions

Khái niệm về hệ phân tán và dung dịch - Hệ phân tán: + Một chất là hạt rất nhỏ được phân bố vào trong chất kia. chất phân tán môi trường phân tán. + Phân loại: üHệ phân tán thô (hệ lơ lửng): d >100 m huyền phù. nhũ tương. üHệ phân tán cao (hệ keo): 1 m < d < 100 m üHệ phân tán phân tử - ion (dung dịch thực): d < 1 m Solutions
SỰ TẠO THÀNH DUNG DỊCH Chất tan Chất phân tán Dung môi Dung dịch Môi trường phân tán Solutions

DUNG DỊCH- là hệ đồng thể bền nhiệt động, gồm không ít hơn hai chất ở trạng thái phân tán phân tử và thành phần có thể biến thiên liên tục trong giới hạn xác định • Dung dịch khí * Không khí • Dung dịch rắn * Thuỷ tinh (Na 2 O, Ca. O tan trong Si. O 2) *Vàng tan trong bạc • Dung dịch lỏng *Dung dịch nước đường(r) +H 2 O dung dịch) *Dung dịch H 2 SO 4(SO 3(k) + H 2 O dung dịch) *Rượu Voka (C 2 H 5 OH (l) + H 2 O dung dịch) Solutions

DUNG DỊCH LỎNG Cơ chế tạo thành dd lỏng Ø Quá trình vật lý – quá trình chuyển pha Hcp , Scp Ø Quá trình hoá học -quá trình solvat hoá tương tác giữa chất tan và dung môi Hsol<0 , Ssol<0 Solvat hoá vật lý Solvat hoá học Tương tác giữa tiểu phân và chất tan là yếu tố hàng đầu quyết định sự tạo thành dd Solutions
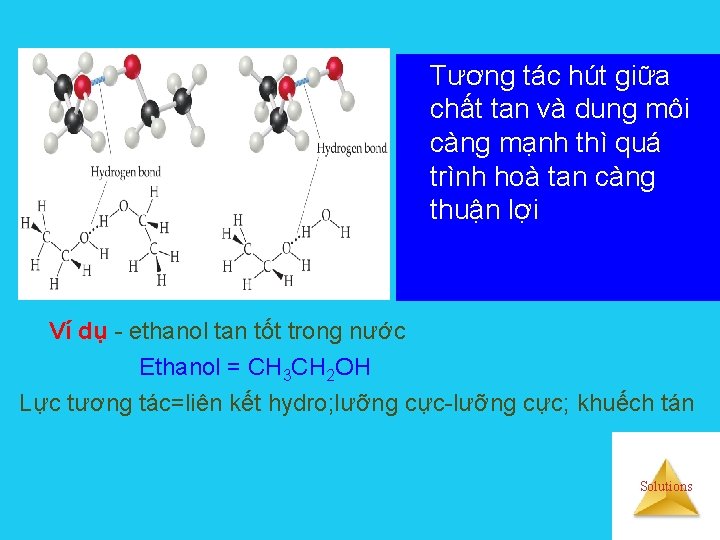
Tương tác hút giữa chất tan và dung môi càng mạnh thì quá trình hoà tan càng thuận lợi Ví dụ - ethanol tan tốt trong nước Ethanol = CH 3 CH 2 OH Lực tương tác=liên kết hydro; lưỡng cực-lưỡng cực; khuếch tán Solutions
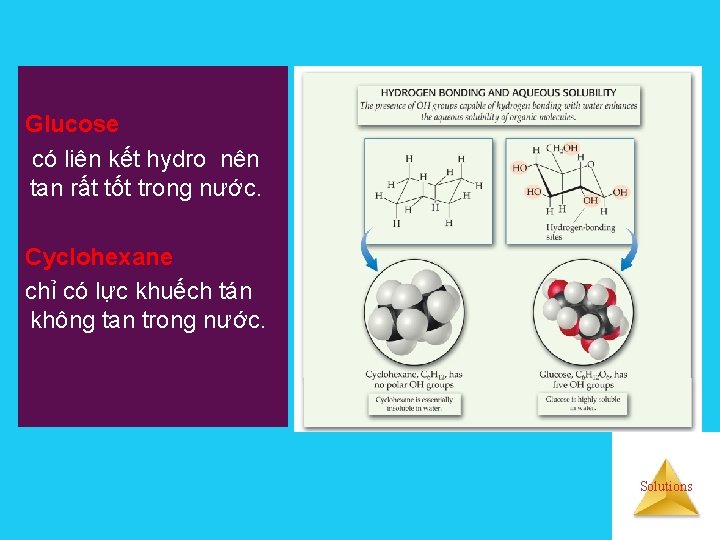
Glucose có liên kết hydro nên tan rất tốt trong nước. Cyclohexane chỉ có lực khuếch tán không tan trong nước. Solutions
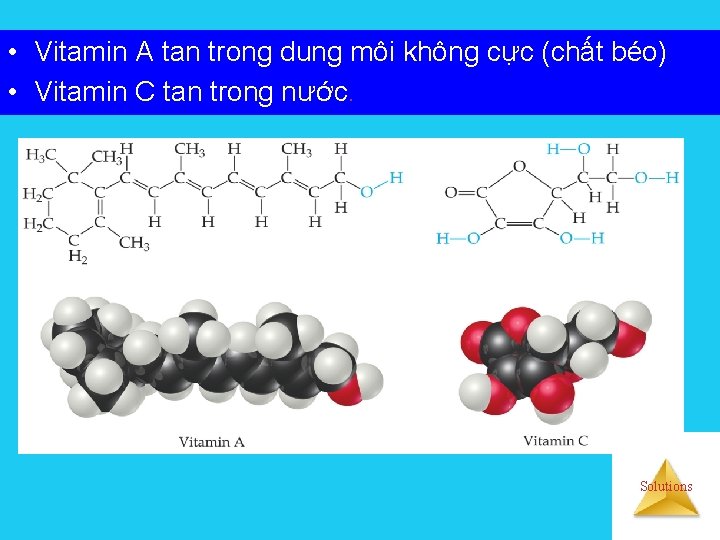
• Vitamin A tan trong dung môi không cực (chất béo) • Vitamin C tan trong nước. Solutions

Vitamin nào tan trong nước và vitamin nào tan trong chất béo? Solutions
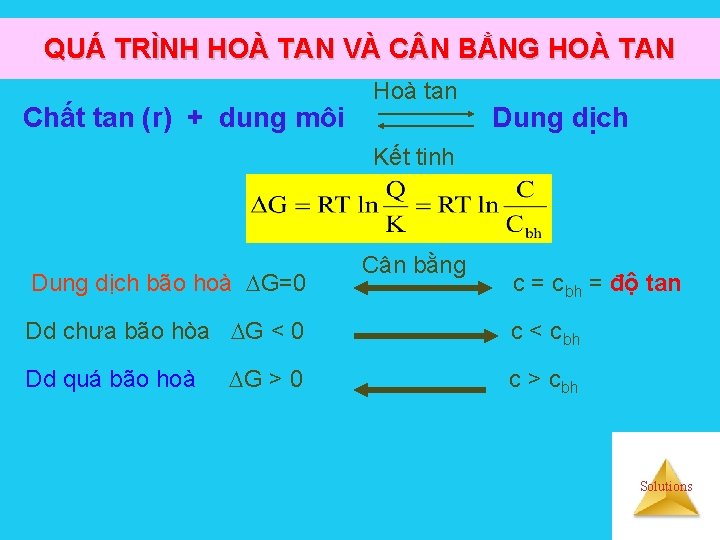
QUÁ TRÌNH HOÀ TAN VÀ C N BẰNG HOÀ TAN Chất tan (r) + dung môi Hoà tan Dung dịch Kết tinh Dung dịch bão hoà G=0 Cân bằng c = c bh = độ tan Dd chưa bão hòa G < 0 c < c bh G > 0 c > c bh Dd quá bão hoà Solutions
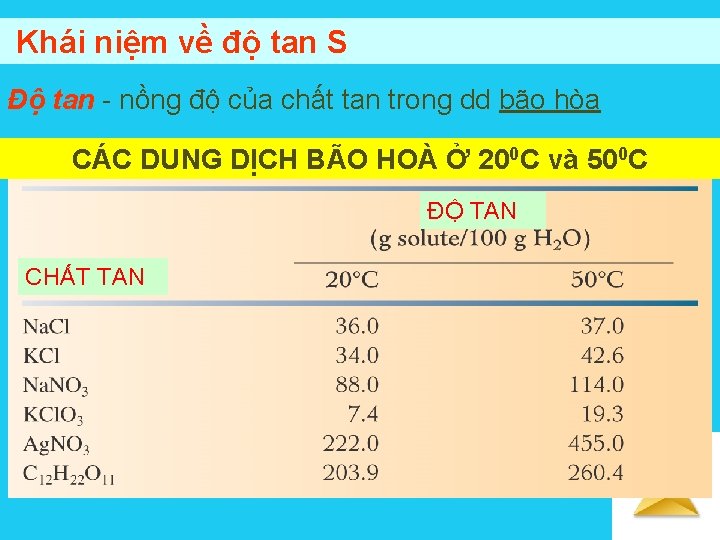
Khái niệm về độ tan S Độ tan - nồng độ của chất tan trong dd bão hòa CÁC DUNG DỊCH BÃO HOÀ Ở 200 C và 500 C ĐỘ TAN CHẤT TAN Solutions

Chất tan là chất rắn S- thường biểu diễn số gam chất tan tối đa trong 100 g dung môi • S > 10 g - chất dễ tan • S < 1 g - chất khó tan • S < 0, 01 g- chất gần như không tan ĐỘ TAN CỦA CÁC HALOGENUA KIM LOẠI KIỀM TRONG H 2 O ĐỘ TAN (số gam muối/100 g dung môi) Solutions

Chất tan là chất khí S- thường biểu diễn bằng số ml khí (tan tối đa) tan trong 100 g dung môi hoặc 100 ml dung môi Chất tan là chất điện ly khó tan S – thường biểu diễn bằng số mol chất điện ly khó tan (tan tối đa) trong 1 lit dung dịch Solutions
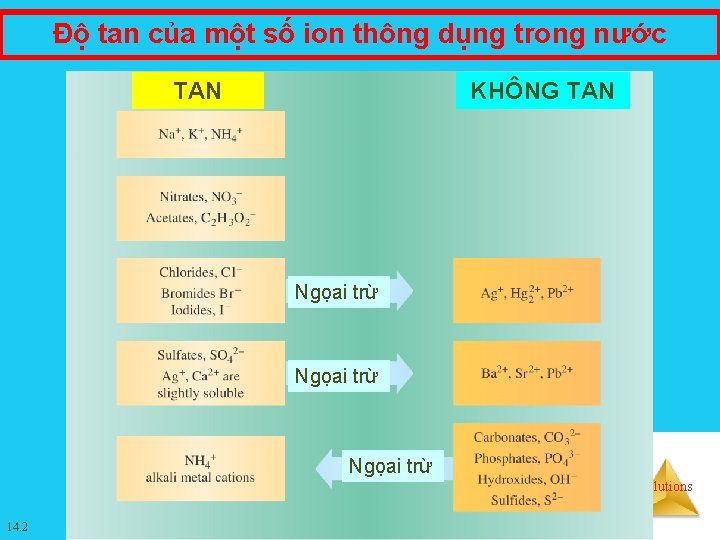
Độ tan của một số ion thông dụng trong nước TAN KHÔNG TAN Ngọai trừ Solutions 14. 2

CÁC YẾU TỐ ẢNH HƯỞNG ĐẾN ĐỘ TAN • Bản chất của dung môi và chất tan • Nhiệt độ, áp suất • Môi trường Solutions

ẢNH HƯỞNG CỦA BẢN CHẤT TAN VÀ DUNG MÔI Chất tương tự tan trong chất tương tự. • Các hợp chất có cực tan tốt trong dung môi có cực hơn là dung môi không cực – Na. Cl thì : • Tan tốt trong nước Độ phân cực của • Tan ít trong ethyl alcohol dung môi • Không tan trong ether và benzene Solutions

• Các chất không cực thì tan tốt trong dung môi không cực hơn là các dung môi có cực. Độ phân cực của dung môi – Benzene thì • Không tan trong nước • Tan trong ether. Solutions
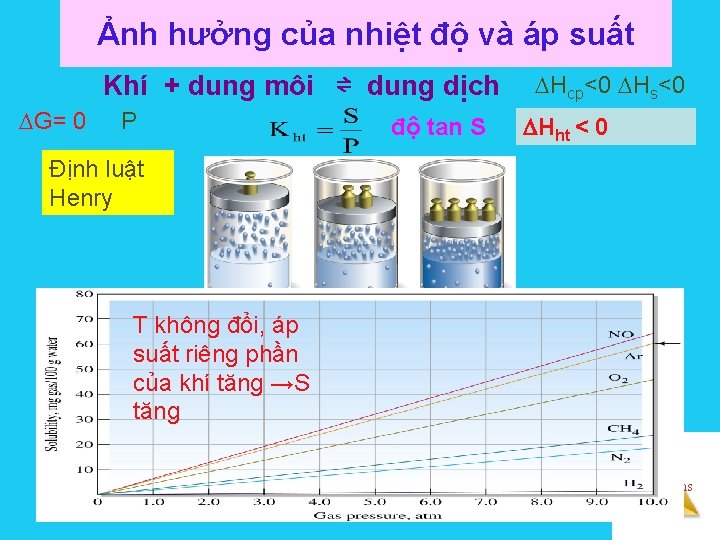
Ảnh hưởng của nhiệt độ và áp suất Khí + dung môi ⇌ dung dịch G= 0 P độ tan S Hcp<0 Hs<0 Hht < 0 Định luật Henry T không đổi, áp suất riêng phần của khí tăng →S tăng Solutions
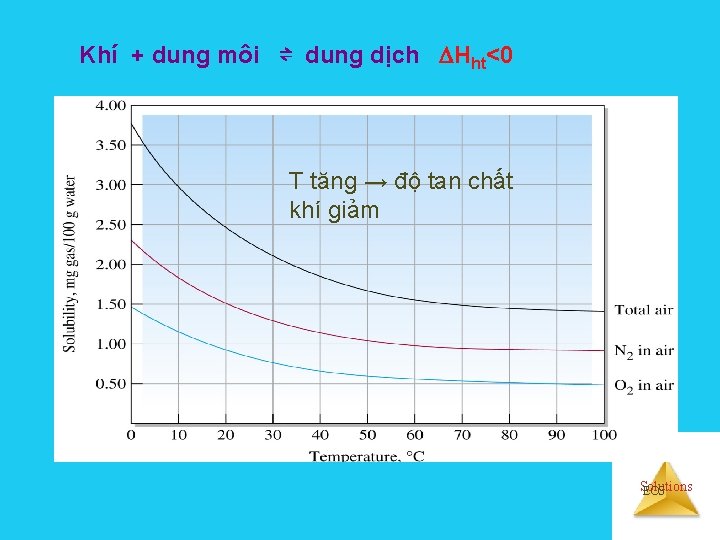
Khí + dung môi ⇌ dung dịch Hht<0 T tăng → độ tan chất khí giảm Solutions EOS
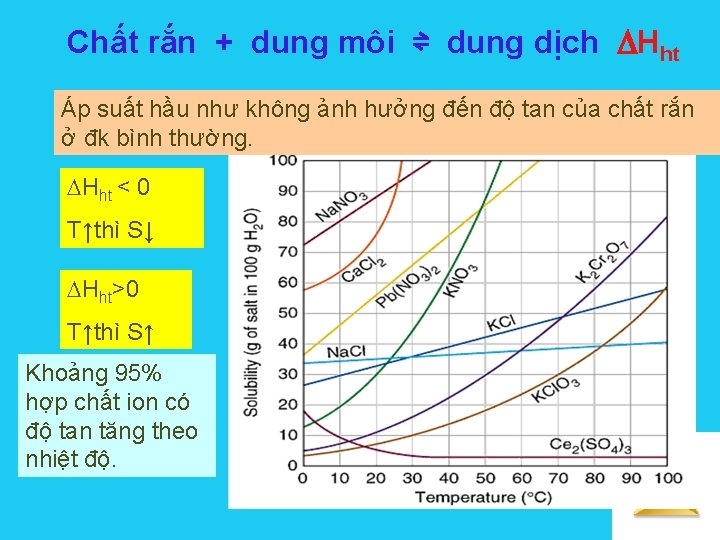
Chất rắn + dung môi ⇌ dung dịch Hht Áp suất hầu như không ảnh hưởng đến độ tan của chất rắn ở đk bình thường. Hht < 0 T↑thì S↓ Hht>0 T↑thì S↑ Khoảng 95% hợp chất ion có độ tan tăng theo nhiệt độ. Solutions

SỰ THAY ĐỔI TÍNH CHẤT NHIỆT ĐỘNG KHI TẠO THÀNH DUNG DỊCH Ght = Hht -T Sht Khí +dm(l) = dung dịch(l) Hht = Hcp (-)+ Hsol(-) <0 Rắn + dm(l) = dung dịch (l) Hht = Hcp (+)+ Hsol(-) <0 hay>0 Sht= Scp(-) - + Ssol (-) <0 Sht= Scp(+) + Ssol (-) >0 Solutions

DUNG DỊCH LÝ TƯỞNG • Là dung dịch có Hht=0 ; Vht=0 ; Uht=0 • Trong dung dịch lực tương tác giữa các tiểu phân cùng loại và khác loại giống nhau. Sự tạo thành dd là do sự tăng entropy. • Tính chất của dd lý tưởng không phụ thuộc vào bản chất tan mà phụ thuộc vào nồng độ của chúng. • Dd lỏng đạt khá tốt đk lý tưởng là dd mà các cấu tử của nó có cấu tạo phân tử và những thuộc tính vật lý và hoá học giống nhau hoặc rất gần nhau: Ø Hỗn hợp các đồng phân quang học. Ø Dd các cấu tử chỉ khác nhau về thành phần đồng vị Ví dụ - H 2 O + D 2 O Ø Dd những chất đồng đẳng cạnh nhau Ví dụ - Benzen + toluen ; hexan +heptan Solutions

Dung dịch thực • Nếu lực tương tác giữa chất tan và dung môi mạnh hơn lực tương tác giữa các tiểu phân cùng loại thì dd này thường có Hht<0 , Vht<0. Loại dd này thường xảy ra cho hệ mà cả hai cấu tử đều có cực. Tương tác hút giữa chúng có thể dẫn tới các quá trình hoá học (solvat hoá, tạo lk hydro, tạo hợp chất hoá học …) Ví dụ - hệ nước và axit nitric • Ngược lại, nếu lực tương tác giữa chất tan và dung môi yếu hơn lực tương tác giữa các tiểu phân cùng loại thì dd này thường có Hht>0 , Vht>0 Loại dd này thường xảy ra cho hệ mà cả hai cấu tử có tính phân cực khác nhau rõ rệt – Ví dụ- hoà tan chất có cực vào dm không cực: aceton trong CS 2 Solutions
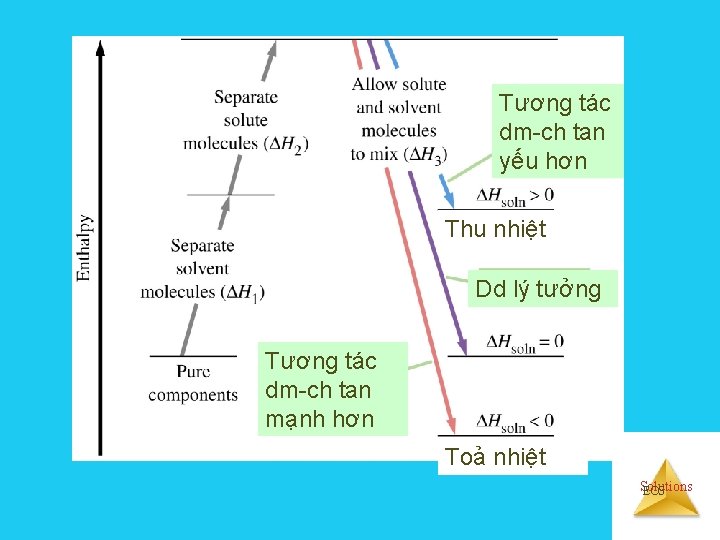
Tương tác dm-ch tan yếu hơn Thu nhiệt Dd lý tưởng Tương tác dm-ch tan mạnh hơn Toả nhiệt Solutions EOS

Dung dịch thực Ethanol và nước có lực tương tác giữa chúng mạnh hơn giữa các ethanol với nhau và giữa các ptử nước với nhau. Nên khi trộn 50 m. L H 2 O + 50 m. L C 2 H 5 OH thì thể tích nhỏ hơn 100 m. L Solutions EOS
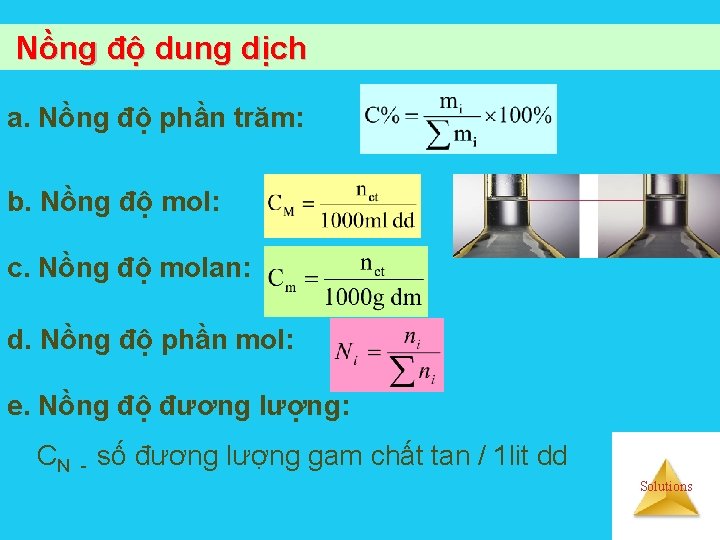
Nồng độ dung dịch a. Nồng độ phần trăm: b. Nồng độ mol: c. Nồng độ molan: d. Nồng độ phần mol: e. Nồng độ đương lượng: CN - số đương lượng gam chất tan / 1 lit dd Solutions

ÁP SUẤT HƠI BÃO HOÀ CỦA CHẤT LỎNG NGUYÊN CHẤT Bay hơi H > 0 Lỏng Hơi Ngưng tụ H < 0 T, G = 0 Kp = (P)cb = P 0 Pcb =P 0(T) Cân bằng pha Áp suất hơi bão hoà của chất lỏng là hằng số ở nhiệt độ xác định và tăng theo nhiệt độ Solutions
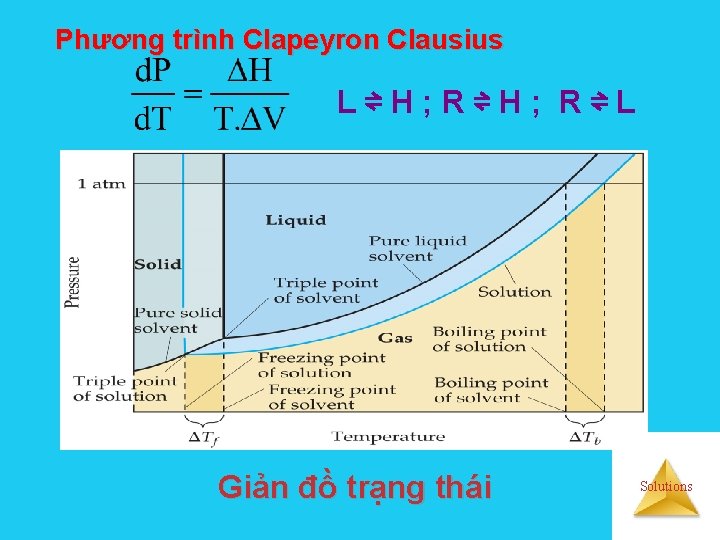
Phương trình Clapeyron Clausius L⇌H; R⇌L Giản đồ trạng thái Solutions

Nhiệt độ sôi của bất cứ pha lỏng nào (nguyên chất hay dung dịch) cũng đều bắt đầu sôi ở nhiệt độ mà tại đó áp suất hơi bão hoà của nó bằng áp suất ngoài. Đối với chất lỏng nguyên chất, khi áp suất ngòai không đổi, nhiệt độ sôi không thay đổi trong suốt quá trình sôi cho đến khi toàn bộ chất lỏng chuyển hết thành hơi. Solutions
Nhiệt độ đông đặc của bất cứ pha lỏng nào (nguyên chất hay dung dịch) cũng đều bắt đầu đông đặc ở nhiệt độ mà tại đó áp suất hơi bão hoà trên pha lỏng bằng với áp suất hơi bão hoà trên pha rắn. Đối với chất lỏng nguyên chất, khi áp suất ngòai không đổi nhiệt độ đông đặc không thay đổi trong suốt quá trình đông đặc. Solutions

Áp suất hơi bão hoà của dung dịch lỏng Áp suất hơi bão hoà của dd là hơi cân bằng với dung dịch lỏng. Áp suất hơi bão hoà của dd bằng tổng áp suất hơi bão hoà của tất cả các cấu tử có trong hệ. Pdd = Pi Áp suất hơi bão hoà của dd lỏng, loãng chứa chất tan không điện ly, không bay hơi chính là áp suất hơi bão hoà của dung môi trong dung dịch. Solutions
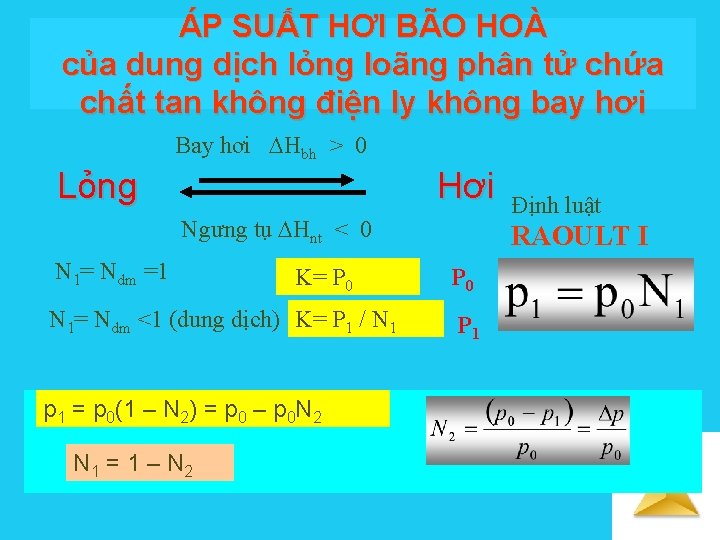
ÁP SUẤT HƠI BÃO HOÀ của dung dịch lỏng loãng phân tử chứa chất tan không điện ly không bay hơi Bay hơi Hbh > 0 Lỏng Hơi Ngưng tụ Hnt < 0 N 1= Ndm =1 K= P 0 N 1= Ndm <1 (dung dịch) K= P 1 / N 1 Định luật RAOULT I P 0 P 1 p 1 = p 0(1 – N 2) = p 0 – p 0 N 2 N 1 = 1 – N 2 Solutions
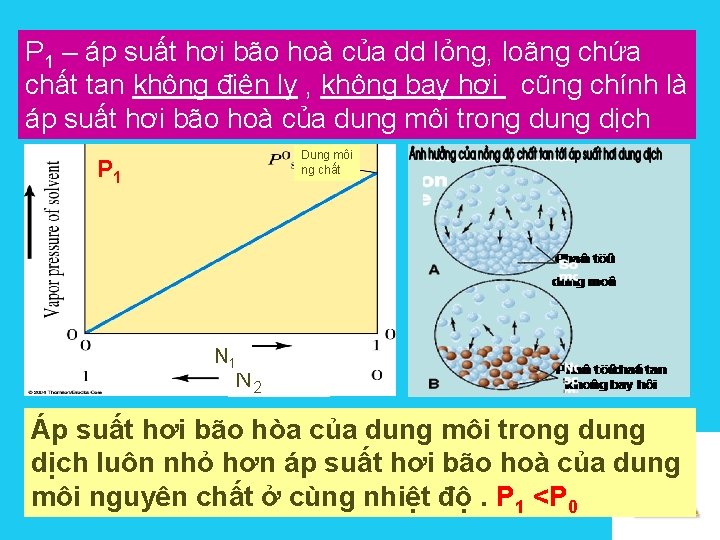
P 1 – áp suất hơi bão hoà của dd lỏng, loãng chứa chất tan không điện ly , không bay hơi cũng chính là áp suất hơi bão hoà của dung môi trong dung dịch Dung môi ng chất P 1 N 2 Áp suất hơi bão hòa của dung môi trong dung dịch luôn nhỏ hơn áp suất hơi bão hoà của dung Solutions môi nguyên chất ở cùng nhiệt độ. P 1 <P 0
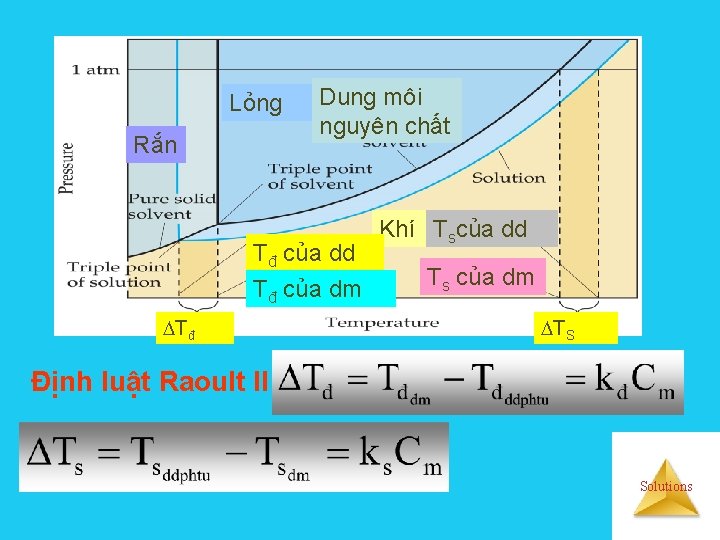
Lỏng Rắn Dung môi nguyên chất Tđ của dd Tđ của dm Tđ Khí Tscủa dd Ts của dm TS Định luật Raoult II Solutions
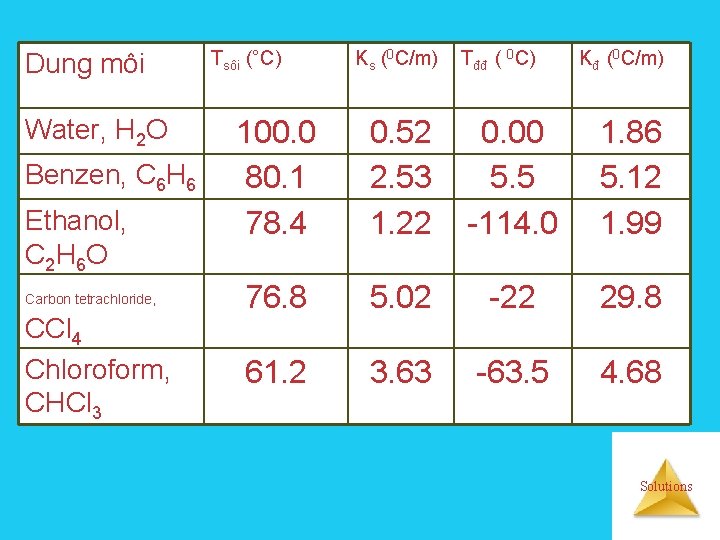
Dung môi Water, H 2 O Benzen, C 6 H 6 Ethanol, C 2 H 6 O Carbon tetrachloride, CCl 4 Chloroform, CHCl 3 Tsôi (°C) Ks (0 C/m) Tđđ ( 0 C) Kđ (0 C/m) 100. 0 80. 1 78. 4 0. 52 2. 53 1. 22 0. 00 5. 5 -114. 0 1. 86 5. 12 1. 99 76. 8 5. 02 -22 29. 8 61. 2 3. 63 -63. 5 4. 68 Solutions
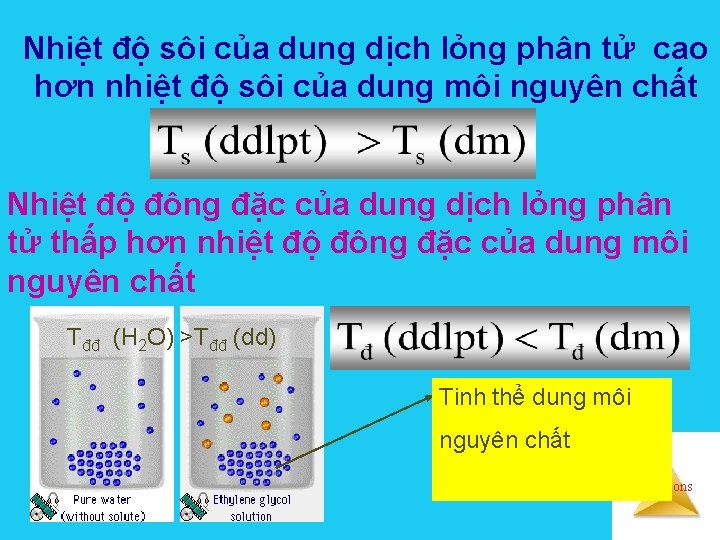
Nhiệt độ sôi của dung dịch lỏng phân tử cao hơn nhiệt độ sôi của dung môi nguyên chất Nhiệt độ đông đặc của dung dịch lỏng phân tử thấp hơn nhiệt độ đông đặc của dung môi nguyên chất Tđđ (H 2 O) >Tđđ (dd) Tinh thể dung môi nguyên chất Solutions

Nhận xét • Đối với dung dịch chưa bão hoà, nhiệt độ sôi là nhiệt độ bắt đầu sôi, nhiệt độ đông đặc là nhiệt độ bắt đầu đông đặc. Trong quá trình sôi hay đông đặc do nồng độ dd tăng liên tục nên nhiệt độ sôi tăng liên tục, nhiệt độ đông đặc giảm liên tục. • Khi dung dịch bão hoà, nhiệt độ sôi và nhiệt độ đông đặc mới là hằng số. Solutions
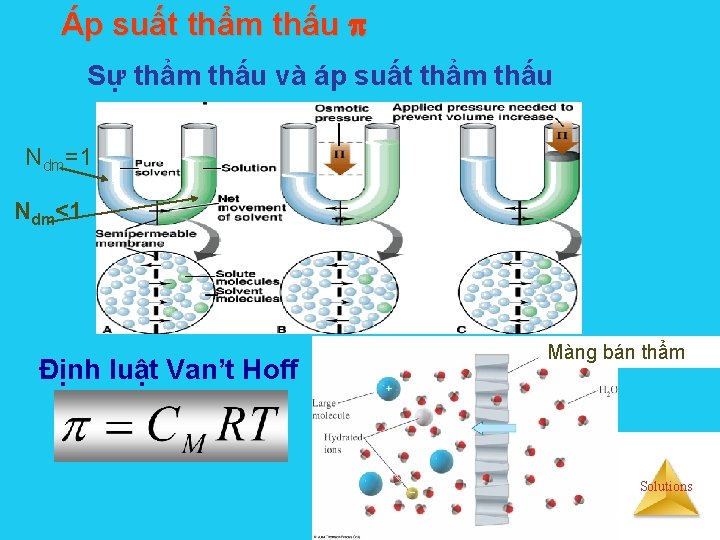
Áp suất thẩm thấu Sự thẩm thấu và áp suất thẩm thấu Ndm=1 Ndm<1 Định luật Van’t Hoff Màng bán thẩm Solutions

Nhận xét Định luật Raoult và Van’t hoff chỉ đúng cho dd lỏng lý tưởng và các dd thực có nồng độ chất tan rất nhỏ (dd loãng) Đối với dd thực (không lý tưởng) áp suất hơi riêng phần có thể có giá trị lớn hơn (sai lệch dương) hoặc bé hơn (sai lệch âm)so với giá trị tính theo đl Raoult. Solutions

Sự khác biệt của dd điện ly so với dd lỏng phân tử Ø Dung dịch điện ly không tuân theo định luật Raoult định luật Van’t Hoff Ø Dung dịch điện ly dẫn điện Solutions
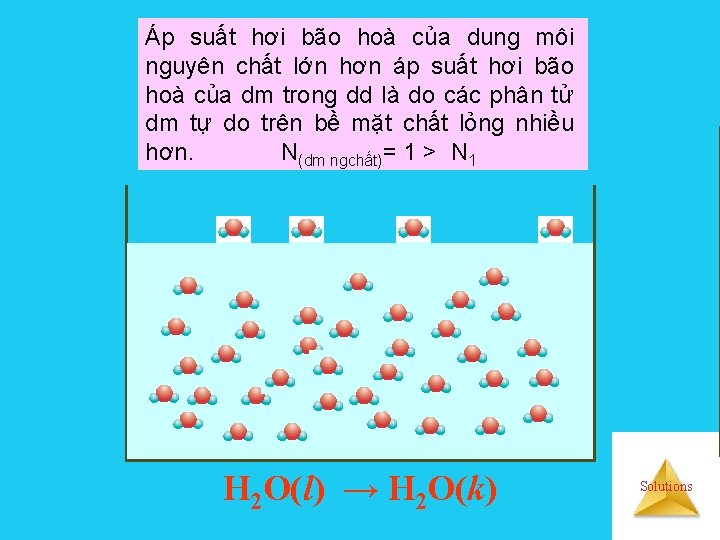
Áp suất hơi bão hoà của dung môi nguyên chất lớn hơn áp suất hơi bão hoà của dm trong dd là do các phân tử dm tự do trên bề mặt chất lỏng nhiều hơn. N(dm ngchất)= 1 > N 1 H 2 O(l) → H 2 O(k) Solutions
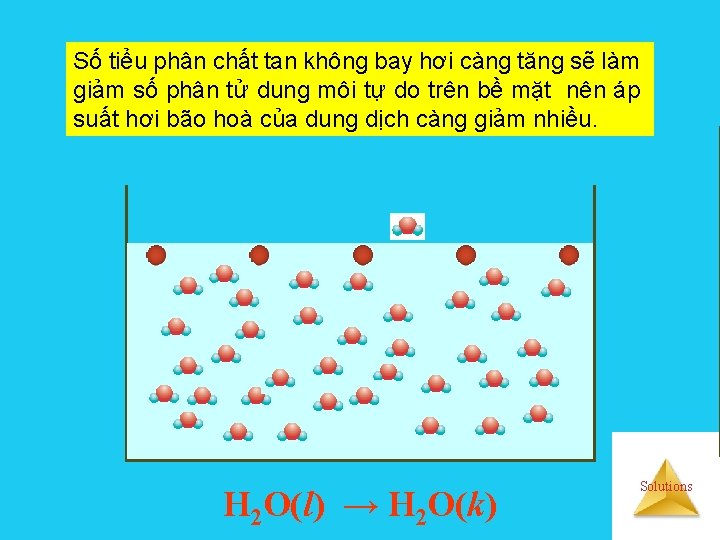
Số tiểu phân chất tan không bay hơi càng tăng sẽ làm giảm số phân tử dung môi tự do trên bề mặt nên áp suất hơi bão hoà của dung dịch càng giảm nhiều. H 2 O(l) → H 2 O(k) Solutions

DUNG DỊCH ĐIỆN LY Dung dịch điện ly không tuân theo các đl Raoult và Van’t Hoff i là hệ số đẳng trương hay hệ số Van’t Hoff i= số tiểu phân ch tan (số ion , số ph tử ch tan không điện ly) số phân tử chất tan hoà tan m- số ion trong 1 phân tử (nguyên dương 2) Dung dich điện ly 1< i m ; Dung dịch lỏng phân tử i=1 1 mol chất (dd điện ly) =N 1 +N 2 Số tiểu phân chất tan = i. N 2 Trong 1000 g dmôi →số tiểu phân chất tan =i. cm Trong 1 lit dung dịch →số tiểu phân chất tan= i. C(mol/l) Solutions
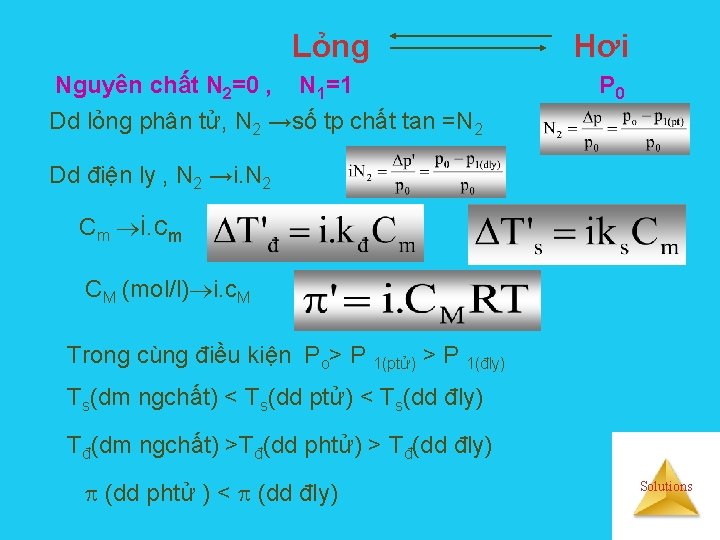
Lỏng Nguyên chất N 2=0 , N 1=1 Dd lỏng phân tử, N 2 →số tp chất tan =N 2 Hơi P 0 Dd điện ly , N 2 →i. N 2 Cm i. cm CM (mol/l) i. c. M Trong cùng điều kiện Po> P 1(ptử) > P 1(đly) Ts(dm ngchất) < Ts(dd ptử) < Ts(dd đly) Tđ(dm ngchất) >Tđ(dd phtử) > Tđ(dd đly) (dd phtử ) < (dd đly) Solutions

Ứng dụng địng luật Raoult làm thay đổi nhiệt độ đông đặc của nước Propylene glycol Dùng làm phụ gia pha trong nước (làm nguội động cơ ô tô) nhằm khắc phục nước đông đặc vào mùa đông. Ethylene glycol – có hại với gia súc Solutions

Để chống hiện tượng đóng băng tuyết vào mùa đông trên các con đường giao thông, theo bạn ta nên chọn các giải pháp nào sau đây : a) Cát, Si. O 2 b) Muối mỏ, Na. Cl c) Ca. Cl 2 Solutions

Dung dịch điện ly dẫn điện Độ dẫn điện riêng - 1 cm 3 dd (s=1 cm 2; d=1 cm) Khi pha loãng giảm Độ dẫn điện đương lượng - V cm 3 (1đlgam ctan) Khi pha loãng tăng Khi pha loãng vô cùng = const Solutions

THUYẾT ĐIỆN LY CỦA ARRHENIUS Phân tử chất điện ly (ax, baz, muối) ION TỰ DO CATION (+) và ANION(-) HCl H+ + Cl- Giải thích được tính dẫn điện và do có sự gia tăng số tiểu phân chất tan nên dd điện ly không tuân theo các đl Raoult Vant’Hoff Cu. SO 4(màu trắng) dd. Cu. SO 4 (màu xanh) Vìsao ? Solutions
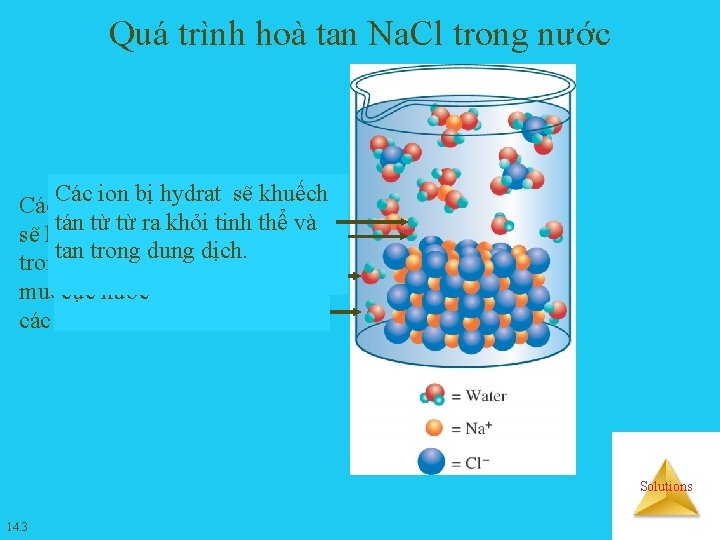
Quá trình hoà tan Na. Cl trong nước Các ion bị hydrat sẽ khuếch giữa các ion Các Khi phânlực tử hút nước có cực tán từ từcác ra khỏi tinh + và - thể yếu ion sẽ tách ravà sẽ hút cácđi, ion Na Cl tan trong dung dịch. baotinh quanh trongvàbị mạng thể các lưỡng cực nước muối, làm yếu lực hút giữa các ion. Solutions 14. 3

THUYẾT ĐIỆN LY CỦA KABLUKOB Chất tan Quá trình solvat hoá (có cực mạnh) (Quá trình hydrat hoá – H 2 O) Dung môi (có cực) ion solvat hoá (ion hydrat hoá) Trong dung dịch không có ion tự do Hợp chất ion quá trình phân ly các ion Na. Cl(r) + (n+m) H 2 O ⇌ Na+. n. H 2 O + Cl-. m. H 2 O Hợp chất cộng hoá trị có cực quá trình ion hoá. HCl (k) + (n+m)H 2 O ⇌ H 3 O+. (n-1)H 2 O + Cl-. m. H 2 O Solutions

Nếu chất tan có nhiều kiểu liên kết hoá học khác nhau thì quá trình phân ly theo trật tự sau: Ø Liên kết ion Ø Cộng hoá trị phân cực mạnh Na. HSO 4 (dd) = Na+ (dd) + HSO 4 -(dd) HSO 4 - (dd)+ H 2 O ⇌ H 3 O+ (dd) + SO 42 - (dd) Sự phân ly không xảy ra cho những lk cộng hoá trị có cực yếu hoặc không phân cực Solutions

Độ điện ly = số phân tử phân ly thành ion Tổng số phân tử hoà tan trong dung dịch 0 1 =0 dd lỏng phân tử =1 điện ly hoàn toàn Công thức xác định độ điện ly n- số mol chất tan hoà tan n- số mol chất tan điện ly nm - số mol ion (n - n) số mol chất tan không điện ly Solutions

Các yếu tố ảnh hưởng đến độ điện ly Ø Bản chất tan và dung môi Dung môi có cực yếu nhỏ Dung môi có cực mạnh lớn Ø Nồng độ dung dịch C giảm thì tăng C 0 thì 1 ØNhiệt độ tăng thường tăng Solutions

Quy ước đánh giá độ điện ly Trong dd nước 0, 1 N ở 250 C. > 30% chất điện ly mạnh 3%< < 30% chất điện ly trung bình < 30% chất điện ly yếu Solutions
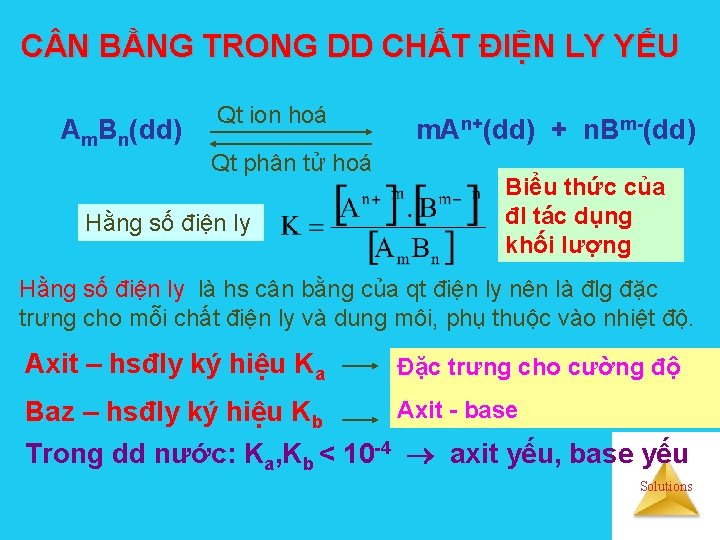
C N BẰNG TRONG DD CHẤT ĐIỆN LY YẾU Am. Bn(dd) Qt ion hoá Qt phân tử hoá Hằng số điện ly m. An+(dd) + n. Bm-(dd) Biểu thức của đl tác dụng khối lượng Hằng số điện ly là hs cân bằng của qt điện ly nên là đlg đặc trưng cho mỗi chất điện ly và dung môi, phụ thuộc vào nhiệt độ. Axit – hsđly ký hiệu Ka Đặc trưng cho cường độ Axit - base Baz – hsđly ký hiệu Kb Trong dd nước: Ka, Kb < 10 -4 axit yếu, base yếu Solutions

QUAN HỆ GIỮA K và AB (dd) A+ (dd) + B-(dd) Ban đầu C 0 Điện ly C 0 Cân bằng C 0(1 - ) C 0 Hằng số điện ly: Biểu thức toán học của đl pha loãng Ostwald Khi << 1 : (1 - ) 1→ Solutions

AXIT - BASE YẾU ĐA BẬC Ø Hằng số điện ly các bậc giảm dần theo trật tự sau: K 1>K 2 >K 3 >K 4… Ø Hằng số điện ly chung : K=K 1. K 2. K 3. K 4… Trong thực tế thường chỉ chú ý đến sự phân ly bậc thứ nhất Muối Đa số muối thuộc loại điện ly mạnh: KCl, Na. F… Các muối điện ly kém : muối axit (H+), muối baz(OH-), muối phức. Solutions

HẰNG SỐ ĐIỆN LY CỦA CÁC AXIT ĐA BẬC Solutions
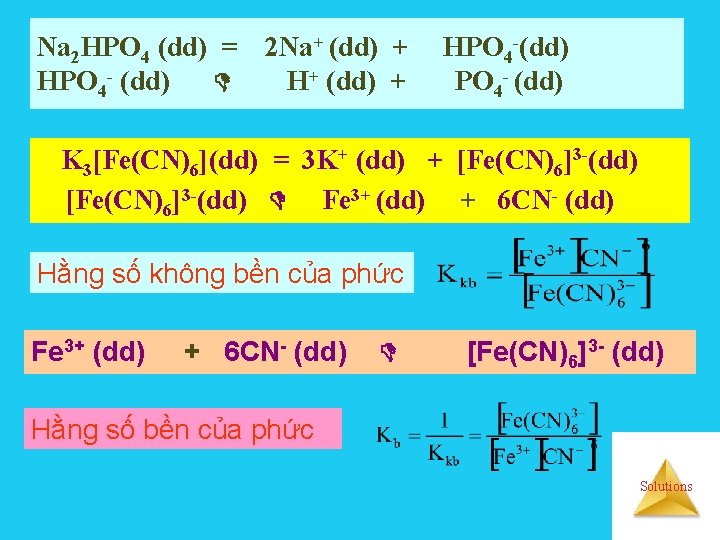
Na 2 HPO 4 (dd) = HPO 4 - (dd) 2 Na+ (dd) + HPO 4 -(dd) PO 4 - (dd) K 3[Fe(CN)6](dd) = 3 K+ (dd) + [Fe(CN)6]3 -(dd) Fe 3+ (dd) + 6 CN- (dd) Hằng số không bền của phức Fe 3+ (dd) + 6 CN- (dd) [Fe(CN)6]3 - (dd) Hằng số bền của phức Solutions
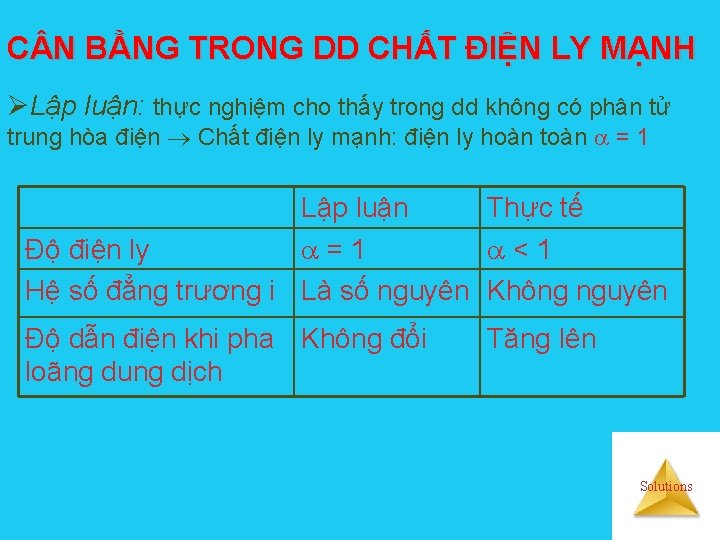
C N BẰNG TRONG DD CHẤT ĐIỆN LY MẠNH ØLập luận: thực nghiệm cho thấy trong dd không có phân tử trung hòa điện Chất điện ly mạnh: điện ly hoàn toàn = 1 Lập luận Thực tế Độ điện ly =1 <1 Hệ số đẳng trương i Là số nguyên Không nguyên Độ dẫn điện khi pha Không đổi loãng dung dịch Tăng lên Solutions
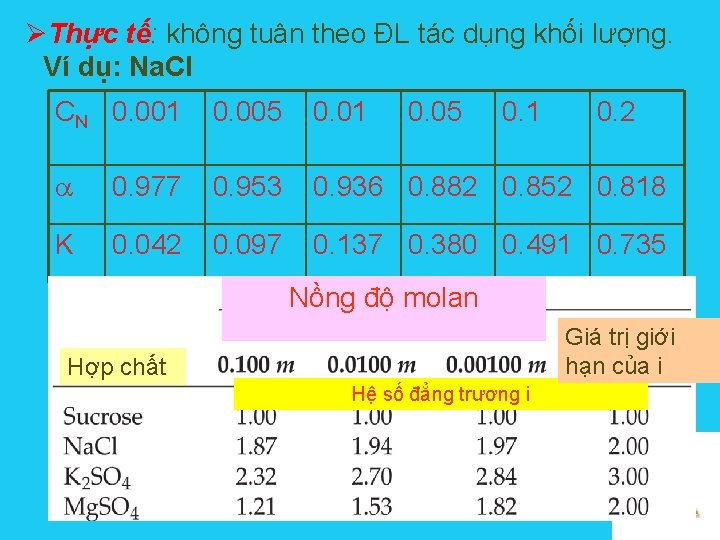
ØThực tế: không tuân theo ĐL tác dụng khối lượng. Ví dụ: Na. Cl CN 0. 001 0. 005 0. 01 0. 05 0. 1 0. 2 0. 977 0. 953 0. 936 0. 882 0. 852 0. 818 K 0. 042 0. 097 0. 137 0. 380 0. 491 0. 735 Nồng độ molan Giá trị giới hạn của i Hợp chất Hệ số đẳng trương i Solutions

Lý thuyết chất điện ly mạnh Trong dung dịch xuất hiện lực hút tương hỗ giữa các ion → bầu khí quyển ion. Khi pha loãng, lực hút tương hỗ giảm, độ dẫn điện tăng. Trong dd chất điện ly mạnh có liên hiệp ion, khi pha loãng các liên hiệp ion phân ly thành các ion đơn giản. → độ điện ly trên thực tế : độ điện ly biểu kiến. → dùng hoạt độ a thay cho nồng độ: a = f. C Solutions

HOẠT ĐỘ (a) – là nồng độ hoạt động mang tính tổng quát hơn nồng độ và áp dụng đl tác dụng khối lượng cho mọi dd chất tan ở các nồng độ khác nhau a = fc f- hệ số hoạt độ 0<f 1 Dd loãng f =1 a = c Dd có nồng độ cao f<1 a = c f phụ thuộc vào : bản chất dung môi, nhiệt độ, điện tích và nồng độ các ion. Solutions

Phương trình của Debye và Huckel Đối với dung dịch nước và ở 250 C: A = 0, 5 Khi I 0, 01 phương trình trên có dạng đơn giản như sau: Solutions
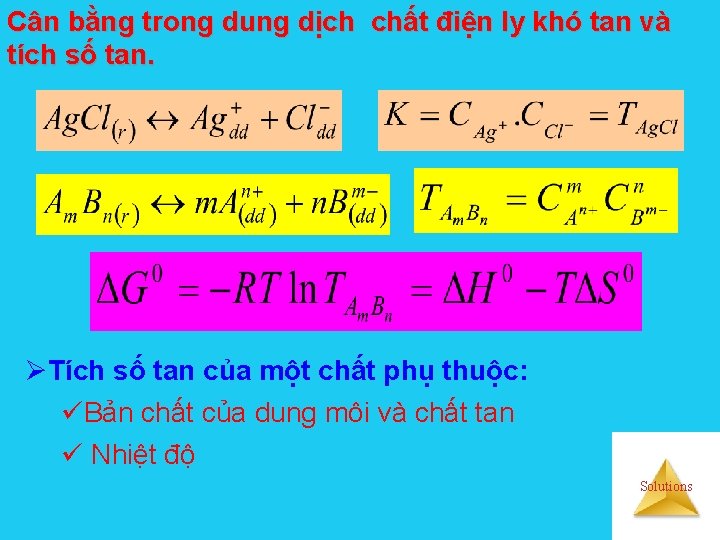
Cân bằng trong dung dịch chất điện ly khó tan và tích số tan. ØTích số tan của một chất phụ thuộc: üBản chất của dung môi và chất tan ü Nhiệt độ Solutions
![Tích số tan và độ tan của chất điện ly khó tan. S[mol/l] m. Tích số tan và độ tan của chất điện ly khó tan. S[mol/l] m.](http://slidetodoc.com/presentation_image_h/d4dc04102df90e6feee89778d492a40a/image-66.jpg)
Tích số tan và độ tan của chất điện ly khó tan. S[mol/l] m. S n. S Độ tan trong nước Solutions

Ảnh hưởng của các ion trong dung dịch đến độ tan của chất điện ly khó tan. ØThêm ion cùng loại: S ØThêm ion khác loại: S Solutions
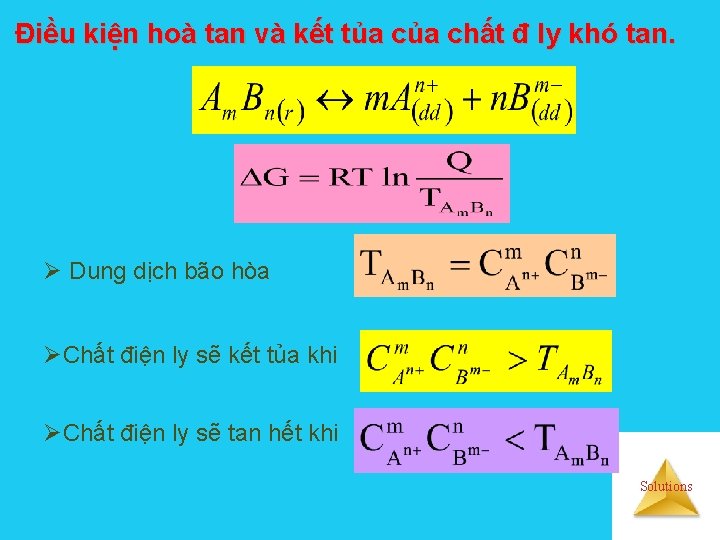
Điều kiện hoà tan và kết tủa chất đ ly khó tan. Ø Dung dịch bão hòa ØChất điện ly sẽ kết tủa khi ØChất điện ly sẽ tan hết khi Solutions
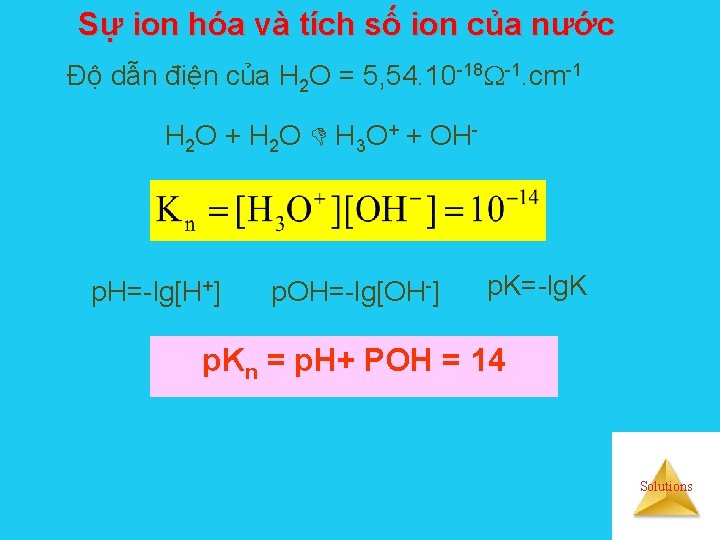
Sự ion hóa và tích số ion của nước Độ dẫn điện của H 2 O = 5, 54. 10 -18 -1. cm-1 H 2 O + H 2 O H 3 O+ + OH- p. H=-lg[H+] p. OH=-lg[OH-] p. K=-lg. K p. Kn = p. H+ POH = 14 Solutions

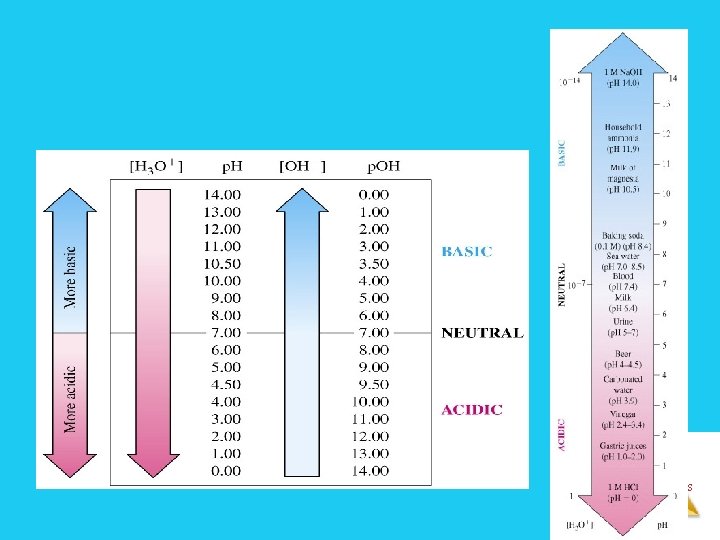
Chỉ số p. H và môi trường dd Ø Trong nước nguyên chất và môi trường trung tính [H+] = [OH-] = 10 -7 Ø Trong p. H = 7 dung dịch axit có môi trường axit [H+] > [OH-] p. H < 7 Ø Trong dung dịch baz có môi trường baz [H+] < [OH-] p. H > 7 Solutions
Solutions

Khái niệm về axit, baz. a. Thuyết cổ điển của Arrhenius b. Thuyết proton Bronsted c. Thuyết electron của Lewis Solutions
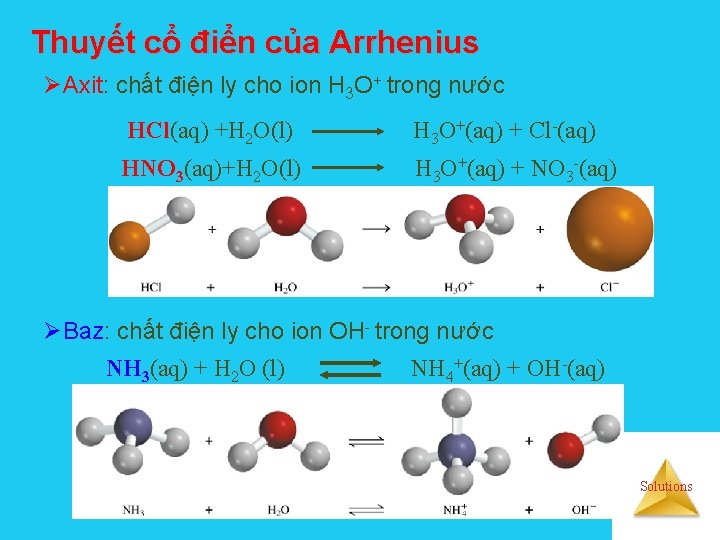
Thuyết cổ điển của Arrhenius ØAxit: chất điện ly cho ion H 3 O+ trong nước HCl(aq) +H 2 O(l) H 3 O+(aq) + Cl-(aq) HNO 3(aq)+H 2 O(l) H 3 O+(aq) + NO 3 -(aq) ØBaz: chất điện ly cho ion OH- trong nước NH 3(aq) + H 2 O (l) NH 4+(aq) + OH-(aq) Solutions
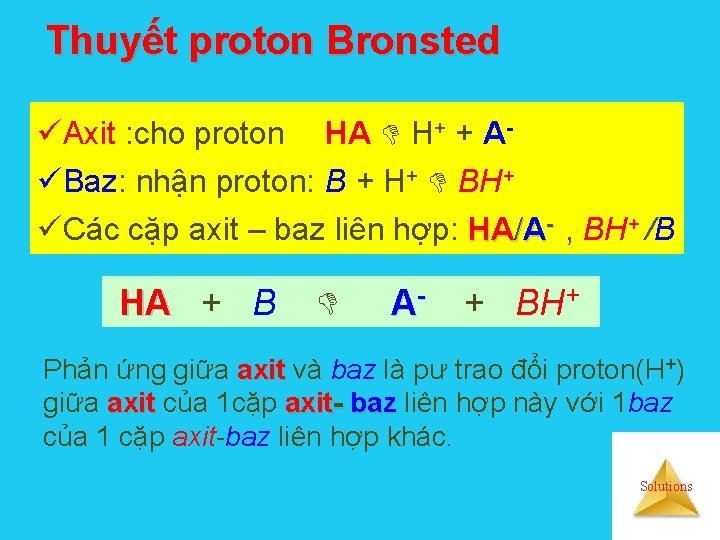
Thuyết proton Bronsted üAxit : cho proton HA H+ + AüBaz: nhận proton: B + H+ BH+ üCác cặp axit – baz liên hợp: HA/A- , BH+ /B HA + B A- + BH+ Phản ứng giữa axit và baz là pư trao đổi proton(H+) giữa axit của 1 cặp axit- baz liên hợp này với 1 baz của 1 cặp axit-baz liên hợp khác. Solutions

Phản ứng giữa các cặp axit baz liên hợp Cặp liên hợp Acid + Base + Acid Cặp liên hợp Reaction 1 HF + H 2 O F– + H 3 O+ Reaction 2 HCOOH + CN– HCOO– + HCN Reaction 3 NH 4+ + CO 32– NH 3 + HCO 3– Reaction 4 H 2 PO 4– + OH– HPO 42– Reaction 5 H 2 SO 4 + N 2 H 5+ HSO 4– + HPO 42– + SO 32– PO 43– + Reaction 6 + H 2 O N 2 H 62+ Solutions HSO 3–

Dự đoán axit, baz Bronsted Axit – là chất phải chứa H+ Phân tử trung hoà : HCl, HNO 3, HF…. Cation có chứa H+ : NH 4+ Anion có chứa H : HSO 4 - , H 2 PO 4 - …. Cation kim loại trong nước : Fe 2+(aq) ; Al 3+(aq). . ØCation cấu hình khí trơ có q 2/ r càng lớn tính axit càng mạnh ØCation có điện tích và bán kính tương đương, cấu hình: 18 e – (18 e +2 e) – (18 e> >8 e ) tính axit mạnh hơn cấu hình 8 e Solutions
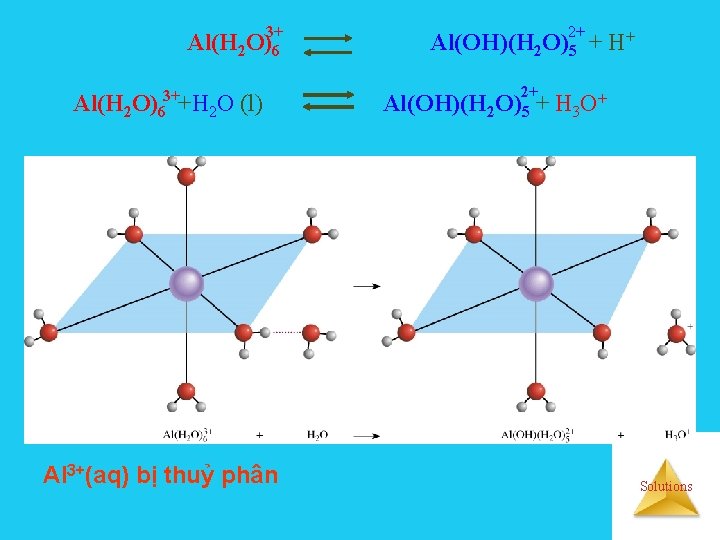
3+ Al(H 2 O)63++H 2 O (l) Al 3+(aq) bị thuỷ phân 2+ Al(OH)(H 2 O)5 + H+ 2+ Al(OH)(H 2 O)5 + H 3 O+ Solutions
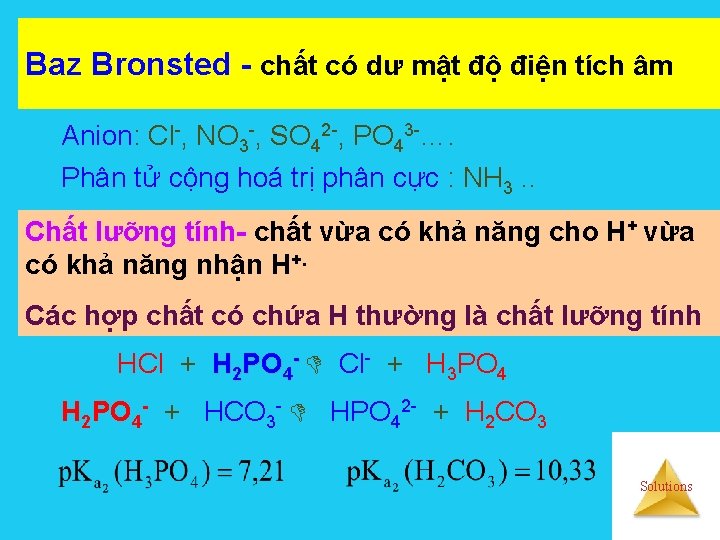
Baz Bronsted - chất có dư mật độ điện tích âm Anion: Cl-, NO 3 -, SO 42 -, PO 43 -…. Phân tử cộng hoá trị phân cực : NH 3. . Chất lưỡng tính- chất vừa có khả năng cho H+ vừa có khả năng nhận H+. Các hợp chất có chứa H thường là chất lưỡng tính HCl + H 2 PO 4 - Cl- + H 3 PO 4 H 2 PO 4 - + HCO 3 - HPO 42 - + H 2 CO 3 Solutions

Dung môi proton hoá Ø Là hợp chất cộng hoá trị phân cực có chứa H nên có khả năng trao đổi proton (chất lưỡng tính) Ø Thường tạo lk H 2 nên Tsvà Tnc cao. Ø Có tính phân cực mạnh nên có khả năng hoà tan nhiều chất (có cực). Ø Có thể tự ion hoá một phần khi ở trạng thái lỏng. Hằng số cân bằng gọi là hằng số tự proton hoá Kd Solutions
![H 2 O + H 2 O H 3 O + OH- kn= [OH-][H H 2 O + H 2 O H 3 O + OH- kn= [OH-][H](http://slidetodoc.com/presentation_image_h/d4dc04102df90e6feee89778d492a40a/image-80.jpg)
H 2 O + H 2 O H 3 O + OH- kn= [OH-][H 3 O+] NH 3 + NH 3 NH 2 - + NH 4+ kd= [NH 2 -][NH 4+] HD + HD D- + H 2 D+ Kd = [D-][H 2 D+] Solutions
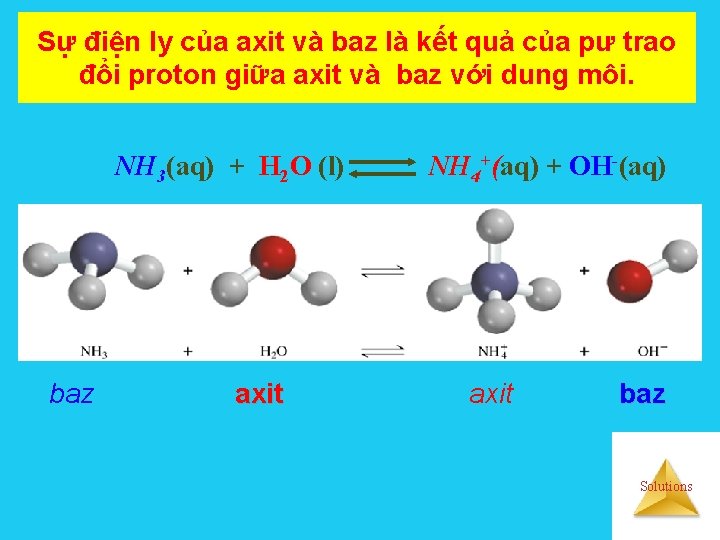
Sự điện ly của axit và baz là kết quả của pư trao đổi proton giữa axit và baz với dung môi. NH 3(aq) + H 2 O (l) baz axit NH 4+(aq) + OH-(aq) axit baz Solutions
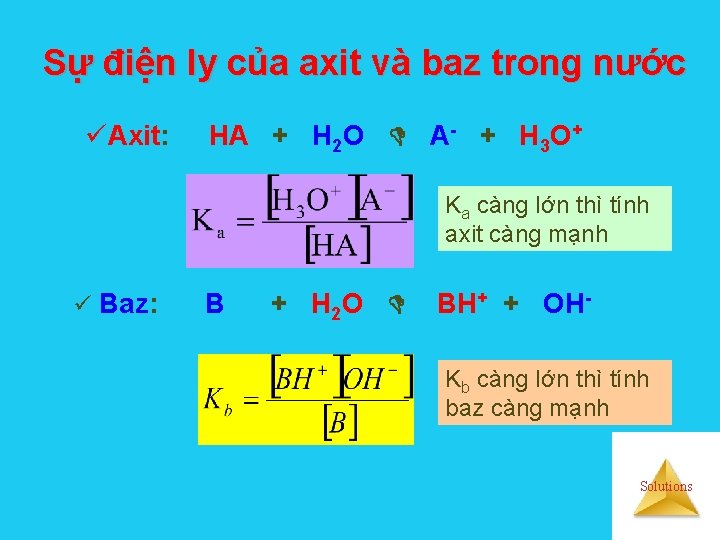
Sự điện ly của axit và baz trong nước üAxit: HA + H 2 O A- + H 3 O+ Ka càng lớn thì tính axit càng mạnh ü Baz: B + H 2 O BH+ + OHKb càng lớn thì tính baz càng mạnh Solutions
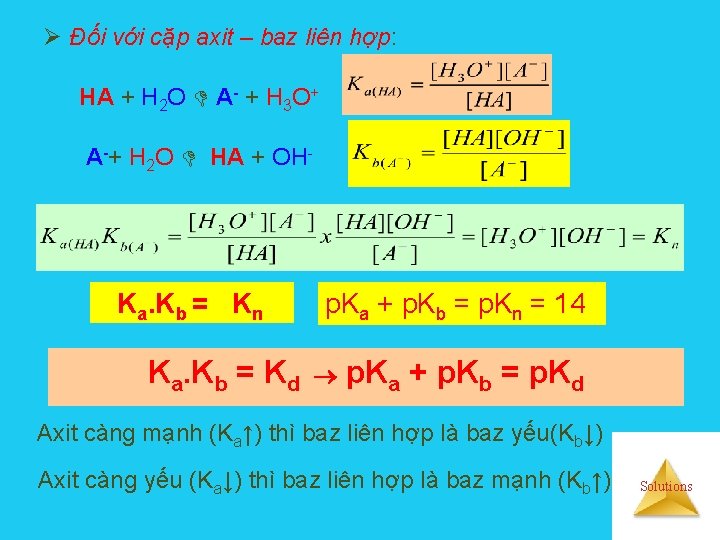
Ø Đối với cặp axit – baz liên hợp: HA + H 2 O A- + H 3 O+ A-+ H 2 O HA + OH- Ka. Kb = Kn Ka. Kb = Kd p. Ka + p. Kb = p. Kn = 14 p. Ka + p. Kb = p. Kd Axit càng mạnh (Ka↑) thì baz liên hợp là baz yếu(Kb↓) Axit càng yếu (Ka↓) thì baz liên hợp là baz mạnh (Kb↑) Solutions
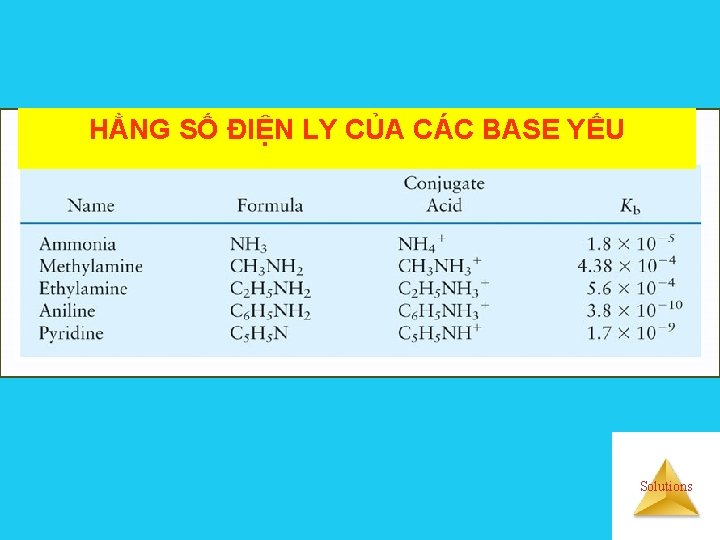
HẰNG SỐ ĐIỆN LY CỦA CÁC BASE YẾU Solutions
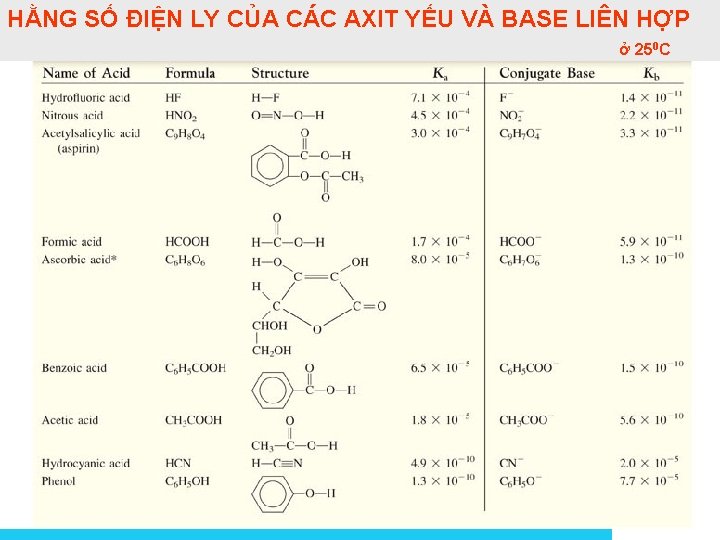
HẰNG SỐ ĐIỆN LY CỦA CÁC AXIT YẾU VÀ BASE LIÊN HỢP ở 250 C Solutions
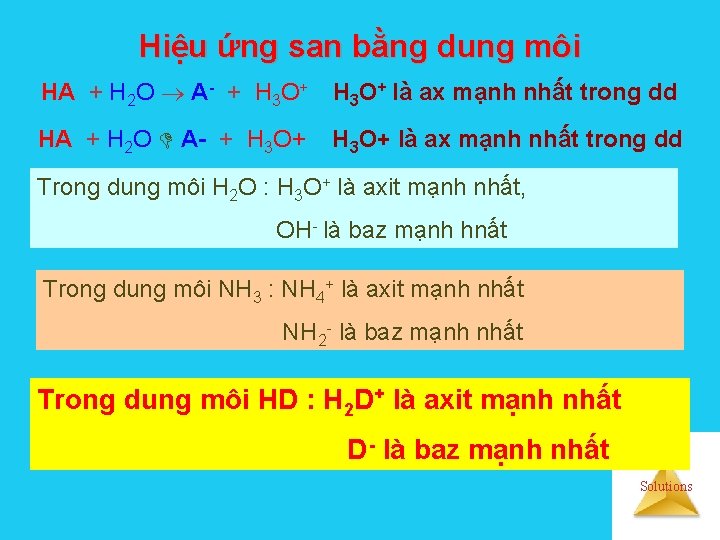
Hiệu ứng san bằng dung môi HA + H 2 O A- + H 3 O+ là ax mạnh nhất trong dd Trong dung môi H 2 O : H 3 O+ là axit mạnh nhất, OH - là baz mạnh hnất Trong dung môi NH 3 : NH 4+ là axit mạnh nhất NH 2 - là baz mạnh nhất Trong dung môi HD : H 2 D+ là axit mạnh nhất D - là baz mạnh nhất Solutions

Ảnh hưởng của dung môi đến cường độ axit baz Hằng số tự proton hoá (Kd ) HD + HD D- + H 2 D+ Kd = [D-][H 2 D+] Kd càng lớn thì tính axit của dung môi càng mạnh. Ái lực proton (AP) HD + H+ =H 2 D+ H = -AP AP càng lớn thì dung môi có tính baz càng mạnh Solutions

Dung môi có AP↑ thì tính axit của chất tan tăng tính baz của chất tan giảm • Trong nước, CH 3 COOH là axit yếu • Trong NH 3 , CH 3 COOH là axit mạnh Dung môi có AP↓ thì tính axit của chất tan giảm tính baz của chất tan tăng Trong dung môi HF, HCl. O 4 không chất nào thể hiện tính axit HNO 3 + HF (dm) H 2 NO 3+ + F- NH 4 OH là baz yếu trong dung môi nước NH 4 OH là baz mạnh trong dung môi axit acetic Solutions

Thuyết electron của Lewis Thuyết Lewis dùng giải thích quá trình tạo phức và tính bền của phức. Axit Lewis: là tiểu phân có dư mật độ điện tích dương và orbital hoá trị trống để nhận cặp electron liên kết từ baz. Dự đoán axit Lewis: ØHầu hết các cation kim loại (Ag+, Co 3+, Cr 3+, Mg 2+. . ) ØCác halogenua của B, Al, Si, Sn ØCác hydrua của B, Al ØCác hợp chất có lk đôi trong những đk thích hợp cũng Solutions thể hiện tính axit
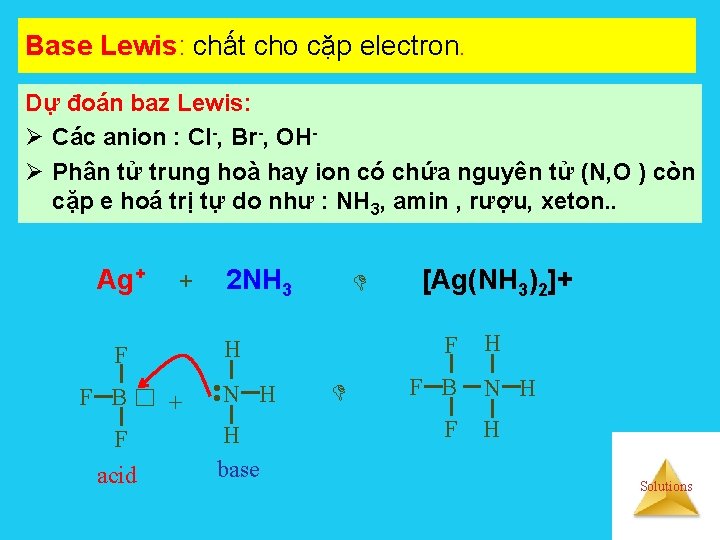
Base Lewis: chất cho cặp electron. Dự đoán baz Lewis: Ø Các anion : Cl-, Br-, OHØ Phân tử trung hoà hay ion có chứa nguyên tử (N, O ) còn cặp e hoá trị tự do như : NH 3, amin , rượu, xeton. . + F F B□ + F acid 2 NH 3 N H H base [Ag(NH 3)2]+ F H • • Ag+ F B F H N H H Solutions
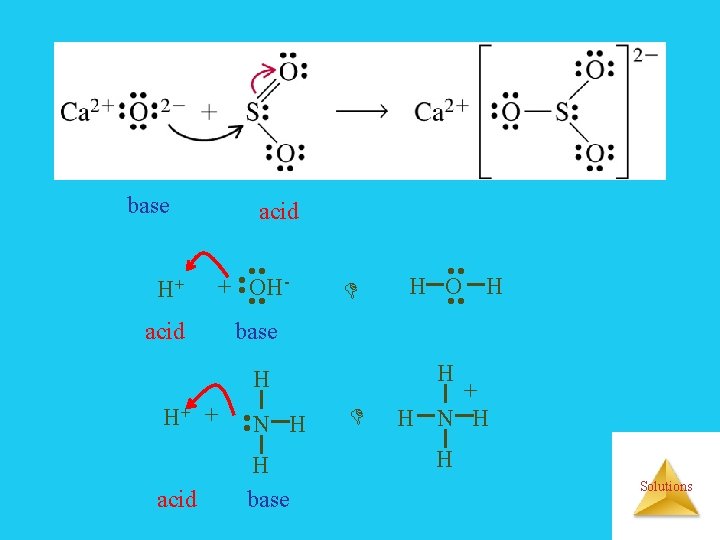
base acid • • + OH • • base • • H+ acid H H acid N H • • H+ + H base • • H O H • • + H N H H Solutions
![HCl, axit mạnh [H+] = [HCl] HF, axit yếu [H+] < [HF] Solutions HCl, axit mạnh [H+] = [HCl] HF, axit yếu [H+] < [HF] Solutions](http://slidetodoc.com/presentation_image_h/d4dc04102df90e6feee89778d492a40a/image-92.jpg)
HCl, axit mạnh [H+] = [HCl] HF, axit yếu [H+] < [HF] Solutions
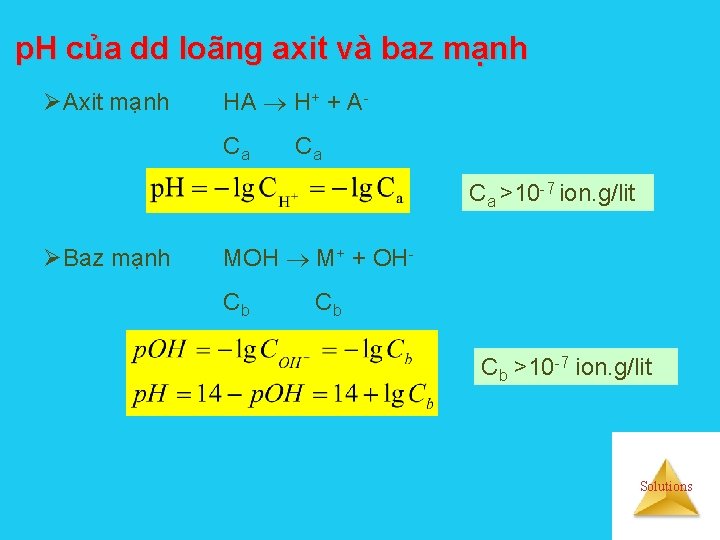
p. H của dd loãng axit và baz mạnh ØAxit mạnh HA H+ + ACa Ca Ca >10 -7 ion. g/lit ØBaz mạnh MOH M+ + OHCb Cb Cb >10 -7 ion. g/lit Solutions
Axit mạnh và base mạnh HCl CH 3 CO 2 H Thymol Blue chỉ thị p. H < 1. 2 < p. H < 2. 8 < p. H Solutions
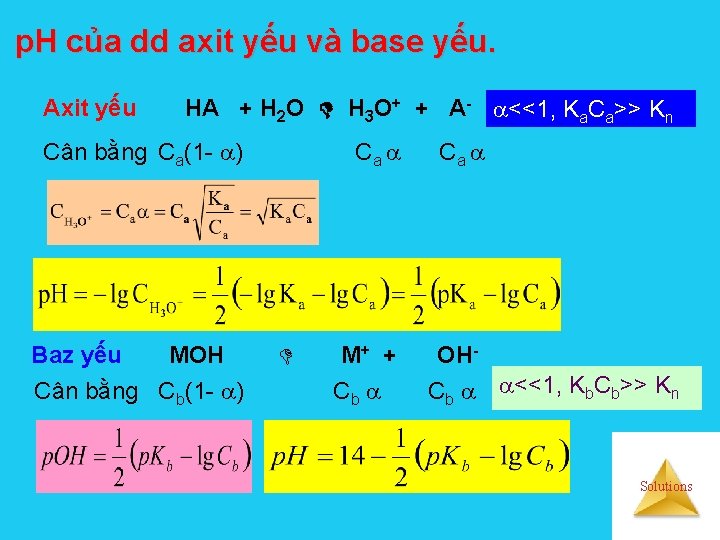
p. H của dd axit yếu và base yếu. Axit yếu HA + H 2 O H 3 O+ + A- <<1, Ka. Ca>> Kn Cân bằng Ca(1 - ) Baz yếu MOH Cân bằng Cb(1 - ) Ca M+ + OH- Cb <<1, Kb. Cb>> Kn Solutions

Đối với axit , base yếu đa bậc Khi tính p. H dung dịch ta chỉ dựa vào bậc phân ly thứ nhất Ví dụ : tính p. H dung dịch H 2 CO 3 0, 01 M. Solutions
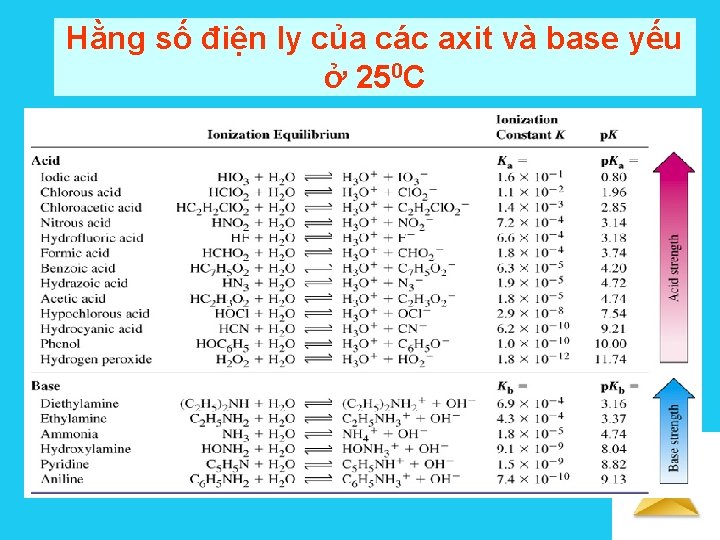
Hằng số điện ly của các axit và base yếu ở 250 C Solutions

Đo p. H của giấm Đo p. H của dd NH 3 Solutions

Các phương pháp đo p. H cho các dd nước (a) Giấy đo p. H (định tính) (b) Máy đo p. H(định lượng) Solutions

p. H của dung dịch đệm. ØĐịnh nghiã: Dung dịch đệm là dd có p. H ≈ const khi thêm lượng nhỏ axit mạnh hoặc baz mạnh hoặc pha loãng dd. ØCấu tạo (HA / A- ) ü Đệm axit: axit yếu + muối của nó CH 3 COOH+CH 3 COONa ü Đệm baz: base yếu + muối của nó NH 3. H 2 O+ NH 4 Cl ü Đệm trung tính : hỗn hợp các muối axit yếu ØCơ chế tác dụng của dung dịch đệm CH 3 COOH CH 3 COO- + H+ (1) CH 3 COONa CH 3 COO- + Na+ üThêm axit mạnh: cb (1) ← üThêm base mạnh: H+ + OH- → H 2 O: lượng H+↓→ cb (1) → üPha loãng dd, độ điện ly CH 3 COOH ↑ Solutions
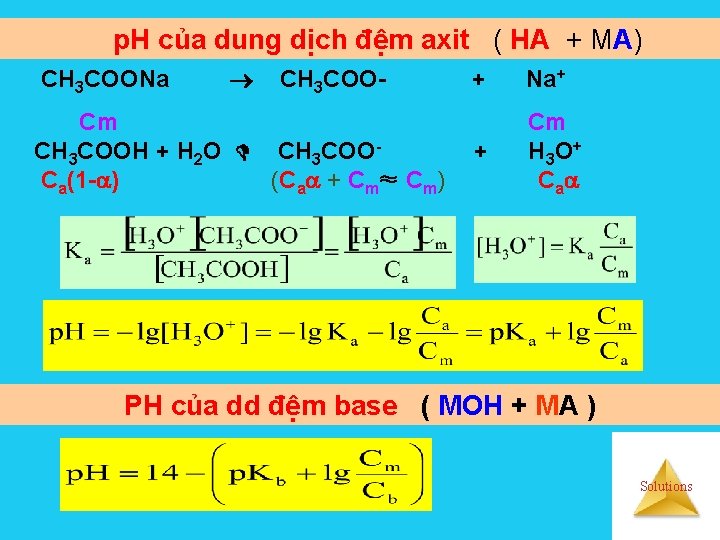
p. H của dung dịch đệm axit ( HA + MA) CH 3 COONa CH 3 COO- Cm CH 3 COOH + H 2 O CH 3 COOCa(1 - ) (Ca + Cm≈ Cm) + Na+ + Cm H 3 O + C a PH của dd đệm base ( MOH + MA ) Solutions
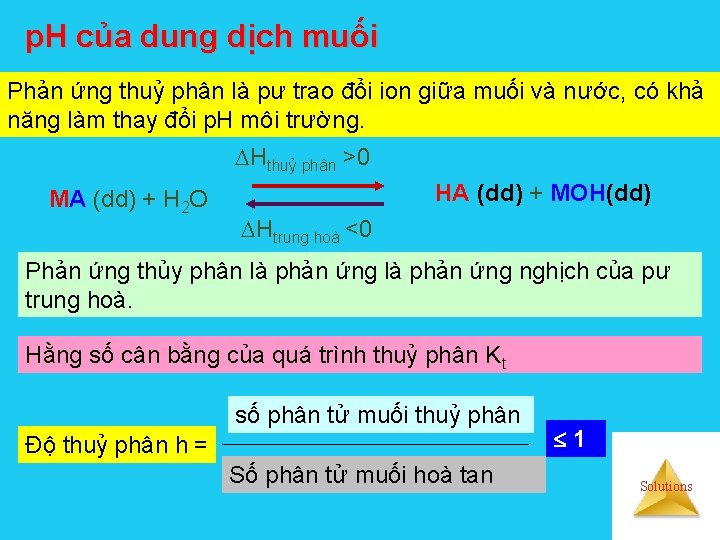
p. H của dung dịch muối Phản ứng thuỷ phân là pư trao đổi ion giữa muối và nước, có khả năng làm thay đổi p. H môi trường. Hthuỷ phân >0 MA (dd) + H 2 O HA (dd) + MOH(dd) Htrung hoà <0 Phản ứng thủy phân là phản ứng nghịch của pư trung hoà. Hằng số cân bằng của quá trình thuỷ phân Kt số phân tử muối thuỷ phân Độ thuỷ phân h = Số phân tử muối hoà tan 1 Solutions

Do muối có lk ion nên khi hoà tan trong nước sẽ phân ly hòan toàn thành các ion bị hydrat hoá M+ (aq) + A- (aq) +H 2 O MOH (aq) + HA (aq) ; H >0 Theo thuyết axit - base Bronsted : M+. n. H 2 O / M(OH). (n-1)(H 2 O) là cặp axit- base liên hợp HA / A- là cặp axit - baz liên hợp Cation của muối (M+) là axit bronsted Anion của muối ( A-) là base bronsted Vậy pư thuỷ phân thực chất là pư trao đổi proton giữa các ion của muối với các ptử nước. Hay pư thuỷ phân là pư axit base Bronsted. Solutions

Muối nào sẽ bị thuỷ phân ? • Nếu cation của muối (M+) là axit mạnh hơn nước (MOH là base yếu), nó sẽ nhường H+ cho nước cation muối bị thuỷ phân làm cho p. Hmtr <7 Ag+ n. H 2 O + H 2 O Ag(OH)(n-1)H 2 O + H 3 O+ NH 4+ (aq) + H 2 O NH 3 (aq) + H 3 O+ • Nếu anion của muối (A-) là baz mạnh hơn nước (HA là axit yếu), nó sẽ nhận H+ của nước làm tăng OH anion muối bị thuỷ phân làm cho p. Hmtr >7 CH 3 COO- + H 2 O CH 3 COOH + OHTất cả các muối (MA) đều bị thuỷ phân trừ muối được tạo thành từ axit mạnh (HA) và base mạnh (MOH) Solutions
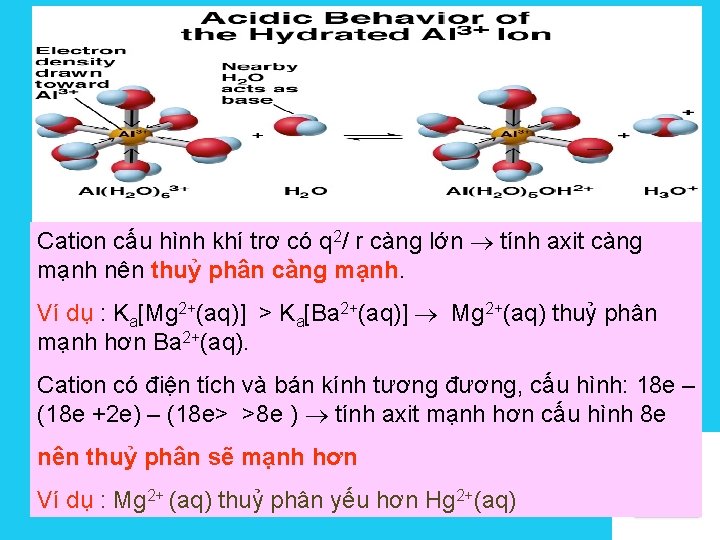
Cation cấu hình khí trơ có q 2/ r càng lớn tính axit càng mạnh nên thuỷ phân càng mạnh. Ví dụ : Ka[Mg 2+(aq)] > Ka[Ba 2+(aq)] Mg 2+(aq) thuỷ phân mạnh hơn Ba 2+(aq). Cation có điện tích và bán kính tương đương, cấu hình: 18 e – (18 e +2 e) – (18 e> >8 e ) tính axit mạnh hơn cấu hình 8 e nên thuỷ phân sẽ mạnh hơn Ví dụ : Mg 2+ (aq) thuỷ phân yếu hơn Hg 2+(aq) Solutions
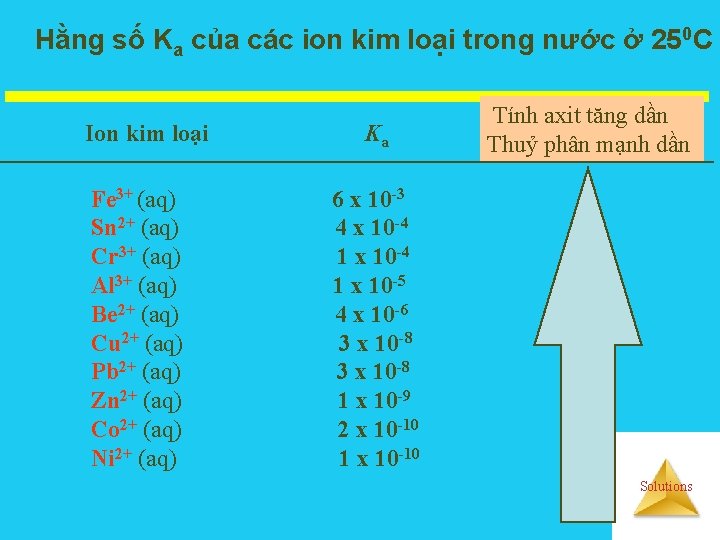
Hằng số Ka của các ion kim loại trong nước ở 250 C Ion kim loại Fe 3+ (aq) Sn 2+ (aq) Cr 3+ (aq) Al 3+ (aq) Be 2+ (aq) Cu 2+ (aq) Pb 2+ (aq) Zn 2+ (aq) Co 2+ (aq) Ni 2+ (aq) Ka Tính axit tăng dần Thuỷ phân mạnh dần 6 x 10 -3 4 x 10 -4 1 x 10 -5 4 x 10 -6 3 x 10 -8 1 x 10 -9 2 x 10 -10 1 x 10 -10 Solutions

CƯỜNG ĐỘ CỦA CẶP AXIT BASE LIÊN HỢP HA A- Các anion (A-) có tính base càng mạnh sẽ thuỷ phân càng mạnh trong nuớc. Solutions
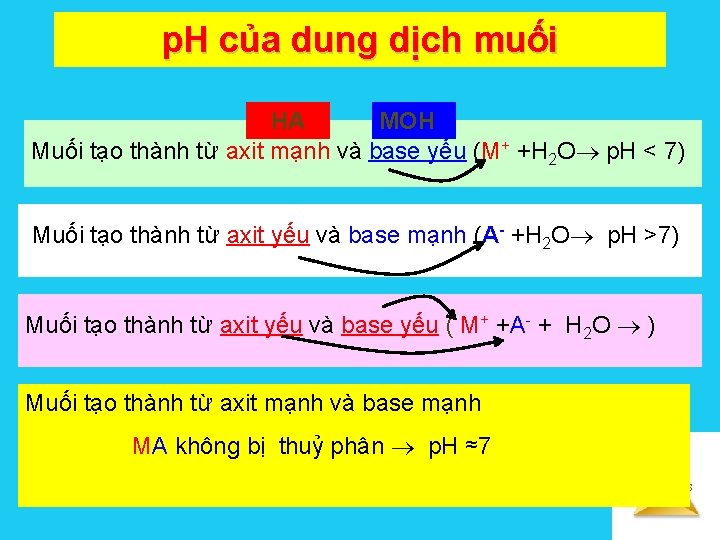
p. H của dung dịch muối HA MOH Muối tạo thành từ axit mạnh và base yếu (M+ +H 2 O p. H < 7) Muối tạo thành từ axit yếu và base mạnh (A- +H 2 O p. H >7) Muối tạo thành từ axit yếu và base yếu ( M+ +A- + H 2 O ) Muối tạo thành từ axit mạnh và base mạnh MA không bị thuỷ phân p. H ≈7 Solutions
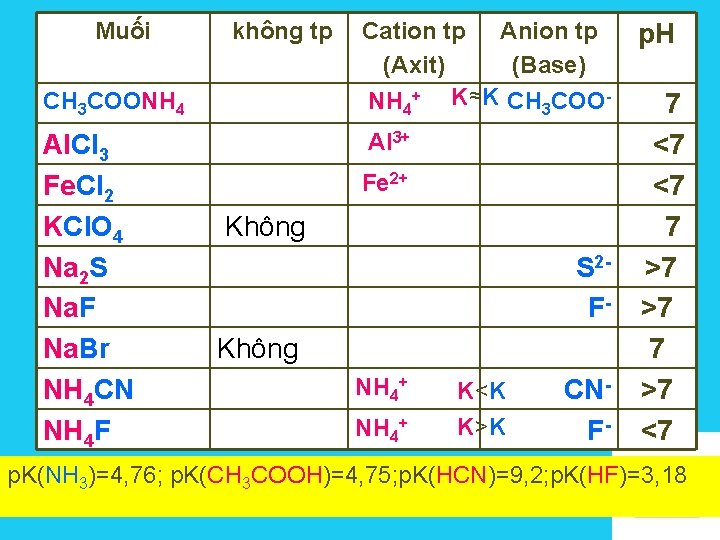
Muối không tp CH 3 COONH 4 Al. Cl 3 Fe. Cl 2 KCl. O 4 Na 2 S Na. F Na. Br NH 4 CN NH 4 F Cation tp Anion tp (Axit) (Base) NH 4+ K≈K CH 3 COOAl 3+ Fe 2+ Không S 2 FKhông NH 4+ K<K K>K CNF- p. H 7 <7 <7 7 >7 >7 <7 p. K(NH 3)=4, 76; p. K(CH 3 COOH)=4, 75; p. K(HCN)=9, 2; p. K(HF)=3, 18 Solutions

Solutions

ØMuối tạo thành từ axit yếu (Ka) và baz mạnh PH >7 ü Sự điện ly: MA ü Sự thủy phân: → M+ (axy) + A- (base mạnh hơn H 2 O) A - + H 2 O ⇌ HA + OHCm(1 -h) C mh ü Hằng số thủy phân: ü Độ thủy phân: ü Tính p. H: >7 Solutions
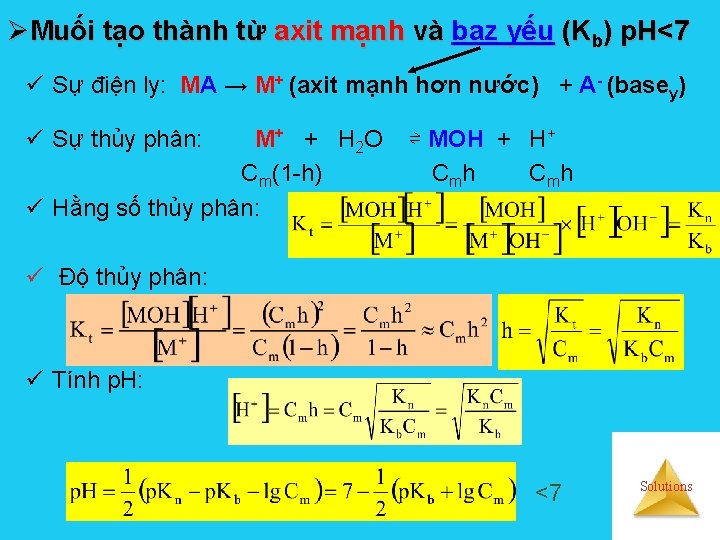
ØMuối tạo thành từ axit mạnh và baz yếu (Kb) p. H<7 ü Sự điện ly: MA → M+ (axit mạnh hơn nước) + A- (basey) ü Sự thủy phân: M+ + H 2 O Cm(1 -h) ü Hằng số thủy phân: ⇌ MOH + H+ C mh ü Độ thủy phân: ü Tính p. H: <7 Solutions
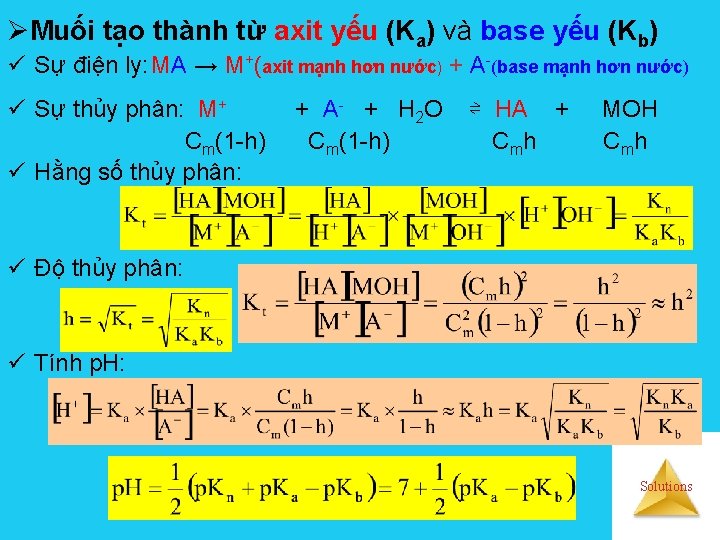
ØMuối tạo thành từ axit yếu (Ka) và base yếu (Kb) ü Sự điện ly: MA → M+(axit mạnh hơn nước) + A-(base mạnh hơn nước) ü Sự thủy phân: M+ Cm(1 -h) ü Hằng số thủy phân: + A - + H 2 O Cm(1 -h) ⇌ HA + C mh MOH C mh ü Độ thủy phân: ü Tính p. H: Solutions

NHẬN XÉT Hằng số thuỷ phân Kt phụ thuộc vào : Bản chất của muối và nhiệt độ Độ thuỷ phân h phụ thuộc vào: ü Ka và Kb của axit và baz liên hợp với các ion của muối, được tạo thành trong qt thuỷ phân, chúng có giá trị càng nhỏ thì độ thuỷ phân càng tăng. ü Cm càng nhỏ thì độ thuỷ phân tăng (trừ muối tạo thành từ axit yếu và baz yếu ) ü Nhiệt độ tăng thì độ thuỷ phân tăng. Solutions

Cách tính p. H của các dung dịch a. p. H của dd axit mạnh và base mạnh. b. p. H của dd axit yếu và base yếu. c. p. H của dung dịch đệm. d. p. H của dung dịch muối Solutions

Pha loãng dung dịch Bình định mức dd. A 1 M pipet • Pha loãng nồng độ dung dịch A từ 1 M xuống 0, 02 M Dùng pipet hút 10, 00 ml dd A 1 M cho vào bình định mức 500 ml +nước vào cho đến vạch chuẩn của bình lắc đều dd. A 0, 02 M Solutions

Phản ứng trung hoà HCl (dd) +Na. OH(dd) = Na. Cl (dd) + H 2 O H 3 O+ + OH- = 2 H 2 O ; H 0298 = -13, 36 kcal = - 55, 84 k. J Hiệu ứng nhiệt tiêu chuẩn là hằng số, không phụ thuộc vào loại axit mạnh và base mạnh tham gia phản ứng. Phản ứng đến cùng, không có phản ứng thuỷ phân xảy ra Điểm tương đương : VNa. OH. CNa. OH(N) = VHCl. CHCl(N) Tại điểm tương đương p. H =7 Solutions

Cho dd Na. OH 0, 10 N vào buret tới vạch chuẩn (mức 0) Dùng phép chuẩn độ axit base để xác định nồng độ axit VNa. OH. CNa. OH(N) = VHCl. CHCl(N) 0 Cho 10, 00 ml dd axit HCl chưa biết nồng độ + 100 ml nước cất + 3 giọt phenolphatalein vào bình tam giác (erlen) Solutions

Chuẩn độ dd HCl bằng dd Na. OH dd. Na. OH 0, 10 N 0 24, 6 Dd HCl CHCl ? Nhỏ từ từ dd Na. OH từ burét xuống bình tam giác và lắc đều dd trong bình cho đến khi dung dịch trong bình bắt đầu chuyển sang màu hồng nhạt (bền trong 30 giây) đọc thể tích dd. Na. OH đã dùng trên buret V=24, 6 ml tính nồng độ dd HCl theo đl đương lượng. CHCl = 0, 25 N Solutions
- Slides: 119