Chimie Terminale S Enseignement de spcialit Dcoupage horaire


































- Slides: 41

Chimie Terminale S Enseignement de spécialité

Découpage horaire • 11 séances TP ou activités • 3 séances exercices et évaluation

Objectifs • Consolider et diversifier la culture scientifique • Développer des compétences expérimentales

Progressions possibles • Les activités du chimiste (selon les quatre parties du B. O. ) • Thème directeur Une contrainte articuler enseignement obligatoire et enseignement de spécialité

Document d’accompagnement • 40 documents rédigés pour – exercer un choix pédagogique – réaliser différents types d’activités • Quelques références bibliographiques d’autres manipulations envisageables • Des documents complémentaires à l’intention de l’enseignant

Choix pédagogique • Centrer sur la compréhension des protocoles et des techniques • Permettre un travail par thème • Respecter la liberté pédagogique de l’enseignant

Types d’activités • Manipulation élève • Autres activités – recherche documentaire – étude d’un texte – analyse d’un protocole écrit ou d’une manipulation filmée – etc. • Exercices d’entraînement

Onze séances autour d’un thème… • Textile et papier • Médecine et pharmacie • Boissons et alimentation • Chimie et art • Chimie et agriculture

Thème « médecine et pharmacie » Partie A (2 séances) • Extraction de l’eugénol (A 01) • Principes actifs d’un médicament (A 07) Partie B (2 séances) • Synthèse du paracétamol (B 1) • Synthèse de l’essence de Wintergreen (B 4) ou synthèse d’un polyester biodégradable (fil chirurgical)

Thème « médecine et pharmacie » Partie C (4 séances) • Bleu de méthylène dans un collyre (C 01) • Vitamine C dans un comprimé et/ou eau oxygénée officinale (oxydoréduction) • Ions bicarbonate dans un comprimé (acidebase) (C 09) • Ions chlorure dans un lait maternisé (conductimétrie) (C 14) • Ions calcium et magnésium dans un comprimé (complexation) (C 12)

Thème « médecine et pharmacie » Partie D (3 séances) • Préparation de l’alumine : matière première des pâtes dentifrice, pansements gastriques (D 1) • Formulation d’un médicament (activité documentaire) • « Dans la poubelle du pharmacien… » (activité documentaire)

Tableaux récapitulatifs Pour choisir une manipulation en fonction • de l’espèce chimique extraite, synthétisée, dosée… • des techniques mises en œuvre • des réinvestissements possibles • du thème directeur choisi • du domaine d’application

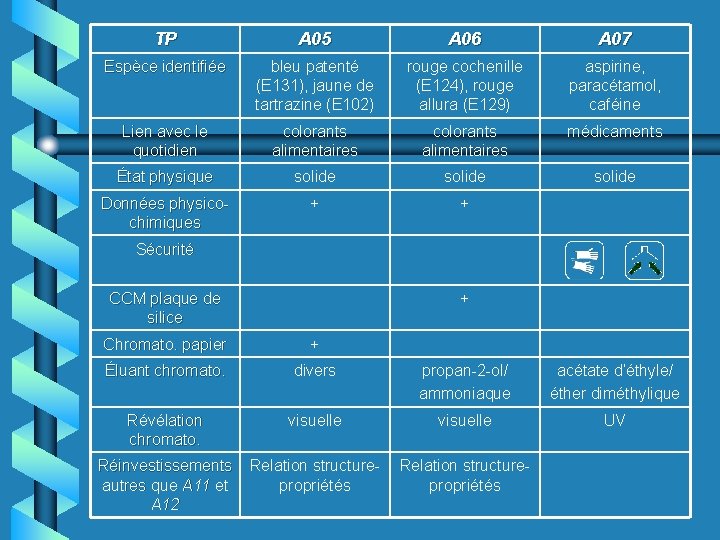
TP A 05 A 06 A 07 Espèce identifiée bleu patenté (E 131), jaune de tartrazine (E 102) rouge cochenille (E 124), rouge allura (E 129) aspirine, paracétamol, caféine Lien avec le quotidien colorants alimentaires médicaments État physique solide Données physicochimiques + + Sécurité CCM plaque de silice + Chromato. papier + Éluant chromato. divers propan-2 -ol/ ammoniaque acétate d’éthyle/ éther diméthylique Révélation chromato. visuelle UV Réinvestissements autres que A 11 et A 12 Relation structurepropriétés

Partie A : un exemple A 05 – Colorants alimentaires dans un sirop • Chromatographie de partage sur papier • Influence de la nature de l’éluant (relation structure-propriétés) • Mise en œuvre d’une technique d’extraction des colorants (fixation sur la laine)

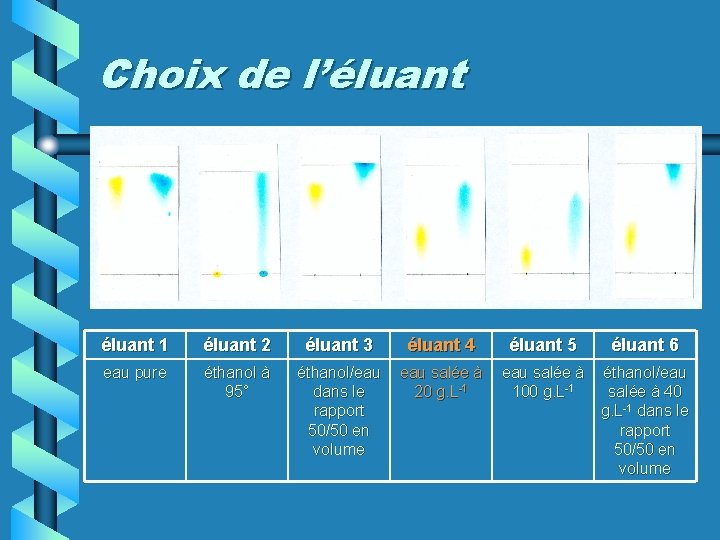
Choix de l’éluant 1 éluant 2 éluant 3 éluant 4 éluant 5 éluant 6 eau pure éthanol à 95° éthanol/eau dans le rapport 50/50 en volume eau salée à 20 g. L-1 eau salée à 100 g. L-1 éthanol/eau salée à 40 g. L-1 dans le rapport 50/50 en volume

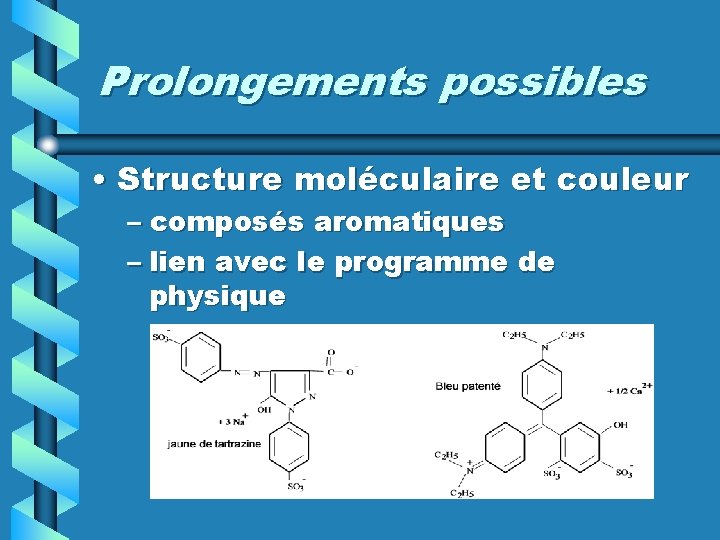
Prolongements possibles • Structure moléculaire et couleur – composés aromatiques – lien avec le programme de physique

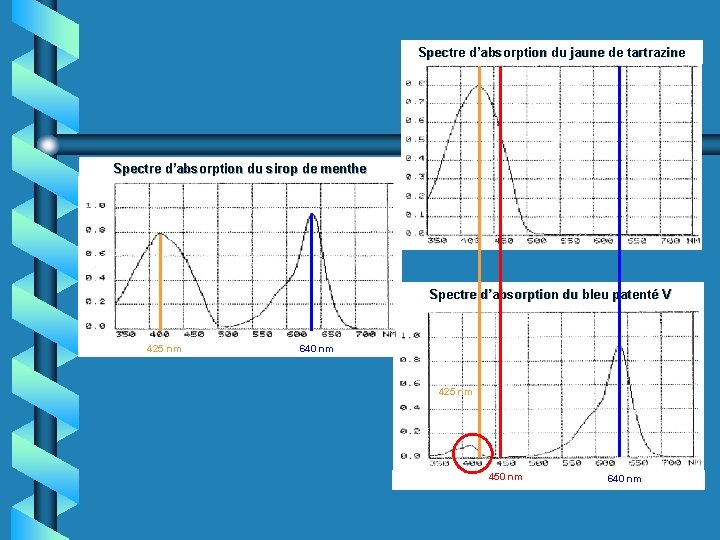
Prolongements possibles • Spectres d’absorption des colorants du sirop de menthe Situation « Au vu des spectres d’absorption, est-il possible de déterminer les concentrations deux espèces contenues dans le sirop de menthe ? »

Spectre d’absorption du jaune de tartrazine Spectre d’absorption du sirop de menthe Spectre d’absorption du bleu patenté V 425 nm 640 nm 425 nm 450 nm 640 nm

Partie B • Compétences exigibles – compétences expérimentales, différentes techniques, sécurité – justification des étapes d’un protocole – groupe caractéristique amide • Réinvestissements Seconde et Première S • Approfondissements enseignement obligatoire de Terminale S

Réinvestissements Seconde et Première S • Lire et écrire des formules chimiques – – – squelettes carbonés groupes caractéristiques isomérie Z et E • Reconnaître des types de réactions • Tableau descriptif de l’évolution du système

Approfondissements enseignement obligatoire de Terminale S • État d’équilibre d’un système, rendement • Contrôle de la transformation • Réactions compétitives • Groupes caractéristiques (ester, anhydride d’acide)

Synthèses proposées • • Paracétamol Butanone Acide benzoïque Esters odorants Vanilline Synthèses proposées en Première S Autres…

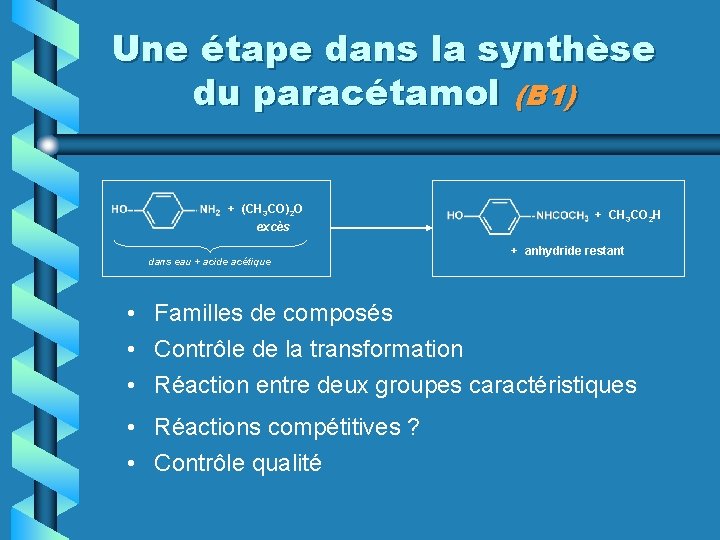
Une étape dans la synthèse du paracétamol (B 1) + (CH 3 CO)2 O excès dans eau + acide acétique + CH 3 CO 2 H + anhydride restant • Familles de composés • Contrôle de la transformation • Réaction entre deux groupes caractéristiques • Réactions compétitives ? • Contrôle qualité

Partie C Effectuer des contrôles de qualité • Dosages par étalonnage • Titrages directs ou indirects - réaction d’oxydoréduction réaction acido-basique autres (précipitation et complexation)

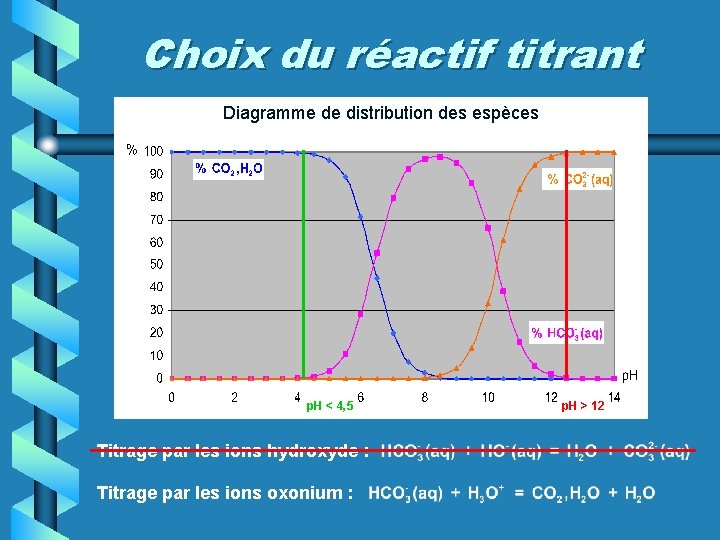
Partie C : des exemples C 09 – Ions hydrogénocarbonate contenus dans une eau de boisson Situation À l’aide du diagramme de distribution des espèces, quel réactif titrant utiliser pour doser une espèce ampholyte : espèce acide ou espèce basique ?

Choix du réactif titrant Diagramme de distribution des espèces p. H < 4, 5 Titrage par les ions hydroxyde : Titrage par les ions oxonium : p. H > 12

Démarche • Titrage des ions hydrogénocarbonate – – à l’aide d’un p. H-mètre à l’aide d’un indicateur coloré approprié Utilisation possible d’un logiciel de simulation • Comparaison à l’information portée sur l’étiquette

Partie C : des exemples C 14 – Ions chlorure dans un lait • Titrage des ions chlorure suivi par conductimétrie • Application du critère d’évolution pour justifier le choix du réactif titrant

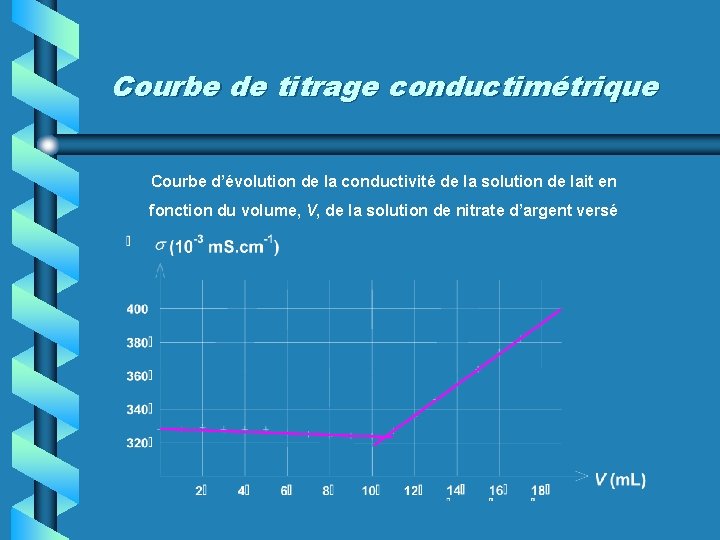
Courbe de titrage conductimétrique Courbe d’évolution de la conductivité de la solution de lait en fonction du volume, V, de la solution de nitrate d’argent versé

Application du critère d’évolution pour la réaction support du titrage Situation 1, 0 m. L de solution de nitrate d’argent de concentration molaire 1, 0. 10 -2 mol. L-1 est ajouté à 250 m. L de lait préalablement dilué contenant 1, 0 g. L-1 d’ions chlorure. Ag+(aq) + Cl-(aq) = Ag. Cl(s) K = 109, 7 5, 0. 109 [Ag+] = 4, 0. 10 -5 mol. L-1 et [Cl-] = 2, 8. 10 -4 mol. L-1 Calcul de Qr, i dans l’état initial du système : Qr, i < K : le système évolue vers la K = 5, 0. 109 formation du chlorure d’argent (sens direct)

Des manipulations connues… Des réinvestissements possibles • Application du critère d’évolution pour les titrages • Réactions compétitives – indicateurs de fin de réaction (précipitation, complexation, oxydoréduction) – diagrammes de distribution • Groupes caractéristiques • Types de réactions…

Partie D : de la matière première à la formulation • Séparer : une étape dans l’élaboration d’un métal • Électrolyser : fabriquer, purifier, protéger, embellir • Formuler, conditionner • Récupérer 3 séances

Partie D : un exemple D 1 – Production d’un oxyde, l’alumine, à partir d’un minerai, la bauxite Pourcentage en masse (bauxite rouge de l’Hérault) Al 2 O 3, n H 2 O Fe 2 O 3 Si. O 2 Ti. O 2 54 20 4 3 H 2 O 19

Démarche et objectifs • Expériences simples – comprendre le principe de l’extraction de l’alumine – mettre en évidence l’importance d’une propriété, l’acidobasicité, sur un procédé industriel

Démarche et objectifs • Purification de l’alumine en quatre étapes – dissolution de l’alumine contenue dans le minerai en milieu basique – élimination des impuretés par décantation et filtration – régénération de l’alumine par précipitation de l’hydroxyde d’aluminium – calcination de l’hydroxyde d’aluminium : obtention de l’alumine purifiée

Prolongement expérimental possible dosage de l’élément fer dans la bauxite dissolution de l’alumine décantation et filtration traitement des « impuretés » solides : dissolution en milieu acide de l’oxyde de fer précipitation de l’hydroxyde d’aluminium calcination de l’hydroxyde d’aluminium

Dosage de l’élément fer • Réduction des ions fer(III) en ions fer(II) par le zinc • Titrage d’oxydoréduction par les ions dichromate

Prolongements possibles en activité documentaire • Extraction industrielle de l’alumine à partir de la bauxite : procédé Bayer • Principe de la réduction électrolytique de l’oxyde d’aluminium liquide • L’industrie de l’aluminium, quels risques pour la santé ? • Le tri sélectif des déchets et récupération de l’aluminium

Usine d’aluminium, Gardanne, 15 mai 1898 L’alumine à Gardanne de 1893 à nos jours, P. MIOCHE, PUG 1994

Pour finir… • Le document d’accompagnement à paraître au fur et à mesure http: //membres. lycos. fr/groupexperts ou http: //groupexperts. dyndns. org et prochainement sur le site Eduscol • Appels à contributions davous@ccr. jussieu. fr • Offres de formation : hydrométallurgie, J. L. Vignes, IUFM Créteil
