Chimica generale e inorganica Prof Simone Ciofi Baffoni

Chimica generale e inorganica Prof. Simone Ciofi Baffoni Dipartimento di Chimica & Centro di Ricerca di Risonanze Magnetiche (CERM) Via L. Sacconi 6 50019 Sesto Fiorentino TELEFONO: 055 -4574192 E-mail: ciofi@cerm. unifi. it http: //www. cerm. unifi. it/people/simone-ciofi-baffoni/34 didattica/335 -prof-ciofi-baffoni-corso-di-laurea-inscienze-biologiche Lezioni del Gruppo A (A-L): Aula A presso Scienze Fisiologiche
http: //www. cerm. unifi. it/people/simone-ciofi-baffoni

Struttura del corso Le prove di esame comprendono uno scritto e un orale Durante il corso si faranno due compitini suddivisi in diversi argomenti del corso: i) Il primo si svolgerà a fine novembre ii) Il secondo si svolgerà a inizio gennaio Se entrambi sono superati si accede direttamente all’orale, altrimenti si svolge uno scritto che comprende esercizi relativi al 1° e 2° compitino, una settimana circa prima dell’orale. Superato lo scritto, l’orale deve NECESSARIAMENTE essere svolto all’interno dello stesso appello.

Testi consigliati I. Bertini, C. Luchinat, F. Mani CHIMICA, Seconda Edizione Casa Editrice Ambrosiana I. Bertini, C. Luchinat, F. Mani STECHIOMETRIA, Un avvio allo studio della chimica Casa Editrice Ambrosiana

Programma del Corso I° Parte - La materia: Struttura dell’atomo, Legami chimici, Stati di aggregazione della materia II° Parte – Trasformazione della materia: Reazioni chimiche, Termodinamica, Cinetica chimica, Equilibri chimici in fase gassosa, Equilibri chimici in soluzione, Elettrochimica.

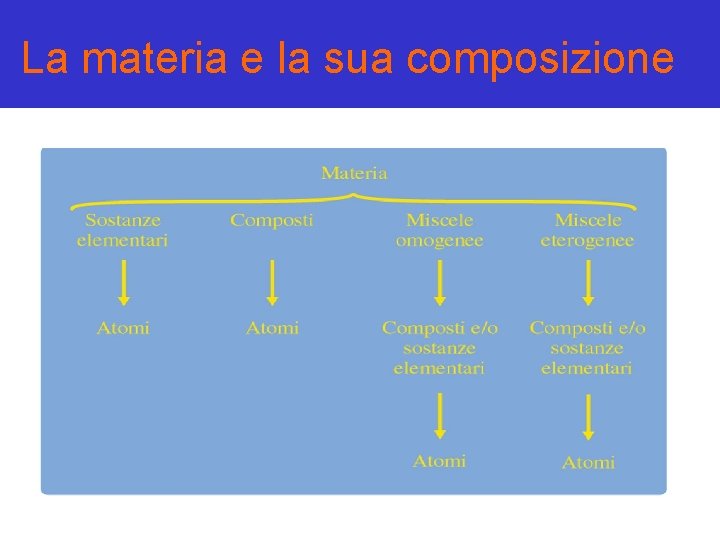
La materia è tutto ciò che possiede massa ed occupa spazio

Le sostanze La materia è costituita da sostanze Quando esse sono formate da atomi di una sola specie atomica si chiamano sostanze elementari Quando esse sono formate da atomi di specie diverse si chiamano sostanze composte o composti

Le miscele La materia è costituita da miscele omogenee o eterogenee di sostanze elementari e/o composti Una miscela omogenea è un sistema monofasico La fase è una parte di un sistema fisicamente definita, ed è caratterizzata da proprietà chimiche e fisiche costanti al suo interno Esempi di miscela omogenea sono l’acqua di mare, l’aria.

La Composizione dell’Atmosfera Componenti Principali, % in volume • • • Azoto (N 2): 78, 08% Ossigeno (O 2): 20, 95% Argon (Ar): 0. 93% Vapore acqueo (H 2 O): 0, 33% Anidride carbonica (CO 2): 0, 032% (320 ppm)

La Composizione dell’Atmosfera Componenti Secondari • • Neon (Ne): 0, 00181% (18 ppm) Elio (He): 0, 0005% (5 ppm) Metano (CH 4): 0, 0002% (2 ppm) Idrogeno (H 2): 0, 00005% (0, 5 ppm) Kripton (Kr): 0, 000011% (0, 11 ppm) Xeno (Xe): 0, 000008% (0, 08 ppm) Ozono (O 3): 0, 000004% (0, 04 ppm) Sono anche presenti, in tracce, Ossidi di azoto (NO, NO 2, N 2 O), Monossido di carbonio (CO), Ammoniaca (NH 3), Biossido di zolfo (SO 2), Solfuro di idrogeno (H 2 S).
La materia e la sua composizione
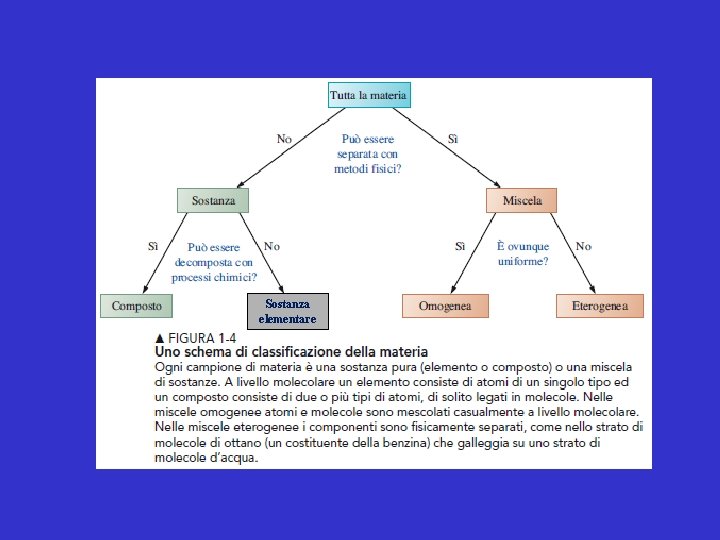
Sostanza elementare

Miscele vs Composti o elementi Miscele omogenee Acciaio Fe-C Composti o elementi Ferro Acqua potabile: H 2 O e sali Acqua marina: H 2 O e Na. Cl Acqua Carbone: C, idrocarburi e altro Carbonio Fe H 2 O C

Teoria atomica della materia Democrito (IV sec a. c. ) La prima teoria atomica è stata formulata dal filosofo greco Democrito, il quale ha affermato che la materia era costituita da piccole particelle indivisibili di tipo diverso, gli atomi (il termine significa proprio indivisibile), e da spazio vuoto. Si tratta di un’ipotesi filosofica, non sostenuta da alcuna verifica sperimentale. Dalton (1808) La teoria atomica proposta da Dalton rispetta i criteri del metodo scientifico in quanto dava una giustificazione alle esperienze, però la prova della reale esistenza degli atomi avvenne in realtà solo un secolo dopo grazie a nuove ricerche di fisici e chimici.

Teoria atomica della materia La teoria di Dalton afferma che: • La materia è costituita da atomi, particelle piccolissime, sferiche, indivisibili e indistruttibili; • Tutti gli atomi di uno stesso elemento sono identici e hanno uguale massa; (quindi: gli atomi dei diversi elementi sono differenti e non hanno la stessa massa) • Gli atomi di un elemento si combinano, per formare un composto, solamente con numeri interi di atomi di altri elementi. • Gli atomi di un elemento non possono essere convertiti in atomi di altri elementi tramite una trasformazione chimica (reazione chimica). • In una reazione chimica gli atomi non sono né creati né distrutti, né trasformati in altri elementi; restano inalterati ma si aggregano in modo diverso, conservandosi interi nel passaggio da un composto all’altro. Quindi, una reazione chimica cambia il rapporto con cui gli atomi si combinano, ma non altera la natura degli atomi

Atomi Gli atomi sono costituiti da particelle subatomiche dette elettroni, protoni e neutroni. Protoni e neutroni formano un minuscolo, denso corpo centrale detto nucleo dell’atomo. Gli elettroni si trovano distribuiti nello spazio intorno al nucleo.
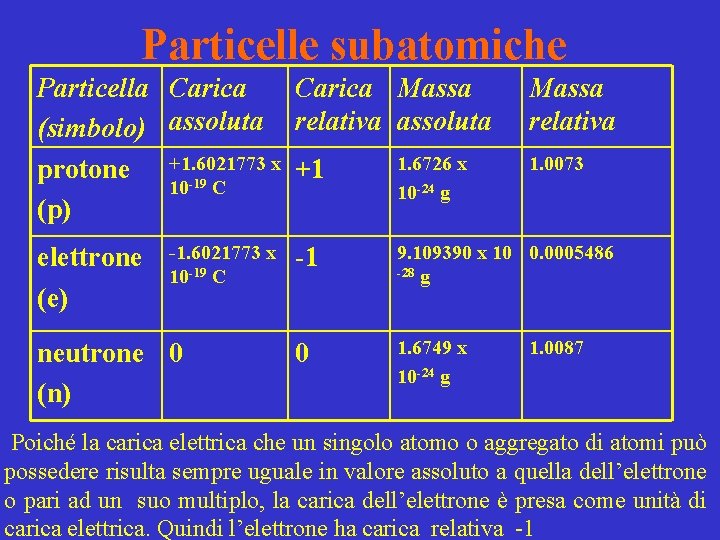
Particelle subatomiche Particella Carica Massa (simbolo) assoluta relativa assoluta 1. 6726 x protone +1. 6021773 x +1 10 -19 C 10 -24 g (p) elettrone (e) -1. 6021773 x 10 -19 C neutrone 0 (n) Massa relativa 1. 0073 -1 9. 109390 x 10 0. 0005486 -28 g 0 1. 6749 x 10 -24 g 1. 0087 Poiché la carica elettrica che un singolo atomo o aggregato di atomi può possedere risulta sempre uguale in valore assoluto a quella dell’elettrone o pari ad un suo multiplo, la carica dell’elettrone è presa come unità di carica elettrica. Quindi l’elettrone ha carica relativa -1

Quark nel protone e nel neutrone In natura, i quark non si trovano mai isolati, ma solo uniti in particelle composte dette adroni, come per esempio il protone e il neutrone. Protoni e neutroni contengono 3 quark ciascuno: • Un protone è composto da 2 quark “Up” (carica 2/3) e un quark “Down” (carica -1/3). • Un neutrone è composto da 1 quark “Up” e 2 quark “Down”.

Struttura dell’atomo • Gli atomi sono costituiti da un nucleo positivo e da elettroni negativi. • Il nucleo ha un raggio di 10 -5 Å. • Il raggio di un atomo è dell'ordine di 1 Å.

Ångstrom simbolo Å -10 1 Ångstrom corrisponde a 10 m Molto usato in chimica perché è dell’ordine di grandezza di un atomo

Gli elementi naturali e artificiali Tutta la materia può essere ricondotta a 90 elementi o specie atomiche diverse, più 22 elementi prodotti artificialmente In Natura si trovano 90 specie atomiche differenti, dette elementi naturali Il primo elemento artificiale sintetizzato in laboratorio fu il tecnezio nel 1937 Gli altri elementi artificiali sono il promezio e i così detti elementi transuranici, cioè gli elementi dal 93 al 112


Nuclidi A Z X Un atomo caratterizzato dal numero atomico Z (numero di protoni) e dal numero di massa A (numero di neutroni e di protoni) è definito un nuclide. Il nuclide neutro ha un numero di elettroni uguale a quello di protoni. Il numero Z caratterizza la specie atomica. 1 H 1 12 C 6 16 O 8 13 C 6

Isotopi Nuclidi con lo stesso Z ma differente A possono esistere e si chiamano isotopi. Una stessa specie atomica ha, di norma, diversi isotopi: si parla di miscela isotopica naturale. Solo 21 elementi sono costituiti da un solo nuclide. 81 specie atomiche hanno almeno un nuclide stabile. Tutti gli isotopi di in elemento hanno le stesse proprietà chimiche 12 C 6 13 C 6 14 C 6

Ioni Un elemento e’ caratterizato dal suo numero atomico Z. Nell’atomo neutro il numero di elettroni è uguale a quello di protoni. Atomi che hanno ceduto o aquistato elettroni rispetto all’atomo neutro si dicono ioni: Catione + Anione -

Sostanze elementari Sono costituite da atomi della stessa specie (stesso numero atomico). He Possono essere formate da: • Singoli atomi • Molecole = aggregati discreti di atomi , cioè unità distinte e separate le une dalle altre, ciascuna delle quali è formata da due o piu’ atomi legati fra loro • Insieme continuo di atomi diamante grafite

Composti Sono costituiti da atomi di specie diverse. Possono essere formati da: proteina • Molecole • Concatenazioni di atomi PVC • Ioni Cloruro di sodio Na+/Cl- DNA

Gli atomi si combinano secondo rapporti definiti per formare composti Formula chimica: deve indicare come minimo quali sono gli elementi che costituiscono la sostanza e in quale rapporto gli atomi di questi elementi si trovano. Questi rapporti fra numeri interi si trovano scritti nelle formule come deponenti a destra del simbolo dell’elemento a cui si riferiscono. H 2 O HCl CO 2 CO

Formula minima e formula molecolare • La formula che arriviamo a scrivere per un composto è detta formula minima (stechiometrica o elementare), ossia le proporzioni minime tra gli elementi di un composto : si ricava dall’analisi elementare della sostanza. Per tutte le sostanze è possibile scrivere una formula minima. • Quando una sostanza elementare o un composto è costituito da molecole, la formula che indica il numero di atomi di ciascun elemento nella molecola è chiamata formula molecolare.

L'analisi elementare • L’ analisi elementare di un composto è la determinazione delle percentuali in massa degli elementi presenti nel composto. Da queste percentuali è possibile risalire alla formula minima; per trovare la vera formula molecolare occorre altro dato sperimentale (spesso si deve determinare la massa molare della sostanza).

Formula molecolare La formula molecolare fornisce piu’ informazioni della formula minima: Non si limita a definire le proporzioni tra gli elementi di un composto, ma specifica il numero esatto di atomi di ciascun elemento facente parte di una molecola del composto. Es. Sostanze elementari P 4, S 8, I 2 Sostanze composte NH 3, CO 2, HNO 3 Alcune sostanze NON sono costituite da molecole discrete ma da una concatenazione continua di atomi e pertanto esse sono identificate dalla sola formula minima: Es: Na. Cl, Ca. Cl 2, Fe, C, Si. O 2

Formula minima e formula molecolare Fe Ne HCl Na. Cl

Le formule delle sostanze FORMULA IONICA: i composti possono essere costituiti da atomi o gruppi di atomi con una carica elettrica risultante. L’insieme di questi gruppi in un composto deve essere tale che la carica risultante totale sia nulla. E’ il caso dei composti salini Per es. la sostanza con formula minima Na. SO 4 è in realtà costituita da ioni Na+ e ioni S 2 O 82 - nel rapporto 2: 1 e quindi la sua formula corretta è Na 2 S 2 O 8 Queste due formule rappresentano la stessa sostanza. Solo una delle due è corretta Quale e perché? H 8 O 4 N 2 S (NH 4)2 SO 4

Le formule delle sostanze FORMULA DI STRUTTURA: Rappresentazione la concatenazione dei legami fra gli atomi e la disposizione degli atomi nello spazio in una molecola CO 2, CH 4, HNO 3

Reazione chimica • La combinazione degli atomi in un composto può cambiare solo quando avviene una reazione chimica • Una reazione chimica cambia il rapporto con cui gli atomi si combinano, ma non altera la natura degli atomi C + O 2 CO 2

Formalismo reagenti a. A + b. B c. C + d. D prodotti Un’equazione chimica rappresenta il più fedelmente possibile il processo reale e quindi la natura delle specie che vi prendono parte. Si devono quindi utilizzare le formule (molecolari o minime) che rappresentano le varie sostanze.

Equazione chimica reagenti a. A + b. B c. C + d. D prodotti Conservazione della massa: la massa totale dei reagenti e dei prodotti non varia durante la reazione. Si deve avere lo stesso numero di atomi per ogni elemento, anche se in composti differenti, in ambedue i membri dell’equazione.

Bilanciamento di reazioni C + O 2 CO 2 N 2 + 3 H 2 2 NH 3 CH 4 + 2 O 2 CO 2 + 2 H 2 O

Coefficiente stechiometrico Il coefficiente stechiometrico di ciascuna specie che compare nella reazione è il numero di molecole o atomi di quella specie, nella reazione così come è stata bilanciata. N 2 + 3 H 2 1/2 N 2 + 3/2 H 2 2 NH 3
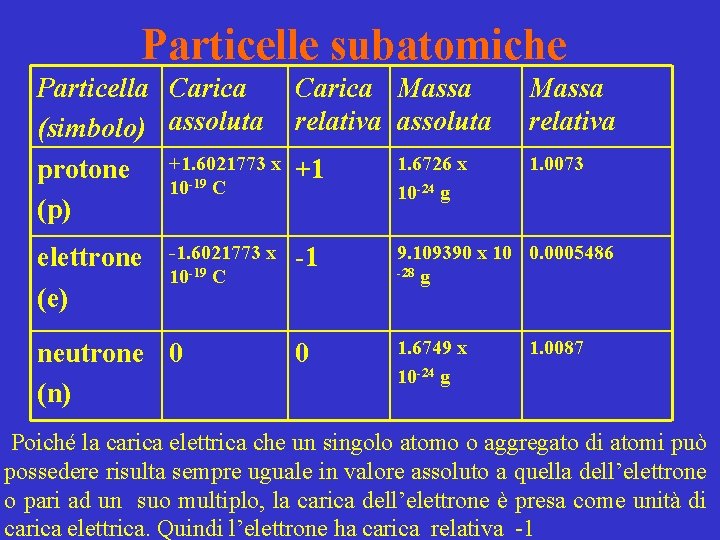
Particelle subatomiche Particella Carica Massa (simbolo) assoluta relativa assoluta 1. 6726 x protone +1. 6021773 x +1 10 -19 C 10 -24 g (p) elettrone (e) -1. 6021773 x 10 -19 C neutrone 0 (n) Massa relativa 1. 0073 -1 9. 109390 x 10 0. 0005486 -28 g 0 1. 6749 x 10 -24 g 1. 0087 Poiché la carica elettrica che un singolo atomo o aggregato di atomi può possedere risulta sempre uguale in valore assoluto a quella dell’elettrone o pari ad un suo multiplo, la carica dell’elettrone è presa come unità di carica elettrica. Quindi l’elettrone ha carica relativa -1
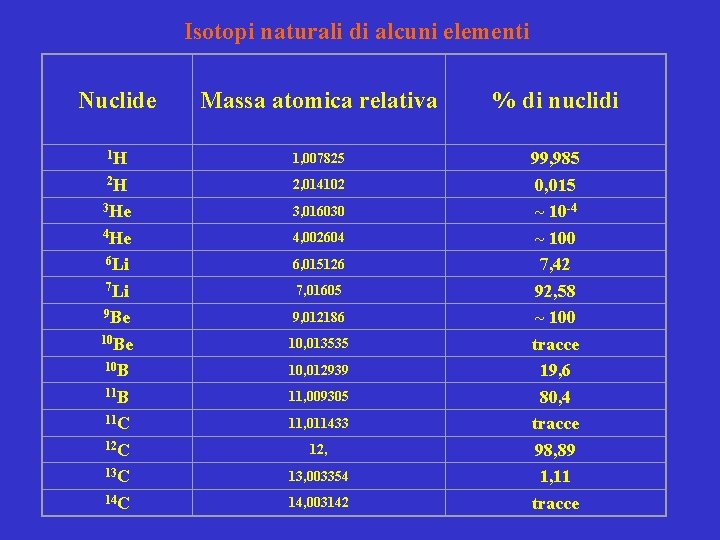
Isotopi naturali di alcuni elementi Nuclide Massa atomica relativa % di nuclidi 1 H 1, 007825 2 H 2, 014102 3 He 3, 016030 4 He 4, 002604 6 Li 6, 015126 7 Li 7, 01605 9 Be 9, 012186 10 Be 10, 013535 10 B 10, 012939 11 B 11, 009305 11 C 11, 011433 12 C 12, 13 C 13, 003354 14 C 14, 003142 99, 985 0, 015 ~ 10 -4 ~ 100 7, 42 92, 58 ~ 100 tracce 19, 6 80, 4 tracce 98, 89 1, 11 tracce

Massa atomica relativa dei nuclidi La massa di un nuclide è troppo piccola rispetto all’unità di misura del kg. Viene quindi definita in rapporto a 1/12 della massa di 12 C è l’unità quella di un nuclide di riferimento = u. m. a. in fisica, dalton (Da) in biologia. E’ una nuova unità di misura della massa 1 u. m. a = 1 Da = 1, 66053782(83) 10 -24 g

Massa atomica relativa dei nuclidi La massa atomica relativa del nuclide 13 C = 13, 003354 è quindi un numero puro che esprime quante volte la massa del nuclide 13 C contiene 1/12 della massa del nuclide 12 C La massa atomica relativa di un atomo di ossigeno è 16 volte l'unità di massa atomica, cioè 16 u, mentre la massa di un atomo di fluoro è circa 19 volte l'unità di massa atomica, cioè 19 u. Pertanto: la massa atomica relativa indica quante volte la massa di un atomo è maggiore rispetto a un dodicesimo della massa del carbonio-12.



Perche’ la massa del 12 C è stata scelta uguale proprio a 12 e non 1, oppure 100?
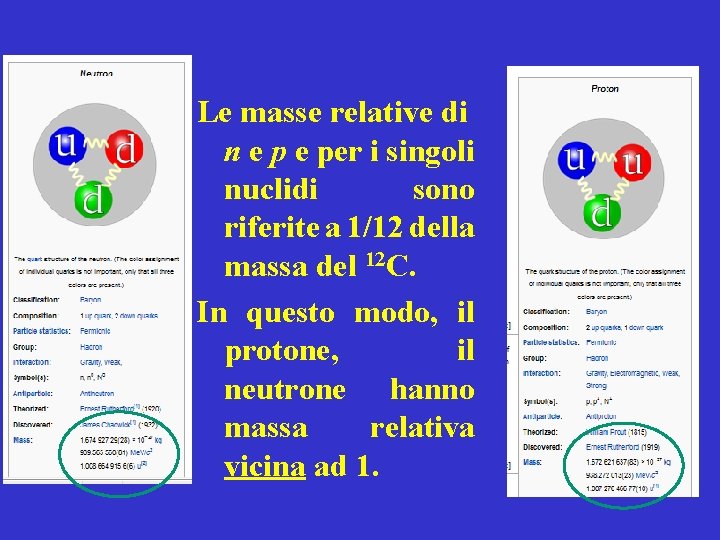
Le masse relative di n e per i singoli nuclidi sono riferite a 1/12 della massa del 12 C. In questo modo, il protone, il neutrone hanno massa relativa vicina ad 1.

La massa dei vari nuclidi è vicina al numero di massa A.

Peso atomico Si definisce peso atomico di un elemento la massa relativa e media di quell'elemento rispetto ad 1/12 della massa di un nuclide di 12 C. Esercizio: Quale é il peso atomico dell’idrogeno?
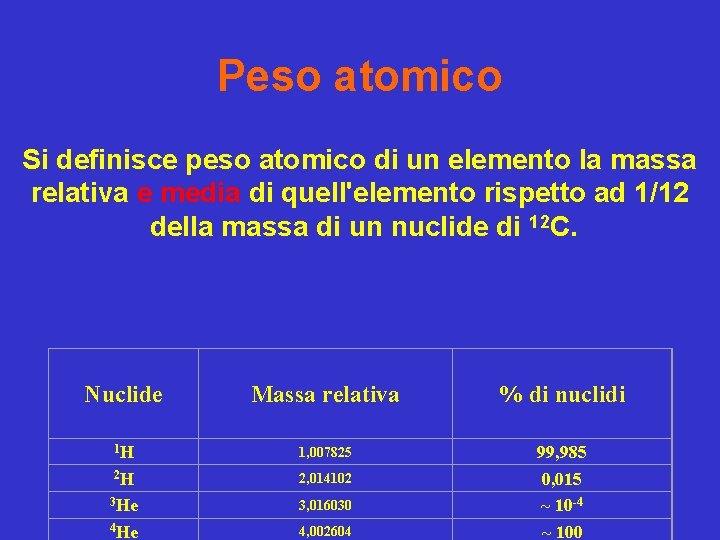
Peso atomico Si definisce peso atomico di un elemento la massa relativa e media di quell'elemento rispetto ad 1/12 della massa di un nuclide di 12 C. Nuclide Massa relativa % di nuclidi 1 H 1, 007825 2 H 2, 014102 3 He 3, 016030 4 He 4, 002604 99, 985 0, 015 ~ 10 -4 ~ 100

Peso atomico Si definisce peso atomico di un elemento la massa relativa e media di quell'elemento rispetto ad 1/12 della massa di un nuclide di 12 C. Il peso atomico dell'idrogeno è: 1, 007825 × 0, 9985 + 2, 014102 × 0, 0015 = 1, 007976 Nuclide Massa relativa % di nuclidi 1 H 1, 007825 2 H 2, 014102 3 He 3, 016030 99, 985 0, 015 ~ 10 -4
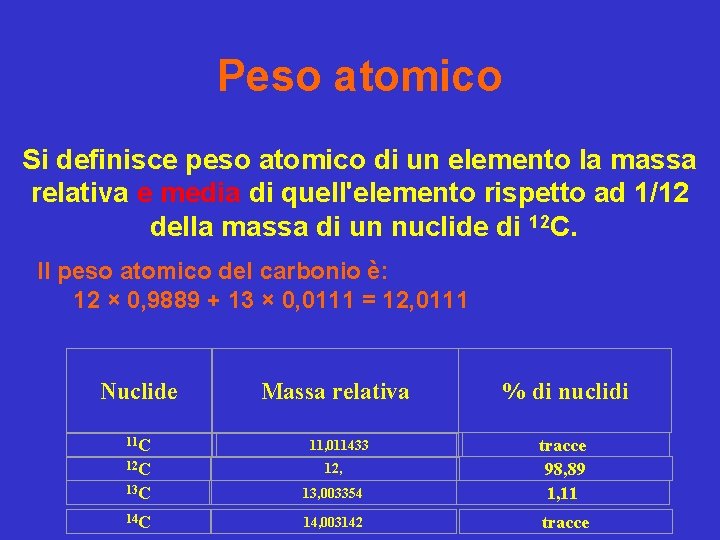
Peso atomico Si definisce peso atomico di un elemento la massa relativa e media di quell'elemento rispetto ad 1/12 della massa di un nuclide di 12 C. Il peso atomico del carbonio è: 12 × 0, 9889 + 13 × 0, 0111 = 12, 0111 Nuclide 11 C Massa relativa % di nuclidi 11, 011433 12 C 12, 13 C 13, 003354 tracce 98, 89 1, 11 14 C 14, 003142 tracce

• Si definisce PESO ATOMICO di un elemento la massa relativa e media di quell'elemento rispetto ad 1/12 della massa di un nuclide di 12 C
Tavola periodica 1, 0078

Peso molecolare: somma dei pesi atomici di tutti gli elementi contenuti in una molecola di una sostanza elementare o di un composto 1. I 2: 126. 9 x 2= 253. 8 2. H 2 SO 4: (1. 00798 x 2) + 32. 064 + (15. 999 x 4) = 98. 076

Quando una sostanza non è formata da molecole discrete ma da un insieme infinito di atomi o ioni, si parla di peso formula 1. Na. Cl: 22. 9898 + 35. 453 = 58. 443 2. K 2 Cr 2 O 7: (39. 10 x 2) + (51. 996 x 2) + (15. 999 x 7) = 294. 2 3. Si. O 2 = 28. 0855 + (2 x 15. 999) = 60. 0835

Peso atomico, peso molecolare, peso formula sono in realtà delle masse. I chimici usano spesso i termini peso atomico (PA) di un elemento al posto di massa atomica (MA) e peso molecolare (PM) di un composto al posto di massa molecolare (MM). Queste dizioni risultano improprie, perchè le quantità in esame sono masse e non pesi.
- Slides: 57