Chimica Analitica Equilibri in soluzione Acidi poliprotici Abbiamo

Chimica Analitica Equilibri in soluzione

Acidi poliprotici Abbiamo visto finora lo sviluppo matematico attraverso il quale, note le costanti di dissociazione di un acido mono-, di- o poli-protico, possiamo ricavare il diagramma di distribuzione. Applicazioni di queste conoscenze riguardano – campo chimico analitico – campo biomedico – campo ambientale – campo industriale

Campo analitico Il primo tipo di applicazione riguarda il campo chimico analitico. Ø Dalle curve di distribuzione possiamo prevedere l’aspetto delle curve di titolazione per un dato acido Ø la conoscenza del tipo di curve di titolazione permette di progettare in modo attendibile la titolazione in laboratorio: scelta dell’indicatore, flessi attesi nel caso di una titolazione potenziometrica, etc.

Campo biomedico Applicazioni importanti si hanno in campo biomedico Ø Un farmaco è una molecola che per esplicare la sua azione con particolari meccanismi biochimici deve arrivare ed agire su un particolare organo (organo bersaglio). Ø La maggior parte dei farmaci sono caratterizzati dalla presenza di gruppi acidi (carbossilici, fenolici, SH etc. ) e/o di gruppi basici (generalmente atomi di azoto sia di gruppi amminici che di raggruppamenti eterociclici).
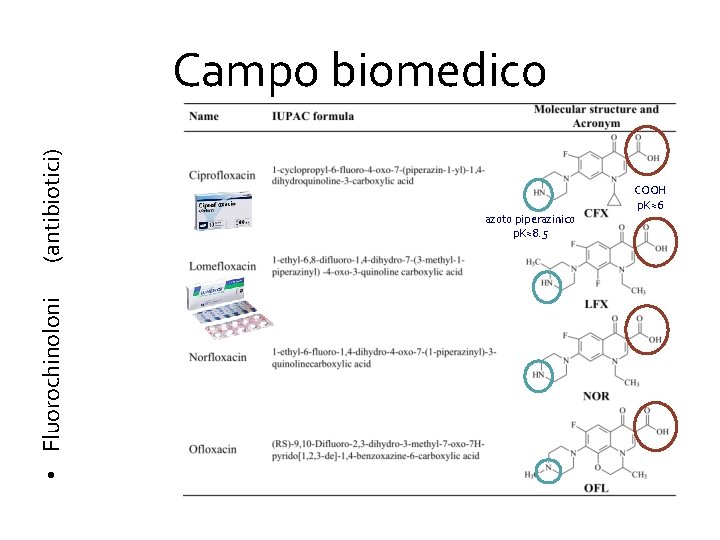
• Fluorochinoloni (antibiotici) Campo biomedico azoto piperazinico p. K≈8. 5 COOH p. K≈6
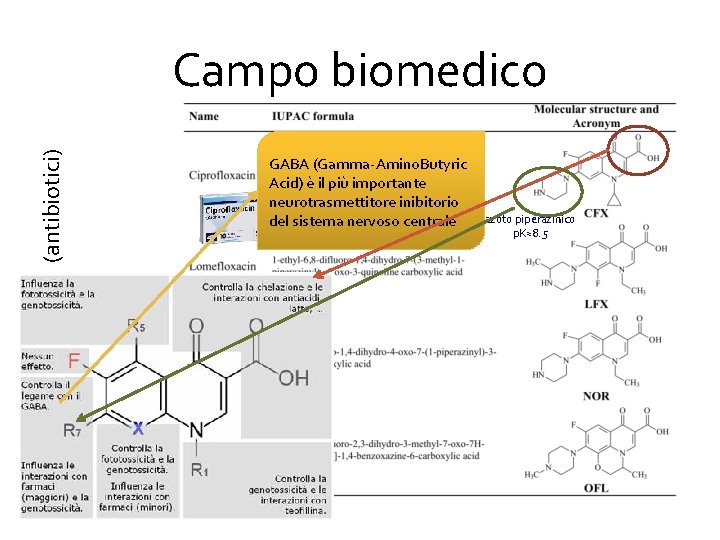
• Fluorochinoloni (antibiotici) Campo biomedico GABA (Gamma-Amino. Butyric Acid) è il più importante neurotrasmettitore inibitorio del sistema nervoso centrale azoto piperazinico p. K≈8. 5
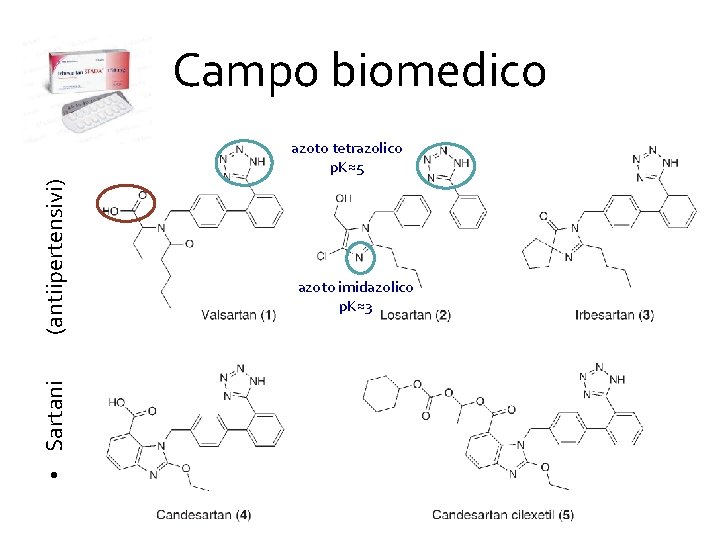
Campo biomedico • Sartani (antiipertensivi) azoto tetrazolico p. K≈5 azoto imidazolico p. K≈3
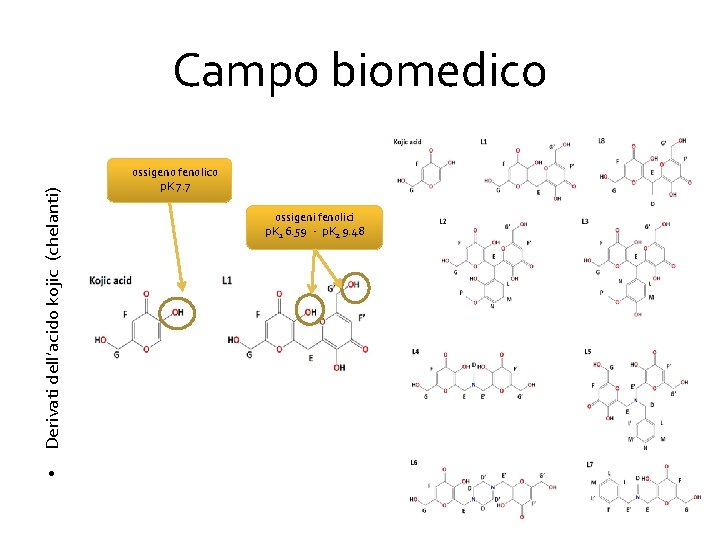
• Derivati dell’acido kojic (chelanti) Campo biomedico ossigeno fenolico p. K 7. 7 ossigeni fenolici p. K 1 6. 59 - p. K 2 9. 48

Acido kojico L’acido Kojico è un inibitore della tirosinasi. La tirosinasi è un enzima contenente rame presente nei tessuti vegetali ed animali che catalizza la produzione di melanina e altri pigmenti per ossidazione della tirosina. L’acido kojico è largamente utilizzato per proteggere dall’imbrunimento i prodotti alimentari quali la carne ed i prodotti a base di carne, la frutta e i suoi derivati. È utilizzato, inoltre, nell’industria cosmetica e in quella farmaceutica.


Campo biomedico Il farmaco per arrivare all’organo bersaglio deve 1 essere assorbito intestinalmente, 2 trasportato attraverso il circolo sanguigno fino all’organo bersaglio, 3 dal sangue deve passare all’interno delle cellule superando le membrane cellulari. Sia l’assorbimento intestinale che l’assorbimento all’interno delle cellule richiedono il passaggio di membrane lipidiche. Perché questo possa avvenire in quantità apprezzabili devono essere soddisfatte diverse condizioni.

Lipinski's rule of five also known as the Pfizer's rule of five or simply the Rule of five (RO 5) is a rule of thumb to evaluate druglikeness or determine if a chemical compound with a certain pharmacological or biological activity has properties that would make it a likely orally active drug in humans. The rule was formulated by Christopher A. Lipinski in 1997. The rule describes molecular properties important for a drug's pharmacokinetics in the human body, including their absorption, distribution, metabolism, and excretion ("ADME"). However, the rule does not predict if a compound is pharmacologically active.

Lipinski's rule of five Le regole di Lipinski ‘Rule of five (RO 5)’ stabiliscono che si può avere un buon assorbimento per via orale di una molecola quando: Coefficiente di ripartizione acqua/ottanolo 1) PM < 500 g/mol; 2) log P <5; 3) < 5 gruppi donatori di protoni per la formazione di legami idrogeno presenti nella molecola (espressi come somma di gruppi OH e NH); 4) < 10 gruppi accettori di protoni per la formazione di legami idrogeno sono presenti nella molecola (espressi come somma di atomi O e N).

Lipinski's rule of five log P <5 Coefficiente di ripartizione acqua/ottanolo La lipofilicità di una molecola è stimata dal coefficiente di ripartizione acquaottanolo (P). Una molecola è tanto più solubile in acqua quanto maggiore è la sua carica, e, viceversa, è tanto più solubile in ottanolo quanto minore è la sua carica. Pertanto quanto maggiore è la carica di una molecola, tanto meno sarà assorbita gastro-intestinalmente e tanto meno sarà capace di attraversare le membrane cellulari.

Campo ambientale Tutti gli ioni metallici a determinati valori di p. H formano degli idrossidi insolubili. La formazione degli idrossidi ha luogo come una reazione di dissociazione acida di acquo-ioni in cui i protoni vengono persi dalle molecole d’acqua di coordinazione.
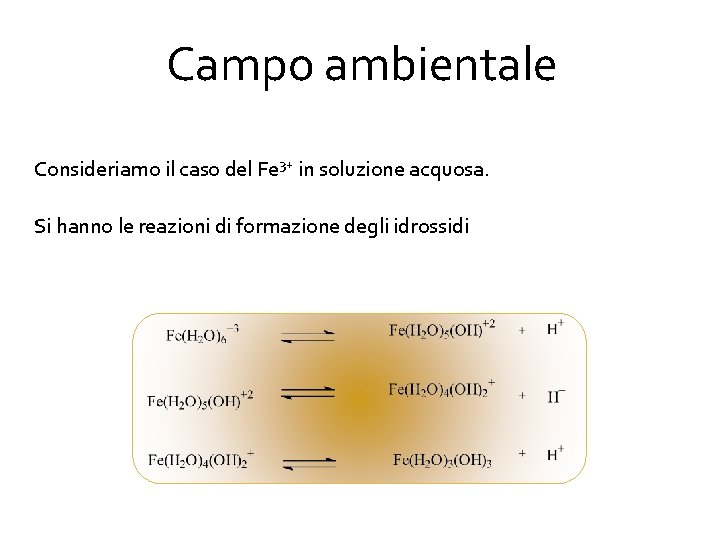
Campo ambientale Consideriamo il caso del Fe 3+ in soluzione acquosa. Si hanno le reazioni di formazione degli idrossidi
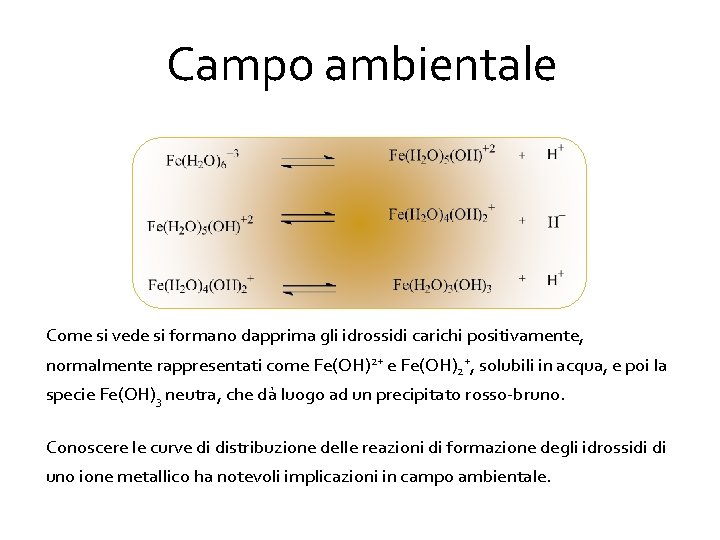
Campo ambientale Come si vede si formano dapprima gli idrossidi carichi positivamente, normalmente rappresentati come Fe(OH)2+, solubili in acqua, e poi la specie Fe(OH)3 neutra, che dà luogo ad un precipitato rosso-bruno. Conoscere le curve di distribuzione delle reazioni di formazione degli idrossidi di uno ione metallico ha notevoli implicazioni in campo ambientale.

Campo ambientale Le reazioni di formazione di idrossidi insolubili trova larga applicazione in campo industriale e ambientale per la rimozione di ioni metallici tossici dai reflui industriali prima del loro riversamento in acque superficiali (fiumi, laghi, mare). Un refluo industriale può contenere diversi ioni metallici tossici e in diverse concentrazioni. Tutti gli ioni metallici sono caratterizzati da una parte da definiti limiti di legge relativi alle acque di scarico, alle acque per uso umano, etc. dall’altra da valori delle costanti degli equilibri di formazione degli idrossidi caratteristici di ogni ione.
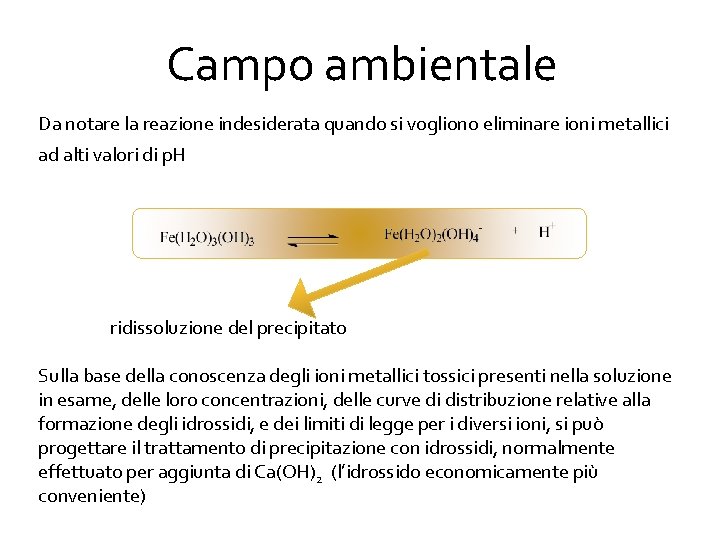
Campo ambientale Da notare la reazione indesiderata quando si vogliono eliminare ioni metallici ad alti valori di p. H ridissoluzione del precipitato Sulla base della conoscenza degli ioni metallici tossici presenti nella soluzione in esame, delle loro concentrazioni, delle curve di distribuzione relative alla formazione degli idrossidi, e dei limiti di legge per i diversi ioni, si può progettare il trattamento di precipitazione con idrossidi, normalmente effettuato per aggiunta di Ca(OH)2 (l’idrossido economicamente più conveniente)

Campo ambientale Consideriamo un refluo industriale contenente una certa quantità di cadmio che deve essere abbattuta per legge a 0. 02 mg/L prima di essere conferito all’esterno dello stabilimento. Per la precipitazione dei metalli in genere si usano le cosiddette vasche a calce. Il prodotto di solubilità dell’idrossido di cadmio è PS = [Cd 2+] x [OH-]2 = 2. 5 x 10 -15 Considerando che il p. H della vasca a calce sia 9, la concentrazione di OH = 10 -5 Il peso atomico del cadmio è 112. 4

Campo ambientale • Limite di legge per il Cadmio = 0. 02 mg/L • PS = [Cd 2+] x [OH-]2 = 2. 5 x 10 -15 • [OH-] = 10 -5 • Peso atomico 112. 4 A p. H 9, la concentrazione di cadmio libero è [Cd 2+] = PS/[OH-]2 [Cd 2+] = 2. 5 x 10 -15/(10 -5)2 = 2. 5 x 10 -5 M [Cd 2+] = (2. 5 x 10 -5 M x 112. 4 g/mol) g/L = 0. 0028 g/L = 2. 8 mg/L
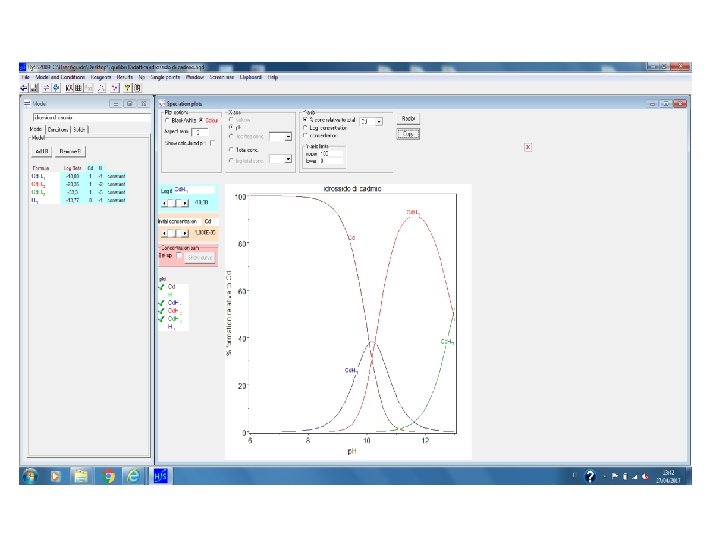
Baes & Messmer, The hydrolysis of cations, Wiley, 1976
Campo ambientale Supponiamo che uno ione metallico tossico sia presente in un corso d’acqua. Dal punto di vista della tossicità sono importanti sia la sua concentrazione, sia le specie in cui si presenta (diversamente protonate, stato d’ossidazione, etc) in funzione delle diverse caratteristiche del sistema (il p. H dell’acqua del fiume, l’ossigeno disciolto, etc ). La tossicità delle diverse specie solubili può essere molto diversa e le specie insolubili che vanno a depositarsi nel fondo del corso d’acqua (sedimento) potrebbero addirittura essere prive di tossicità. Grafico di distribuzione o di speciazione

Campo ambientale

Campo ambientale


Grafico di titolazione Come ricavare la curva di titolazione dalle curve di distribuzione Le curve di distribuzione che abbiamo calcolato servendoci di un foglio Excel, per un acido triprotico, note le costanti di dissociazione, possono essere usate per calcolare il grafico di titolazione. p. H in funzione della quantità di titolante aggiunto

Grafico di titolazione Un grafico di titolazione viene normalmente riportato come p. H verso Vtitolante. Per una migliore valutazione grafica è piu utile riportare il p. H in funzione del rapporto tra le moli di titolante aggiunto e quelle iniziali dell’acido. I flessi relativi ai diversi punti di viraggio cadranno a numeri interi, cioè il primo flesso si avrà ad 1 (dopo l’aggiunta di un numero di moli di titolante uguale al numero di moli di acido totale), il secondo a 2 e così via

Grafico di titolazione Per ottenere il grafico di titolazione facciamo uso della relazione di bilancio di carica, che si esprimerà nella forma [Na+] + [H+] = [OH-] + [H 2 L-] + 2[HL 2 -] + 3[L 3 -] dove [Na+] è la quantità di base aggiunta. La relazione si riarrangia in

Grafico di titolazione Si calcola il rapporto totale nello stesso foglio Excel in cui sono stati calcolati i valori delle frazioni delle varie specie dell’acido. . Nel primo membro a destra bisogna considerare la concentrazione dell’acido totale, per cui come vedremo si ottengono delle curve diverse.
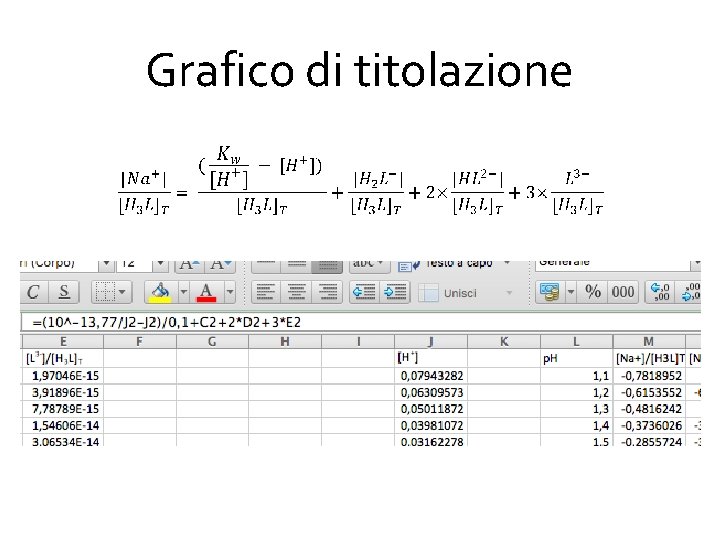
Grafico di titolazione
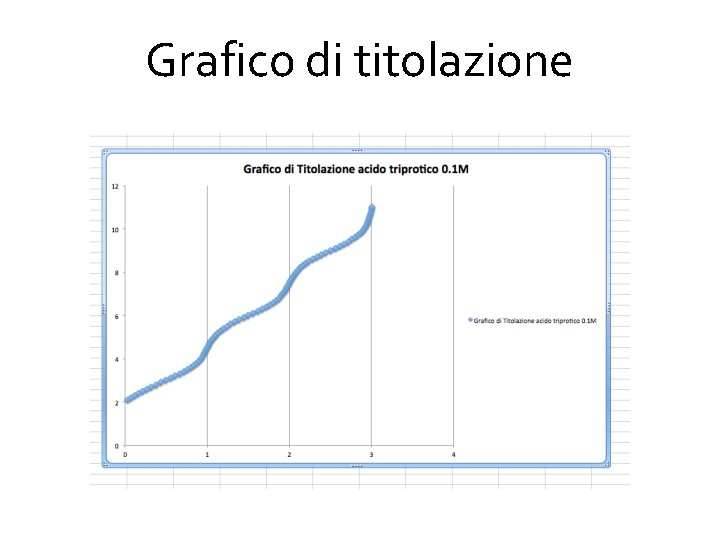
Grafico di titolazione
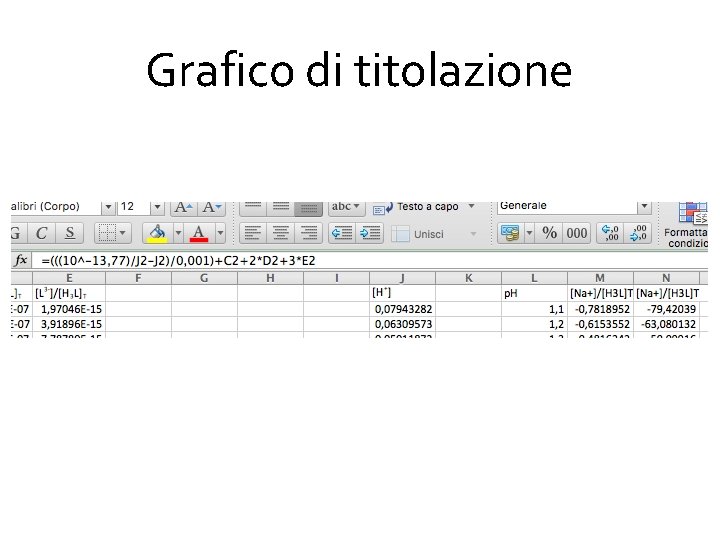
Grafico di titolazione
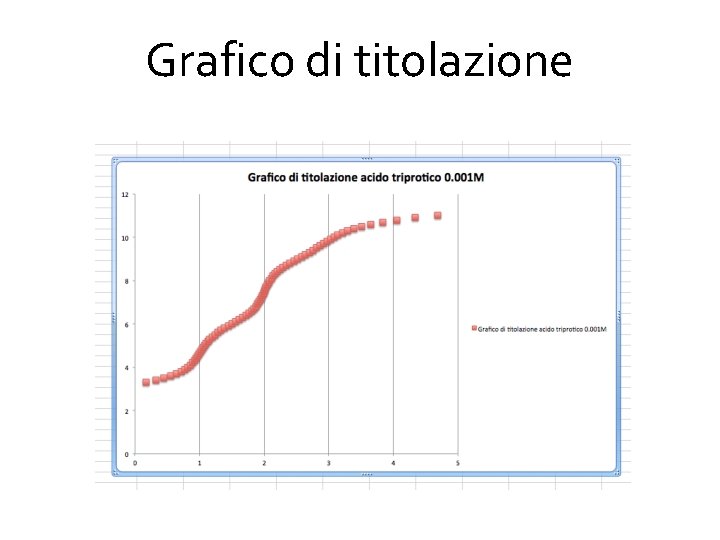
Grafico di titolazione
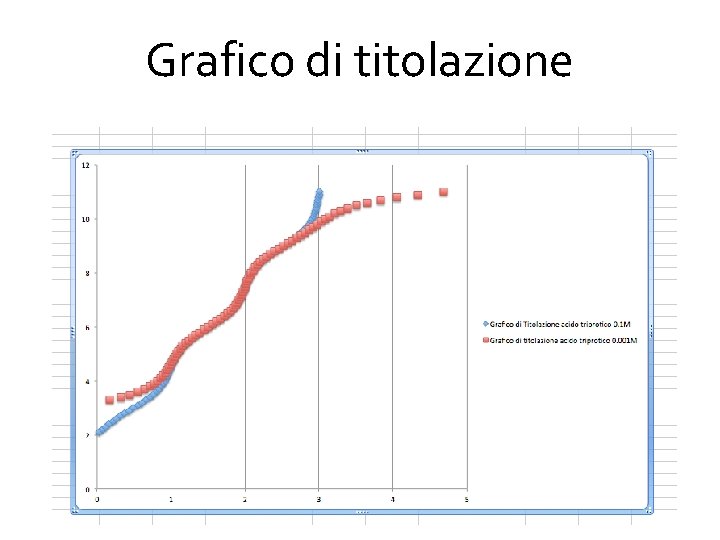
Grafico di titolazione
- Slides: 35