ChemieOlympiade Forschungsthema Der Atombau Stand 21 10 2021
Chemie-Olympiade Forschungsthema: Der Atombau Stand 21. 10. 2021

2

Das ist geschehen Eure Mitforscher John Dalton, Joseph John Thomson und Niels Bohr nehmen momentan an der diesjährigen Chemie. Olympiade teil. Das Forschungsthema, mit dem sie sich beschäftigen, ist der Bau der Atome. Jeder drei Forscher hat ein Atom-Modell entwickelt und euch einen Brief geschrieben, in dem sie jeweils über ihre Erfolge, aber auch Probleme berichten. [1] John Dalton [2] Joseph John Thomson 3 [3] Niels Bohr

4
Mit dieser Kiste kannst du… 1. mehrere Vorstellungen vom Bau des Atoms kennen lernen und 2. sehr viel über den Sinn (und Unsinn) von Modellen erfahren, z. B. warum es überhaupt mehrere Modelle für ein und dasselbe gibt. Hierfür sind keine Vorkenntnisse erforderlich. 5

6

Aufgabe 1 von 3 Findet euch bitte in einer Dreier-Gruppe zusammen. In der Kiste, die euch eure Mitforscher geschickt haben, findet ihr drei Briefe, von Dalton, Thomson und Bohr sowie Baumaterial. Jeder nimmt sich einen anderen Brief, den er für sich alleine liest und die darin enthaltene Aufgabe bearbeitet. Ihr dürft euer Perioden-System der Elemente verwenden. Schreibt eure Überlegungen beim Bauen in das Labor. Tagebuch. 7

8

9
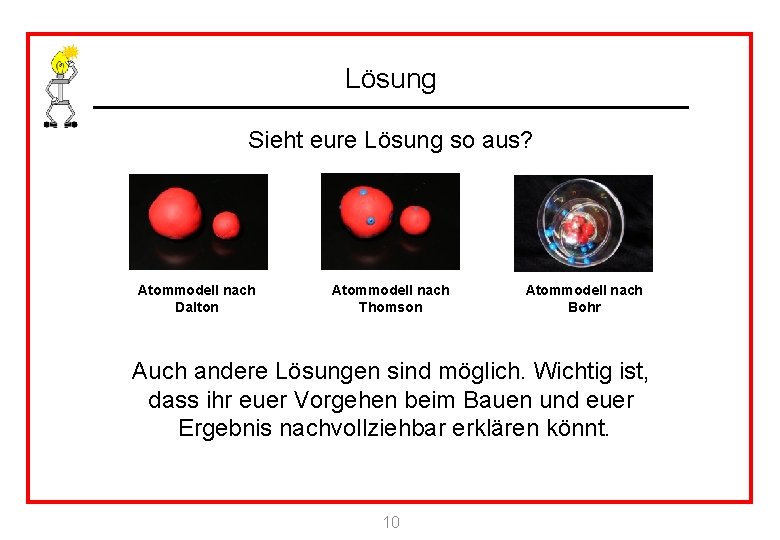
Lösung Sieht eure Lösung so aus? Atommodell nach Dalton Atommodell nach Thomson Atommodell nach Bohr Auch andere Lösungen sind möglich. Wichtig ist, dass ihr euer Vorgehen beim Bauen und euer Ergebnis nachvollziehbar erklären könnt. 10

Aufgabe 2 von 3 Nachdem nun jeder ein Atom-Modell nach der Vorstellung einer eurer drei Mitforscher nachgebaut hat, arbeitet ihr wieder zusammen. Beschreibt jetzt jeweils euer Modell für die beiden anderen Gruppen-Mitglieder. Nehmt dabei das nachgebaute Modell zur Hilfe. Notiert wichtige Modell-Kennzeichen in euer Labor. Tagebuch. 11

12

Aufgabe 3 von 3 Jeder, Dalton, Thomson und Bohr sind der Meinung, dass jeweils ihr Atom-Modell das Beste, das der anderen beiden aber falsch sein. Das ist ein ernsthaftes Problem. Es muss entschieden werden, welches Modell Mess. Ergebnisse oder Eigenschaften von Atomen am besten erklären kann. Diskutiert die drei Modelle in der Gruppe. 13

14
15

Hilfe Vergleicht die drei Modelle nach folgenden Gesichtspunkten: 1. Hilft das Modell, die Abspaltung oder Aufnahme von Elektronen (also die Ionen-Bildung) zu verstehen? 2. Untersuchungen haben gezeigt, dass sich manche Elektronen leichter abspalten lassen als andere. Entscheidet, welches Atom-Modell diesen Befund berücksichtigt. 3. Bei Atomen konnte festgestellt werden, dass sich die Elektronen an bestimmten Stellen häufiger befinden als an anderen. Entscheidet auch hier, welches der Modelle diesen Befund berücksichtigt. 16

17

Lösung 1. Die Modelle von Thomson und Bohr sind hilfreich, das von Dalton nicht. Dalton beschreibt Atome als winzig kleine, unveränderliche und unteilbare Teilchen. 2. Dass sich manche Elektronen leichter abspalten lassen erklärt nur das Modell nach Bohr. Bei Dalton können keine Elektronen abgespalten werden (siehe 1. ). Nach Thomson sind Atome kompakte Kugeln, in denen die positive Ladung gleichmäßig das gesamte Teilchen durchsetzt. Es gibt also keinen Grund, warum manche Elektronen leichter abzuspalten wären. 3. Dass sich Elektronen an manchen Stellen im Atom häufiger befinden, kann keines der Modelle erklären. 18

Die Schwierigkeit mit Modellen Modelle sind nie vollständige Abbilder Wirklichkeit: sie können immer nur einen Teil darstellen bzw. erklären. Ein Modell ist dann hilfreich, wenn man damit das, was einen gerade interessiert, erklären kann. Es ist nicht hilfreich, wenn es bei dieser Erklärung zu Widersprüchen kommt. Modelle sind selten wirklich falsch. Interessieren andere Gesichtspunkte, so kann eben ein anderes Modell hilfreich sein. Kein Modell kann alles erklären. Daher ist kein Modell immer und unter allen Umständen hilfreich. Deswegen können mehrere Modelle nützlich sein. Diese Aussage lässt sich auf alle Arten von Modellen verallgemeinern. 19

20

Das sollte bleiben: 1. Daltons Modell ist hilfreich, wenn man sich die drei Aggregat-Zustände erklären möchte. 2. Bohrs Modell hilft zu verstehen, warum bei der Bildung von Ionen nur bestimmte entstehen, z. B. Al 3+ und nicht Al 2+ oder Al 5+. 3. Dass sich Elektronen an manchen Stellen im Atom häufiger befinden, kann keines der drei Modelle erklären. Schlussfolgerung: Es muss mindestens noch ein anderes Modell geben, in das man den Befund 3 einarbeiten muss. 21

22

Teste dich selbst Geht nun geschlossen in der Gruppe zu eurem Betreuer und nehmt die gebauten Modelle mit. Dort findet ihr ein weiteres Atom-Modell, so wie es sich vor etwa 70 Jahren George Elbert Kimball gedacht hatte. Beurteilt dieses neue Modell nach denselben Kriterien wie vorhin. Notiert das Ergebnis im Labor-Tagebuch. 23

24

Teste dich selbst Verfasst bitte jeder einen Antwort-Brief an seinen Forscher. Beantwortet erst seine Fragen aus dem Brief. Beschreibt dann kurz die drei anderen Modelle und fertigt jeweils eine einfache Skizze an. Die Briefe könnt ihr eurem Betreuer geben, damit sie an Dalton, Thomson und Bohr weiter geleitet werden . Räumt die Materialien bitte wieder an ihren Platz in die Kiste. 25

26

Selbsteinschätzung Ordne dich gedanklich einem Smiley zu. Wie sicher kannst du entscheiden, für welche Erklärung die drei Atom-Modelle jeweils hilfreich sind? • Hast du ein grünes Smiley gewählt, freu dich, alles perfekt. • Hast du ein gelbes Smiley gewählt, geh nochmals die Briefe durch oder berate dich mit deinen Gruppenmitgliedern. • Hast du ein rotes Smiley gewählt, frag den Betreuer nach einem Rat. 27

28

Diese Anleitung wurde gefertigt von Marie-Madeleine Böhm. Im Rahmen der Arbeit zur Zulassung zum Ersten Staatsexamen, gefertigt in der Abteilung für Didaktik der Chemie an der Universität Bayreuth. Quellen: J. Söllner http: //daten. didaktikchemie. uni-bayreuth. de/umethoden/0_einf. htm, Stand 24. 09. 2013 E. Wawra, H. Dolzing, E. Müllner: Chemie verstehen, 5. Aufl. UTB, 2009, S. 14 -15 Bildnachweis: [1]: http: //loc. gov/pictures/resource/cph. 3 b 12511/; Stand 04. 07. 2016 [2]: https: //commons. wikimedia. org/wiki/File: Jj-thomson 2. jpg? uselang=de; Stand 13. 06. 2016 [3]: http: //schools-wikipedia. org/images/319301. jpg. htm; Stand 04. 07. 2013 Alle weiteren Bilder und Graphiken wurden in der Abteilung Didaktik der Chemie, Universität Bayreuth erstellt. 29
- Slides: 29