CHEMIEGESCHICHTE bersicht 1 Alchemie 2 Von der Alchemie

CHEMIEGESCHICHTE

Übersicht 1. Alchemie 2. Von der Alchemie zur modernen Chemie 3. Öffentliche Schaustellungen 4. Feuer 5. Schulrelevanz
1. ALCHEMIE

1. Alchemie • Alchemie vom arabischen Wort "al kymia" = "Kunst der Ägypter" oder vom griechischen Wort "χυμεία" (chymeia) = "Lehre des Gießens" • Entstehung im 1. Jhd. n. Chr. in Ägypten (Alexandria)
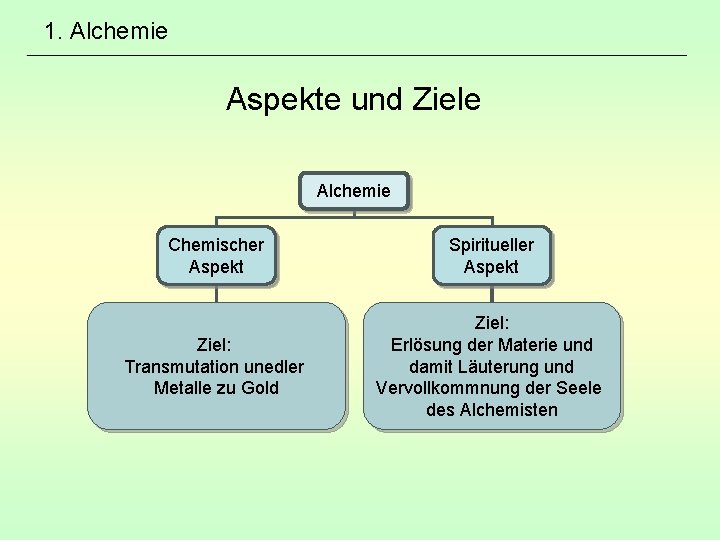
1. Alchemie Aspekte und Ziele Alchemie Chemischer Aspekt Spiritueller Aspekt Ziel: Transmutation unedler Metalle zu Gold Ziel: Erlösung der Materie und damit Läuterung und Vervollkommnung der Seele des Alchemisten
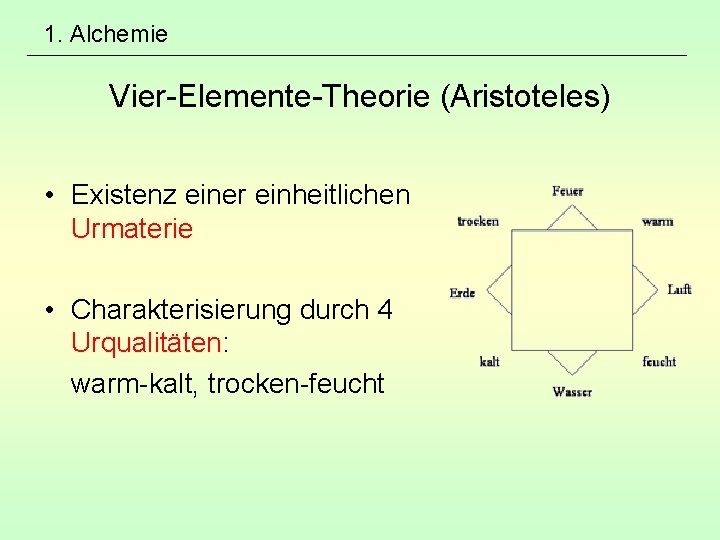
1. Alchemie Vier-Elemente-Theorie (Aristoteles) • Existenz einer einheitlichen Urmaterie • Charakterisierung durch 4 Urqualitäten: warm-kalt, trocken-feucht
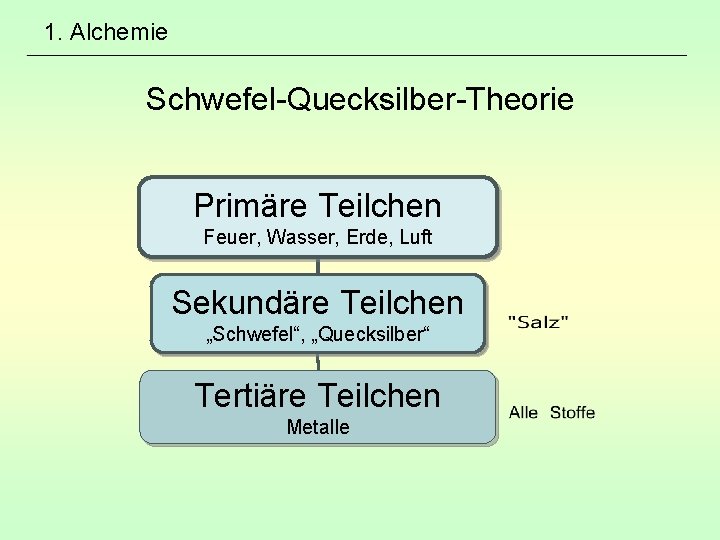
1. Alchemie Schwefel-Quecksilber-Theorie Primäre Teilchen Feuer, Wasser, Erde, Luft Sekundäre Teilchen „Schwefel“, „Quecksilber“ Tertiäre Teilchen Metalle
1. Alchemie Deutung chemischer Reaktionen • Die Eigenschaften von Stoffen Prinzipien • Übertragung/Austausch von Prinzipien Änderung der stofflichen Qualitäten
1. Alchemie Der Stein der Weisen • Substanz, mit welcher die Transmutation gelingen soll • Träger der richtigen Qualitäten Folgende Eigenschaften müssen erfüllt sein: Färben Eindringen Fixieren

1. Alchemie Entdeckungen • Neben den schon im Altertum bekannten Elementen entdeckten die Alchemisten u. a. : – As (13. Jhd. Albertus Magnus) – Zn (13. Jhd. ) – P (17. Jhd. Henning Brand) • wiederentdeckt wurde: – Porzellan (17. Jhd. Johann Friedrich Böttger) – Schwarzpulver

1. Alchemie Stoffklassifikation und -kennzeichnung • Stoffklassifikation: Somata, Asomata, Pneumata • Kennzeichnung mittels Symbolen ohne Einheitlichkeit • Symbole spiegeln oft Analogievorstellungen wieder Element Gold Silber Au Ag Alchemistisches Symbol Heutiges Symbol

1. Alchemie in Europa • Einführung: 12. Jhd. durch Araber • Um 1250: weitere Verbreitung nach Erscheinung von „De mineralibus“ (Albertus Magnus) • Spätes 13. Jhd. : Verbot und Verfolgung durch katholische Kirche • bis 18. Jhd. : Interesse an Alchemie
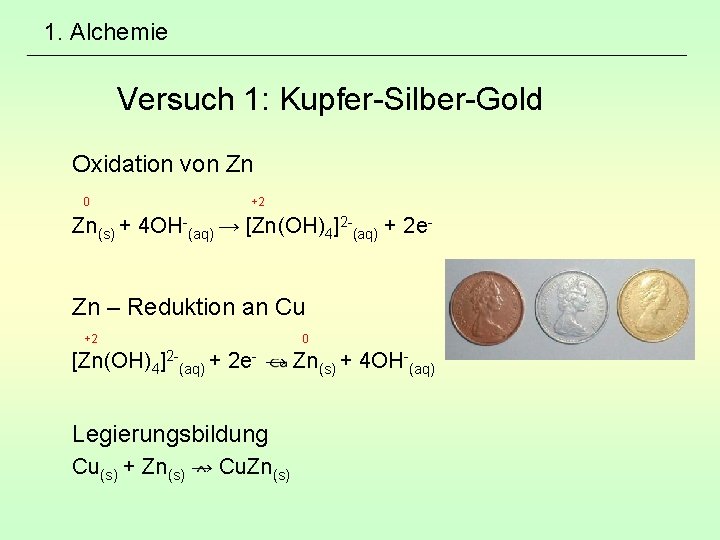
1. Alchemie Versuch 1: Kupfer-Silber-Gold Oxidation von Zn 0 +2 Zn(s) + 4 OH-(aq) → [Zn(OH)4]2 -(aq) + 2 e- Zn – Reduktion an Cu +2 0 [Zn(OH)4]2 -(aq) + 2 e- → Zn(s) + 4 OH-(aq) Legierungsbildung Cu(s) + Zn(s) → Cu. Zn(s)

2. VON DER ALCHEMIE ZUR MODERNEN CHEMIE

2. Von der Alchemie zur modernen Chemie Chemiatrie (Iatrochemie) • Begründer: Paracelsus (1493 – 1541) (Theophrast von Hohenheim) • Neue Zielsetzung der Chemie: – Kein Gold, sondern Medizin • Krankheit: Überfluss oder Mangel chemischer Prinzipien im Körper Folge: Chemisches Experiment im Mittelpunkt

2. Von der Alchemie zur modernen Chemie Zweifel an der chemischen Theorie • Robert Boyle (1627 -1691) • Ziel: Verifizierung alchemistischer Theorien mittels chem. Experiment • Diskussion der Ergebnisse in „The sceptical Chymist“ („Der skeptische Chemiker“ 1661) • Ergebnis: chemische Lehre ist unzulänglich

2. Von der Alchemie zur modernen Chemie Phlogistontheorie • Begründer: Georg Ernst Stahl (1660 – 1734) • Redox-Theorie • Phlogiston: „Feuerstoff“ Unterform des Elements Erde

2. Von der Alchemie zur modernen Chemie Deutung von Redox-Reaktionen 1. Verbrennung: Holz → Asche + Phlogiston Je besser ein Stoff brennt, desto mehr Phlogiston enthält er 2. Metallverkalkung und -reduktion : Metall → Phlogiston + Metallkalk + Phlogiston → Metall

2. Von der Alchemie zur modernen Chemie Phlogiston und gasförmige Stoffe • Isolierungsversuche Entdeckung gasförmiger Stoffe – Joseph Priestley (1733 – 1804): O 2, SO 2, CO, Stickoxide – Henry Cavendish (1731 – 1810): H 2 – Carl-Wilhelm Scheel (1742 – 1786): N 2, Cl 2, HCl(g), H 2 S
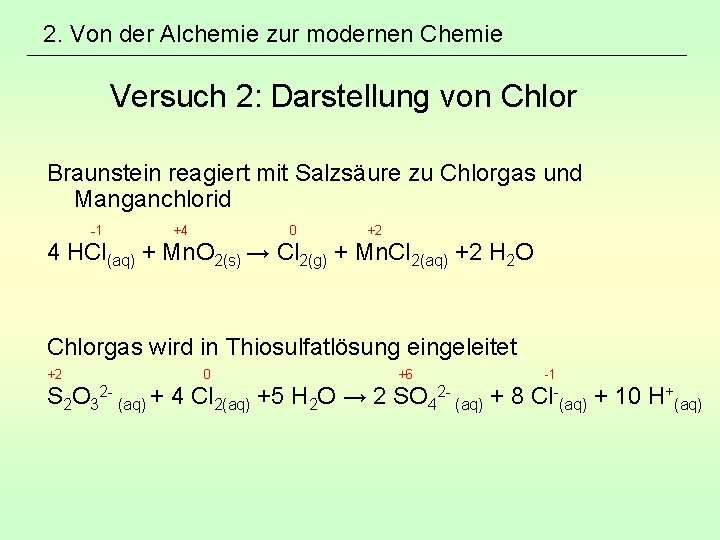
2. Von der Alchemie zur modernen Chemie Versuch 2: Darstellung von Chlor Braunstein reagiert mit Salzsäure zu Chlorgas und Manganchlorid -1 +4 0 +2 4 HCl(aq) + Mn. O 2(s) → Cl 2(g) + Mn. Cl 2(aq) +2 H 2 O Chlorgas wird in Thiosulfatlösung eingeleitet +2 0 +6 -1 S 2 O 32 - (aq) + 4 Cl 2(aq) +5 H 2 O → 2 SO 42 - (aq) + 8 Cl-(aq) + 10 H+(aq)

2. Von der Alchemie zur modernen Chemie Versuch 3: Verbrennen von Eisenwolle Eisen wird oxidiert 0 0 +3 +2 +3 -2 3 Fe + 2 O 2 → Fe(Fe. Fe)O 4 Beobachtung: Die Masse des Eisenoxids ist höher als die des Eisens.

2. Von der Alchemie zur modernen Chemie Problem der Theorie • Wieso nimmt die Masse zu, obwohl Phlogiston das Metall verlässt? Lösungsansätze • Stahl: „negatives Gewicht“ des Phlogistons • Boyle: Aufnahme von Feuerteilchen

2. Von der Alchemie zur modernen Chemie Die Rolle des Sauerstoffs bei der Verbrennung • abgeschl. Raum: bis 1/5 Luft verbraucht • Vakuum: Sublimation • Reduktion von Quecksilberoxid Sauerstoff • Reaktion: Wasserstoff und Sauerstoff Wasser

2. Von der Alchemie zur modernen Chemie • Vermutung von Antoine Laurent de Lavoisier (1743 – 1794): Sauerst off verbindet sich mit der verbrennenden Substanz • Widerspruch zu Boyles Erkenntnis • Wiederholung Boyles Versuche keine Gewichtszunahme feststellbar

2. Von der Alchemie zur modernen Chemie Gesetz der Erhaltung der Masse (Lomonossow/Lavoisier) „Im Verlauf einer chemischen Reaktion lässt sich kein Verlust oder Gewinn von Masse beobachten; die Gesamtmasse aller reagierenden Stoffe ist gleich der Gesamtmasse aller Produkte“

2. Von der Alchemie zur modernen Chemie Deutung von Redox-Reaktionen 1. Verbrennung: Holz + Sauerstoff → Asche + Kohlenstoffoxid + Wärmestoff 2. Metallverkalkung und -reduktion Metall + Sauerstoff → Metallkalk + Wärmestoff Metallkalk + Kohle → Metall + Kohlenstoffoxid

2. Von der Alchemie zur modernen Chemie Wasser ist kein Element • Bei Verbrennung von „air inflammable“ (Wasserstoff) entsteht Wasser • Vermutung: Wasser ist kein Element • Beweis: Zersetzung des Wassers und Nachweis des Wasserstoffs
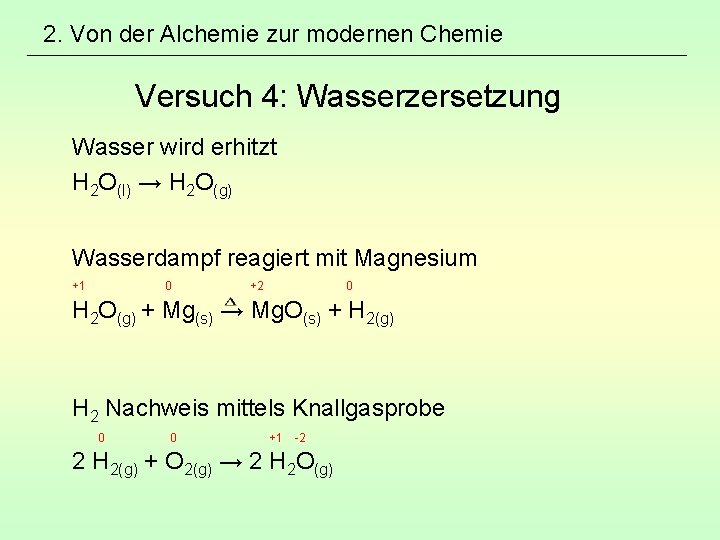
2. Von der Alchemie zur modernen Chemie Versuch 4: Wasserzersetzung Wasser wird erhitzt H 2 O(l) → H 2 O(g) Wasserdampf reagiert mit Magnesium +1 0 +2 0 H 2 O(g) + Mg(s) → Mg. O(s) + H 2(g) H 2 Nachweis mittels Knallgasprobe 0 0 +1 -2 2 H 2(g) + O 2(g) → 2 H 2 O(g)

2. Von der Alchemie zur modernen Chemie Wasserzersetzung nach Lavoisier

4. ÖFFENTLICHE SCHAUSTELLUNGEN

3. Öffentliche Schaustellungen Jahrmarkt • Jahrmarkt: wichtige Institution früherer Jahrhunderte • Versorgung mit Waren, ärztlicher Hilfe, Medikamenten und Unterhaltung • Unterhaltung: Quacksalber Darbietung chemischer Experimente

3. Öffentliche Schaustellungen Öffentliche Experimentalvorlesungen • Ausgehendes 18. und 19. Jhd. : gesellschaftliches Interesse an Naturwissenschaften • pompöse, theatralische Experimentalvorlesungen Einfluss von Jahrmarktschemie • Etablierung in Deutschland: Justus Liebig (1803 – 1873) Ziel: Naturwissenschaften als Allgemeinbildung

3. Öffentliche Schaustellungen • Lavoisier: Verbrennung eines Diamanten auf offener Straße • Zuvor Nachweis im Labor Diamant ist Kohlenstoff

3. Öffentliche Schaustellungen Versuch 5: Verbrennung von Graphit wird oxidiert 0 0 +4 -2 C(s) + O 2(g) → CO 2(g) CO 2 -Nachweis mittels Calciumhydroxidlösung CO 2(g) + Ca(OH)2(aq) → Ca. CO 3(s) + H 2 O

4. FEUER

4. 2 Erfindung des Feuerzeugs Feuer im Altertum Feuererzeugung mittels - Feuerquirl/ Bogenfeuerbohrer (reiben von Hartholzstäbchen in weichem Holz) - Feuerstein und leicht brennbares Material (z. B. Zunder)

4. 2 Erfindung des Feuerzeugs Tunkhölzer • Erfinder: Chancel 1805 in Paris • Zündköpfe: Kaliumchlorat, Schwefel und Gummi-Arabikum • Eintauchen in Schwefelsäure Zündung • Verschwanden mit der Erfindung der Sicherheitshölzer
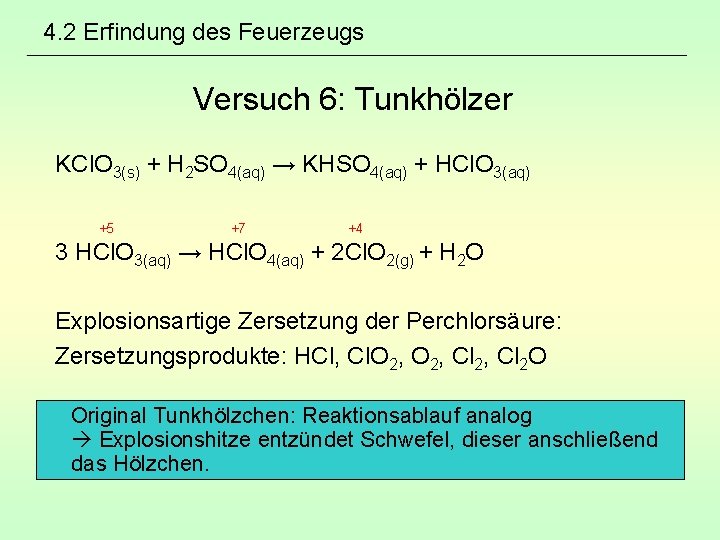
4. 2 Erfindung des Feuerzeugs Versuch 6: Tunkhölzer KCl. O 3(s) + H 2 SO 4(aq) → KHSO 4(aq) + HCl. O 3(aq) +5 +7 +4 3 HCl. O 3(aq) → HCl. O 4(aq) + 2 Cl. O 2(g) + H 2 O Explosionsartige Zersetzung der Perchlorsäure: Zersetzungsprodukte: HCl, Cl. O 2, Cl 2 O Original Tunkhölzchen: Reaktionsablauf analog Explosionshitze entzündet Schwefel, dieser anschließend das Hölzchen.

5. Schulrelevanz • Historisch entwickelnder Einstieg • Wecken von Interesse an Chemie • Nachvollziehen von Entwicklungen, um größeres Verständnis zu entwickeln • Geschichte im Lehrplan – – Die chemische Reaktion Elementgruppen Elektrolyse und Ionenbegriff Atombau, Periodensystem und Ionenbindung

ENDE

ZUSATZMATERIAL

Alchemie • Im Altertum bekannte Elemente: – C, S, Cu, Ag, Fe, Sn, Sb, Hg, Pb, Bi, Pt, Au
![Alchemie [Zn(OH)4]2 - diffundiert in das Cu-Gitter und wird dort reduziert. Grund: E([Zn(OH)4]2 -|Zn. Alchemie [Zn(OH)4]2 - diffundiert in das Cu-Gitter und wird dort reduziert. Grund: E([Zn(OH)4]2 -|Zn.](http://slidetodoc.com/presentation_image_h2/873ca10aaaf8bd304c76232ed1c25fc8/image-43.jpg)
Alchemie [Zn(OH)4]2 - diffundiert in das Cu-Gitter und wird dort reduziert. Grund: E([Zn(OH)4]2 -|Zn. Cu) > E([Zn(OH)4]2 -|Zn. Zn) • Triebkraft: Oberflächenlegierungsbildung
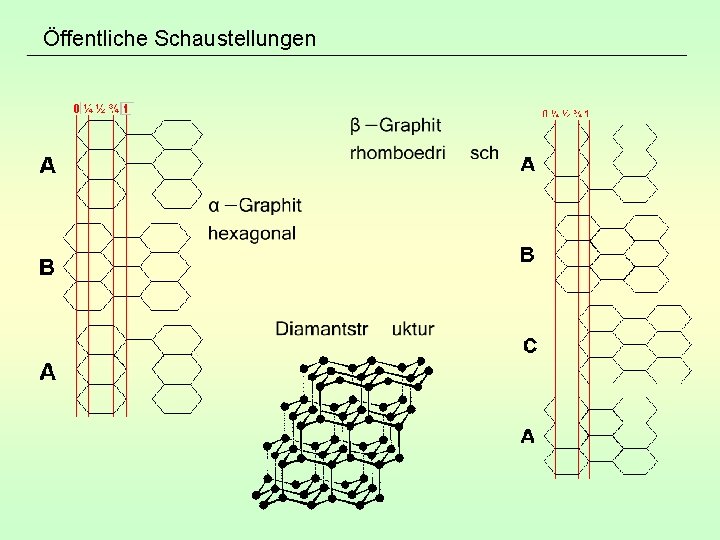
Öffentliche Schaustellungen

Erfindung des Feuerzeugs Döbereiner Feuerzeug • Johann Wolfgang Döbereiner (1780 – 1849) • Erforschung Wirkung von Platin auf Flüssigkeiten und Gase • Kenntniss von Lavoiers Wasserzersetzungsexperiment und dessen Synthese aus Wasserstoff und Sauerstoff • 27. 07. 1823 Entzündung von Knallgas an Platinoberfläche

Erfindung des Feuerzeugs Döbereiner Feuerzeug • 03. 08. 1823: Entwicklung des Döbereiner Feuerzeugs
- Slides: 46