Chemick vazba VY32 INOVACECHE18 AUTOR Ing Ladislava Semerdov

Chemická vazba VY-32 -INOVACE-CHE-18 AUTOR: Ing. Ladislava Semerádová ANOTACE: Výukový materiál je určen pro studenty 1. ročníku SŠ. Může být použit při výkladu teorie chemické vazby KLÍČOVÁ SLOVA: nepolární, polární kovalentní vazba, iontová vazba, kovová vazby, elektronegativita

Chemická vazba: • Soudržné síly mezi atomy v chemických látkách • Vzniká tehdy, má-li nové seskupení atomů menší energii než jednotlivé atomy Disociační energie (vazebná energie) • Energie nutná k rozrušení chemické vazby

Elektronegativita X • vlastnost atomu, vyjadřující jeho schopnost přitahovat vazebné elektrony • bezrozměrná relativní veličina • označení X • nejvyšší X má atom fluoru X(F) = 4 • všechny ostatní prvky se k němu vztahují
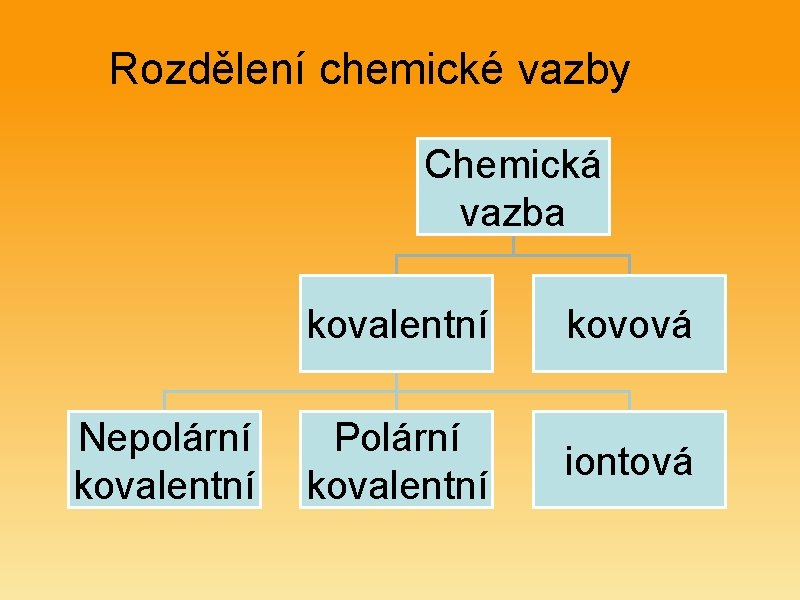
Rozdělení chemické vazby Chemická vazba Nepolární kovalentní kovová Polární kovalentní iontová

1. Kovalentní vazba • pokud se dva atomy k sobě přiblíží na vzdálenost řádově pm(10 -12 m) začne na valenční elektrony každého z atomů působit přitažlivá síla druhého jádra • některé z valenčních elektronů začnou atomy sdílet • sdílené elektrony se pohybují v okolí obou jader a v oblasti mezi jádry • celková energie se tím zmenší • sdílení elektronů představuje chemickou vazbu

Druhy kovalentních vazeb Společně sdílené elektronové páry mohou být mezi atomy rozloženy: • A) rovnoměrně –oba atomy jsou přibližně stejně „silné“ – mají podobnou hodnotu elektronegativity – vytváří nepolární kovalentní vazbu • B) společný elektronový pár je deformován a je přesunut směrem k „silnějšímu“ atomu (má větší hodnotu elektronegativity) – vniká vazba polární kovalentní • C) jeden z atomů je natolik silný, že elektron s druhým atomem nesdílí, ale odejme jej – vniká vazba iontová
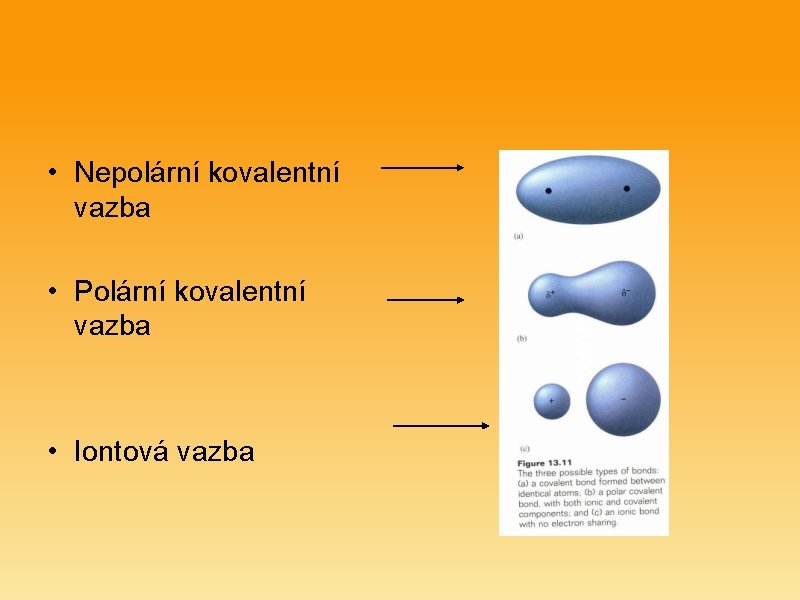
• Nepolární kovalentní vazba • Polární kovalentní vazba • Iontová vazba

1. 1. Nepolární kovalentní vazba • Rozdíl elektronegativity ( X) mezi atomy je menší než 0, 4 • X < 0, 4 • Sdílené elektronové páry jsou mezi atomy rozloženy rovnoměrně • molekula Cl 2

1. 2. Polární kovalentní • Pokud je rozdíl elektronegativit • 0, 4 < X < 1, 7 • Je vazebný elektronový pár již zřetelněji posunut k elektronegativnějšímu atomu • Vznik molekuly HCl 1 H 1 s • 1 2 3 p 5 Cl [ He ] 3 s 2 • 17

• Vzniklé molekuly mají elektrický dipól • V oblasti atomu s vyšší X se projevuje částečný(parciální) záporný náboj • V oblasti atomu s menší X vzniká parciální kladný náboj +
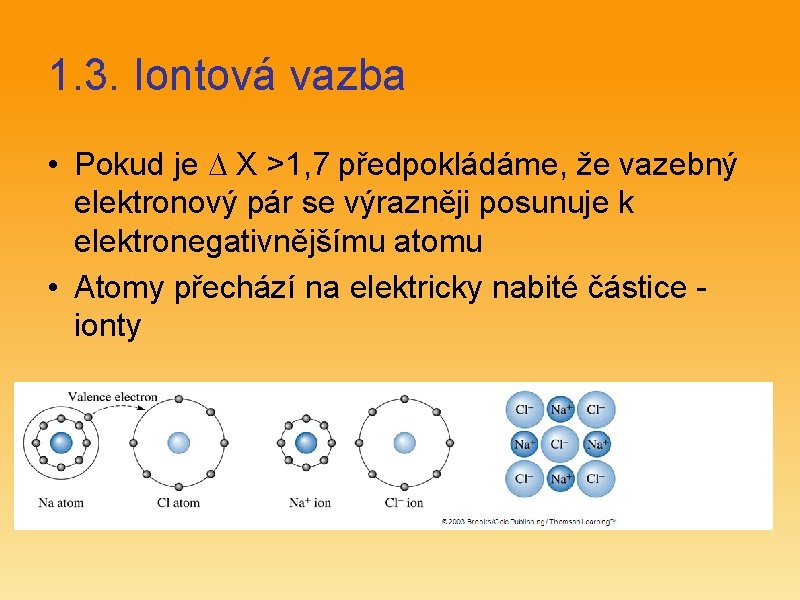
1. 3. Iontová vazba • Pokud je X >1, 7 předpokládáme, že vazebný elektronový pár se výrazněji posunuje k elektronegativnějšímu atomu • Atomy přechází na elektricky nabité částice ionty
![Vznik vazby Na. Cl • • 1 Na [ Ne ] 3 s 11 Vznik vazby Na. Cl • • 1 Na [ Ne ] 3 s 11](http://slidetodoc.com/presentation_image_h2/f9055cb5f85eca39f883b30a8776d670/image-12.jpg)
Vznik vazby Na. Cl • • 1 Na [ Ne ] 3 s 11 10 2 3 p 5 Cl [ Ne ] 3 s 17 10 • Oba vzniklé ionty jsou k sobě poutány elektrostatickými interakcemi.

Charakter chemická vazby: • Zda tedy mezi atomy vzniká vazba nepolární kovalentní, polární kovalentní nebo iontová rozhoduje rozdíl elektronegativit vázaných atomů • Hranice mezi jednotlivými vazbami byly stanoveny dohodou

Charakter chemické vazby ovlivňuje skupenství látek: • Nepolární vazba – plynné látky – N 2, Cl 2 • Polární vazba – kapaliny - HCl, H 2 O • Iontová vazba – pevné látky - Na. Cl

Kovová vazba • Vzniká mezi atomy kovů, • X jsou poměrně nízké a vzájemně se příliš neliší • Uspořádání atomů je pravidelné – kovy patří k látkám krystalickým • valenční elektrony nevytváří vazebné elektronové páry, • ale jsou volně pohyblivé • a sdíleny všemi obklopujícími atomy, ze kterých se stávají kationty • Volně pohyblivé elektrony vytváří elektronový plyn, který je příčinou charakteristických vlastností kovů ( elektrická a tepelná vodivost, kujnost…. )

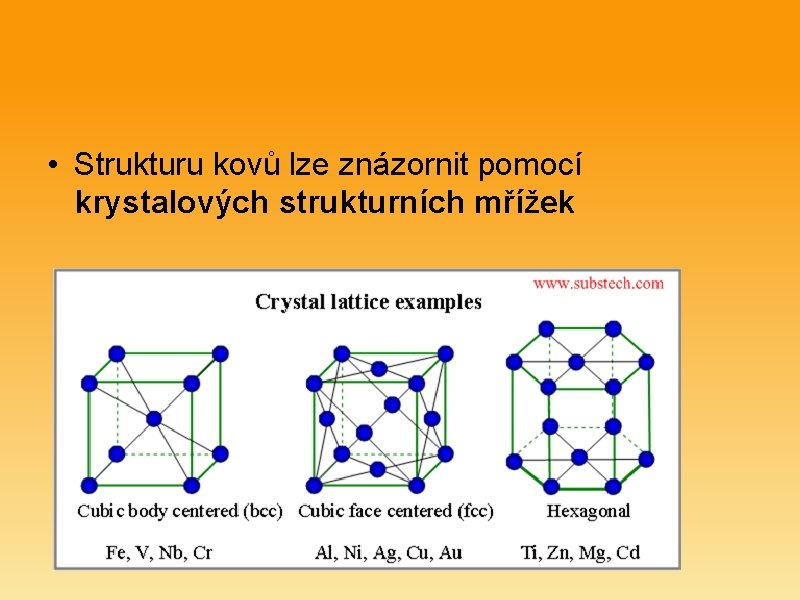
• Strukturu kovů lze znázornit pomocí krystalových strukturních mřížek

Úkoly Jaké vazebné síly působí v pevných látkách • KCl • C (diamant) • Ca. F 2 • Si. C • Fe

Z postavení prvků v periodické tabulce, ve které z uvedených sloučenin je vazba polárnější (iontovější) • A) Ca. F 2 Ca. Cl 2 • B) Be. O Mg. O • C) Si. O 2 Pb. O 2 • D) CCl 4 Si. Cl 4

POUŽITÉ ZDROJE: DUŠEK, Bohuslav a Vratislav FLEMR. Obecná a anorganická chemie pro gymnázia. SPN, 2007. ISBN 80 -7235 -369 -1. [online]. [cit. 2014 -04 -05]. Dostupné z: cs. wikipedia. org www. glassschool. cz
- Slides: 20