Chemick vazba Paed Dr Ivana Tpferov Stedn prmyslov

Chemická vazba Paed. Dr. Ivana Töpferová Střední průmyslová škola, Mladá Boleslav, Havlíčkova 456 CZ. 1. 07/1. 5. 00/34. 0861 MODERNIZACE VÝUKY

Anotace: výuková prezentace v prvním ročníku studia Předmět: chemie Ročník: I. ročník SŠ Tematický celek: obecná chemie Klíčová slova: chemická vazba, molekula, sloučenina, elektrony, elektronegativita, vazba, vazebná energie, typy vazeb, vaznost, délka vazby Forma: vysvětlování, demonstrace Datum vytvoření: 22. 8. 2013

Chemická vazba většina chemických látek obsahuje atomy vázané do molekul nebo krystalů

Atomy a molekuly Chemické látky se skládají z atomů. Jen málo látek tvoří jednotlivé atomy (He). Většina chemických látek se skládá ze sloučených atomů, které jsou k sobě vázány silami (tzv. chemickou vazbou) a vytvářejí sloučeniny. Molekula je částice složená ze dvou nebo více atomů: • z atomů stejného prvku (H 2, P 4) • z atomů různých prvků (H 2 O, Na. Cl) Chemická sloučenina je chemická látka vzniklá sloučením atomů dvou nebo více různých prvků.

Chemické sloučeniny Sloučenina je vždy tvořena molekulami. Rozdělení: podle původu Ø anorganické Ø organické podle počtu sloučených prvků Ø dvouprvkové Ø tříprvkové Ø víceprvkové Uveďte příklady jednotlivých druhů sloučenin.

Podmínky vzniku chemické vazby 1. Atomy se k sobě přiblíží tak, aby se překryly jejich elektronové obaly. 2. Atomy musí mít elektrony v orbitalech uspořádány tak, aby z nich mohly vzniknout vazebné páry. 3. Atomy musí mít vhodnou prostorovou orientaci pro vznik chemické vazby. 4. Chemická vazba se mezi atomy vytvoří jedině tehdy, když dojde při tomto ději k uvolnění určitého množství vazebné (disociační) energie (k. J. mol-1).
Chemická vazba chemická vazba ATOM MOLEKULA Chemická vazba vzniká tehdy, má-li nové seskupení atomů menší energii než jednotlivé atomy. Molekuly mají nižší energii než jednotlivé atomy a jsou proto stálejší. Chemická vazba vznikne spojením atomů pomocí valenčních elektronů (zjednodušené).

Typy chemických vazeb • podle rozdílu elektronegativit (∆X), které vazbu tvoří: elektronegativita (X) = schopnost atomu přitahovat elektrony chemické vazby 1. vazba nepolární 0 < ∆X < 0, 4 2. vazba polární 0, 4 < ∆X < 1, 7 3. vazba iontová ∆X > 1, 7 Obr. 1 Polární vazba v HCl

Typy chemických vazeb • podle způsobu vzniku: 1. kovalentní = vznikne mezi částicemi, jejichž překrývající se orbitaly obsahují jeden elektron 2. donor akceptorová (koordinačně kovalentní) = vytvoří se mezi donorem (dárcem) a akceptorem (příjemcem) elektronového páru Mezi vazbou kovalentní a koordinačně kovalentní je rozdíl ve způsobu, jak tyto vazby vznikají. Jinak tyto vazby mají stejné vlastnosti, např. energii a prostorové uspořádání.
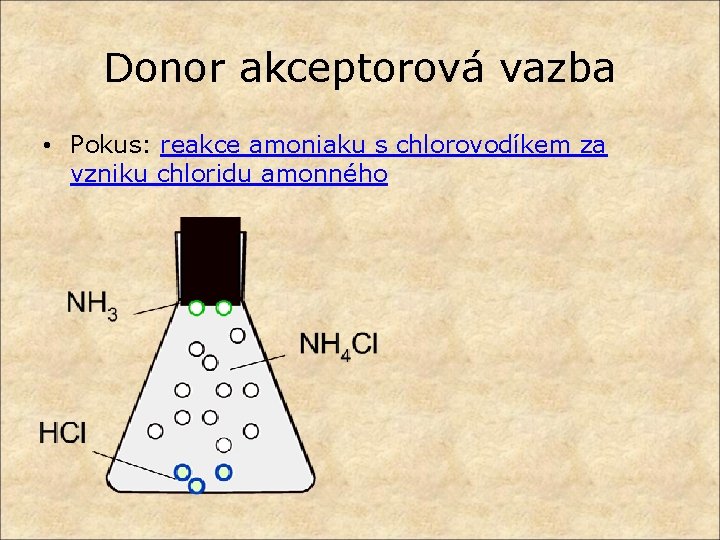
Donor akceptorová vazba • Pokus: reakce amoniaku s chlorovodíkem za vzniku chloridu amonného

Typy chemických vazeb • podle počtu vazebných elektronových párů mezi stejnými nebo různými vazebnými partnery: 1. jednoduchá 2. dvojná 3. trojná Vaznost je číslo, které udává, kolik kovalentních vazeb s jinými atomy daný atom vytváří.

Chemická vazba Vznik molekuly vodíku H + H →H−H (H 2) Vznik molekuly kyslíku : +: → (O 2) Vznik molekuly chlorovodíku H + | → H – Cl volný elektron − vazebný elektronový pár
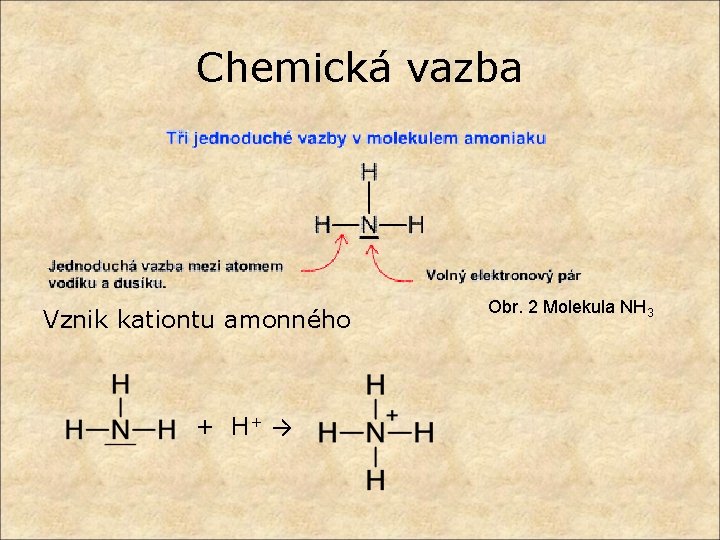
Chemická vazba Vznik kationtu amonného + H+ → Obr. 2 Molekula NH 3
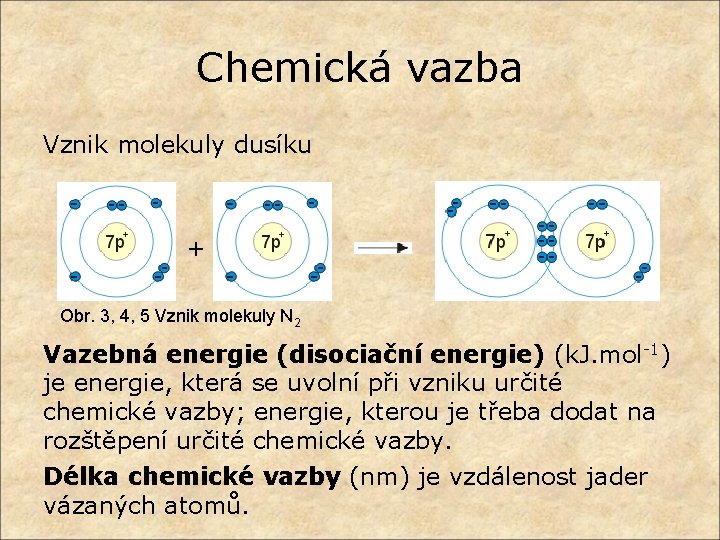
Chemická vazba Vznik molekuly dusíku + Obr. 3, 4, 5 Vznik molekuly N 2 Vazebná energie (disociační energie) (k. J. mol-1) je energie, která se uvolní při vzniku určité chemické vazby; energie, kterou je třeba dodat na rozštěpení určité chemické vazby. Délka chemické vazby (nm) je vzdálenost jader vázaných atomů.
![Seznam obrázků: Obr. 1 Polární vazba v HCl. Zdroj: Wikimedia 18. 4. 2007 [online]. Seznam obrázků: Obr. 1 Polární vazba v HCl. Zdroj: Wikimedia 18. 4. 2007 [online].](http://slidetodoc.com/presentation_image_h2/840c3fcbf16d322afa7e658ba78c5290/image-15.jpg)
Seznam obrázků: Obr. 1 Polární vazba v HCl. Zdroj: Wikimedia 18. 4. 2007 [online]. [vid. 22. 8. 2013]. Dostupné z: http: //cs. wikipedia. org/wiki/Soubor: Polarni_vazba. JPG Obr. 2 Molekula NH 3. Zdroj: chemvazba. moxo. cz [online]. [vid. 22. 8. 2013]. Dostupné z: http: //chemvazba. moxo. cz/Vyvoj/jednoducha_vazba. gif Obr. 3, 4 5 Vznik molekuly N 2. Zdroj: www. zschemie. euweb. cz [online]. [vid. 22. 8. 2013]. Dostupné z: http: //www. zschemie. euweb. cz/molekuly/molekulan 2. gif

Použité zdroje: • MACH, J. , PLUCKOVÁ, I. , ŠIBOR, J. Chemie pro 8. ročník. Úvod do obecné a anorganické chemie. Brno: NOVÁ ŠKOLA, s. r. o. , 2010. ISBN 978 -80 -7289 -133 -7. • ŠKODA, J. , DOULÍK, P. Chemie 8 učebnice pro základní školy a víceletá gymnázia. Plzeň: Fraus, 1. vydání, 2006. ISBN 80 -7238 -442 -2. • FLEMR, V. , DUŠEK, B. Chemie I pro gymnázia (obecná anorganická chemie). Praha. SPN, a. s. , 2001. ISBN 807235 -147 -8. • BANÝR, J. , BENEŠ, P. A KOLEKTIV. Chemie pro střední školy. Praha: SPN, a. s. , 1995. ISBN 80 -85937 -11 -5.
- Slides: 16