CHEMICK VAZBA Mgr Lenka Fierov Snahou vech systm

CHEMICKÁ VAZBA Mgr. Lenka Fišerová

Snahou všech systémů ( i atomů) je dosáhnout stavu o největší stabilitě a nejmenší energii. • Nejstabilnější elektronová konfigurace atomu je stav, kdy jsou zcela zaplněné valenční orbitaly elektrony (příp. zcela prázdné val. orbitaly) – mají ji VZÁCNÉ PLYNY. 1 s 2 He: ↑↓ 2 He: 1 s 2 s ↑↓ ↑↓ 1 s 2 2 p ↑↓ ↑↓ ↑↓ 10 Ne: 18 Ar: 2 p ↑↓ ↑↓ : 1 s 2 2 p 6 3 s ↑↓ ↑↓ 3 p ↑↓ ↑↓ ↑↓ 18 Ar : 1 s 2 2 p 6 3 s 2 3 p 6 Mgr. Lenka Fišerová

Způsoby, jak atomy dosáhnou stabilní konfigurace vzácného plynu: 1. Tvorba iontů: - přijetím chybějících e- vzniká anion (částice se záporným elektrickým nábojem) 9 F + e- F¯ 9 e- 10 e- F¯ : [10 Ne ] - odevzdáním přebytečných e- vzniká kation (částice s kladným el. nábojem) 11 Na - e- Na+ 11 e- 10 e- Na+ : [10 Ne ] 2. Vznik chemické vazby vznik molekuly podstata: společné sdílení valenčních e- vazebnými partnery (atomy) Vznik molekuly H 2 H● + ●H H● ●H 1 H: 1 s 1 H 2: 1 s 2 = [2 He ] Mgr. Lenka Fišerová

Chemická vazba = síla, kterou jsou k sobě navzájem poutány sloučené atomy v molekule (příp. atomy či ionty v krystalu) prostřednictvím valenč. elektronů • Vazba = interakce, pouto. . Mgr. Lenka Fišerová

Podmínky vzniku chemické vazby Srážková teorie: 1. Atomy se musí k sobě přiblížit a srazit se. 2. Při srážce musí mít atomy dostatečně velkou energii k překonání odpudivých sil mezi atomy. (+) jádro 1. atomu (+) jádro 2. atomu e- 1. atomu e- 2. atomu 3. Atomy se musí k sobě přiblížit tak, aby se překryly jejich valenční orbitaly. 4. Valenční e- (y) v orbitalech vázaných atomů musí mít opačný spin (být vhodně prostorově orientovány) , aby z nich mohl vzniknout vazebný elektronový pár(y) ↑↓ Mgr. Lenka Fišerová

Délka vazby = vzdálenost jader atomů vázaných v molekule (mezijaderná vzdálenost) hodnoty: desetiny nm (nm = 10 - 9 m) Př. HCl: O 2 : H 2 : délka vazby H-Cl = 0, 128 nm délka vazby O-O = 0, 121 nm délka vazby H-H = 0, 074 nm Při této mezijaderné vzdálenosti jsou odpudivé a přitažlivé síly mezi atomy vyrovnány a systém (molekula) má minimální energii – je stabilnější. odpudivé síly: (+) jádro 1. atomu e - 1. atomu přitažlivé síly: (+) jádro 2. atomu e- Mgr. Lenka Fišerová

Energie chemické vazby Chemické vazby vznikají a zanikají při chem. reakcích. • Při vzniku chemické vazby ( tvorba molekuly ) se energie uvolňuje tzv. VAZEBNÁ ENERGIE (- hodnota E ) = Energie uvolněná při vzniku chem. vazby. • Pro štěpení chem. vazby ( rozpad molekuly ) je nutné energie dodat (energie se spotřebovává). tzv. DISOCIAČNÍ ENERGIE (+ hodnota E) = Energie, kterou je nutno dodat pro štěpení chem. vazby. ▼ Pro chem. vazbu platí: VAZEBNÁ ENERGIE = DISOCIAČNÍ ENERGIE vznik H 2 : E(H - H) = - 458 k. J. mol-1 štěpení H 2 : E(H - H) = 458 k. J. mol-1 ► hodnoty obou energií jsou stejné, liší se pouze znaménkem Čím je vazebná (disociační) energie větší, tím je vazba pevnější. Mgr. Lenka Fišerová

- v chem. tabulkách je uvedena tzv. Molární vazebná energie (= energie vazeb 1 molu látky) - (řádově stovky) k. J. mol-1 př. H 2 E(H - H) = - 458 k. J. mol-1 Mgr. Lenka Fišerová
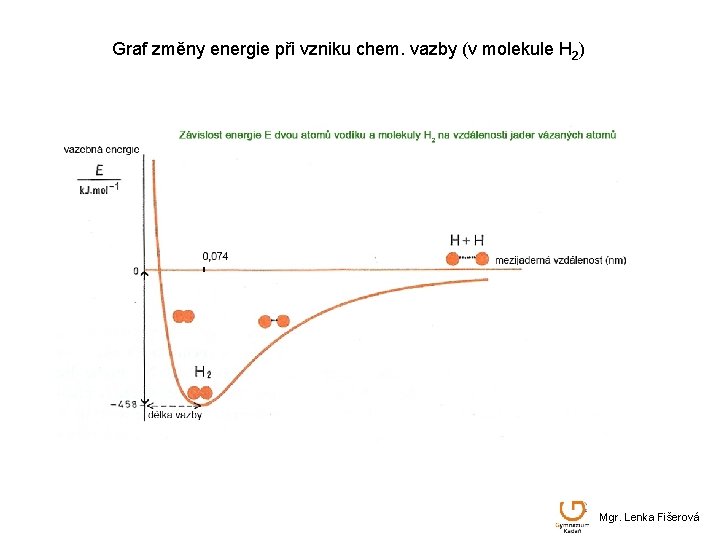
Graf změny energie při vzniku chem. vazby (v molekule H 2) Mgr. Lenka Fišerová
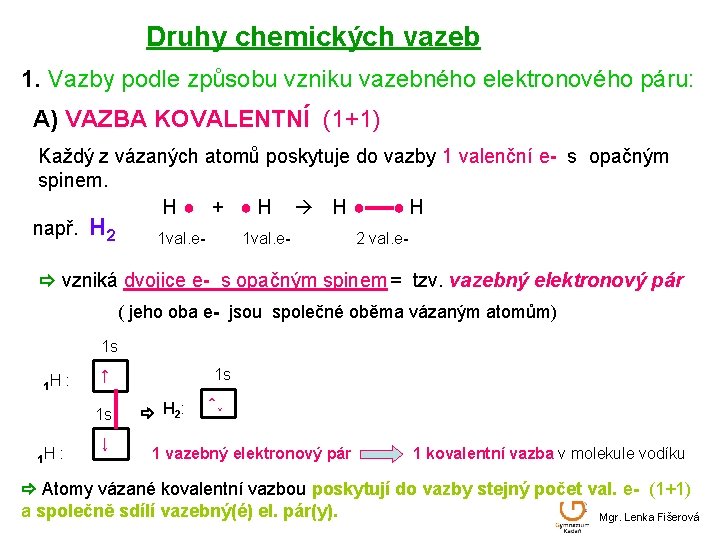
Druhy chemických vazeb 1. Vazby podle způsobu vzniku vazebného elektronového páru: A) VAZBA KOVALENTNÍ (1+1) Každý z vázaných atomů poskytuje do vazby 1 valenční e- s opačným spinem. H● + ●H H● ●H např. H 2 1 val. e 2 val. e vzniká dvojice e- s opačným spinem = tzv. vazebný elektronový pár ( jeho oba e- jsou společné oběma vázaným atomům) 1 s 1 H : ↑ 1 s 1 H : ↓ 1 s H 2 : ↑↓ 1 vazebný elektronový pár 1 kovalentní vazba v molekule vodíku Atomy vázané kovalentní vazbou poskytují do vazby stejný počet val. e- (1+1) a společně sdílí vazebný(é) el. pár(y). Mgr. Lenka Fišerová
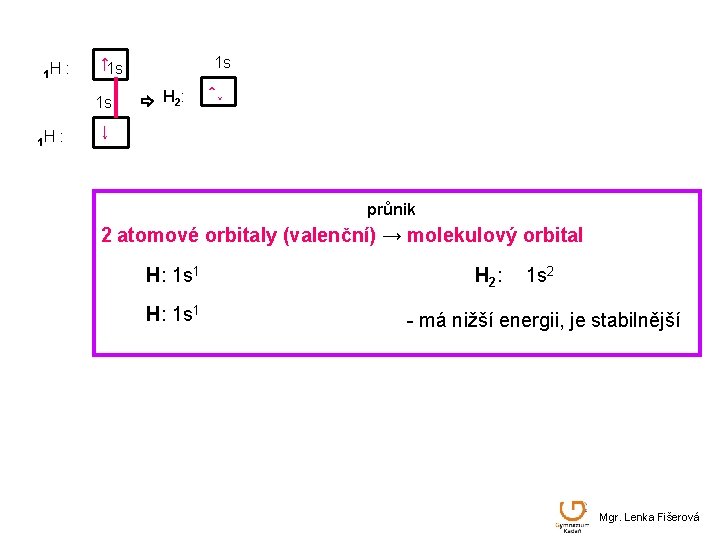
1 H : ↑ 1 s 1 s 1 H : 1 s H 2 : ↑↓ ↓ průnik 2 atomové orbitaly (valenční) → molekulový orbital H: 1 s 1 H 2 : 1 s 2 - má nižší energii, je stabilnější Mgr. Lenka Fišerová
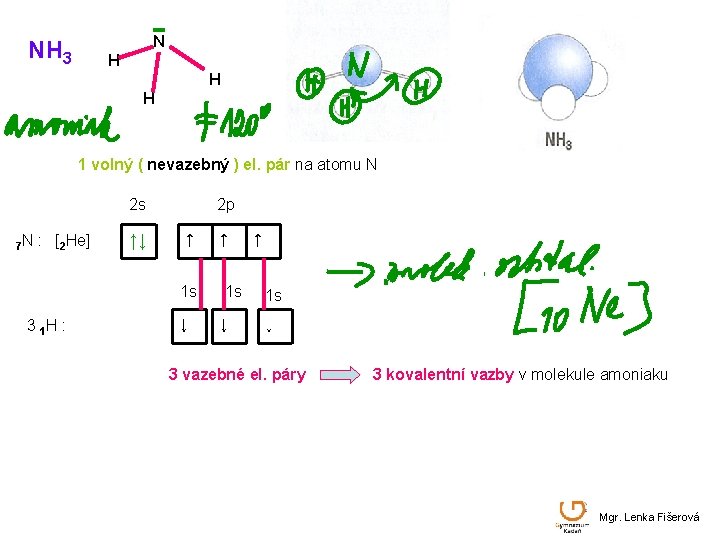
N NH 3 H H H 1 volný ( nevazebný ) el. pár na atomu N 2 s 7 N : [2 He] ↑↓ 2 p ↑ 1 s 3 1 H : ↓ ↑ 1 s ↓ 3 vazebné el. páry 3 kovalentní vazby v molekule amoniaku Mgr. Lenka Fišerová
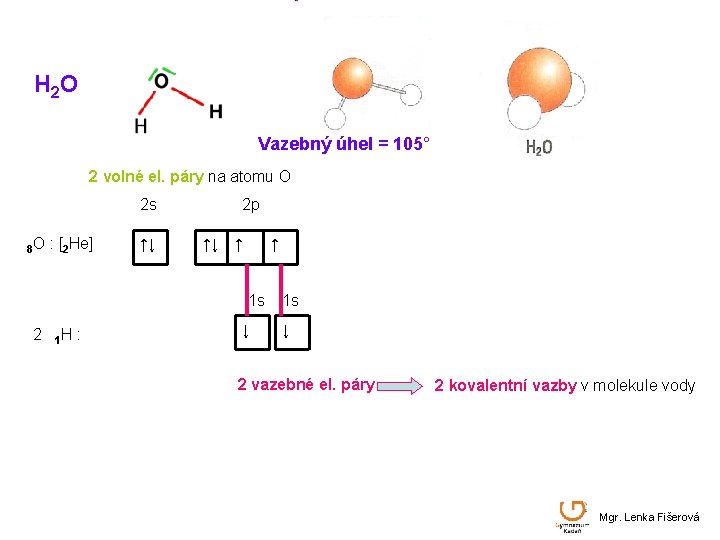
H 2 O Vazebný úhel = 105° 2 volné el. páry na atomu O 2 s 8 O : [2 He] ↑↓ 2 p ↑↓ ↑ ↑ 1 s 2 1 H : ↓ 1 s ↓ 2 vazebné el. páry 2 kovalentní vazby v molekule vody Mgr. Lenka Fišerová
![CH 4 2 s 6 C : [2 He] ↑↓ 2 p ↑ 2 CH 4 2 s 6 C : [2 He] ↑↓ 2 p ↑ 2](http://slidetodoc.com/presentation_image_h/aab066e2ec1800133c9924e8ad4c47e3/image-14.jpg)
CH 4 2 s 6 C : [2 He] ↑↓ 2 p ↑ 2 s 6 C ٭ : [2 He] ↑ 2 p ↑ 1 s 1 s 4 1 H : ↓ ↑ ↓ 4 vazebné el. páry ↑ ↑ 1 s ↓ 4 kovalentní vazby v molekule methanu Mgr. Lenka Fišerová

Vaznost atomu ( prvku) = číslo, které udává počet kovalentních vazeb vycházejících z atomu prvku ve sloučenině (neboli počet vazebných elektronových párů, které atom sdílí jinými atomy). Např. atom H : jednovazný ( vždy) – H 2 , HCl , H 2 O …… atom O : dvojvazný ( zpravidla) – O 2 , H 2 O , H 2 SO 4…. . atom N : trojvazný ( nejčastěji ) – N 2 , NH 3 , …. . čtyřvazný - pouze v NH 4+ atom C : čtyřvazný (zpravidla ) – organické slouč. (např. CH 4), CO 2 , H 2 CO 3…. . dvojvazný – pouze v CO Chemickou vazbu zprostředkovávají valenční elektrony. Oktetové pravidlo : Prvky 2. a 3. periody si tvorbou molekuly doplňují počet valenčních e- na 8 (stabilní el. konfigurace vzácného plynu s 2 p 6) Mgr. Lenka Fišerová
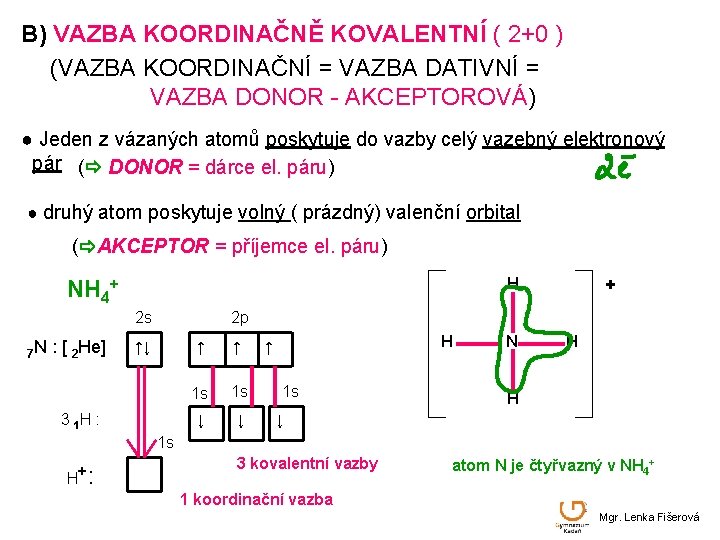
B) VAZBA KOORDINAČNĚ KOVALENTNÍ ( 2+0 ) (VAZBA KOORDINAČNÍ = VAZBA DATIVNÍ = VAZBA DONOR - AKCEPTOROVÁ) ● Jeden z vázaných atomů poskytuje do vazby celý vazebný elektronový pár ( DONOR = dárce el. páru) ● druhý atom poskytuje volný ( prázdný) valenční orbital ( AKCEPTOR = příjemce el. páru) H NH 4+ 2 s 7 N : [ 2 He] + 2 p ↑↓ 3 1 H : ↑ ↑ 1 s 1 s ↓ ↓ H ↑ 1 s N H H ↓ 1 s H+ : 3 kovalentní vazby atom N je čtyřvazný v NH 4+ 1 koordinační vazba Mgr. Lenka Fišerová
![H 3 O + 2 s 8 O : [2 He] ↑↓ 2 p H 3 O + 2 s 8 O : [2 He] ↑↓ 2 p](http://slidetodoc.com/presentation_image_h/aab066e2ec1800133c9924e8ad4c47e3/image-17.jpg)
H 3 O + 2 s 8 O : [2 He] ↑↓ 2 p ↑↓ ↑ 1 s 2 1 H : H+ : ↓ 1 s atom O je trojvazný v H 3 O + ↑ 1 s ↓ 2 kovalentní vazby 1 koordinační vazba Kovalentní a koordinačně kovalentní vazba se liší pouze ve způsobu vzniku, vlastnosti obou vazeb jsou stejné ( např. stejná pevnost…. . ). Mgr. Lenka Fišerová
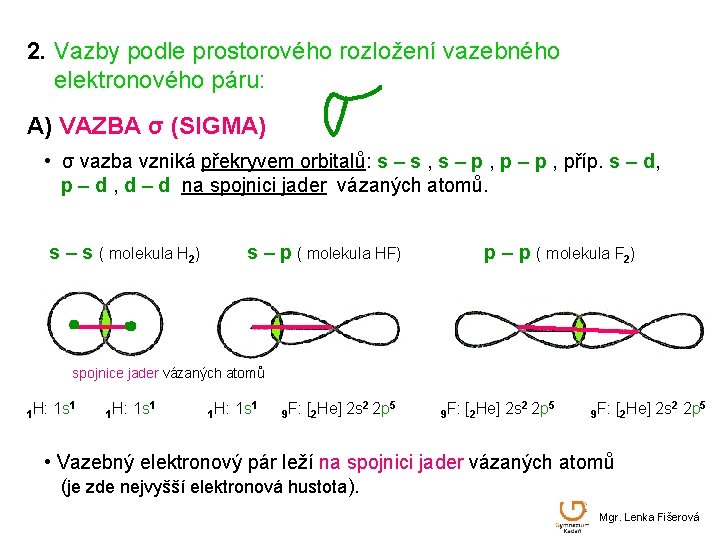
2. Vazby podle prostorového rozložení vazebného elektronového páru: A) VAZBA σ (SIGMA) • σ vazba vzniká překryvem orbitalů: s – s , s – p , příp. s – d, p – d , d – d na spojnici jader vázaných atomů. s – s ( molekula H 2) s – p ( molekula HF) p – p ( molekula F 2) spojnice jader vázaných atomů 1 H: 1 s 1 9 F: [2 He] 2 s 2 2 p 5 • Vazebný elektronový pár leží na spojnici jader vázaných atomů (je zde nejvyšší elektronová hustota). Mgr. Lenka Fišerová
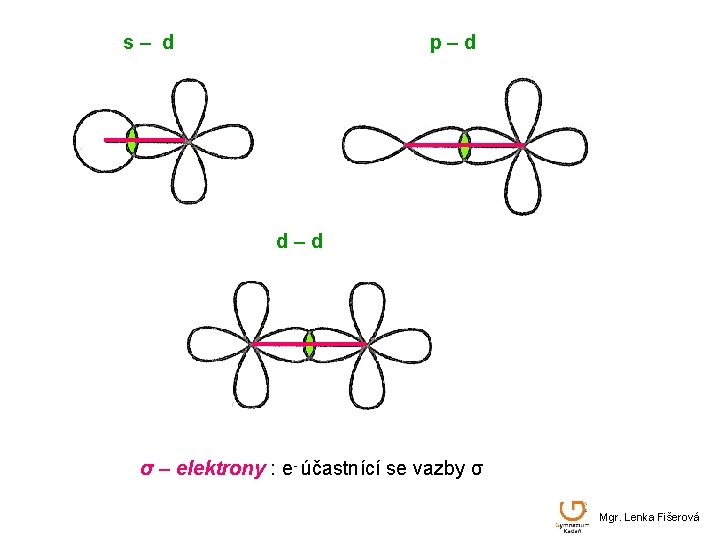
s– d p–d d–d σ – elektrony : e- účastnící se vazby σ Mgr. Lenka Fišerová
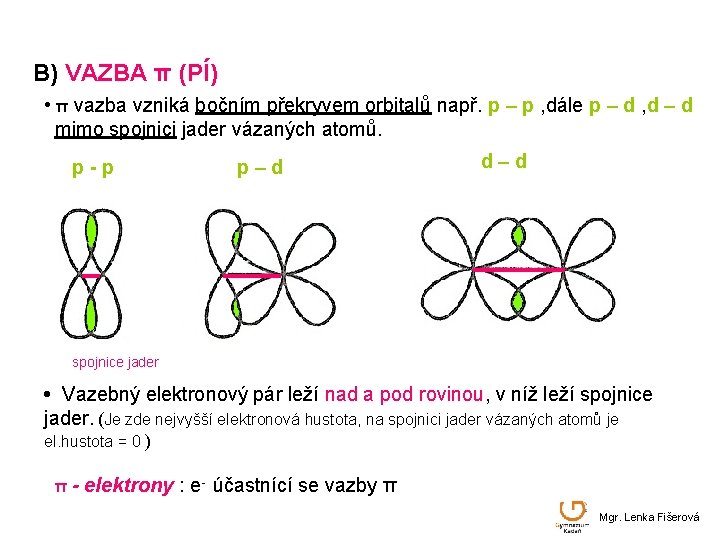
B) VAZBA π (PÍ) • π vazba vzniká bočním překryvem orbitalů např. p – p , dále p – d , d – d mimo spojnici jader vázaných atomů. p-p p–d d–d spojnice jader • Vazebný elektronový pár leží nad a pod rovinou, v níž leží spojnice jader. (Je zde nejvyšší elektronová hustota, na spojnici jader vázaných atomů je el. hustota = 0 ) π- elektrony : e- účastnící se vazby π Mgr. Lenka Fišerová
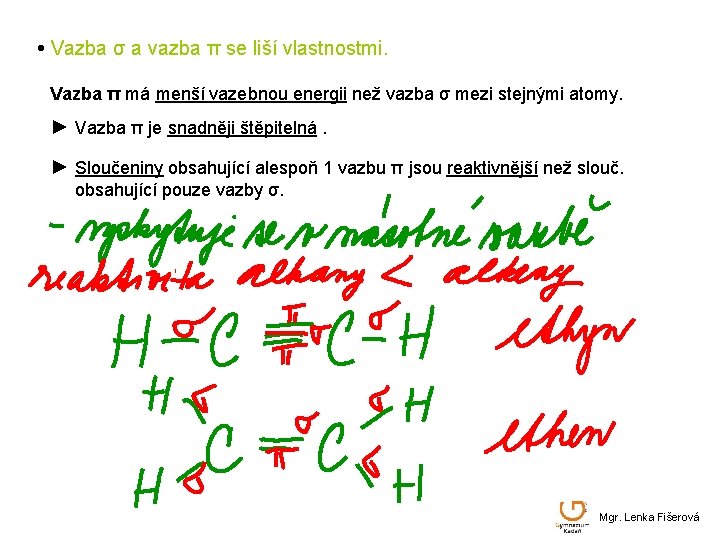
• Vazba σ a vazba π se liší vlastnostmi. Vazba π má menší vazebnou energii než vazba σ mezi stejnými atomy. ► Vazba π je snadněji štěpitelná. ► Sloučeniny obsahující alespoň 1 vazbu π jsou reaktivnější než slouč. obsahující pouze vazby σ. Mgr. Lenka Fišerová

3. Vazby( kovalentní) podle počtu sdílených elektronových párů: A) VAZBA JEDNODUCHÁ • Vázané atomy spolu sdílejí pouze 1 vazebný elektronový pár. Např. H 2 , F 2 , HF… H 2 : H • • H → H • σ 1 s • H 1 H: jednoduchá vazba ↑ atom H je jednovazný 1 s 1 H: ↓ Vazba jednoduchá je vazbou σ , neboť se při jejím vzniku uvolní více E než u vazby π (σ má větší vazebnou E). B) VAZBA NÁSOBNÁ • Vázané atomy spolu sdílejí více vazebných elektronových párů. Mgr. Lenka Fišerová
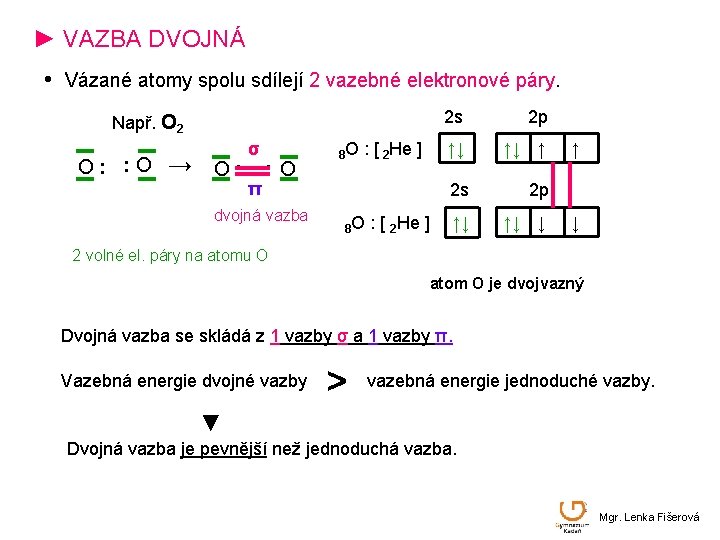
► VAZBA DVOJNÁ • Vázané atomy spolu sdílejí 2 vazebné elektronové páry. Např. O 2 O: : O σ → O: : O 8 O : [ 2 He ] π dvojná vazba 8 O : [ 2 He ] 2 s 2 p ↑↓ ↑↓ ↑ 2 s 2 p ↑↓ ↑↓ ↓ ↑ ↓ 2 volné el. páry na atomu O atom O je dvojvazný Dvojná vazba se skládá z 1 vazby σ a 1 vazby π. Vazebná energie dvojné vazby > vazebná energie jednoduché vazby. ▼ Dvojná vazba je pevnější než jednoduchá vazba. Mgr. Lenka Fišerová

►VAZBA TROJNÁ • Vázané atomy spolu sdílejí 3 vazebné elektronové páry. 2 s Např. N 2 N. : : . N → N π σN π trojná vazba 7 N : [2 He ] ↑↓ 2 p ↑ 2 s 7 N : [2 He ] ↑↓ ↑ ↑ 2 p ↓ ↓ ↓ 1 volný el. pár na atomu N atom N je trojvazný Trojná vazba se skládá z 1 vazby σ a 2 vazeb π. Vazebná energie trojné vazby ▼ > vazebná energie dvojné vazby Trojná vazba je pevnější než dvojná vazba. Mgr. Lenka Fišerová
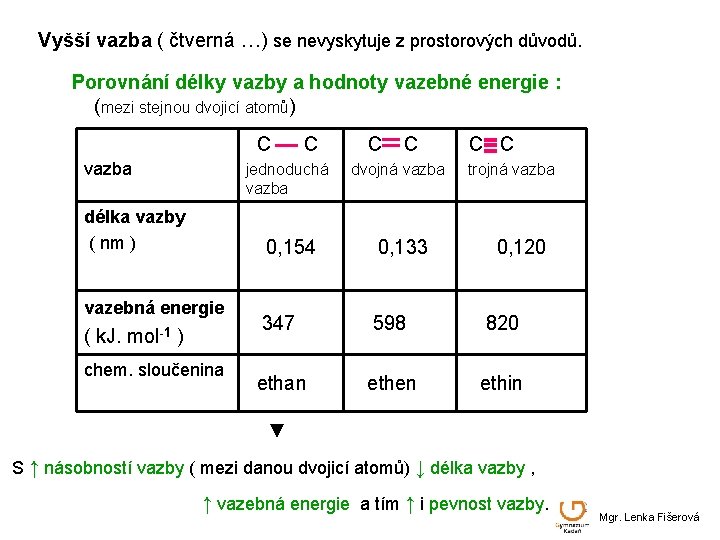
Vyšší vazba ( čtverná …) se nevyskytuje z prostorových důvodů. Porovnání délky vazby a hodnoty vazebné energie : (mezi stejnou dvojicí atomů) C vazba délka vazby ( nm ) vazebná energie ( k. J. mol-1 ) chem. sloučenina C C C jednoduchá vazba dvojná vazba trojná vazba 0, 154 0, 133 347 598 820 ethan ethen ethin 0, 120 ▼ S ↑ násobností vazby ( mezi danou dvojicí atomů) ↓ délka vazby , ↑ vazebná energie a tím ↑ i pevnost vazby. Mgr. Lenka Fišerová

Vaznost atomu ( prvku) = číslo, které udává počet kovalentních vazeb vycházejících z atomu prvku ve sloučenině (neboli počet vazebných elektronových párů, které atom sdílí jinými atomy). Např. atom H : jednovazný ( vždy) – H 2 , HCl , H 2 O …… atom O : dvojvazný ( zpravidla) – O 2 , H 2 O , H 2 SO 4…. . atom N : trojvazný ( nejčastěji ) – N 2 , NH 3 , …. . čtyřvazný - pouze v NH 4+ atom C : čtyřvazný (zpravidla ) – organické slouč. (např. CH 4), CO 2 , H 2 CO 3…. . dvojvazný – pouze v CO Chemickou vazbu zprostředkovávají valenční elektrony. Oktetové pravidlo : Prvky 2. a 3. periody si tvorbou molekuly doplňují počet valenčních e- na 8 (stabilní el. konfigurace vzácného plynu s 2 p 6) Mgr. Lenka Fišerová

4. Vazby podle rozdílu elektronegativit ( ∆ X ) vázaných atomů : Elektronegativita atomu X = míra schopnosti atomu urč. prvku přitahovat k sobě valenční elektrony sdílené s jiným atomem ( e- chem. vazby ) A) VAZBA NEPOLÁRNÍ - kovalentní vazba - např. H 2 , O 2 , F 2 , CH 4 , CS 2 , CCl 4 …. . H 2 : X(H) = 2, 2 CH 4 : X(C) = 2, 5 X(H) = 2, 2 CS 2 : X(C) = 2, 5 X (S) = 2, 4 ∆X (H – H) = X(H) – X(H) = 2, 2 – 2, 2 = 0 ∆X (C – H) = X(C) – X(H) = 2, 5 – 2, 2 = 0, 3 ∆X (C – S) = X(C) – X(S) = 2, 5 – 2, 4 = 0, 1 ∆X < 0, 4 = ► Oba vázané atomy přitahují e- chem. vazby stejně nebo přibližně stejně velkou silou. ( Žádný atom nepřitáhne vazebný el. pár k sobě. ) Rovnoměrné rozložení vazebného elektronového páru mezi oba vázané atomy. Mgr. Lenka Fišerová

B) VAZBA POLÁRNÍ - kovalentní vazba - např. HCl , H 2 O , NH 3 , SO 2 , HNO 3 …. HCl : X(H) = 2, 2 X(Cl) = 2, 8 ∆X (H – Cl) = X(Cl) – X(H) = 2, 8 – 2, 2 = 0, 6 H ◄ Cl ∆X (H – O) = X(O) – X(H) = 3, 5 – 2, 2 = 1, 3 O ◄ 0, 4 < ∆X < 1, 7 H ▼ H 2 O : X(H) = 2, 2 X(O) = 3, 5 H ► Vázané atomy přitahují e- chem. vazby různě velkou silou. Nerovnoměrné rozložení vazebného elektronového páru mezi vázané atomy. Na atomech vznikají parciální (částečné) náboje δ (delta). Atom s ↑ X (např. Cl) přitahuje vazebný el. pár blíže k sobě vznikne na něm parciální záporný náboj δ -. δ+ δ 2δ- H ◄ Cl δ+ H ▼ O ▼ Na atomu s ↓ X (např. H) vzniká parciální kladný náboj δ +. δ+ H Mgr. Lenka Fišerová

3. VAZBA IONTOVÁ = extrémně polární vazba - vazba v iontových sloučeninách např. Na. Cl , KF , KCl , Na 2 O, Ca. O…. Na. Cl : X (Na) = 1, 00 X (Cl) = 2, 8 ∆X (Na. Cl) = X (Cl) – X (Na) = 2, 8 – 1, 00 = 1, 8 KF : X (K) = 0, 91 X (F) = 4, 1 ∆X (KF) = X (F) – X (K) = 4, 1 – 0, 91 = 3, 19 Ca. O : X (Ca) = 1, 00 X (O) = 3, 5 ∆X (Ca. O) = X (O) – X (Ca) = 3, 5 – 1, 00 = 2, 5 ∆X > 1, 7 = Atom s ↑X (např. Cl )zcela přitáhne vazebné e- k sobě vzniká z něj anion ( Cl- ). Z atomu s ↓ X ( např. Na) vzniká kation ( Na+ ). Na+ Cl- Mezi ionty se nevyskytuje vazebný el. pár. Iontová vazba = elektrostatické přitahování opačně nabitých iontů (kationtů a aniontů). Mgr. Lenka Fišerová
- Slides: 29