Chemick vazba Ing L Johnov Z Lom Chemick

Chemická vazba Ing. L. Johnová ZŠ Lom

Chemická vazba Vzniká utvořením vazebného elektronového páru mezi dvěma valenčními elektrony Schopnost atomu přitahovat vazebný elektronový pár se nazývá ELEKTRONEGATIVITA Vazebný pár přitahuje atom, který má větší ELEKTRONEGATIVITU Podle rozdílu hodnot elektronegativit atomů prvků, které tvoří vazbu, rozlišujeme několik druhů chemických vazeb

Chemické vazby Kovalentní - nepolární kovalentní - polární kovalentní Iontová

Chemické vazby Nepolární chemická vazba – vzniká mezi atomy se stejným protonovým číslem, jejich rozdíl elektronegativit je nulový. Sloučeniny s touto vazbou se nazývají nepolární sloučeniny.

Chemické vazby Polární chemická vazba – vzniká mezi atomy, jejichž rozdíl elektronegativit je menší než 1, 7 Sloučeniny s touto vazbou se nazývají polární sloučeniny.

Chemické vazby Iontová chemická vazba – vzniká mezi atomy, jejichž rozdíl elektronegativit je větší než 1, 7. Při iontové vazbě vznikají ionty Sloučeniny s touto vazbou se nazývají iontové sloučeniny.
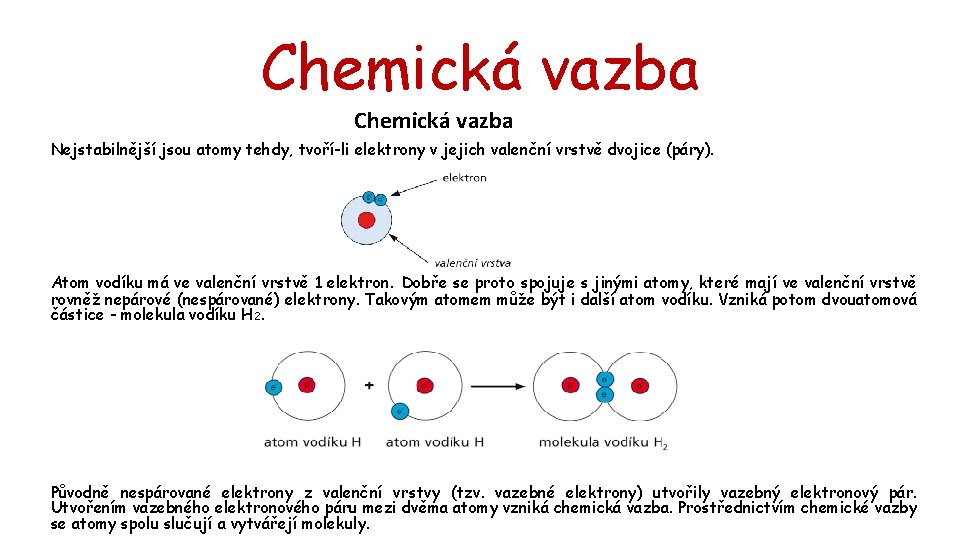
Chemická vazba Nejstabilnější jsou atomy tehdy, tvoří-li elektrony v jejich valenční vrstvě dvojice (páry). Atom vodíku má ve valenční vrstvě 1 elektron. Dobře se proto spojuje s jinými atomy, které mají ve valenční vrstvě rovněž nepárové (nespárované) elektrony. Takovým atomem může být i další atom vodíku. Vzniká potom dvouatomová částice - molekula vodíku H 2. Původně nespárované elektrony z valenční vrstvy (tzv. vazebné elektrony) utvořily vazebný elektronový pár. Utvořením vazebného elektronového páru mezi dvěma atomy vzniká chemická vazba. Prostřednictvím chemické vazby se atomy spolu slučují a vytvářejí molekuly.
- Slides: 7