Chemick vazba I Molekuly krystaly a chemick vazba

Chemická vazba I

Molekuly, krystaly a chemická vazba: Seznámili jste se s periodickou tabulkou a víte, že dnes již obsahuje 111 prvků. Jsou ale známy miliony různých látek, a to díky schopnosti prvků slučovat se. §Základními stavebními jednotkami většiny látek jsou MOLEKULY. Mohou být složeny z atomů • téhož prvku • různých prvků O 2 H 2 O §Velký počet vázaných částic může být obsažen v různých typech KRYSTALŮ. Protože jsou atomy vázány značnými silami, jsou molekuly a krystaly velmi stálé. Tyto síly nazýváme CHEMICKÉ VAZBY.
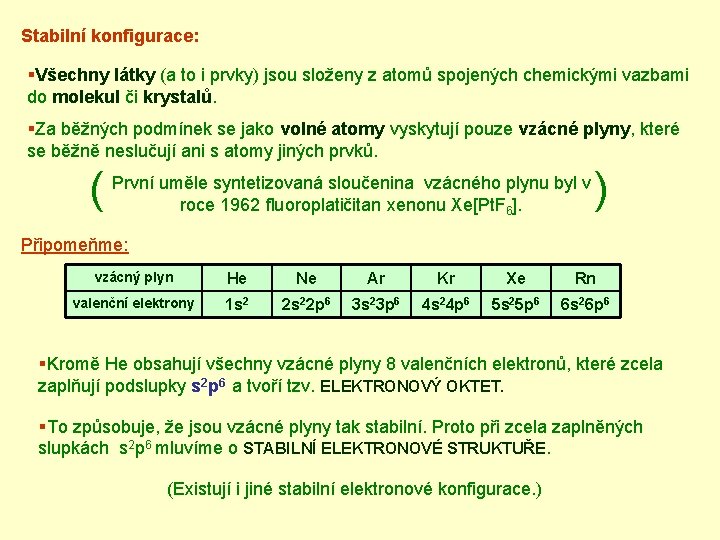
Stabilní konfigurace: §Všechny látky (a to i prvky) jsou složeny z atomů spojených chemickými vazbami do molekul či krystalů. §Za běžných podmínek se jako volné atomy vyskytují pouze vzácné plyny, které se běžně neslučují ani s atomy jiných prvků. syntetizovaná sloučenina vzácného plynu byl v ( První uměle ) roce 1962 fluoroplatičitan xenonu Xe[Pt. F ]. 6 Připomeňme: vzácný plyn He Ne Ar Kr Xe Rn valenční elektrony 1 s 2 2 s 22 p 6 3 s 23 p 6 4 s 24 p 6 5 s 25 p 6 6 s 26 p 6 §Kromě He obsahují všechny vzácné plyny 8 valenčních elektronů, které zcela zaplňují podslupky s 2 p 6 a tvoří tzv. ELEKTRONOVÝ OKTET. §To způsobuje, že jsou vzácné plyny tak stabilní. Proto při zcela zaplněných slupkách s 2 p 6 mluvíme o STABILNÍ ELEKTRONOVÉ STRUKTUŘE. (Existují i jiné stabilní elektronové konfigurace. )
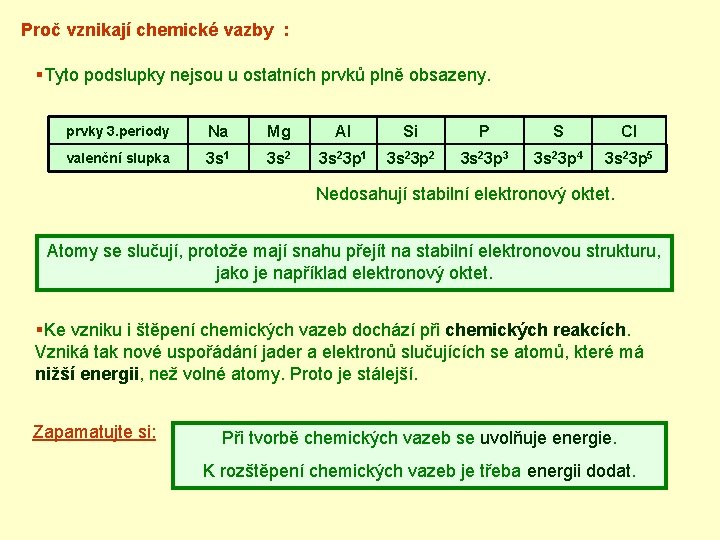
Proč vznikají chemické vazby : §Tyto podslupky nejsou u ostatních prvků plně obsazeny. prvky 3. periody Na Mg Al Si P S Cl valenční slupka 3 s 1 3 s 23 p 2 3 s 23 p 3 3 s 23 p 4 3 s 23 p 5 Nedosahují stabilní elektronový oktet. Atomy se slučují, protože mají snahu přejít na stabilní elektronovou strukturu, jako je například elektronový oktet. §Ke vzniku i štěpení chemických vazeb dochází při chemických reakcích. Vzniká tak nové uspořádání jader a elektronů slučujících se atomů, které má nižší energii, než volné atomy. Proto je stálejší. Zapamatujte si: Při tvorbě chemických vazeb se uvolňuje energie. K rozštěpení chemických vazeb je třeba energii dodat.
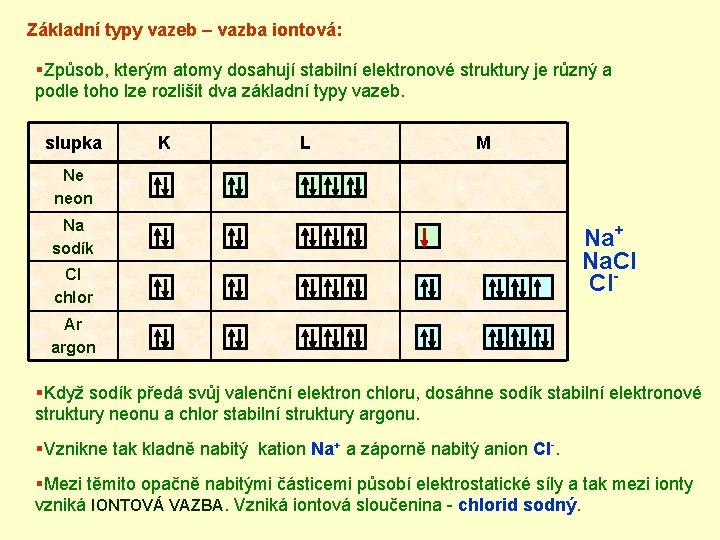
Základní typy vazeb – vazba iontová: §Způsob, kterým atomy dosahují stabilní elektronové struktury je různý a podle toho lze rozlišit dva základní typy vazeb. slupka K L M Ne neon Na sodík Cl chlor Na+ Na. Cl Cl- Ar argon §Když sodík předá svůj valenční elektron chloru, dosáhne sodík stabilní elektronové struktury neonu a chlor stabilní struktury argonu. §Vznikne tak kladně nabitý kation Na+ a záporně nabitý anion Cl-. §Mezi těmito opačně nabitými částicemi působí elektrostatické síly a tak mezi ionty vzniká IONTOVÁ VAZBA. Vzniká iontová sloučenina - chlorid sodný.

Struktura chloridu sodného: §Vzorec Na. Cl je pouze vzorec stechiometrický, vyjadřuje poměr zastoupení prvků. § Ve skutečnosti každý kation přitahuje všechny okolní anionty a každý anion všechny okolní kationty. §Vzniká tak energeticky nejvýhodnější prostorové uspořádání, v němž se pravidelně střídají kladné a záporné ionty. Krystalová struktura Na. Cl: Sůl kamenná – Na. Cl: Na+ Cl -
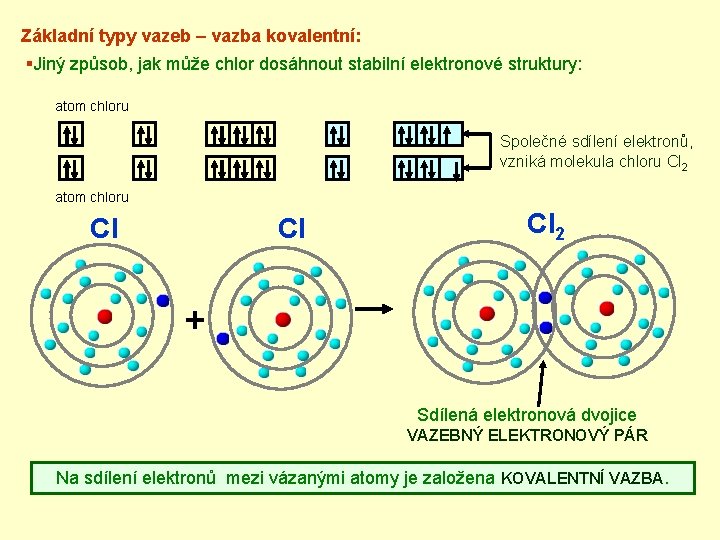
Základní typy vazeb – vazba kovalentní: §Jiný způsob, jak může chlor dosáhnout stabilní elektronové struktury: atom chloru Společné sdílení elektronů, vzniká molekula chloru Cl 2 atom chloru Cl Cl Cl 2 + Sdílená elektronová dvojice VAZEBNÝ ELEKTRONOVÝ PÁR Na sdílení elektronů mezi vázanými atomy je založena KOVALENTNÍ VAZBA.

Teorie vazeb: §Podobně jako vznikaly různé modely atomu, vznikaly i teorie chemické vazby. §Současné teorie jsou již velmi rozvinuté a umožňují předpovídat: • tvary molekul • pevnost vazeb • vlastnosti molekul • mechanismy jejich reakcí §Přesto využíváme i jednodušší teorie vazeb, které nám dokáží poskytnout základní představu a informace. Příkladem je Lewisova představa vazby, jako „sdíleného elektronového páru“.

Lewisovy elektronové vzorce: Gilbert Newton Lewis (1875 -1946), americký fyzikální chemik §Podle Lewisovy teorie elektronový pár tvořící kovalentní vazbu (VAZEBNÝ PÁR) zůstává umístěn mezi dvojicí vázaných atomů. §Pár valenčních elektronů, který se vazby neúčastní se nazývá VOLNÝ PÁR. §Podle počtu vazebných elektronových párů rozlišujeme VAZBU JEDNODUCHOU, DVOJNOU A TROJNOU. §Lewisova představa dále vychází z poznání, že u velké řady sloučenin je splněno OKTETOVÉ PRAVIDLO (atomy se snaží při vzniku vazby dosáhnout stabilní konfigurace - oktetu) (V případě vodíku jde o doplnění na elektronovou konfiguraci helia – 1 s 2 – dublet. ) Tato pravidla umožňují sestavování LEWISOVÝCH ELEKTRONOVÝCH VZORCŮ, které vyjadřují rozmístění vazeb a volných párů v molekule.
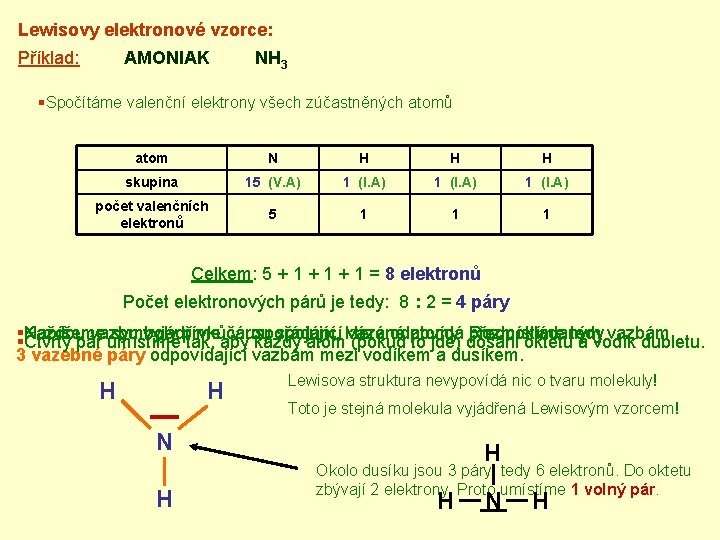
Lewisovy elektronové vzorce: Příklad: AMONIAK NH 3 §Spočítáme valenční elektrony všech zúčastněných atomů atom N H H H skupina 15 (V. A) 1 (I. A) počet valenčních elektronů 5 1 1 1 Celkem: 5 + 1 + 1 = 8 elektronů Počet elektronových párů je tedy: 8 : 2 = 4 páry §§Každou Napíšeme vazbu symboly vyjádříme prvků čárou v uspořádání, spojující vázané odpovídá atomy. Rozmístíme předpokládaným vazbám. Čtvrtý pár umístíme tak, aby každý atomkteré (pokud to jde) dosáhl oktetutedy a vodík dubletu. 3 vazebné páry odpovídající vazbám mezi vodíkem a dusíkem. H H Lewisova struktura nevypovídá nic o tvaru molekuly! Toto je stejná molekula vyjádřená Lewisovým vzorcem! N H H Okolo dusíku jsou 3 páry, tedy 6 elektronů. Do oktetu zbývají 2 elektrony. Proto umístíme 1 volný pár. H N H
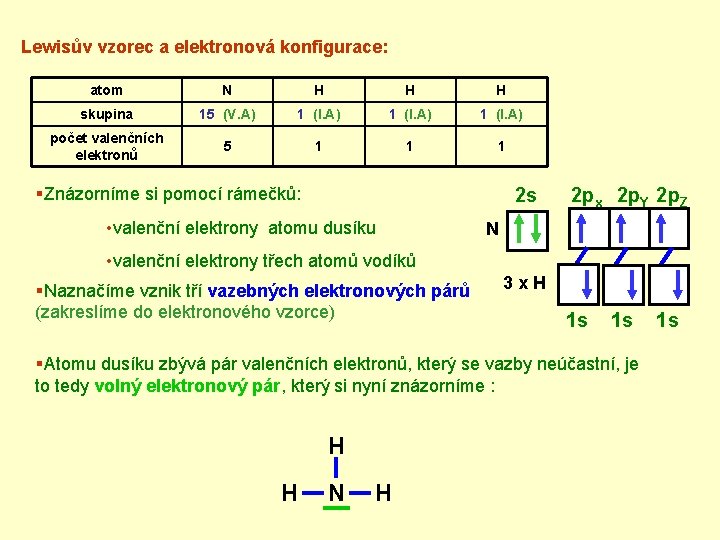
Lewisův vzorec a elektronová konfigurace: atom N H H H skupina 15 (V. A) 1 (I. A) počet valenčních elektronů 5 1 1 1 §Znázorníme si pomocí rámečků: 2 s • valenční elektrony atomu dusíku 2 px 2 p. Y 2 p. Z N • valenční elektrony třech atomů vodíků §Naznačíme vznik tří vazebných elektronových párů (zakreslíme do elektronového vzorce) 3 x. H 1 s 1 s §Atomu dusíku zbývá pár valenčních elektronů, který se vazby neúčastní, je to tedy volný elektronový pár, který si nyní znázorníme : H H N H 1 s
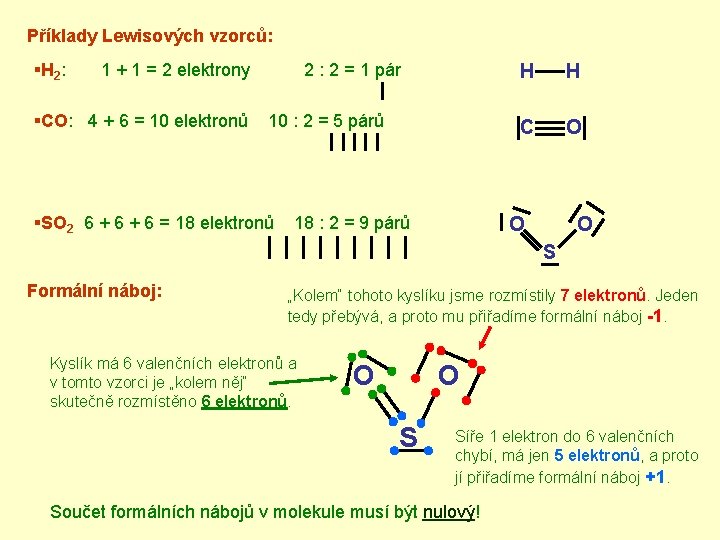
Příklady Lewisových vzorců: § H 2 : 1 + 1 = 2 elektrony §CO: 4 + 6 = 10 elektronů 2 : 2 = 1 pár 10 : 2 = 5 párů §SO 2 6 + 6 = 18 elektronů 18 : 2 = 9 párů H H C O O O S Formální náboj: „Kolem“ tohoto kyslíku jsme rozmístily 7 elektronů. Jeden tedy přebývá, a proto mu přiřadíme formální náboj -1. Kyslík má 6 valenčních elektronů a v tomto vzorci je „kolem něj“ skutečně rozmístěno 6 elektronů. O O S Síře 1 elektron do 6 valenčních chybí, má jen 5 elektronů, a proto jí přiřadíme formální náboj +1. Součet formálních nábojů v molekule musí být nulový!
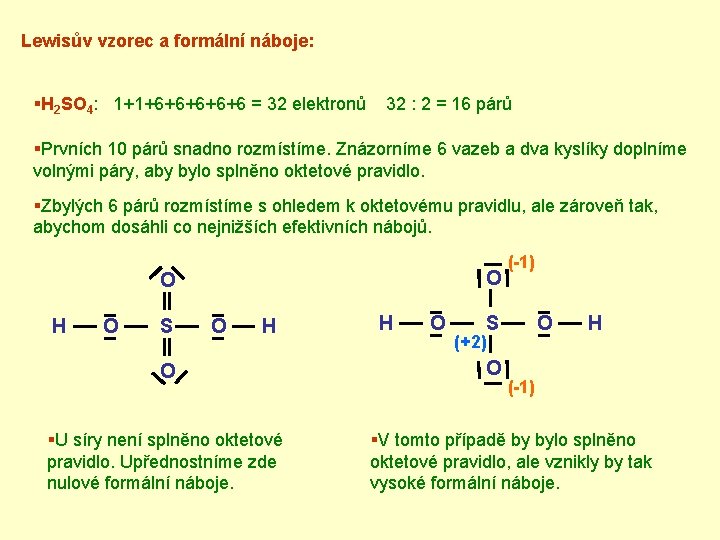
Lewisův vzorec a formální náboje: §H 2 SO 4: 1+1+6+6+6 = 32 elektronů 32 : 2 = 16 párů §Prvních 10 párů snadno rozmístíme. Znázorníme 6 vazeb a dva kyslíky doplníme volnými páry, aby bylo splněno oktetové pravidlo. §Zbylých 6 párů rozmístíme s ohledem k oktetovému pravidlu, ale zároveň tak, abychom dosáhli co nejnižších efektivních nábojů. O O H O S O H O §U síry není splněno oktetové pravidlo. Upřednostníme zde nulové formální náboje. H O (-1) S O (+2) O H (-1) §V tomto případě by bylo splněno oktetové pravidlo, ale vznikly by tak vysoké formální náboje.
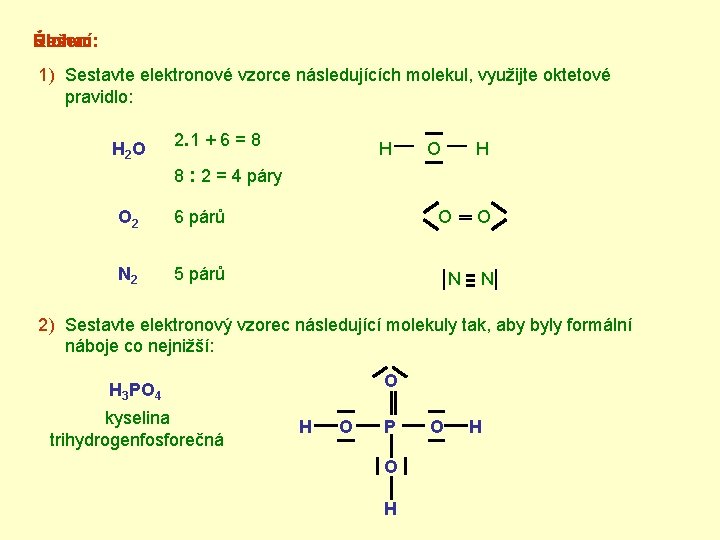
Úloha: Řešení: 1) Sestavte elektronové vzorce následujících molekul, využijte oktetové pravidlo: H 2 O 2. 1 + 6 = 8 H— O — H 8 : 2 = 4 páry O 2 6 párů O═O N 2 5 párů │N ≡ N│ 2) Sestavte elektronový vzorec následující molekuly tak, aby byly formální náboje co nejnižší: O H 3 PO 4 kyselina trihydrogenfosforečná H O P O H

Závěr: §Atomy se ve snaze dosáhnout stabilní elektronové konfigurace spojují chemickými vazbami do molekul. §Toto uspořádání je tedy stabilnější a má nižší energii, než volné atomy. Při vzniku vazby se uvolňuje energie, k jejímu štěpení je třeba energii dodat. §Lewisova představa vazby: • vazba kovalentní: je tvořena elektronovým párem, který je sdílen vázanými atomy Sdílený elektronový pár nazýváme vazebný elektronový pár Pár valenčních elektronů, který se vazby neúčastní se nazývá volný elektronový pár • vazba iontová je tvořena opačně nabitými ionty, které jsou přitahovány elektrostatickými silami
- Slides: 15