CHEMICK REAKCIE IX ronk o s chemick reakcie







- Slides: 13

CHEMICKÉ REAKCIE IX. ročník

Čo sú chemické reakcie? Chemické reakcie sú deje, pri ktorých sa látky menia /z určitých chem. látok vznikajú iné chem. látky/. Reaktanty sú látky, ktoré vstupujú do chem. reakcie, navzájom reagujú. Produkty sú látky, vznikajú chem. reakciou. Pri chem. reakcii sa reaktanty menia na produkty Schéma zápisu: reaktanty produkty

Chem. reakcia horčíka s kyslíkom Kúsok horčíkovej pásky vložíme do plameňa kahana. Horčík horí oslnivým plameňom. Po skončení horenia vznikne biela prášková látka – oxid horečnatý Schéma zápisu: reaktanty horčík + kyslík produkty oxid horečnatý

Zákon zachovania hmotnosti pri chemických reakciách Celková hmotnosť všetkých rektantov sa rovná celkovej hmotnosti všetkých produktov. Pri chem. reakcii zreagovalo 8 g vodíka a 64 g kyslíka. Koľko gramov vody vzniklo? Schéma zápisu: reaktanty produkty vodík + kyslík voda 8 g + 64 g = 72 g Chem. reakciou vzniklo 72 g vody.

Chemické rovnice Chemická rovnica je presný zápis chemickej reakcie pomocou značiek a vzorcov. Počty atómov pred a po reakcii zapisujeme stechiometrickými koeficientami Počet a druh atómov sa pri chemických reakciách nemení. Ø Pri chemických reakciách atómy nevznikajú ani nezanikajú Ø Atóm jedného prvku sa nemôže premeniť na atóm iného prvku Ø V priebehu reakcie nastáva spájanie, oddeľovanie a preskupovanie atómov (John Dalton)

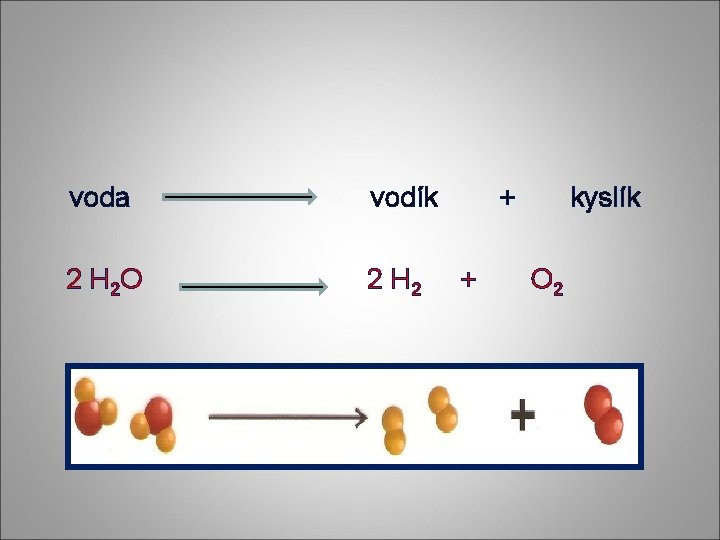
voda vodík 2 H 2 O 2 H 2 + + kyslík O 2

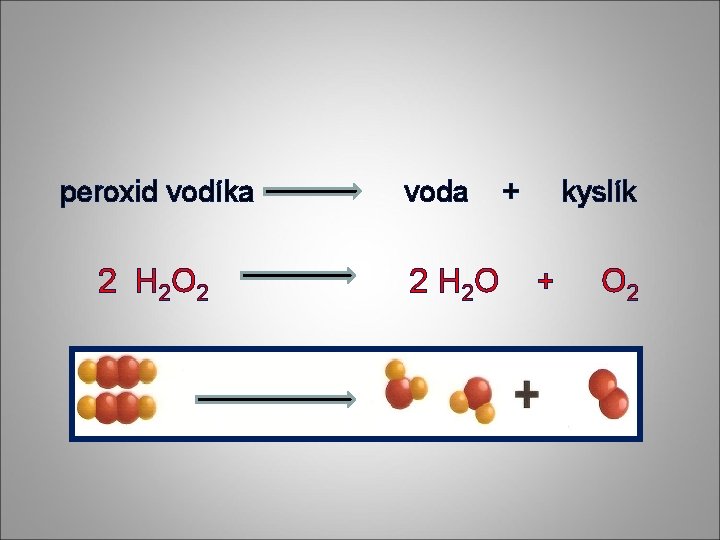
peroxid vodíka 2 H 2 O 2 voda 2 H 2 O + kyslík + O 2

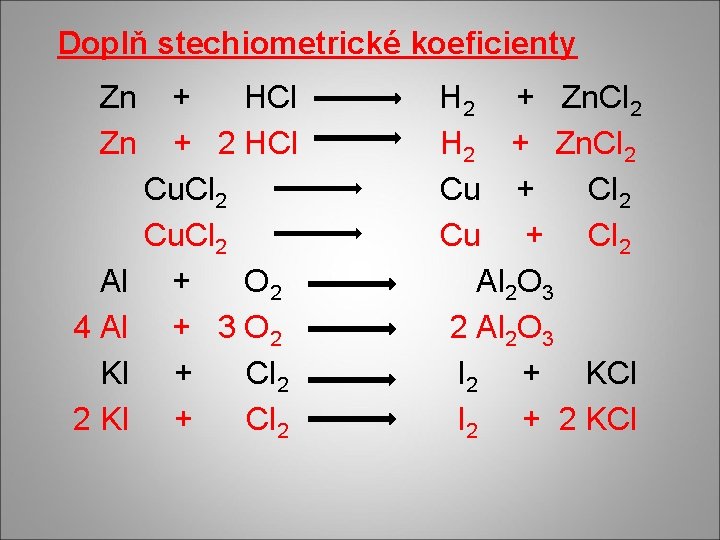
Doplň stechiometrické koeficienty Zn Zn Al 4 Al KI 2 KI + HCl + 2 HCl Cu. Cl 2 + O 2 + 3 O 2 + Cl 2 H 2 + Zn. Cl 2 Cu + Cl 2 Al 2 O 3 I 2 + KCl I 2 + 2 KCl

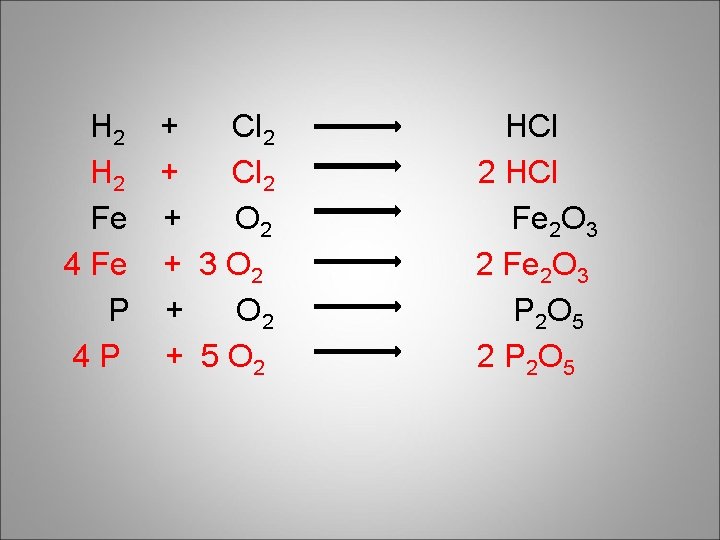
H 2 + Cl 2 Fe + O 2 4 Fe + 3 O 2 P + O 2 4 P + 5 O 2 HCl Fe 2 O 3 2 Fe 2 O 3 P 2 O 5 2 P 2 O 5

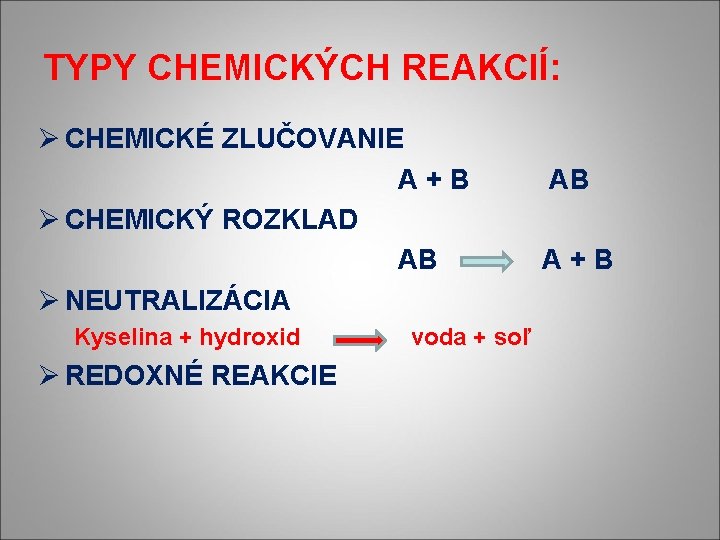
TYPY CHEMICKÝCH REAKCIÍ: Ø CHEMICKÉ ZLUČOVANIE A+B Ø CHEMICKÝ ROZKLAD AB Ø NEUTRALIZÁCIA Kyselina + hydroxid Ø REDOXNÉ REAKCIE voda + soľ AB A+B

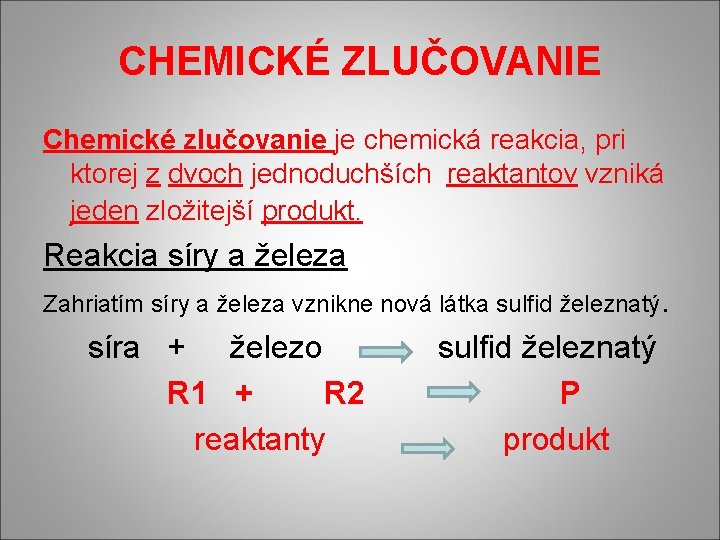
CHEMICKÉ ZLUČOVANIE Chemické zlučovanie je chemická reakcia, pri ktorej z dvoch jednoduchších reaktantov vzniká jeden zložitejší produkt. Reakcia síry a železa Zahriatím síry a železa vznikne nová látka sulfid železnatý. síra + železo R 1 + R 2 reaktanty sulfid železnatý P produkt

CHEMICKÝ ROZKLAD Chemický rozklad je chemická reakcia, pri ktorej z jedného zložitejšieho reaktantu vznikajú dva alebo viac jednoduchších produktov. Reakcia rozkladu oxidu ortuťnatého Oxid ortuťnatý sa teplom rozkladá na ortuť a kyslík Oxid ortuťnatý R Reaktant ortuť + kyslík P 1 + P 2 produkty

Zdroj: E. Adamkovič: Chémia 8 A. Velikanič, T. Šramko: Chemická čítanka www. google. sk Mariana Pavelčáková, ZŠ Belehradská 21, Košice • http: //www. eaktovka. sk/catalogue/view/chemia-pre-8 -rocnik-zakladnej-skolya-3 -rocnik-gymnazia-s-osemrocnym-studiom-1/back: Y 2 F 0 YWxv. Z 3 Vl. L 215