Chemick kinetika Reakn rychlost rychlost vzniku ltky Arrheniova











- Slides: 13

Chemická kinetika Reakční rychlost, rychlost vzniku látky, Arrheniova rovnice

Mikrokinetika a Makrokinetika v Mikrokinetické prvky – – stejné ve všech zařízeních souvisí s chováním malých částic – molekul studuje fyzikální chemie např. difuzní koeficient, rychlostní konstanta v Makrokinetické prvky – – závislé na konkrétním zařízení souvisí se soustavou jako celkem (velikostí reaktoru) studuje chemické inženýrství např. objem reaktoru, koeficient přestupu tepla Institute of Chemical Technology - Prague, Technicka 5, 166 28 Praha, Czech Republic

Rychlost vzniku složky v Počet molů složky vzniklé v jednotce objemu reakční směsi za jednotku času v Přímo měřitelná veličina v + látka přibývá v - látka ubývá Institute of Chemical Technology - Prague, Technicka 5, 166 28 Praha, Czech Republic

Rychlost reakce v Definiční stechiometrická rovnice – stechiometrická rovnice může být libovolným násobkem popisu mechanismu v Rychlost reakce – hodnota rychlosti reakce závisí na použité stechiometrické rovnici Institute of Chemical Technology - Prague, Technicka 5, 166 28 Praha, Czech Republic

Rychlostní rovnice v Jednoduchá nevratná reakce v Ideální chování Institute of Chemical Technology - Prague, Technicka 5, 166 28 Praha, Czech Republic

Empirická rychlostní rovnice v Reálný systém – řád reakce • • vyjadřuje neideálnost citlivosti rychlosti reakce na koncentraci při ideálním chování je totožný s molekularitou může být necelistvý nutno experimentálně zjistit – možno použít i jiné funkce než mocninné • využití ve specializovaných oblastech Institute of Chemical Technology - Prague, Technicka 5, 166 28 Praha, Czech Republic

Závislost rychlostní konstanty na teplotě v Arrheniova rovnice Institute of Chemical Technology - Prague, Technicka 5, 166 28 Praha, Czech Republic

Př. 1 – Rychlost reakce v Oxidace ethanolu – C 2 H 5 OH + ½ O 2 CH 3 CHO + H 2 O – 2 C 2 H 5 OH + O 2 2 CH 3 CHO + 2 H 2 O v r. CH 3 CHO= 0, 002 mol m-3 s-1 v Dojde se podle obou stechiometrických rovnic ke stejné hodnotě reakční rychlosti ? Institute of Chemical Technology - Prague, Technicka 5, 166 28 Praha, Czech Republic

Př. 2 – Vliv molekulatity/řádu na rychlost v Reakce A B, 2 A B – ideální chování v Rychlostní konstanta 0, 1 m 3 mol-1 s-1 v Koncentrace c = 0, 0 – 2, 0 mol. m-3 v Porovnejte závislosti rychlosti reakce na koncentraci látky A pro obě reakce v Porovnejte se závislostmi relativních rychlostí spočítaných z empirických rychlostních rovnic a = <0; 2> Institute of Chemical Technology - Prague, Technicka 5, 166 28 Praha, Czech Republic

Př. 3 – Závislost k na T v Nakreslete graf závislosti rychlostní konstanty na teplotě pro následující soubory parametrů – k 273, 15 = 0, 1 s-1 – k 273, 15 = 0, 2 s-1 E = 50 k. J – k 273, 15 = 1 s-1 – k 273, 15 = 2 s-1 E = 50 k. J E = 40 k. J – A = 1 E 6 s-1 E = 5 k. J Institute of Chemical Technology - Prague, Technicka 5, 166 28 Praha, Czech Republic

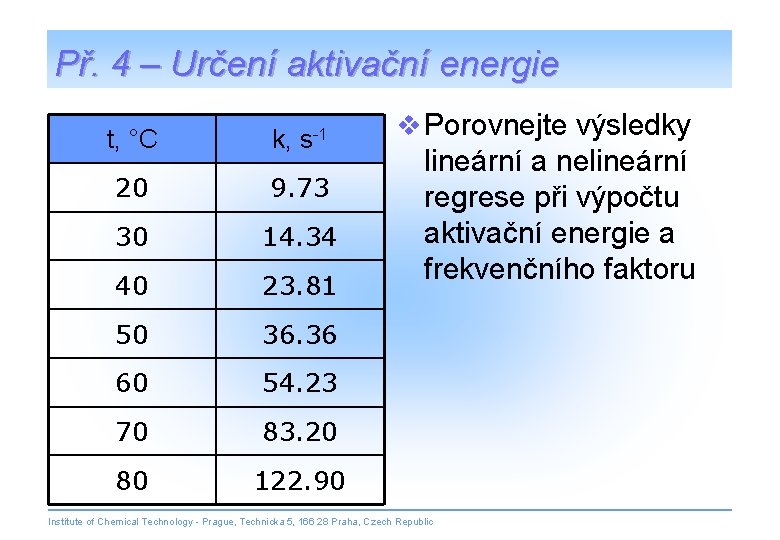
Př. 4 – Určení aktivační energie t, °C k, s-1 20 9. 73 30 14. 34 40 23. 81 50 36. 36 60 54. 23 70 83. 20 80 122. 90 v Porovnejte výsledky lineární a nelineární regrese při výpočtu aktivační energie a frekvenčního faktoru Institute of Chemical Technology - Prague, Technicka 5, 166 28 Praha, Czech Republic

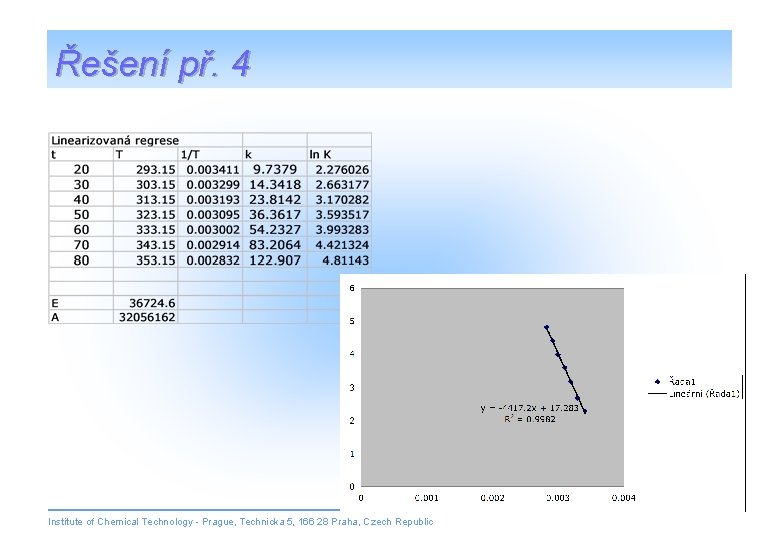
Řešení př. 4 Institute of Chemical Technology - Prague, Technicka 5, 166 28 Praha, Czech Republic

… Institute of Chemical Technology - Prague, Technicka 5, 166 28 Praha, Czech Republic