Chemick kinetika as fyziklnej Chemick kinetika sa zaober

Chemická kinetika- časť fyzikálnej

Chemická kinetika sa zaoberá skúmaním toho ako rýchlo prebiehajú chemické reakcie. Ako sa mení rýchlosť zmenou: teploty? stavu reaktantov? Množstva reaktantov? katalyzátora? povrchu reagujúcich látok?

Prečo je dôležité skúmať kinetiku? Umožní to určiť mechanizmus priebehu chemickej reakcie. Pomôže nám to určiť ako ovplyvniť rýchlosť reakcie.

Priebeh reakcie na molekulovej úrovni

Rýchlosť reakcie Je zmena látkového množstva reaktantu alebo produktu za jednotkový čas v je rýchlosť reakcie (mol s-1) ( m (moles o l B) B) vv== tt

Čo vplýva na rýchlosť reakcie Koncentrácia reaktantov teplota katalyzátor plocha povrchu (v heterogénnych reakciách)
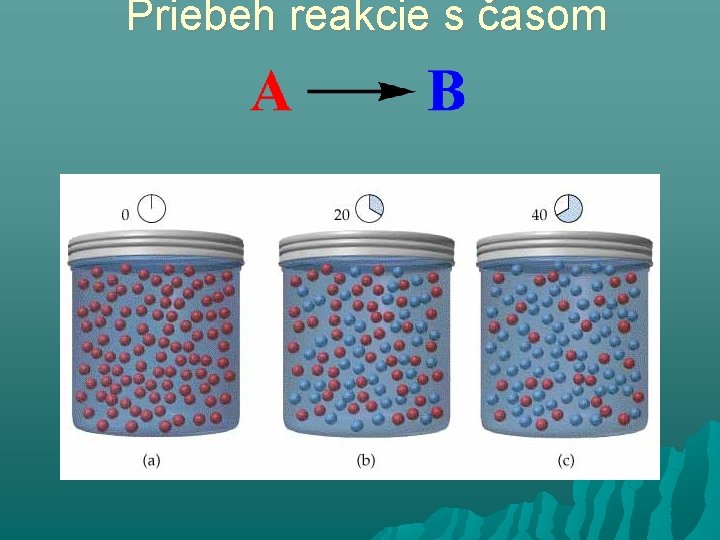
Priebeh reakcie s časom
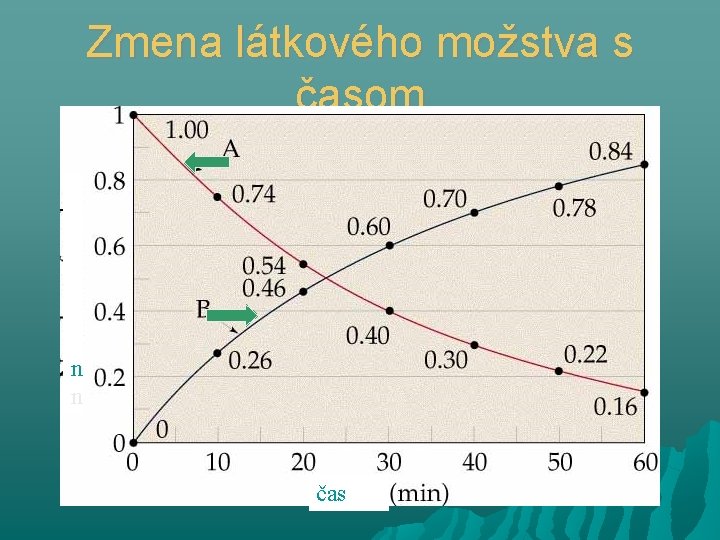
Zmena látkového možstva s časom n n čas
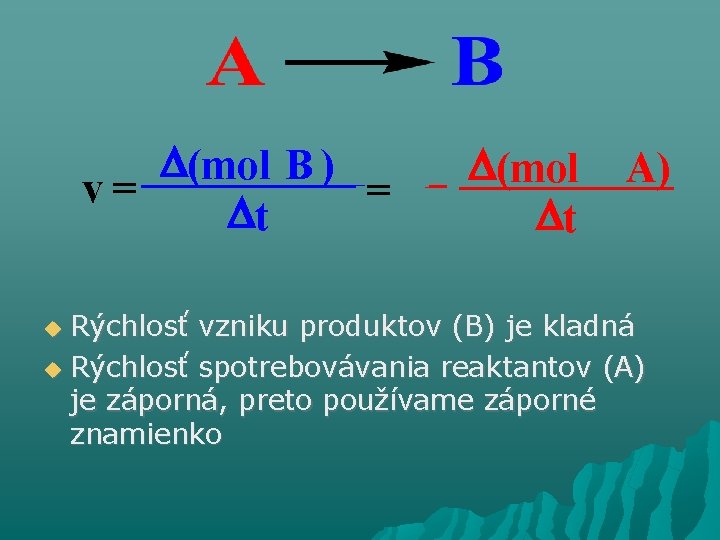
(mol B ) v= = t (mol t A) Rýchlosť vzniku produktov (B) je kladná Rýchlosť spotrebovávania reaktantov (A) je záporná, preto používame záporné znamienko
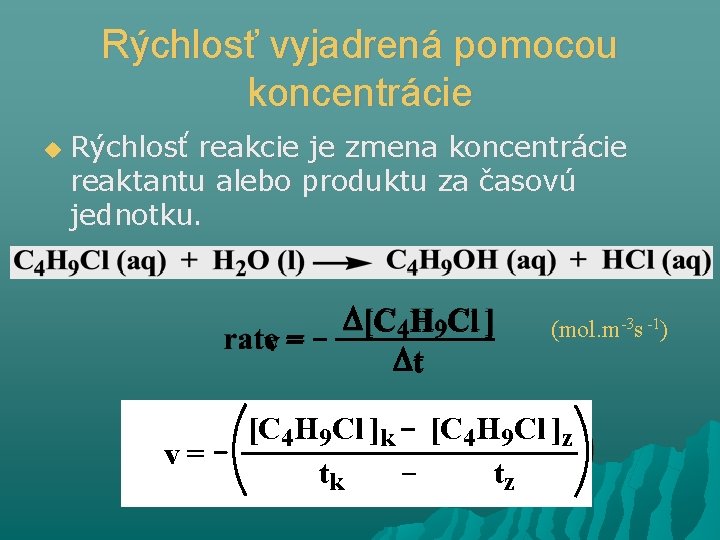
Rýchlosť vyjadrená pomocou koncentrácie Rýchlosť reakcie je zmena koncentrácie reaktantu alebo produktu za časovú jednotku. v= v= [C 4 H 9 Cl ] t [C 4 H 9 Cl ]k tk (mol. m-3 s -1) [C 4 H 9 Cl ]z tz
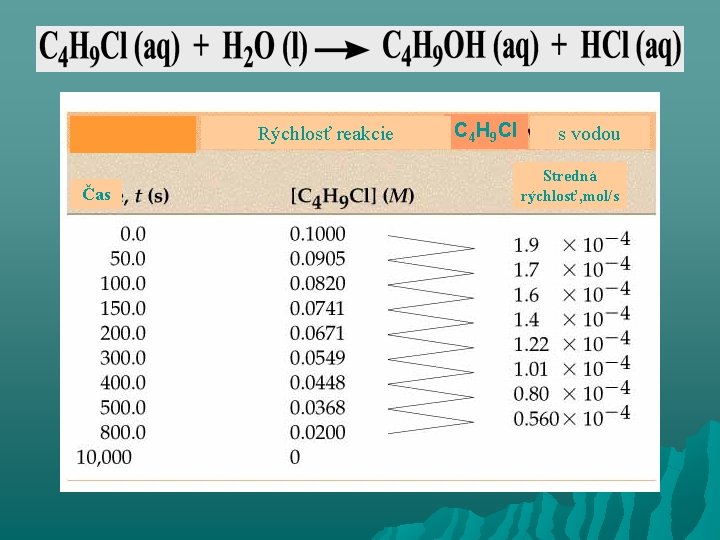
Rýchlosť reakcie Čas C 4 H 9 Cl s vodou Stredná rýchlosť, mol/s
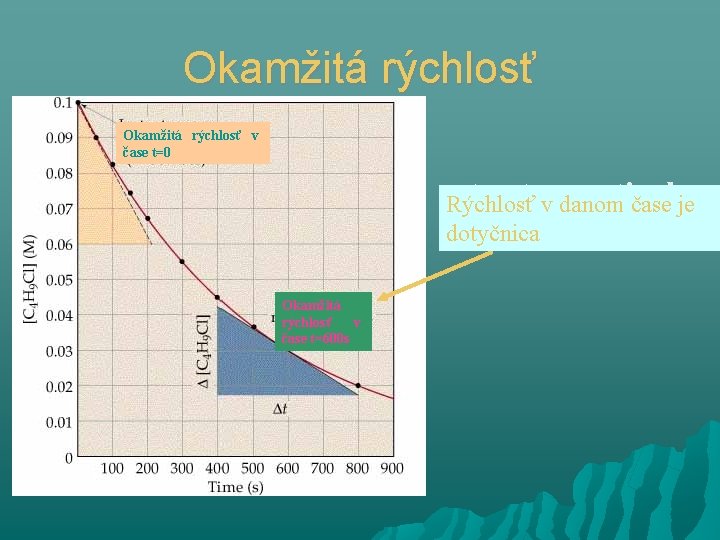
Okamžitá rýchlosť v čase t=0 rate at av danom particular Rýchlosť čase je dotyčnica time - use tangent Okamžitá rýchlosť v čase t=600 s

Relatívne rýchlosti “Rýchlosť rozkladu HI je dvakrát väčšia ako rýchlosť vzniku H 2. ” “Rýchlosť rozkladu HI je dvakrát väčšia ako rýchlosť vzniku I 2. ” “Rýchlosť vzniku H 2 je dvakrát nižšia ako rýchlosť rozkladu of HI. ”
![Relatívne rýchlosti [B] [C] [D] [A] 1 1 v= a = b = c Relatívne rýchlosti [B] [C] [D] [A] 1 1 v= a = b = c](http://slidetodoc.com/presentation_image/1448cce11d2ca1ac936fa59a37333e18/image-14.jpg)
Relatívne rýchlosti [B] [C] [D] [A] 1 1 v= a = b = c =d t t

Kinetické rovnice Diferenciálna – závislosť rýchlosti reakcie od koncentrácie Integrálna– času závislosť koncentrácie od

Kinetická rovnica Vyjadruje rýchlosť reakcie pomocou koncentrácií reaktantov a rýchlostnej konštanty Pre všeobecnú reakciu a. A+b. B+c. C d. D+e. E rýchlosť = k[A]m[B]n[C]y Exponenty (m, n, a y) sa nazývajú poriadok reakcie.
![Kinetická rovnica 2 NO 2 2 NO + O 2 v = k[NO 2]n Kinetická rovnica 2 NO 2 2 NO + O 2 v = k[NO 2]n](http://slidetodoc.com/presentation_image/1448cce11d2ca1ac936fa59a37333e18/image-17.jpg)
Kinetická rovnica 2 NO 2 2 NO + O 2 v = k[NO 2]n k = rýchlostná konštanta n = poriadok reakcie V kinetických rovniciach sa používajú iba koncentrácie reaktantov
![Ako určiť kinetickú rovnicu a. A+b. B c. C+d. D rýchlosť = k[A]x[B]y Udržujeme Ako určiť kinetickú rovnicu a. A+b. B c. C+d. D rýchlosť = k[A]x[B]y Udržujeme](http://slidetodoc.com/presentation_image/1448cce11d2ca1ac936fa59a37333e18/image-18.jpg)
Ako určiť kinetickú rovnicu a. A+b. B c. C+d. D rýchlosť = k[A]x[B]y Udržujeme konštantnú koncentrciu jedného reaktantu (napr. A) Uskutočníme sériu pokusov s cieľom určiť ako vplýva koncentrácia B na začiatočnú rýchlosť reakcie. rýchlosť = (konštanta) [B]y

Ako určiť kinetickú rovnicu Teraz udržiavame konštantnú koncentráciu reaktantu B. Uskutočníme ďalšiu sériu pokusov a sledujeme ako zmena koncentrácie A vplýva na začiatočnú rýchlosť reakcie? rýchlosť = (konštanta [A]x
![Poriadok reakcie a rýchlostná konštanta rýchlosť 2]n. . . = k [reaktant 1]m[reaktant suma Poriadok reakcie a rýchlostná konštanta rýchlosť 2]n. . . = k [reaktant 1]m[reaktant suma](http://slidetodoc.com/presentation_image/1448cce11d2ca1ac936fa59a37333e18/image-20.jpg)
Poriadok reakcie a rýchlostná konštanta rýchlosť 2]n. . . = k [reaktant 1]m[reaktant suma m + n je celkový poriadok reakcie hodnoty m a n sa musia určiť pokusom, nedajú sa určiť zo stechiometrie reakcie Jednotky rýchlostnej konštanty závisia od poriadku reakcie!

Elementárne kroky a molekularita Každá chemická reakcia sa uskutočňuje v elementárnych krokoch Kinetika elementárnych krokov závisí len od počtu molekúl reaktantov v tomto kroku Molekulovosť je počet molekúl rektantov, ktoré sa na tomto kroku zúčastňujú

Reakcie nultého poriadku Rýchlosť nezávisí od koncentrácie! Často sú to katalytické reakcie o v = k[A] = k
![Reakcia nultého poriadku v = -k [A]t = -kt + [A]o [A] smernica t Reakcia nultého poriadku v = -k [A]t = -kt + [A]o [A] smernica t](http://slidetodoc.com/presentation_image/1448cce11d2ca1ac936fa59a37333e18/image-23.jpg)
Reakcia nultého poriadku v = -k [A]t = -kt + [A]o [A] smernica t = -k

Reakcia nultého poriadku-príklad 2 N 2 O (g) 2 N 2 (g) + O 2 (g) Reakcia je katalyzovaná Pt. Zvýšenie počtu molekúl N 2 O neovplyvňuje rýchlosť.

Reakcia prvého poriadku Rýchlosť závisí iba od koncentrácie jediného reaktantu A produkt Príklad: CH 3 NC CH 3 CN
![Reakcia prvého poriadku – A produkt – v = - [A]/ t = k[A] Reakcia prvého poriadku – A produkt – v = - [A]/ t = k[A]](http://slidetodoc.com/presentation_image/1448cce11d2ca1ac936fa59a37333e18/image-26.jpg)
Reakcia prvého poriadku – A produkt – v = - [A]/ t = k[A] – Ako závisí koncentrácia reaktantu od času? k má jednotku (s-1)
![Integrálna kinetická rovnica 1. poriadku v= [A] k[A] = t Integrálna kinetická rovnica 1. poriadku v= [A] k[A] = t](http://slidetodoc.com/presentation_image/1448cce11d2ca1ac936fa59a37333e18/image-27.jpg)
Integrálna kinetická rovnica 1. poriadku v= [A] k[A] = t

Polčas reakcie 1. poriadku

Polčas pre reakciu 1. poriadku Polčas sa vypočíta takto:
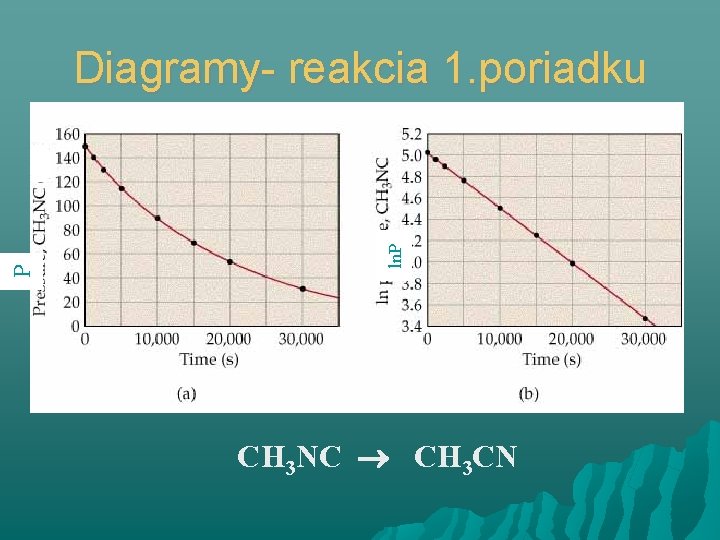
ln. P P Diagramy- reakcia 1. poriadku CH 3 NC CH 3 CN
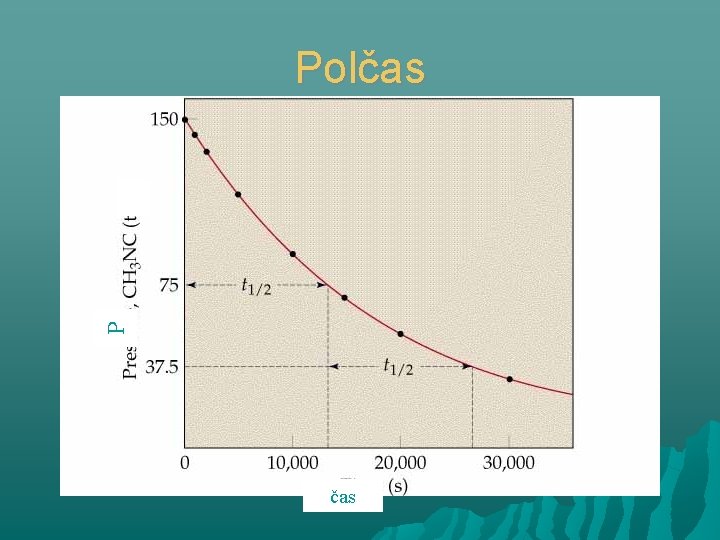
P Polčas

Polčas reakcie 1. poriadku
![Reakcia 2. poriadku A + B produkty v = k[A][B] – A produkty v Reakcia 2. poriadku A + B produkty v = k[A][B] – A produkty v](http://slidetodoc.com/presentation_image/1448cce11d2ca1ac936fa59a37333e18/image-33.jpg)
Reakcia 2. poriadku A + B produkty v = k[A][B] – A produkty v = k[A]2 Reakcia 1 je 1. poriadku pre A a B a celkovo je 2. poriadku Reakcia 2 je 2. poriadku pre A –
![Závislosť koncentrácie od času Pre reakciu druhého poriadku kde v = k[A]2 k má Závislosť koncentrácie od času Pre reakciu druhého poriadku kde v = k[A]2 k má](http://slidetodoc.com/presentation_image/1448cce11d2ca1ac936fa59a37333e18/image-34.jpg)
Závislosť koncentrácie od času Pre reakciu druhého poriadku kde v = k[A]2 k má rozmer (mol/ m³)-1 s -1

Reakcia druhého poriadku Rýchlosť závisí od druhej mocniny koncentrácie jedného reaktantu, alebo od koncentrácií dvoch rôznych reaktantov. A produkty alebo A + B produkty Príklad: NO 2 NO + 1/2 O 2
![Integrovaná kinetická rovnica reakcia 2. poriadku [A] 2 v= t = k[A] Integrovaná kinetická rovnica reakcia 2. poriadku [A] 2 v= t = k[A]](http://slidetodoc.com/presentation_image/1448cce11d2ca1ac936fa59a37333e18/image-36.jpg)
Integrovaná kinetická rovnica reakcia 2. poriadku [A] 2 v= t = k[A]
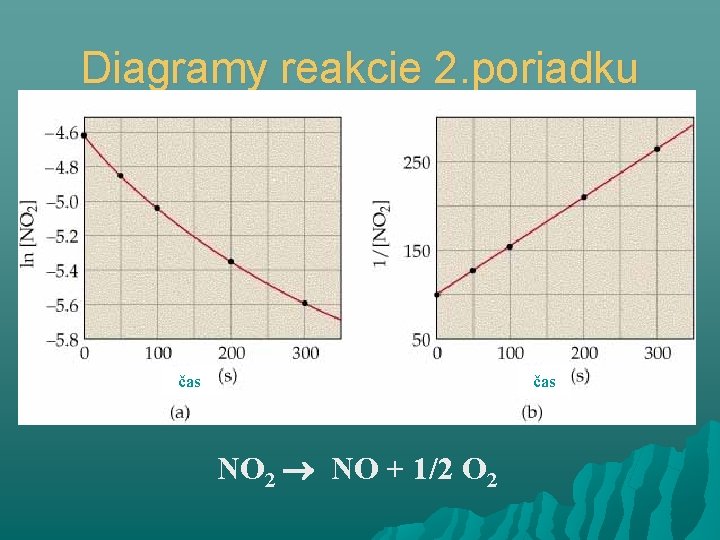
Diagramy reakcie 2. poriadku čas NO 2 NO + 1/2 O 2
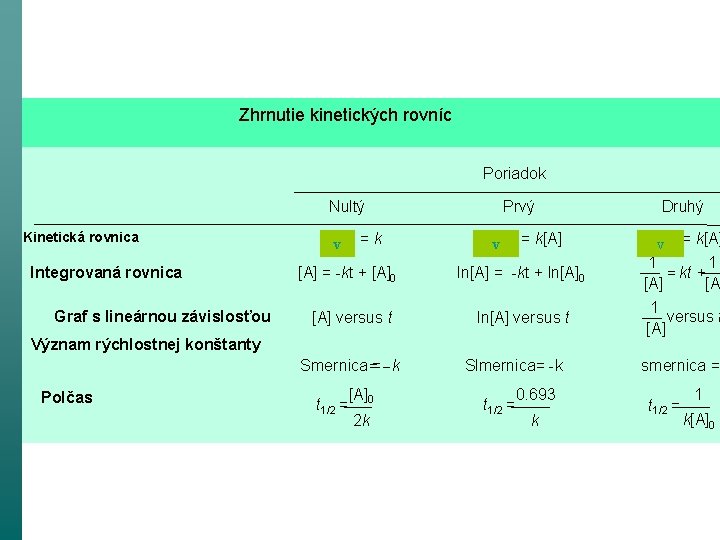
12_06 T Zhrnutie kinetických rovníc Poriadok Nultý Kinetická rovnica Integrovaná rovnica Graf s lineárnou závislosťou Prvý Druhý Rate v =k Rate v = k[A] = -kt + [A]0 ln[A] = -kt + ln[A]0 Rate v = k[A] 1 1 = kt + [A] [A 1 versus t [A] versus t ln[A] versus t Význam rýchlostnej konštanty Smernica==--k Polčas t 1/2 = [A]0 2 k Slmernica= -k t 1/2 = 0. 693 k smernica = t 1/2 = 1 k[A]0

Poriadok reakcie Poriadok rakcie udáva počet výrazov pre koncentráciu v kinetickej rovnici Poriadok reakcie Nultý Prvý Druhý kinetická rovnica jednotky k mol m-3 s s -1 -1 (mol m-3 ) -1 s -1
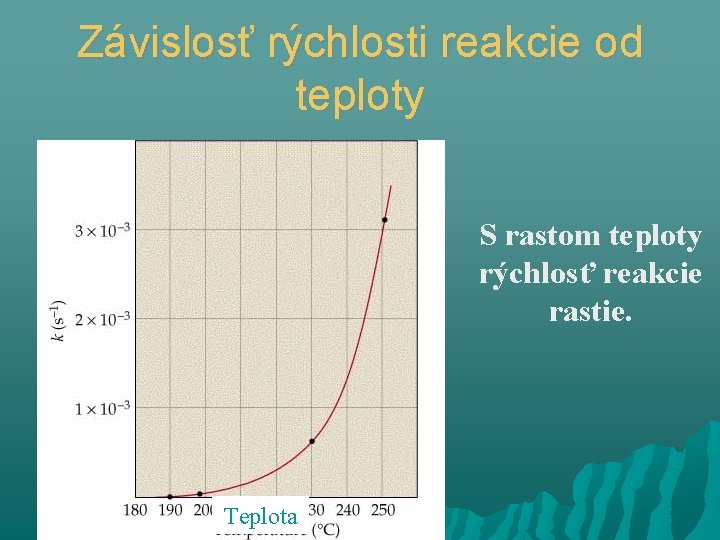
Závislosť rýchlosti reakcie od teploty S rastom teploty rýchlosť reakcie rastie. Teplota

Približné pravidlo pre rýchlosť chemickej reakcie: Rýchlosť reakcie sa ~ zdvojnásobí ak sa teplota zvýši o 10º.

Svante August Arrhenius 1859 -1927
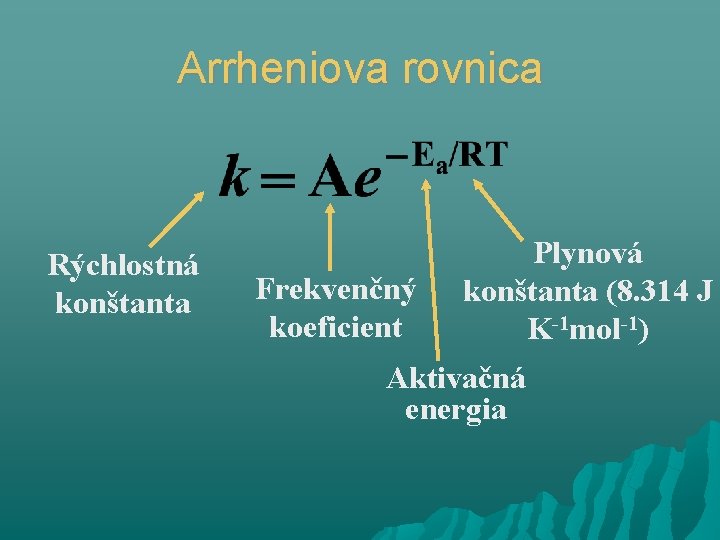
Arrheniova rovnica Rýchlostná konštanta Frekvenčný koeficient Plynová konštanta (8. 314 J K-1 mol-1) Aktivačná energia
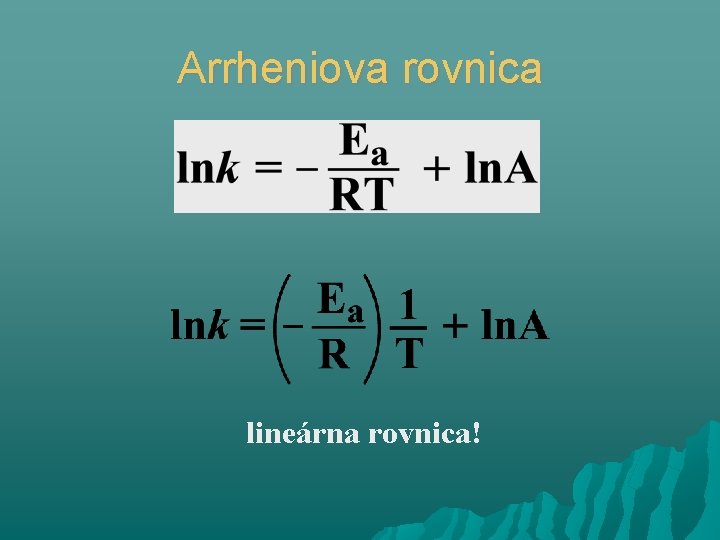
Arrheniova rovnica lineárna rovnica!
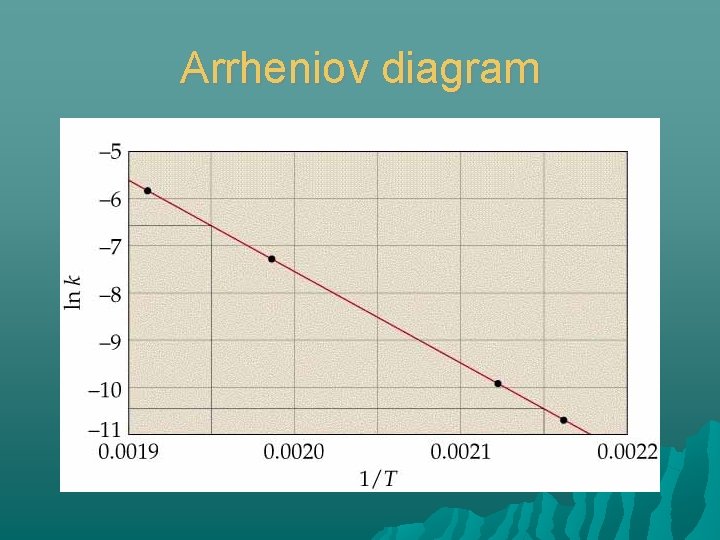
Arrheniov diagram

Arrheniova rovnica Problém Aktivačná energia istej reakcie je 76. 7 k. J/mol. Kokľkokrát rýchlejšie prebehne reakcia pri teplote 50°C ako pri 0°C?

Model chemickej kinetiky Reakcia teploty. sa urýchľuje zvýšením Molekuly sa musia zraziť aby reagovali. Zrážky musia mať dostatočnú energiu. Počas zrážok musia mať molekuly správnu orientáciu.

Teória zrážok Rýchlosť reakcie rastie s teplotou ( uskutočňuje sa viac zrážok) Chemická reakcia prebieha v dôsledku zrážok medzi molekulami reaktantov – t. j. Rýchlosť je priamo úmerná počtu zrážok za jednotku času – A 2 + B 2 produkt v = k[A 2][B 2]
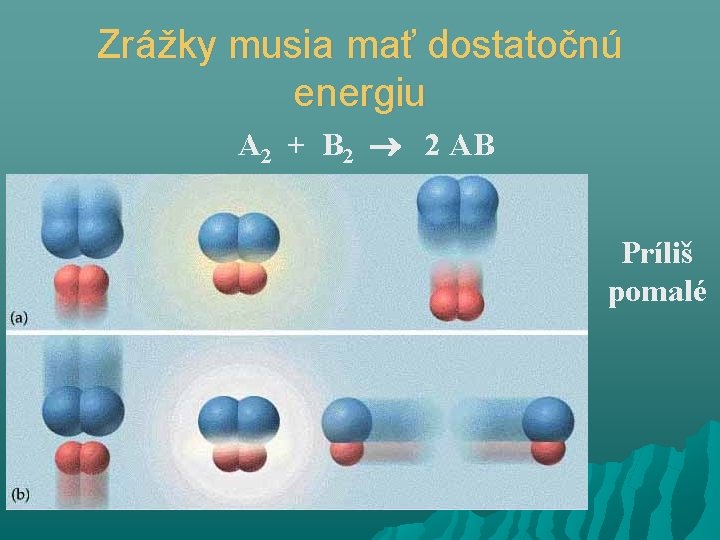
Zrážky musia mať dostatočnú energiu A 2 + B 2 2 AB Príliš pomalé
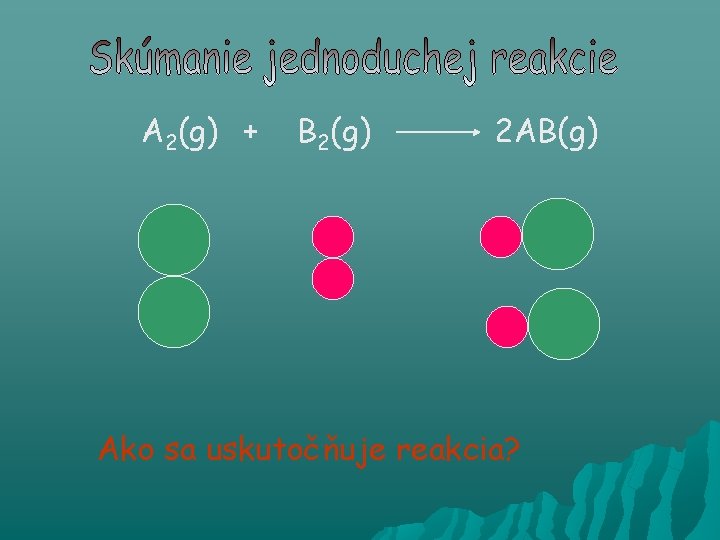
A 2(g) + B 2(g) 2 AB(g) Ako sa uskutočňuje reakcia?
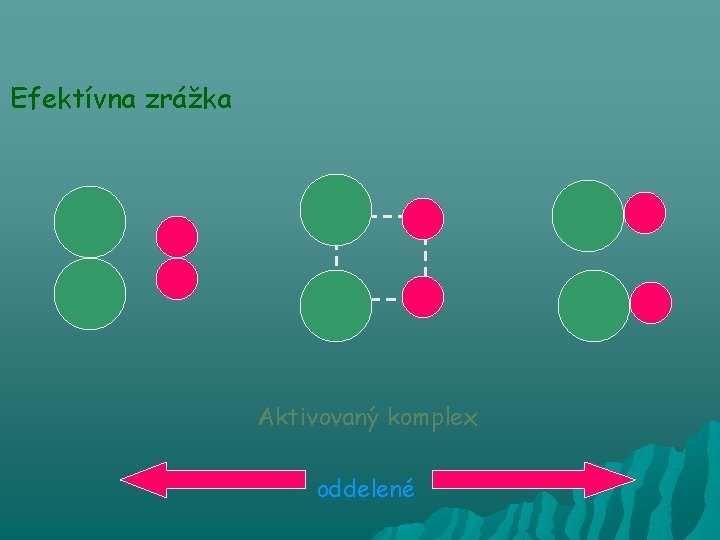
Efektívna zrážka Aktivovaný komplex oddelené

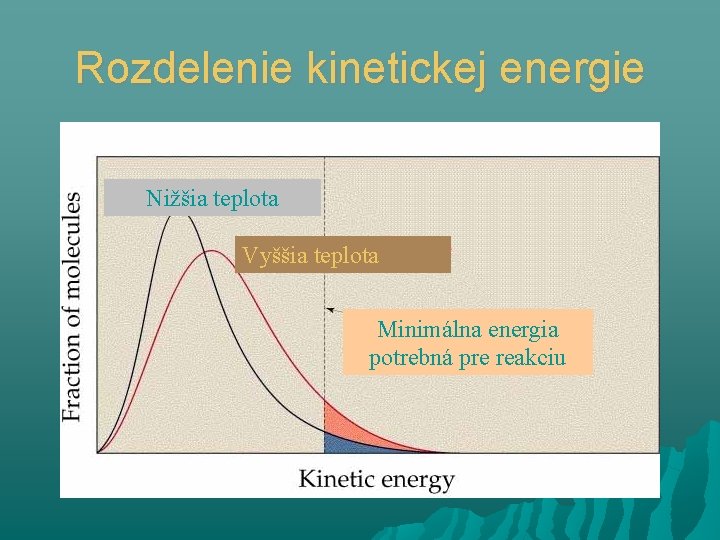
Rozdelenie kinetickej energie Nižšia teplota Vyššia teplota Minimálna energia potrebná pre reakciu
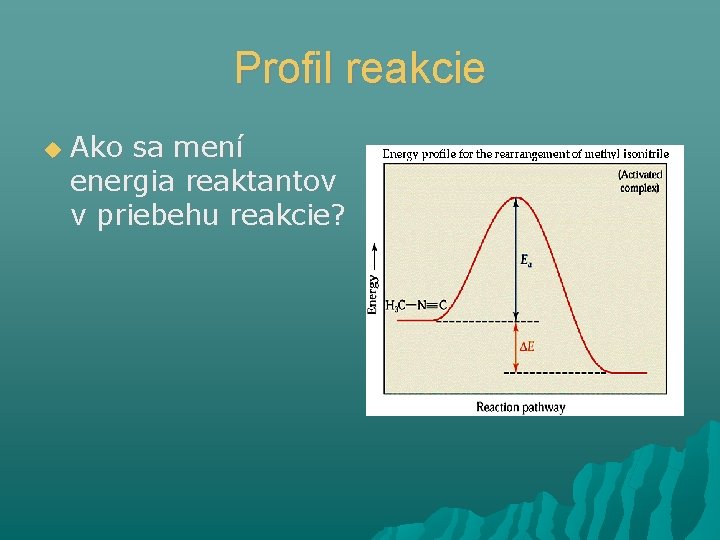
Profil reakcie Ako sa mení energia reaktantov v priebehu reakcie?

Aktivačná energia, Ea Ea = minimálna energia potrebná na spustenie chemickej reakcie. “prahová energia” “energetický kopec” “energetická bariéra”
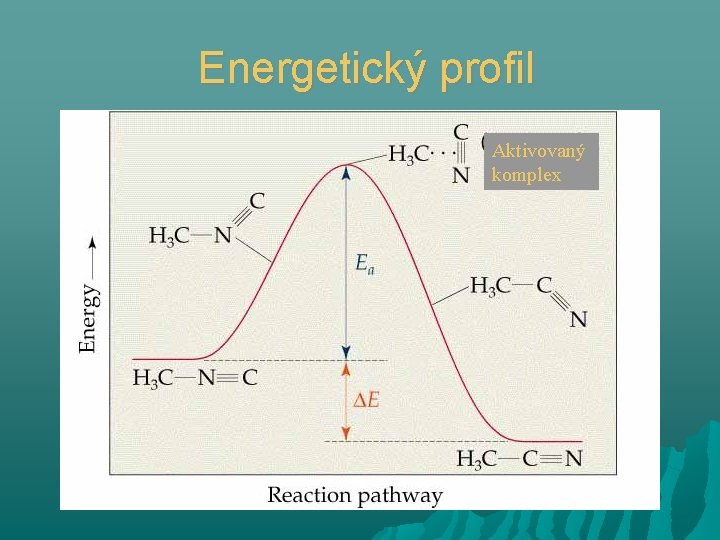
Energetický profil Aktivovaný komplex
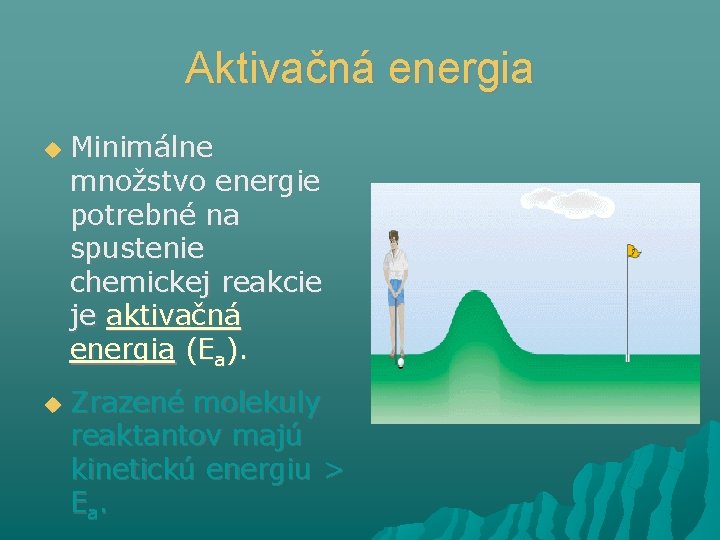
Aktivačná energia Minimálne množstvo energie potrebné na spustenie chemickej reakcie je aktivačná energia (Ea). Zrazené molekuly reaktantov majú kinetickú energiu > Ea.

Aktivovaný komplex Prechodný stav, ktorý vytvárajú molekuly reaktantu. Malá časť molekúl má požadovanú kinetickú energiu na to, aby sa dostali do prechodného stavu Koncentrácia aktivovaého komplexu je veľmi nízka.
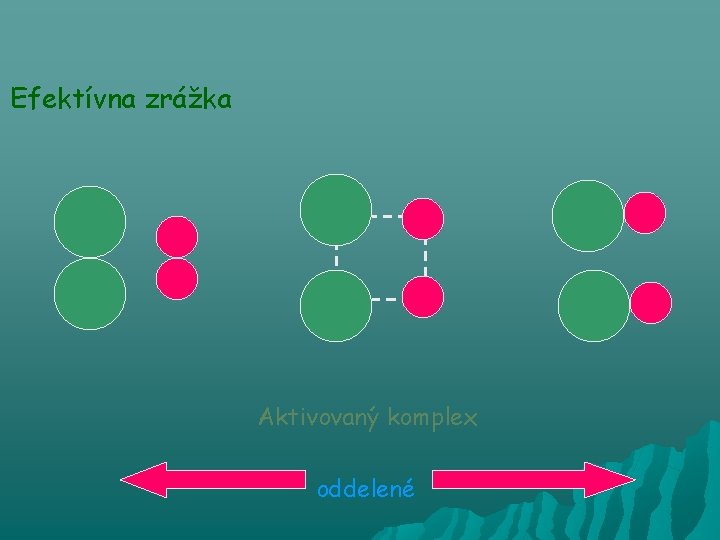
Efektívna zrážka Aktivovaný komplex oddelené

Aktivačná energia a Arrheniova rovnica Reakcia má veľkú aktivačnú energiu malú rýchlostnú konštantupomalá reakcia!! Je potrebné zmerať k pri niekoľkých teplotách R = 8. 314 J/(K mole) T v Kelvinoch!!!
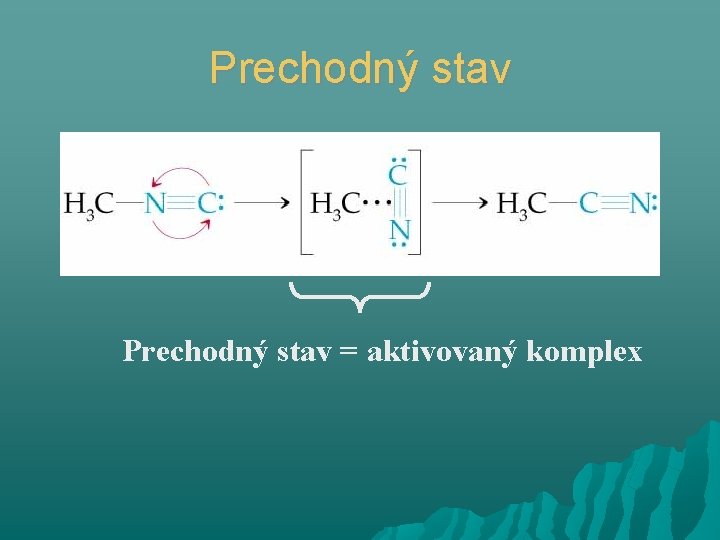
Prechodný stav = aktivovaný komplex

Orientácia zrážok Cl + Cl. NO Cl 2 + NO čas Efektívna zrážka Neefektívna zrážka

V každej chemickej reakcii: Prerušenie väzieb- vyžaduje si to prívod energie Vznik nových väzieb – energia sa uvoľňuje Existuje energetická bariéra, ktorú je treba prekonať – aktivačná energia

Reakčný mechanizmus Reakčný mechanizmus- proces, ktorým prebieha chemická reakcia Elementárny krok – jeden krok (udalosť) v mechanizme

Molekulovosť Počet molekúl, ktoré sa zúčastňujú na elementárnom kroku chemickej reakcie unimolekulárne -1 bimolekulárne -2 trimolekulárne -3
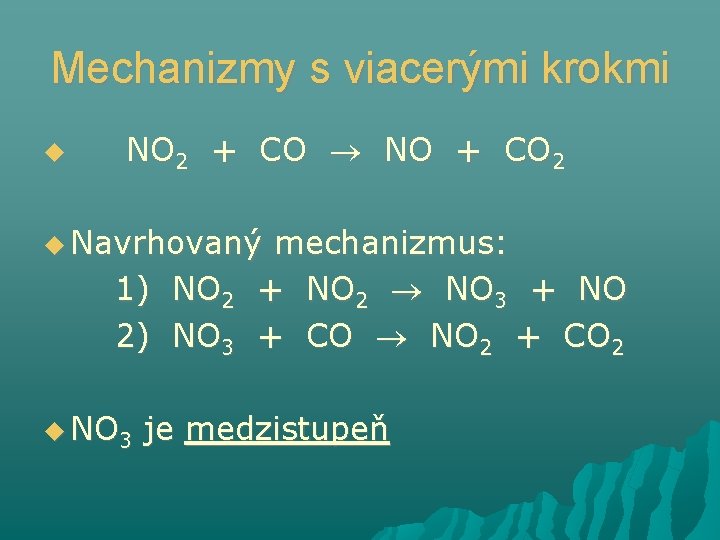
Mechanizmy s viacerými krokmi NO 2 + CO NO + CO 2 Navrhovaný 1) NO 2 2) NO 3 mechanizmus: + NO 2 NO 3 + NO + CO NO 2 + CO 2 je medzistupeň

Požiadavky na mechanizmus Súčet elementárnych rokov musí byť celková stechiometricky vyrovnaná reakcia. Mechanizmus musí súhlasiť s celkovou kinetickou rovnicou.

Kinetické rovnice elementárnych krokov Kinetickú rovnicu môžete napísať priamo pomocou molekulovisti (stechiometrie) elementárneho kroku: – – v 1 = k 1[NO 2]= k 1[NO 2]2 – v 2 = k 2[NO 3][CO]

Kinetika elementárnych krokov Elementárne kroky Unimolekulárny krok Bimolekulárny krok

Kinetika elementárnych krokov Pre krok Trimolekulový krok

Rýchlosť určujúci krok (prirovnanie k situácii v doprave) Situácia 1 – upchatá diaľnica je najpomalší krok v premávke Situácia 2 – upchatý príjazd na most pred vstupom do mesta je najpomalší krok v premávke. Rýchlosť celého procesu ( diaľnicamesto) závisí od toho, ktorý krok je najpomalší – To je rýchlosť určujúci krok.

Rýchlosť určujúci krok = najpomalší krok k 1 Príklad: pomalá 1) NO 2 + NO 2 k NO 3 + NO 2 2) NO 3 + CO NO 2 + CO 2 rýchla

Rýchlosť určujúci krok V reakcii, ktorá pozostáva z viacerých krokov je to najpomalší krok. Preto určuje celkovú rýchlosť reakcie.

Katalýza Katalyzátor je látka, ktorá zvyšuje rýchlosť reakcie bez toho, aby došlo k chemickej zmene katalyzátora Katalyzátor znižuje aktivačnú energiu reakcie obvykle sa pri tom mení mchanizmus reakcie
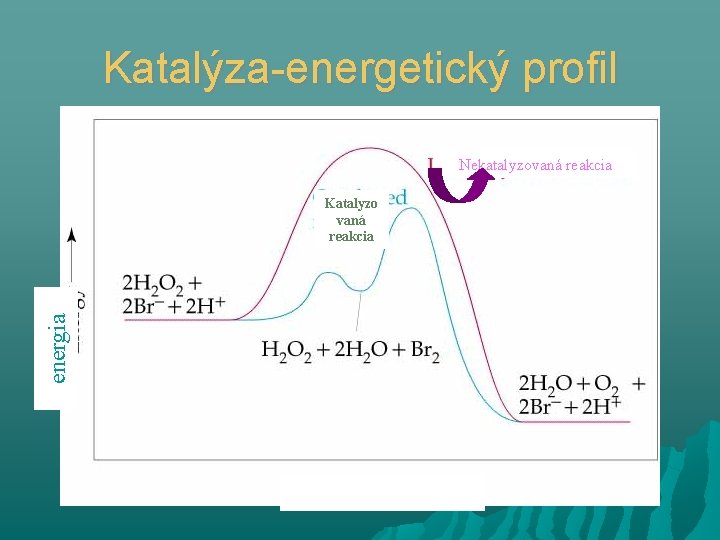
Katalýza-energetický profil Nekatalyzovaná reakcia energia Katalyzo vaná reakcia

Typy katalýzy homogénna–katalyzátor a reagujúce molekuly sú v jednej fáze heterogénna-katalyzátor a reagujúce molekuly sú v odlišných fázach

Kinetika heterogénnych reakcií Prenos reaktantu k difúznej vrstve prúdením Prenos reaktantu cez difúznu vrstvu na medzifázové rozhranie Adsorpcia reaktantu na medzifázovom povrchu Chemická reakcia Desorpcia produktu z medzifázového povrchu Difúzia produktu cez difúznu vrstvu Prenos produktu od dfúznej vrstvy prúdením

Typy heterogénnych reakcií Kvapalina- kvapalina Kvapalina-plyn (bubliny) Plyn-tuhá fáza Tuhá fáza- tuhá fáza
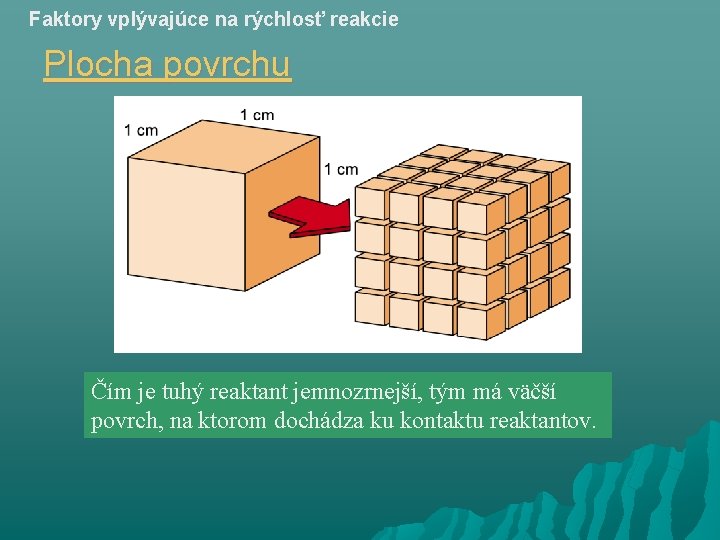
Faktory vplývajúce na rýchlosť reakcie Plocha povrchu Čím je tuhý reaktant jemnozrnejší, tým má väčší povrch, na ktorom dochádza ku kontaktu reaktantov.
Adolph Fick 1829 -1901

Molekulárny pohyb Pohyb tekutín na molekulovej úrovni • Zrážky medzi molekulami sú časté • Pri zrážkach sa zachováva hybnosť • Zrážky spôsobujú, že sa mení smer pohybu molekúl, ktoré by sa ináč pohybovali priamočiaro (1. Newtonov zákon) • Zrážky molúl so stenou nádoby spôsobujú vznik tlaku
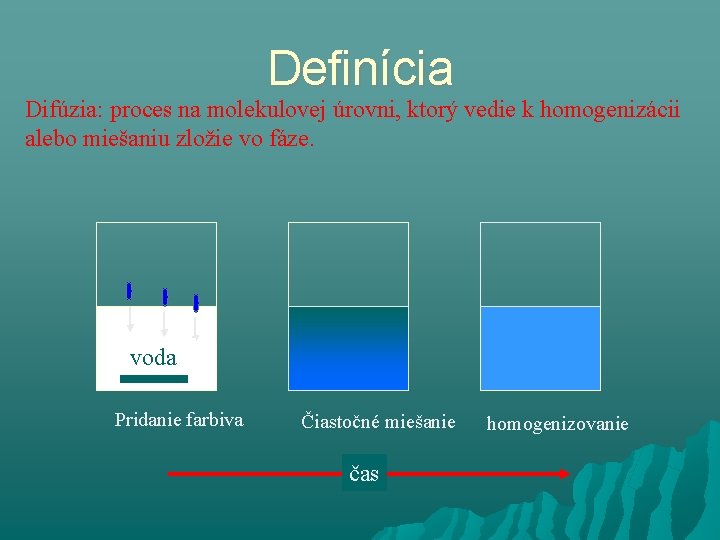
Definícia Difúzia: proces na molekulovej úrovni, ktorý vedie k homogenizácii alebo miešaniu zložie vo fáze. voda water Pridanie farbiva Čiastočné miešanie čas homogenizovanie

Difúzia Prenos atómov (molekúl) z miesta s vyššou koncentráciou na miesto s nižšou koncentráciou Závisí od teploty a rozdielu koncentrácií

Difúziou sa prenáša látka na krátku vzdialenosť Vzdialenosť Doba difúzie 10 m 10 -2 s 1 mm 100 s 10 mm 104 s 1 m 3 roky
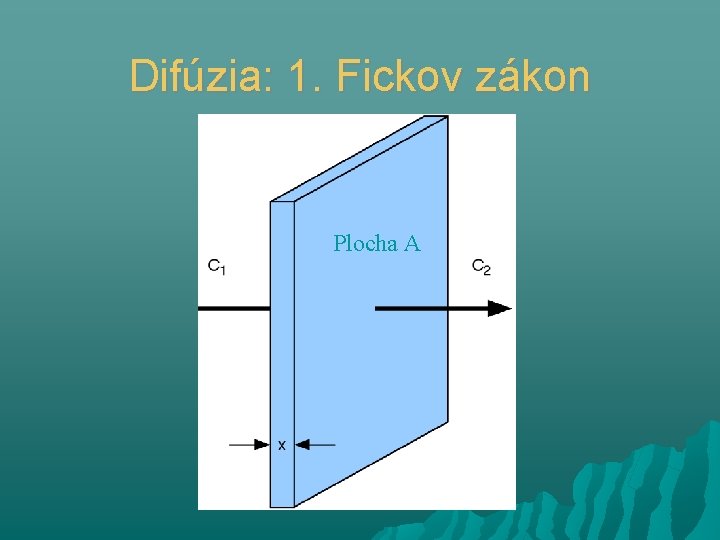
Difúzia: 1. Fickov zákon Plocha A

Difúzia: 1. Fickov zákon

Predpoklady pre Fickov zákon Po hrúbke dosky je konštantný koncentračný gradient Koncentračný gradient sa s časom nemení

Závislosť difúzie od teploty Difúzia je proces, ktorý závisí od teploty podľa dobre známej rovnice: kde D = Difúzny koeficient D 0 = Pre-faktor E = Aktivačná energia Rg = Plynová konštanta T = Teplota
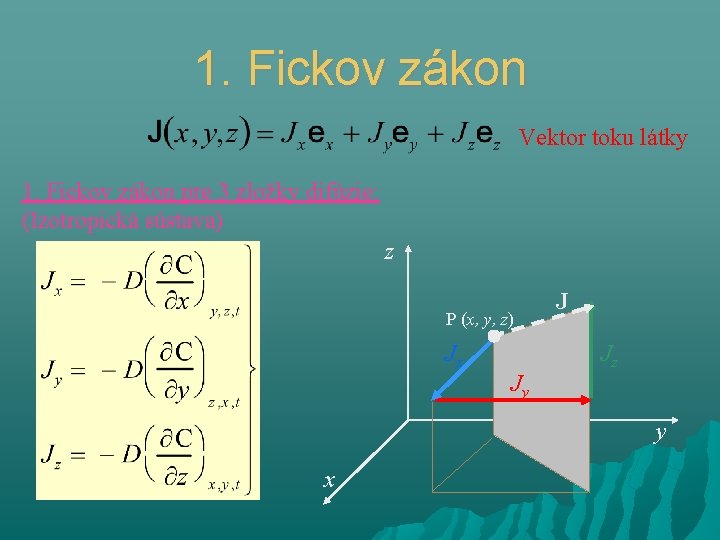
1. Fickov zákon Vektor toku látky 1. Fickov zákon pre 3 zložky difúzie: (Izotropická sústava) z P (x, y, z) Jx Jy J Jz y x

Otázky?
- Slides: 90