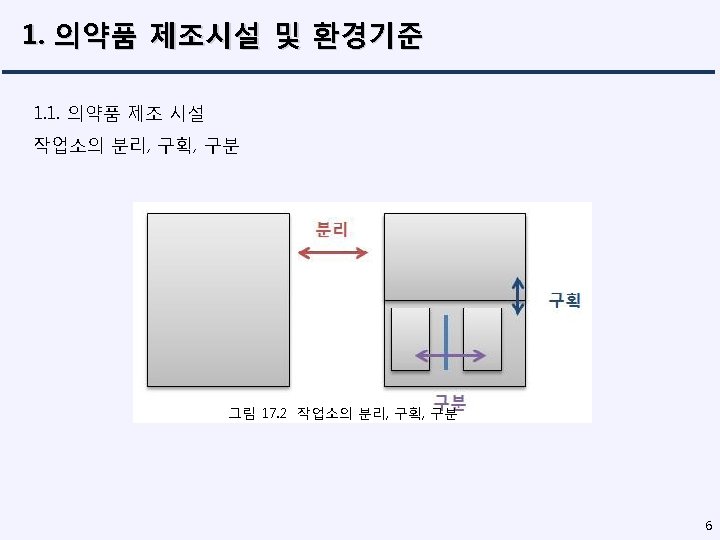
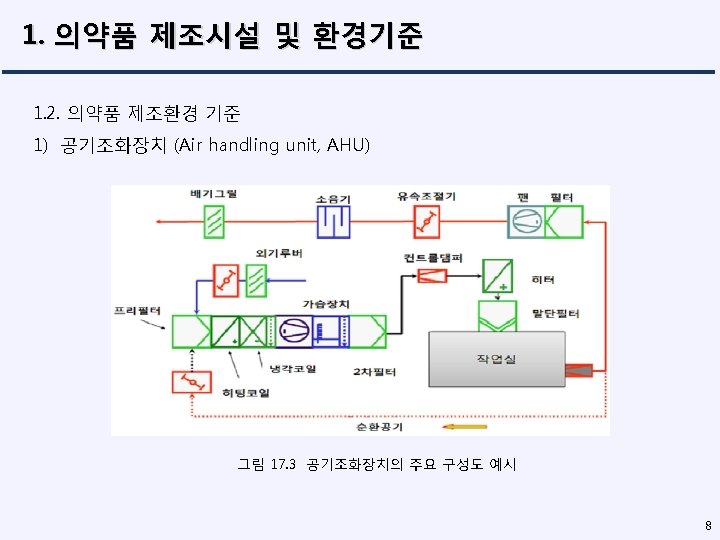
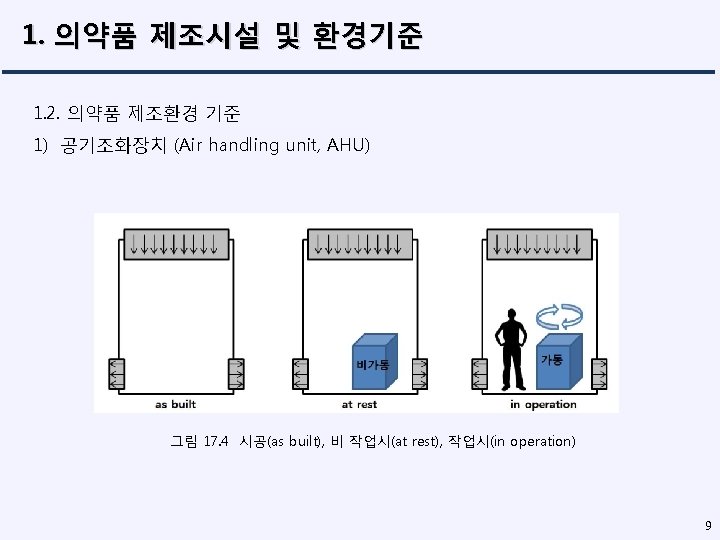
Chapter 17 1 1 1 1 2 2

















































- Slides: 77

Chapter 17 의약품 생산


목차 1. 원료 의약품 제조시설 및 환경기준 1. 1. 의약품의 제조 시설 1. 2. 의약품 제조 환경 기준 2. 무균제제 제조공정 (Sterile-Products) 2. 1. 무균제제 제조 일반 2. 2. 액상 주사제 (Liquid injection) 2. 3. 동결 건조 주사제 (Lyophilization injection) 2. 4. 분말 주사제 (Powder injection) 2. 5. New technology 3. 비무균제제 제조공정 (Non-Sterile-Products) 3. 1. 내용고형제 3. 2. 반고형제 및 액제 (Semi-Solid, Liquid Dosage Form) 4. 물류관리 (Logistics) 4. 1. 물류관리 일반 4. 2. Cold Chain System 4. 3 Pharmaceutical Traceability system 3








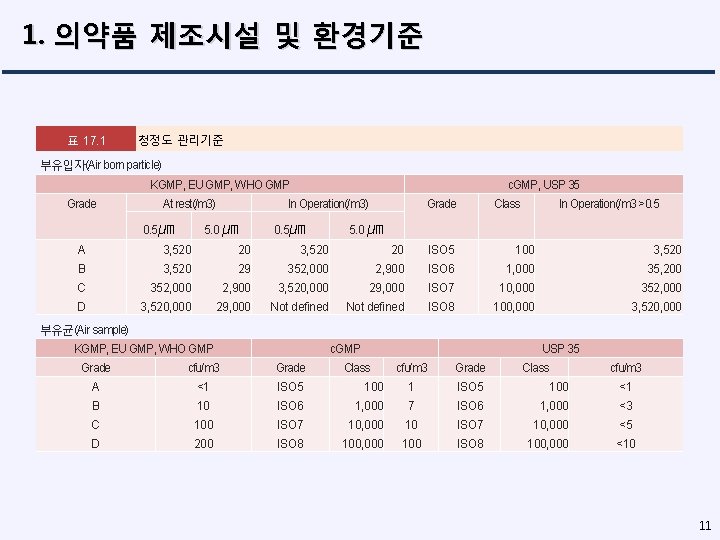
1. 의약품 제조시설 및 환경기준 표 17. 1 청정도 관리기준 부유입자(Air born particle) KGMP, EU GMP, WHO GMP Grade At rest(/m 3) 0. 5㎛ c. GMP, USP 35 In Operation(/m 3) 5. 0 ㎛ 0. 5㎛ Grade Class In Operation(/m 3 >0. 5 5. 0 ㎛ A 3, 520 20 ISO 5 100 3, 520 B 3, 520 29 352, 000 2, 900 ISO 6 1, 000 35, 200 C 352, 000 2, 900 3, 520, 000 29, 000 ISO 7 10, 000 352, 000 D 3, 520, 000 29, 000 Not defined ISO 8 100, 000 3, 520, 000 부유균(Air sample) KGMP, EU GMP, WHO GMP c. GMP Grade cfu/m 3 Grade A <1 ISO 5 B 10 C D USP 35 Class cfu/m 3 Grade Class cfu/m 3 100 1 ISO 5 100 <1 ISO 6 1, 000 7 ISO 6 1, 000 <3 100 ISO 7 10, 000 10 ISO 7 10, 000 <5 200 ISO 8 100, 000 100 ISO 8 100, 000 <10 11

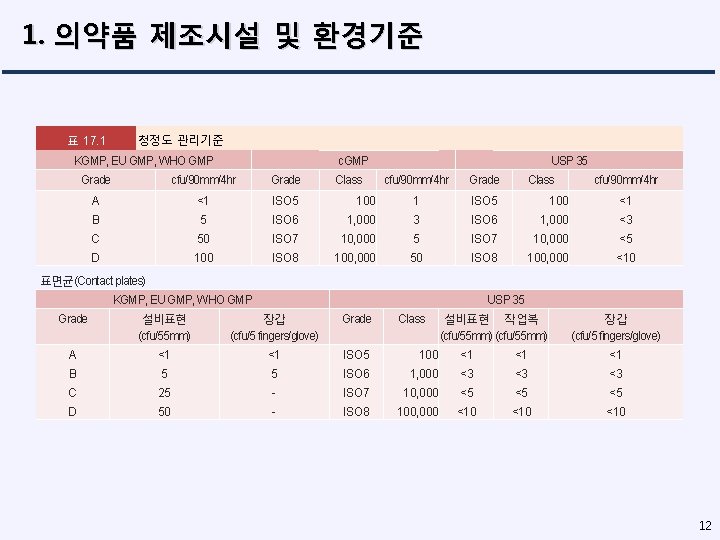
1. 의약품 제조시설 및 환경기준 표 17. 1 청정도 관리기준 KGMP, EU GMP, WHO GMP c. GMP Grade cfu/90 mm/4 hr Grade A <1 ISO 5 B 5 C D Class USP 35 cfu/90 mm/4 hr Grade Class cfu/90 mm/4 hr 100 1 ISO 5 100 <1 ISO 6 1, 000 3 ISO 6 1, 000 <3 50 ISO 7 10, 000 5 ISO 7 10, 000 <5 100 ISO 8 100, 000 50 ISO 8 100, 000 <10 표면균(Contact plates) KGMP, EU GMP, WHO GMP USP 35 Grade 설비표현 (cfu/55 mm) 장갑 (cfu/5 fingers/glove) Grade A <1 <1 ISO 5 100 <1 <1 <1 B 5 5 ISO 6 1, 000 <3 <3 <3 C 25 - ISO 7 10, 000 <5 <5 <5 D 50 - ISO 8 100, 000 <10 <10 Class 설비표현 작업복 (cfu/55 mm) 장갑 (cfu/5 fingers/glove) 12






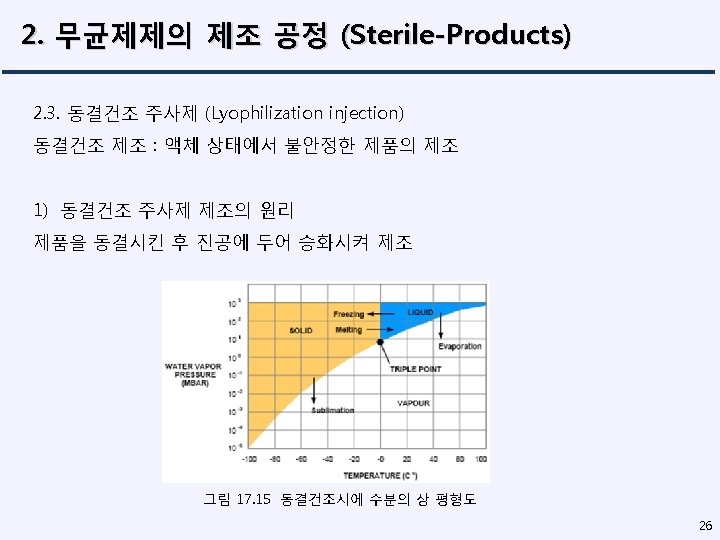
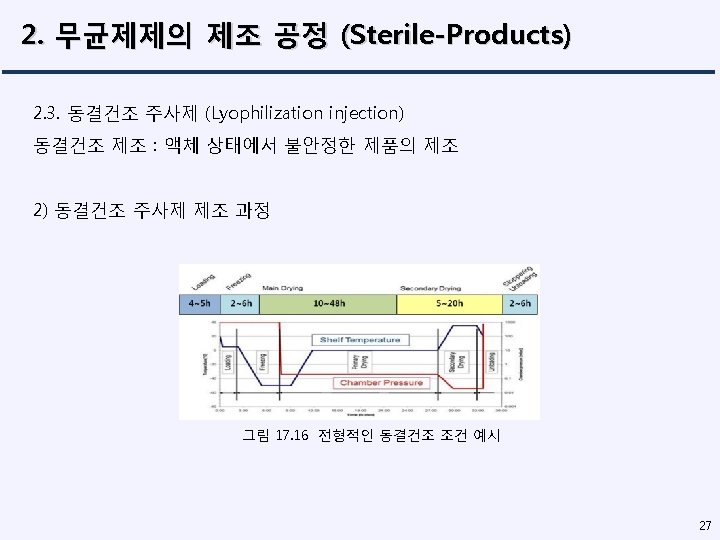
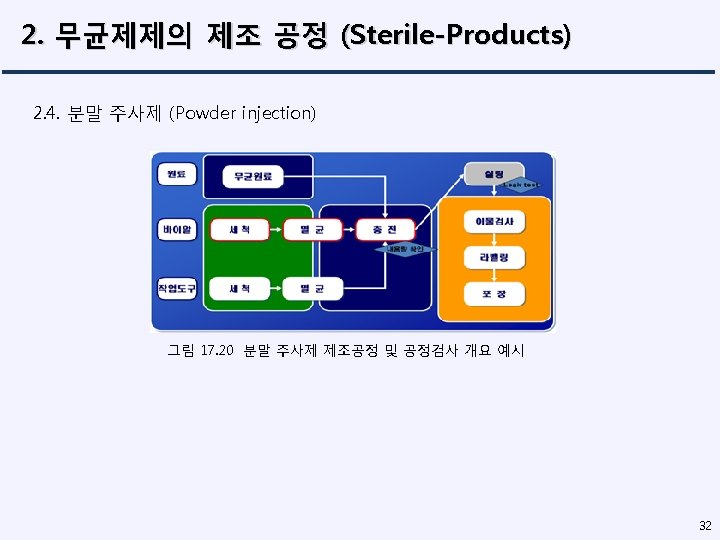
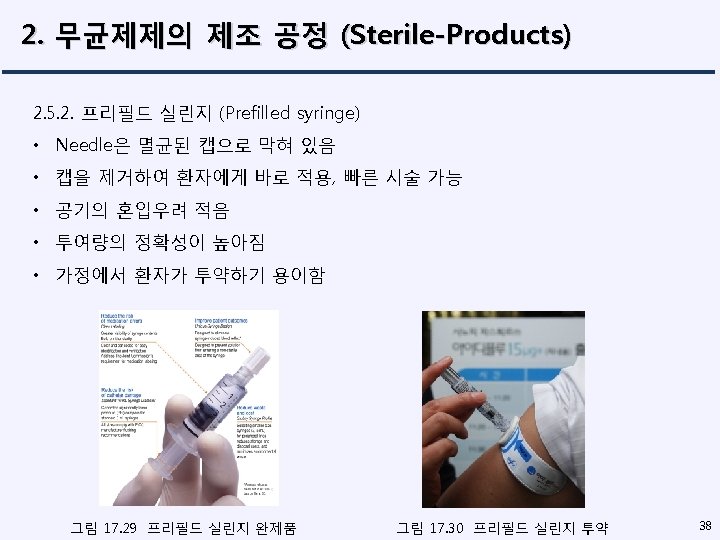
2. 무균제제의 제조 공정 (Sterile-Products) 18


















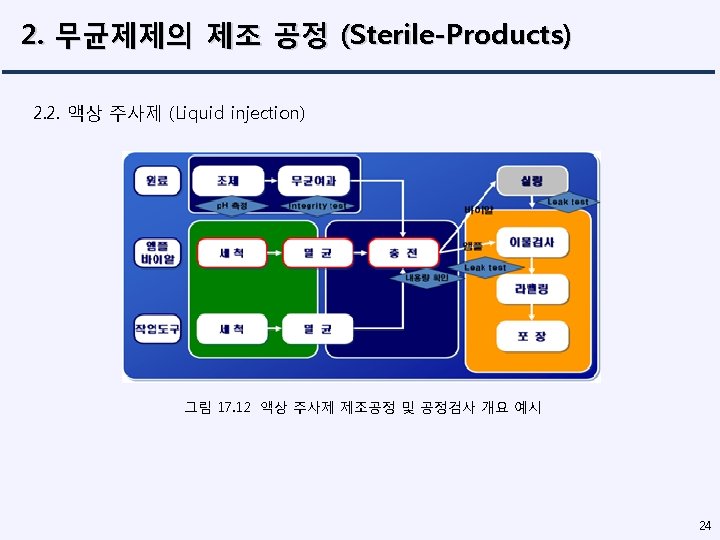
2. 무균제제의 제조 공정 (Sterile-Products) 2. 5. 1. Blow-Fill-Seal 2) Blow-Fill-Seal 제조공정 그림 17. 25 Blow-Fill-Seal 압출, 성형기 그림 17. 26 blow-fill-seal 압출, 성형, 충전과 밀봉 과정 36



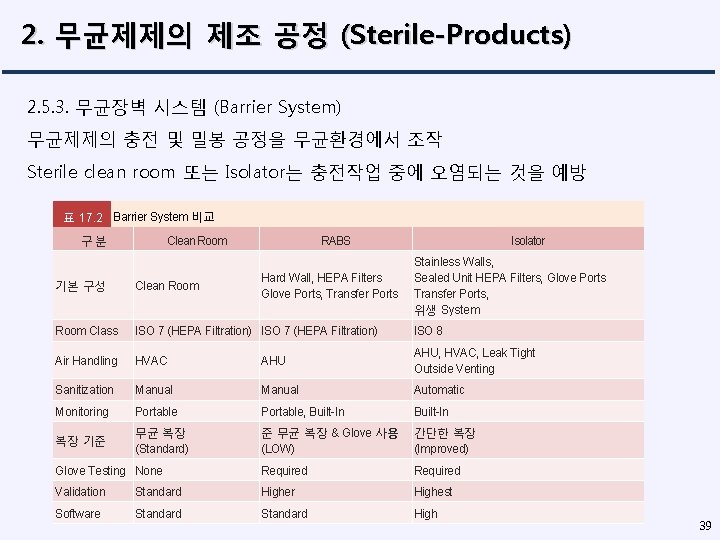
2. 무균제제의 제조 공정 (Sterile-Products) 2. 5. 3. 무균장벽 시스템 (Barrier System) 무균제제의 충전 및 밀봉 공정을 무균환경에서 조작 Sterile clean room 또는 Isolator는 충전작업 중에 오염되는 것을 예방 표 17. 2 Barrier System 비교 구분 Clean Room RABS Hard Wall, HEPA Filters Glove Ports, Transfer Ports Isolator Stainless Walls, Sealed Unit HEPA Filters, Glove Ports Transfer Ports, 위생 System 기본 구성 Clean Room Class ISO 7 (HEPA Filtration) ISO 8 Air Handling HVAC AHU, HVAC, Leak Tight Outside Venting Sanitization Manual Automatic Monitoring Portable, Built-In 복장 기준 무균 복장 (Standard) 준 무균 복장 & Glove 사용 (LOW) 간단한 복장 (Improved) Glove Testing None Required Validation Standard Higher Highest Software Standard High 39

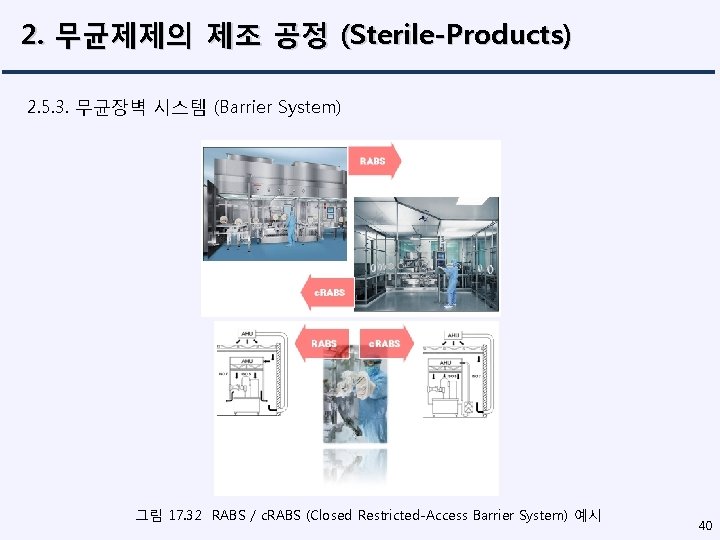
2. 무균제제의 제조 공정 (Sterile-Products) 2. 5. 3. 무균장벽 시스템 (Barrier System) 그림 17. 32 RABS / c. RABS (Closed Restricted-Access Barrier System) 예시 40

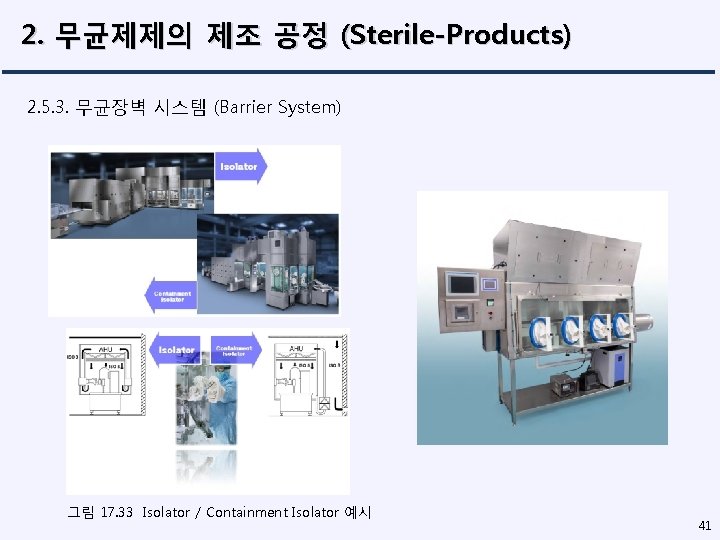
2. 무균제제의 제조 공정 (Sterile-Products) 2. 5. 3. 무균장벽 시스템 (Barrier System) 그림 17. 33 Isolator / Containment Isolator 예시 41


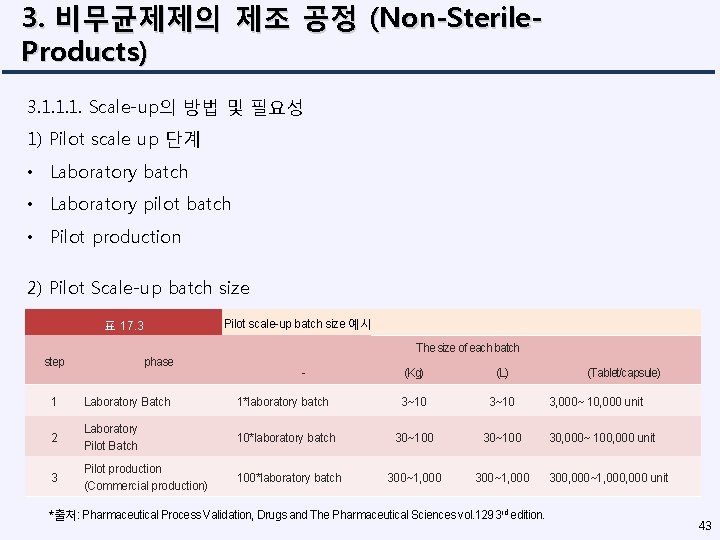
3. 비무균제제의 제조 공정 (Non-Sterile. Products) 3. 1. 1. 1. Scale-up의 방법 및 필요성 1) Pilot scale up 단계 • Laboratory batch • Laboratory pilot batch • Pilot production 2) Pilot Scale-up batch size Pilot scale-up batch size 예시 표 17. 3 step phase The size of each batch - (Kg) (L) 1 Laboratory Batch 1*laboratory batch 3~10 2 Laboratory Pilot Batch 10*laboratory batch 30~100 3 Pilot production (Commercial production) 100*laboratory batch 300~1, 000 *출처: Pharmaceutical Process Validation, Drugs and The Pharmaceutical Sciences vol. 129 3 rd edition. (Tablet/capsule) 3, 000~ 10, 000 unit 30, 000~ 100, 000 unit 300, 000~1, 000 unit 43



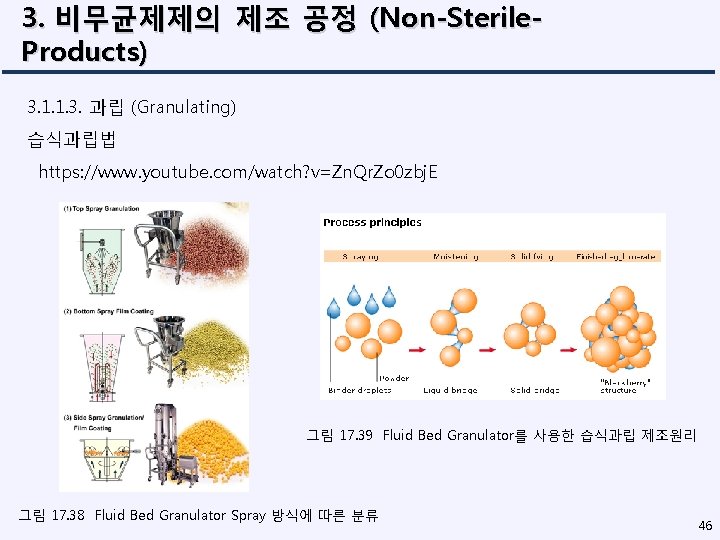
3. 비무균제제의 제조 공정 (Non-Sterile. Products) 3. 1. 1. 3. 과립 (Granulating) 습식과립법 https: //www. youtube. com/watch? v=Zn. Qr. Zo 0 zbj. E 그림 17. 39 Fluid Bed Granulator를 사용한 습식과립 제조원리 그림 17. 38 Fluid Bed Granulator Spray 방식에 따른 분류 46

3. 비무균제제의 제조 공정 (Non-Sterile. Products) 3. 1. 1. 3. 과립 (Granulating) 건식과립법 https: //www. youtube. com/watch? v=Ao_gho 5 Bab 4 47






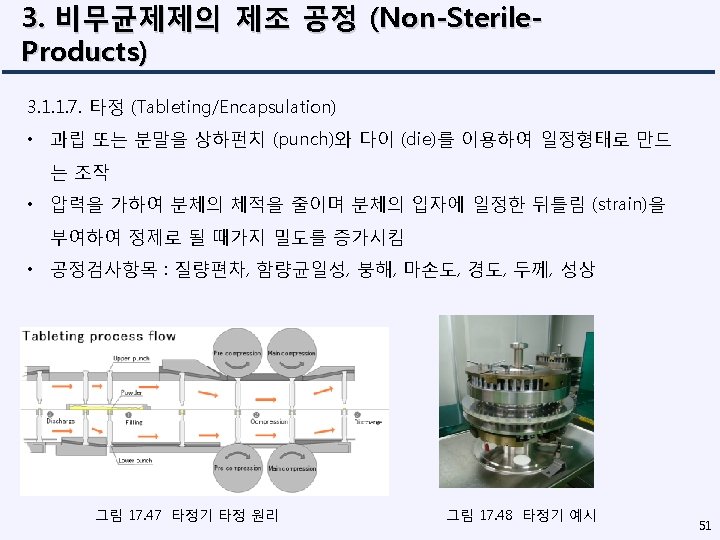
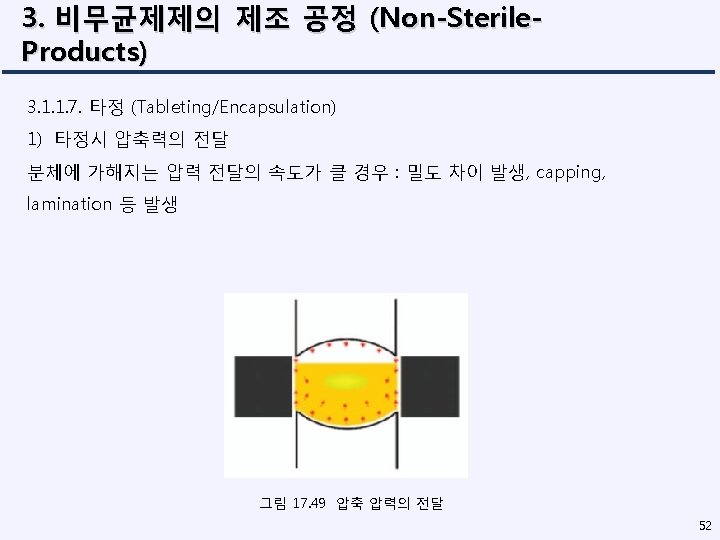
3. 비무균제제의 제조 공정 (Non-Sterile. Products) 3. 1. 1. 7. 타정 (Tableting/Encapsulation) 2) 타정 장애 Binding : Sticking : Capping, Laminating : Cracking : 53























4. 물류 관리 (Logistics) 4. 3. Pharmaceutical traceability system 그림 17. 81 RFID 예시 그림 17. 80 2 D barcode 예시 76

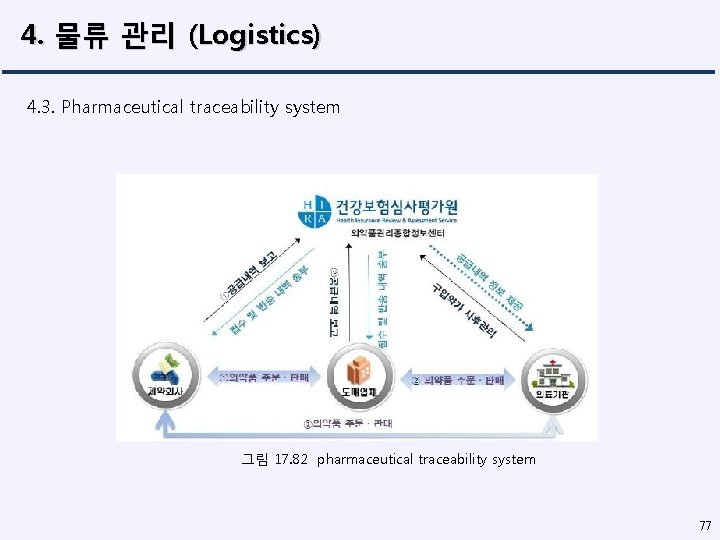
4. 물류 관리 (Logistics) 4. 3. Pharmaceutical traceability system 그림 17. 82 pharmaceutical traceability system 77