CHAPITRE II MLANGES BINAIRES DIPHASS 1 OBJECTIF ET

CHAPITRE II MÉLANGES BINAIRES DIPHASÉS

1 -OBJECTIF ET NOTATIONS Nous allons étudier des mélanges binaires composés de 2 constituants chimiques notés B 1 et B 2; chacun pouvant exister dans une phase a ou une phase b. Ils donnent un mélange plus ou moins polyphasé selon leur miscibilité: nulle, totale ou partielle. On peut avoir jusqu’à 4 constituants physicochimiques : B 1 dans la phase a ; B 1 dans la phase b ; B 2 dans la phase a ; B 2 dans la phase b. On notera a la phase la plus condensée. Elle apparaît en bas du diagramme de phase aux faibles températures ou aux fortes pressions.

2 -FRACTIONS MOLAIRES OU MASSIQUES Pour décrire la constitution de chaque phase, on fait appel aux fraction molaires xif (pour les liquides ou solide) et yi (pour les gaz) ou bien aux fractions massiques wif définies par : Le pourcentage en masse (%), c'est la fraction massique multipliée par cent. Ces fractions sont définies de manière distincte dans chaque phase:

3 -1: LOI DE RAOULT- (Mélange idéal) On sait que les pressions intervenantes dans la construction du diagramme de phase d’un corps sont les pressions de vapeur saturante P 1* et P 2*. La pression relative au mélange des composés B 1 et B 2 est la somme des pressions partiels P 1 et P 2 lorsque le mélange bout. Soit un équilibre liquide - vapeur. Pour des mélange idéaux on a: Pour T=Cte Car pour ; B 1 est pur. Sa pression est la pression de vapeur saturante. D’où Loi de Raoult

3 -2: LOI DE RAOULT- (Représentation graphique) Le composé B 2 se comporte de manière similaire à B 1. On a On peut donc tracer les variations de P 1 et P 2 en fonction de T=Cte

3 -3: LOI DE RAOULT- (Pression totale) Le diagramme isotherme est la représentation des variations de la pression totale P; somme des pressions partielles, en fonction de la fraction molaire d’un composé dans la phase liquide et dans la phase vapeur . P est une fonction affine de La pression partielle s’exprime en fonction de la fraction molaire dans la phase gazeuse par : On exprime en fonction de Ce qui donne P représente une branche d’hyperbole
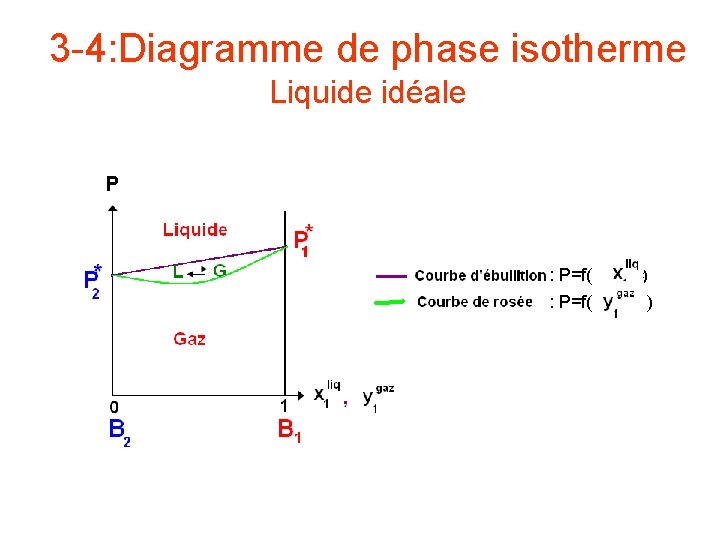
3 -4: Diagramme de phase isotherme Liquide idéale P : P=f( ) : P=f( )

4 -1: LOI DE HENRY Pour un liquide réelle, la relation entre la pression partielle est la fraction molaire devient: Loi de Henry Si k 1>p 1*, la courbe de P 1=f( ) présente une courbure vers le haut et se termine asymptotiquement avec la droite. Si k 1<p 1*, on a l’inverse. On a une situation équivalente pour p 2.
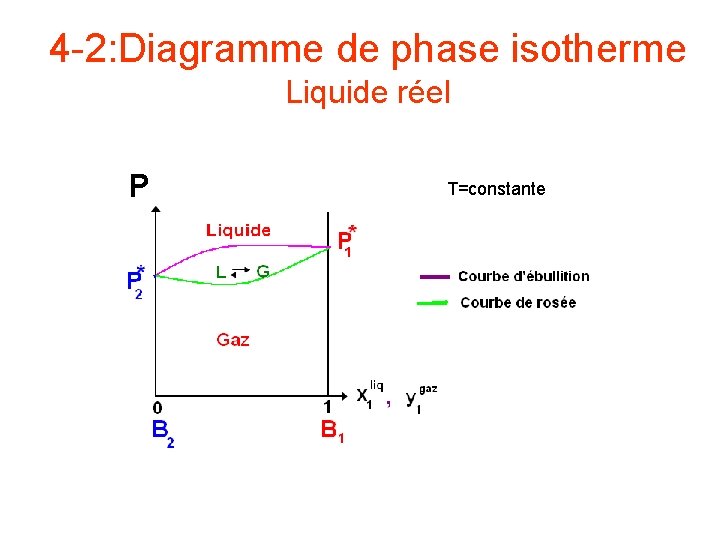
4 -2: Diagramme de phase isotherme Liquide réel P T=constante

5 -1: OBTENTION DU DIAGRAMME DE PHASE ISOBARE À PARTIR DE L’ÉQUATION DE CLAPEYRON On se propose dans un diagramme de phase isobare de tracer les variations de T en fonction de la fraction molaire d’un composé dans la phase liquide et dans la phase vapeur . A partir de l’équation de Clapeyron, on peut transformer l’information sur les pressions de vapeur saturante en données dont les abscisses sont et . Pour la phase liquide: et D’où on a

5 -1: OBTENTION DU DIAGRAMME DE PHASE ISOBARE À PARTIR DE L’ÉQUATION DE CLAPEYRON(suite) Pour la phase gazeuse et D’où Les équations de Clapeyron pour les composés 1 et 2 sont de la forme: Pour chaque valeur de et on peut trouver la valeur de T en fonction de ou de et tracer point par point le diagramme de phase à la pression choisie
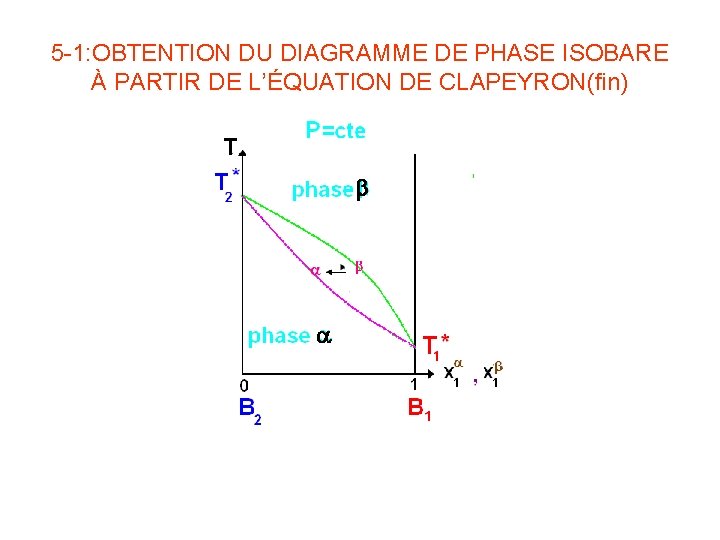
5 -1: OBTENTION DU DIAGRAMME DE PHASE ISOBARE À PARTIR DE L’ÉQUATION DE CLAPEYRON(fin) b a
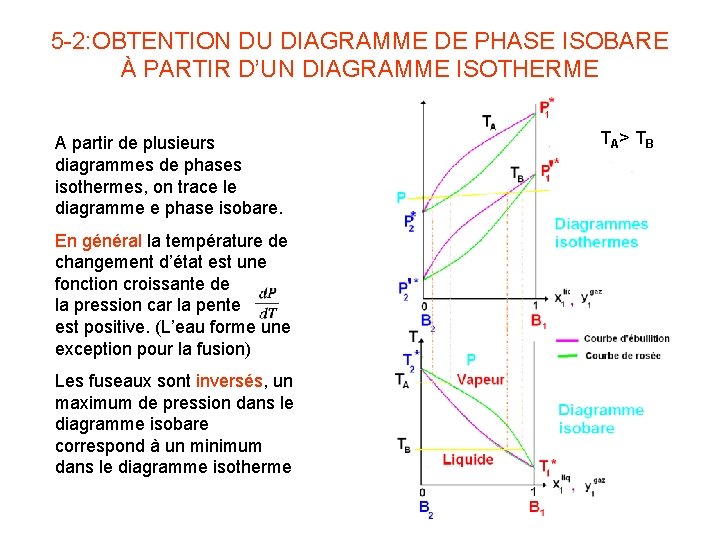
5 -2: OBTENTION DU DIAGRAMME DE PHASE ISOBARE À PARTIR D’UN DIAGRAMME ISOTHERME A partir de plusieurs diagrammes de phases isothermes, on trace le diagramme e phase isobare. En général la température de changement d’état est une fonction croissante de la pression car la pente est positive. (L’eau forme une exception pour la fusion) Les fuseaux sont inversés, un maximum de pression dans le diagramme isobare correspond à un minimum dans le diagramme isotherme TA> TB
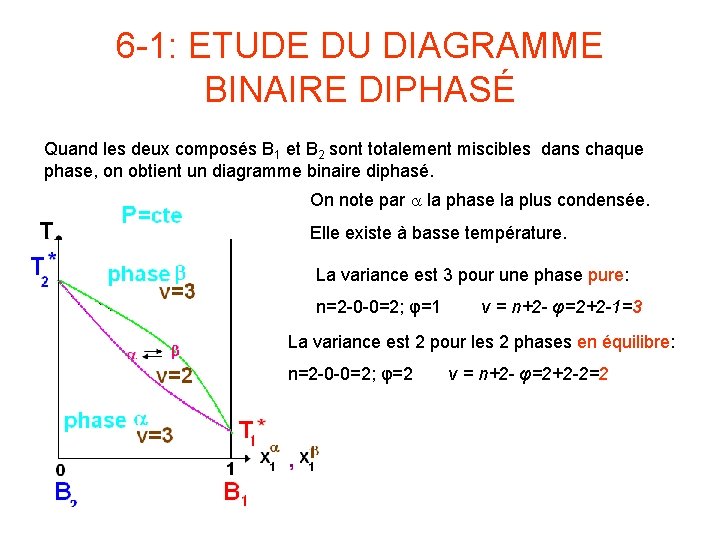
6 -1: ETUDE DU DIAGRAMME BINAIRE DIPHASÉ Quand les deux composés B 1 et B 2 sont totalement miscibles dans chaque phase, on obtient un diagramme binaire diphasé. On note par a la phase la plus condensée. Elle existe à basse température. La variance est 3 pour une phase pure: n=2 -0 -0=2; φ=1 v = n+2 - φ=2+2 -1=3 La variance est 2 pour les 2 phases en équilibre: n=2 -0 -0=2; φ=2 v = n+2 - φ=2+2 -2=2

6 -1: ETUDE DU DIAGRAMME BINAIRE DIPHASÉ(suite) La courbe du bas (en violet) représente les variations de la température en fonction de la fraction molaire et la courbe du haut (en vert) celles en fonction de . La courbe = f( ) coupe l’axe des ordonnées ( =0 ; seul B 2 existe) en , température de changement de phase de B 2. Elle coupe la droite d’équation =1 où seul B 1 existe en , température de changement de phase de B 1. On obtient la valeur de par la relation suivante: = 1 -
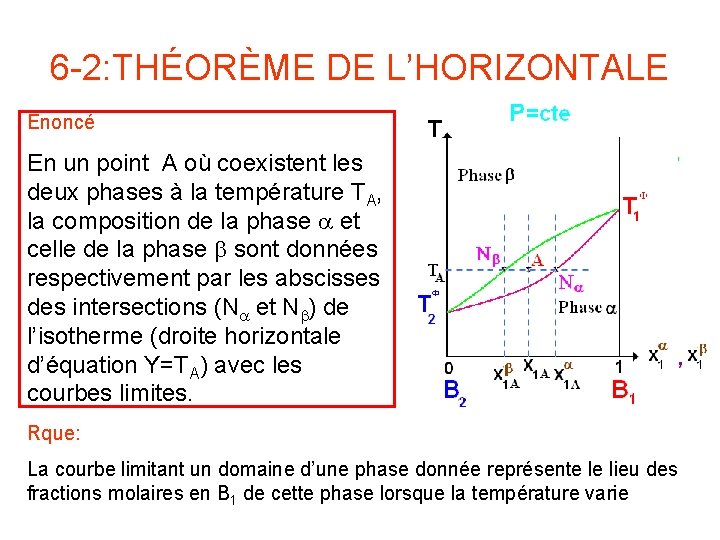
6 -2: THÉORÈME DE L’HORIZONTALE Énoncé En un point A où coexistent les deux phases à la température TA, la composition de la phase a et celle de la phase b sont données respectivement par les abscisses des intersections (Na et Nb) de l’isotherme (droite horizontale d’équation Y=TA) avec les courbes limites. Rque: La courbe limitant un domaine d’une phase donnée représente le lieu des fractions molaires en B 1 de cette phase lorsque la température varie
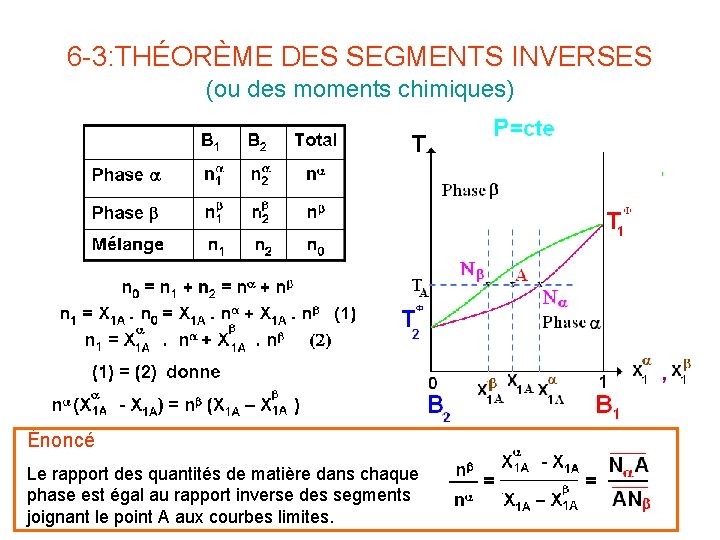
6 -3: THÉORÈME DES SEGMENTS INVERSES (ou des moments chimiques) Énoncé Le rapport des quantités de matière dans chaque phase est égal au rapport inverse des segments joignant le point A aux courbes limites.
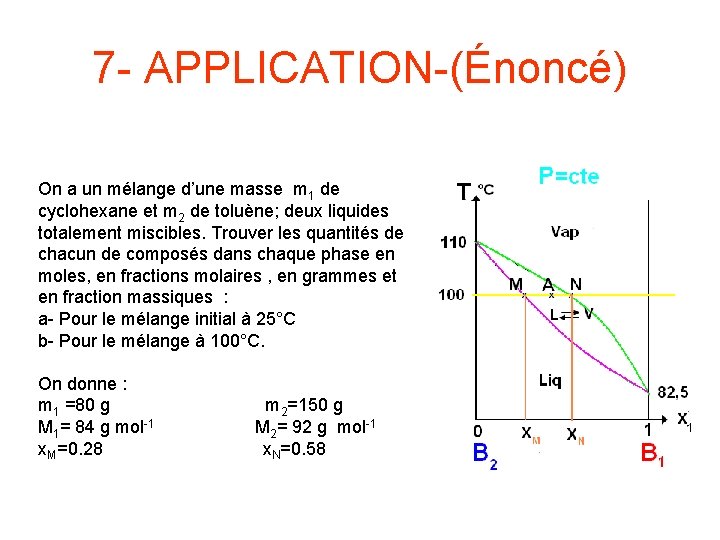
7 - APPLICATION-(Énoncé) On a un mélange d’une masse m 1 de cyclohexane et m 2 de toluène; deux liquides totalement miscibles. Trouver les quantités de chacun de composés dans chaque phase en moles, en fractions molaires , en grammes et en fraction massiques : a- Pour le mélange initial à 25°C b- Pour le mélange à 100°C. On donne : m 1 =80 g m 2=150 g M 1= 84 g mol-1 M 2= 92 g mol-1 x. M=0. 28 x. N=0. 58

7 - APPLICATION-(Réponse) Mélange initial m 1 L=80 g m 2 L=150 g m. Total=230 g n 1= 80/84= 0. 952 mol n 2= 150/92= 1. 630 mol n. Total= n 0 = 2. 582 mol x 1 L= 0. 952/2. 582=0. 369 x 2 L=1. 63/2. 582= 0. 631 w 1 L=80/230 = 0. 347 w 2 L=150/230=1 -0. 347=0. 652 Mélange à 100°C Le point A a les coordonnées (0. 37, 100) Le point N est sur la courbe de rosée. Ses Coordonnées sont (0. 58, 100) Le point M est sur la courbe d’ébullition. Ses coordonnées sont (0. 28, 100) La composition relative de la phase liquide par rapport à la phase vapeur est donnée par le théorème des segments inverses: n. V+n. L=2. 582 mol (2. 33+1)n. V=2. 582 mol n. V= 0. 774 mol n. L=2. 582 -0. 774=1. 807 mol n 1 V=0. 58*n. V=0. 58*0. 774=0. 449 mol n 1 L=0. 28*1. 807=0. 506 mol n 1= 0. 449+0. 506=0. 954 mol (en accord avec 0. 952) n 2 V=(1 -0. 58)*n. V=0. 42*0. 774=0. 325 mol n 2 L=(1 -0. 28)*n. L=0. 72*1. 807=1. 301 mol n 2=0. 325+1. 301=1. 626 mol (en accord avec 1. 630)

7 - APPLICATION-(Réponse-suite) Suite T=100°C x 1 V=0. 58 x 1 L= 0. 28 x 2 V=0. 42 x 2 L=0. 72 Vérification: m 1 V=n 1 V. M 1=0. 449*84=37. 71 g m=(m 1 V + m 1 L)+(m 2 V+m 2 L) m 2 V=n 2 V. M 2= 0. 325*92=29. 90 g =(37. 71+42. 50)+(29. 90+119. 69) m. V=37. 71+29. 9=67. 61 g =80. 21+149. 59 w 1 V= 37. 71/67. 61=0. 56 =229. 8 g w 2 V=29. 9/67. 61=0. 44 =1 -0. 56 m 1 L=n 1 L*M 1=0. 506*84=42. 50 g m 2 L=n 2 L*M 2= 1. 301*92=119. 69 g m. L=42. 50+119. 69=162. 19 g w 1 L= 42. 50/162. 19=0. 26 w 2 L=119. 69/162. 19=0. 74 =1 -0. 26 En accord avec les valeurs initiales
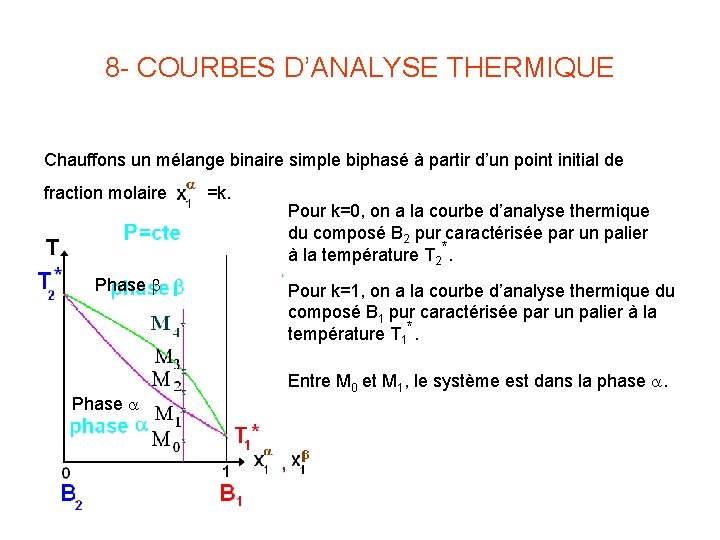
8 - COURBES D’ANALYSE THERMIQUE Chauffons un mélange binaire simple biphasé à partir d’un point initial de fraction molaire =k. Phase b Phase a Pour k=0, on a la courbe d’analyse thermique du composé B 2 pur caractérisée par un palier à la température T 2*. Pour k=1, on a la courbe d’analyse thermique du composé B 1 pur caractérisée par un palier à la température T 1*. Entre M 0 et M 1, le système est dans la phase a.
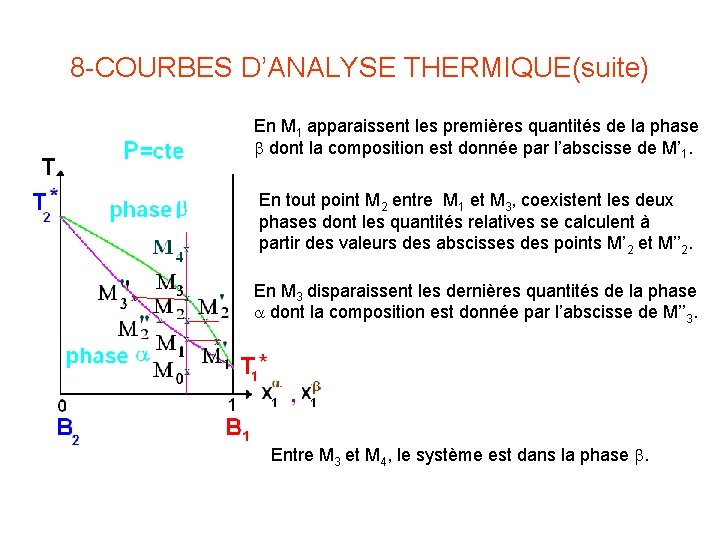
8 -COURBES D’ANALYSE THERMIQUE(suite) En M 1 apparaissent les premières quantités de la phase b dont la composition est donnée par l’abscisse de M’ 1. En tout point M 2 entre M 1 et M 3, coexistent les deux phases dont les quantités relatives se calculent à partir des valeurs des abscisses des points M’ 2 et M’’ 2. En M 3 disparaissent les dernières quantités de la phase a dont la composition est donnée par l’abscisse de M’’ 3. Entre M 3 et M 4, le système est dans la phase b.
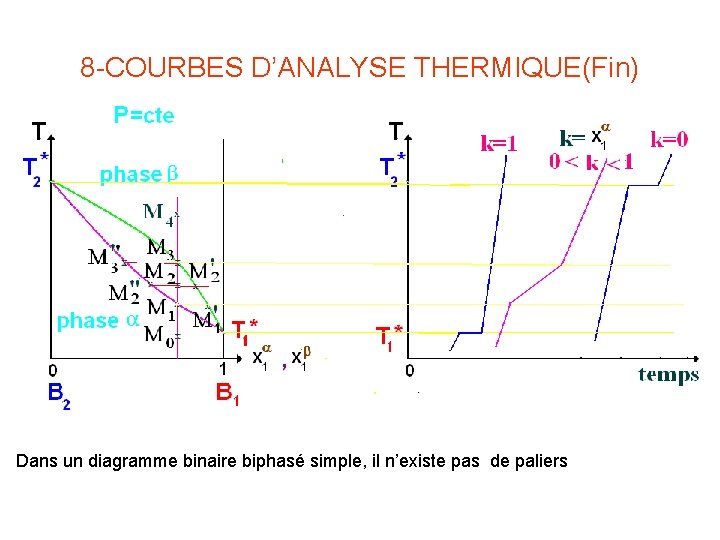
8 -COURBES D’ANALYSE THERMIQUE(Fin) Dans un diagramme binaire biphasé simple, il n’existe pas de paliers

9 -DISTILLATION FRACTIONNÉE On peut effectuer une distillation en réduisant la pression à température constante, mais en général on distille à pression constante en augmentant la température. L’utilisation du diagramme isobare température-composition se fait ainsi: Prenons un mélange de composition a 1 que l’on chauffe en partant de la température ambiante. Ce mélange commence à bouillir à la température T 2. La composition du liquide est alors a 2, pratiquement égale à a 1. Sachant que le constituant le plus volatil est B 2 car il a la température d’ébullition la plus basse; la vapeur en équilibre avec le liquide aura la composition a 21. Si on sépare la vapeur et qu’on la condense complètement, sa composition sera a 3. Ce liquide est donc enrichi en composé le plus volatil B 2 et est plus pauvre en liquide moins volatil B 1. En poursuivant la distillation il sera possible de séparer les liquides B 1 (résidu) et B 2 (distillat).

10 -AZÉOTROPE La séparation des liquides par distillation n’est pas toujours aussi simple, car on peut avoir déviation à la loi de Raoult et formation d’azéotrope. Les figures suivantes montrent des systèmes avec un maximum et un minimum respectivement. Il faut noter que pour l’azéotrope, la composition de la vapeur est identique à celle du liquide. Lorsqu’un mélange forme un azéotrope, ses composantes ne peuvent pas être séparées par distillation simple: Pour un diagramme à maximum; la distillat est l’un des composés pur du mélange selon le fuseau auquel il appartient, défini par sa composition initiale. Dans le diagramme à minimum, on obtient l’azéotrope en fin de distillation.
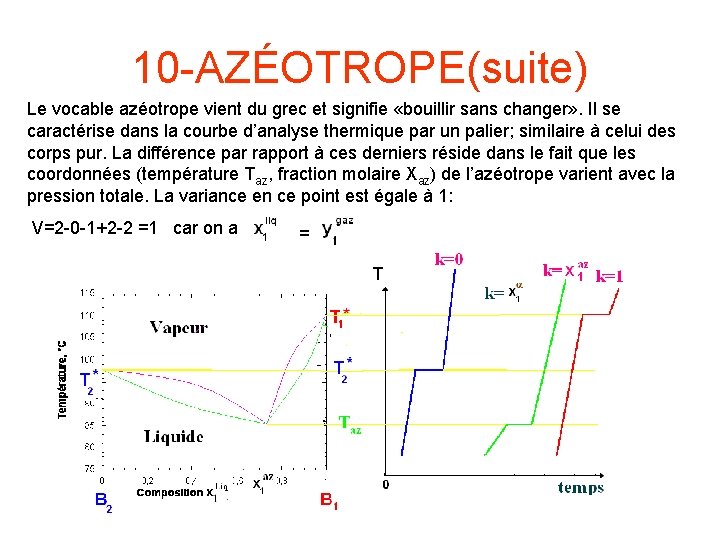
10 -AZÉOTROPE(suite) Le vocable azéotrope vient du grec et signifie «bouillir sans changer» . Il se caractérise dans la courbe d’analyse thermique par un palier; similaire à celui des corps pur. La différence par rapport à ces derniers réside dans le fait que les coordonnées (température Taz, fraction molaire Xaz) de l’azéotrope varient avec la pression totale. La variance en ce point est égale à 1: V=2 -0 -1+2 -2 =1 car on a =

11 -POINT INDIFFÉRENT Pour l’équilibre diphasé Solide-Liquide , on a un diagramme de phase similaire à celui avec azéotrope à minimum. Ce point porte le nom de point indifférent.
- Slides: 27