Chapitre II Les cristaux mtalliques Introduction Il y
















![• La coordinence • Dans cette empilement la coordinence est [X] = [8] • La coordinence • Dans cette empilement la coordinence est [X] = [8]](https://slidetodoc.com/presentation_image_h/bd113677267e9e1b67301f52bc1bfc07/image-33.jpg)







- Slides: 50

Chapitre II Les cristaux métalliques

Introduction • Il y a deux ou trois décennies seulement, un bon critère du développement industriel d’un pays était l’importance de sa production de métaux. • L’intérêt des matériaux métalliques. • Nous allons tous d’abord essayer de dégager les caractères généraux des métaux puis nous étudierons leurs structures

Caractères généraux des métaux • état naturel En général, dans la nature, les métaux se trouvent à l’état de corps composés tels qu’oxydes, sulfure, carbonates… • élément métallique • Les symboles des éléments métalliques se trouvent vers la gauche et vers le bas du tableau de la classification périodique. • Ce qui rend leurs électrons de valences relativement peu attirés par le noyau PI des atomes métalliques sera faible.

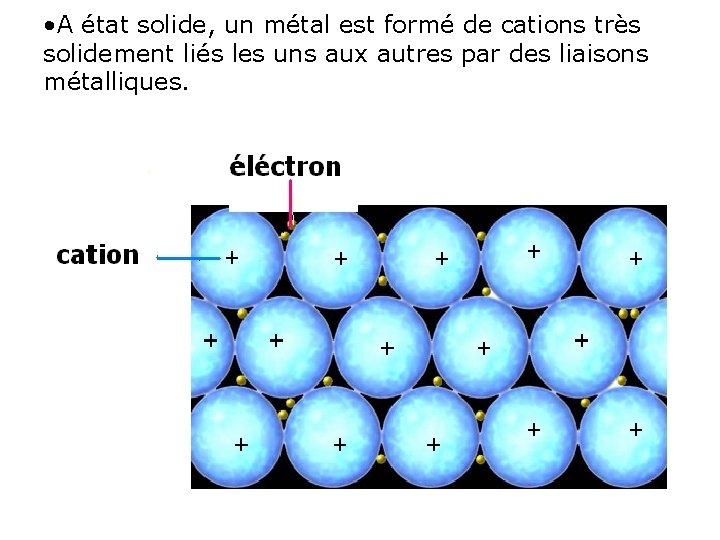
• A état solide, un métal est formé de cations très solidement liés les uns aux autres par des liaisons métalliques. + + +

Liaison métallique • La liaison métallique concerne les éléments possédant peu d’électrons de valence • la force cohésion des métaux provient des interactions électrostatiques entre les ions positifs et le nuage d'électrons délocalisés sur tout le cristal. • Les é peuvent circuler dans tout la structure solide. • L’ensemble reste constamment neutre. • Ce qui confèrent aux métaux leurs remarquables propriétés physiques et mécaniques.

Propriétés physiques Propriétés mécaniques • Ductilité et malléabilité possibilité d'obtenir des - fils par tirage - feuilles par forgeage ou laminage

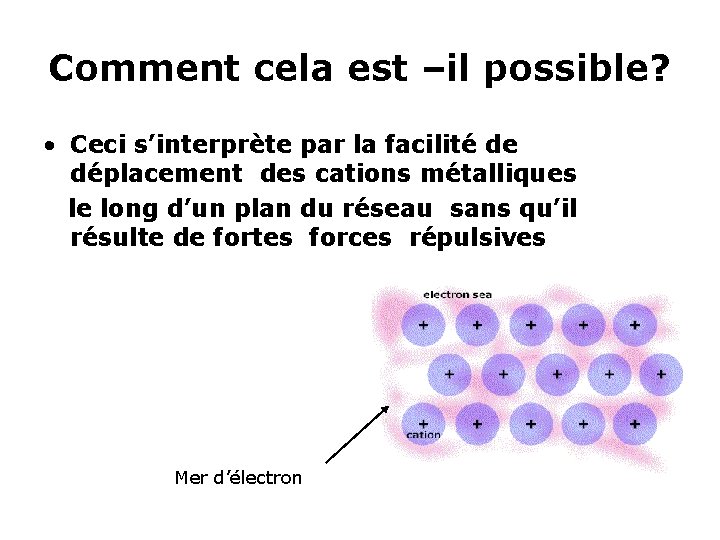
Comment cela est –il possible? • Ceci s’interprète par la facilité de déplacement des cations métalliques le long d’un plan du réseau sans qu’il résulte de fortes forces répulsives Mer d’électron

Propriétés thermiques • Les é de valences sont libres de se déplacer dans toutes les directions du réseau. Ces électrons libres peuvent passer d’un atome à un autre Ils sont appelés des é de conduction • d’excellentes conductivités thermiques et électriques • Le sodium est utilisé comme vecteur thermique dans certaines centrales nucléaires.

Propriété électriques • Les métaux sont d’excellents conducteurs de l’électricité. Une faible différence de potentiel provoque un courant d’électricité relativement important. • Certains métaux sont ferromagnétiques. Cette propriété est de première importance dans l’industrie électrique.

Propriétés optiques • Les métaux sont de bon réflecteurs de la lumière. • Les é libres du métal sont excités par le champs électromagnétique du rayon lumineux incident, • par désexcitation ils réémettent les radiations lumineuses sans perte d’énergie ( Ag; Hg…). • C’est pour cette raison que les métaux brillent. • Parfois ils absorbent certaines radiations lumineuses visibles; le cuivre et l’or absorbent le bleu, ils paraissent alors jaunes

STRUCTURE DES MÉTAUX À L’ÉTAT SOLIDE Les cristaux métalliques cristallisent dans trois systèmes cristallins principaux: • Le cubique à faces centrées • L’hexagonale compacte • Le cubique centré que l'on peut décrire par deux types d'assemblages de sphères rigides: - les empilements compacts - les empilements semi compacts.

Empilements compacts • Dans l’empilement compact, chaque sphère est tangente à six autres sphères identiques formant ainsi un hexagone régulier autour de l’atome central. 6 5 B 4 B 1 B 3 2 Association des atomes dans le plan A

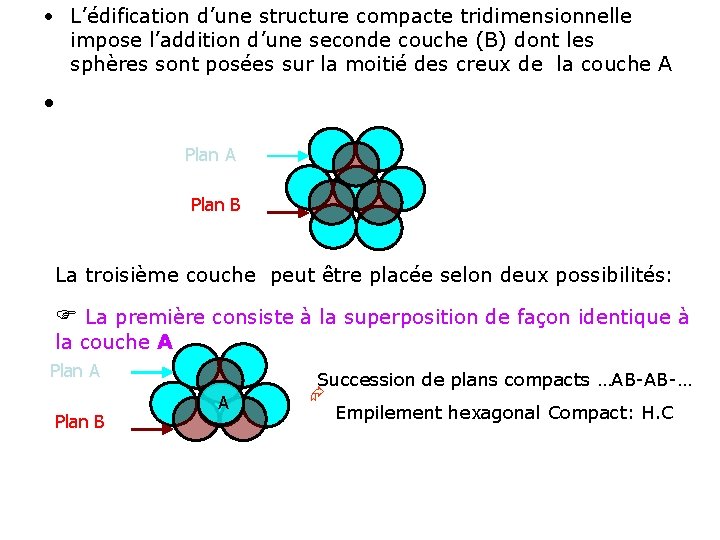
• L’édification d’une structure compacte tridimensionnelle impose l’addition d’une seconde couche (B) dont les sphères sont posées sur la moitié des creux de la couche A • Plan A Plan B La troisième couche peut être placée selon deux possibilités: La première consiste à la superposition de façon identique à la couche A Plan B A Succession de plans compacts …AB-AB-… Empilement hexagonal Compact: H. C

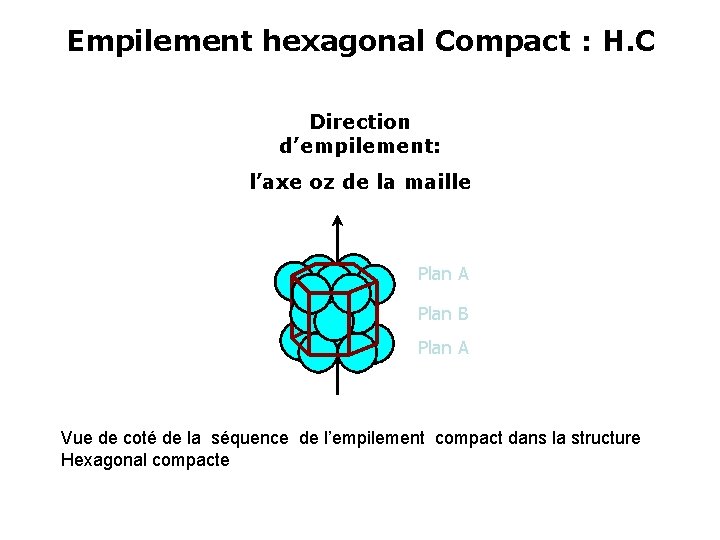
Empilement hexagonal Compact : H. C Direction d’empilement: l’axe oz de la maille Plan A Plan B Plan A Vue de coté de la séquence de l’empilement compact dans la structure Hexagonal compacte

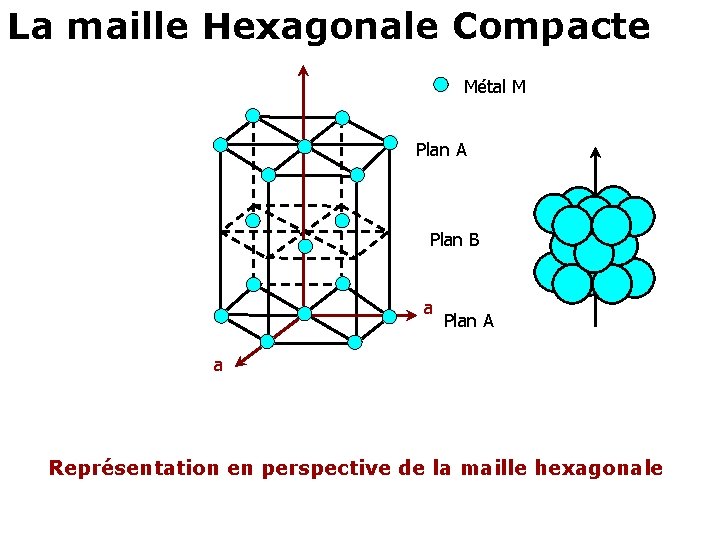
La maille Hexagonale Compacte Métal M Plan A Plan B a Plan A a Représentation en perspective de la maille hexagonale

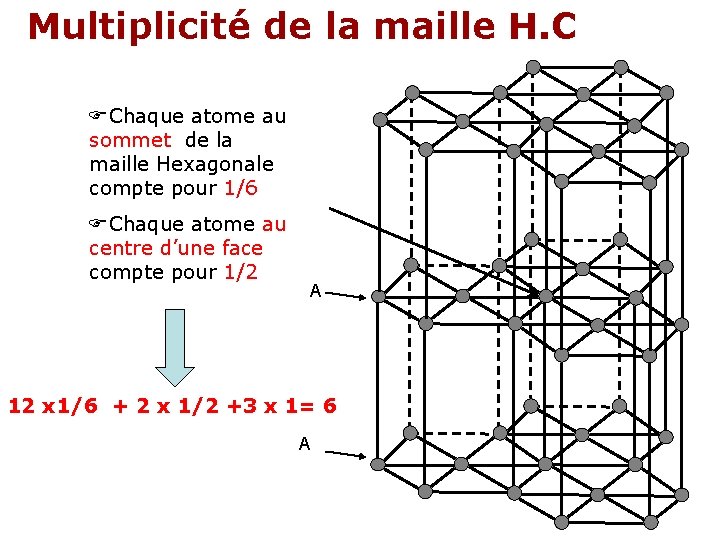
Multiplicité de la maille H. C Chaque atome au sommet de la maille Hexagonale compte pour 1/6 Chaque atome au centre d’une face compte pour 1/2 A 12 x 1/6 + 2 x 1/2 +3 x 1= 6 A

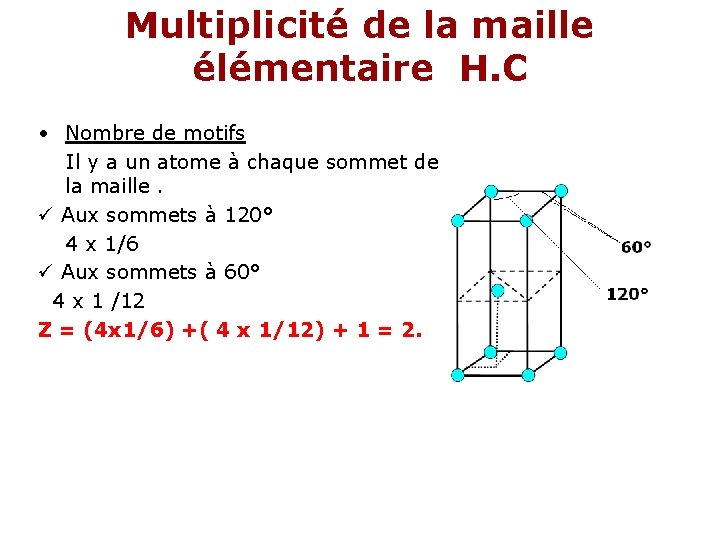
Multiplicité de la maille élémentaire H. C • Nombre de motifs Il y a un atome à chaque sommet de la maille. Aux sommets à 120° 4 x 1/6 Aux sommets à 60° 4 x 1 /12 Z = (4 x 1/6) +( 4 x 1/12) + 1 = 2.

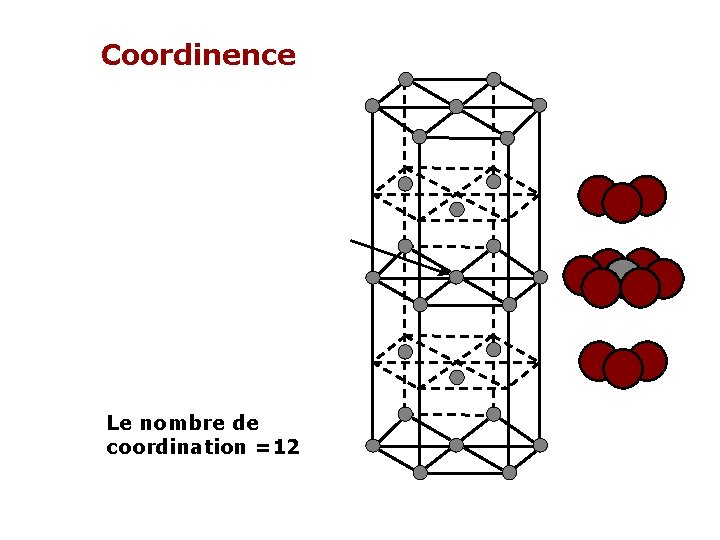
Coordinence Le nombre de coordination =12

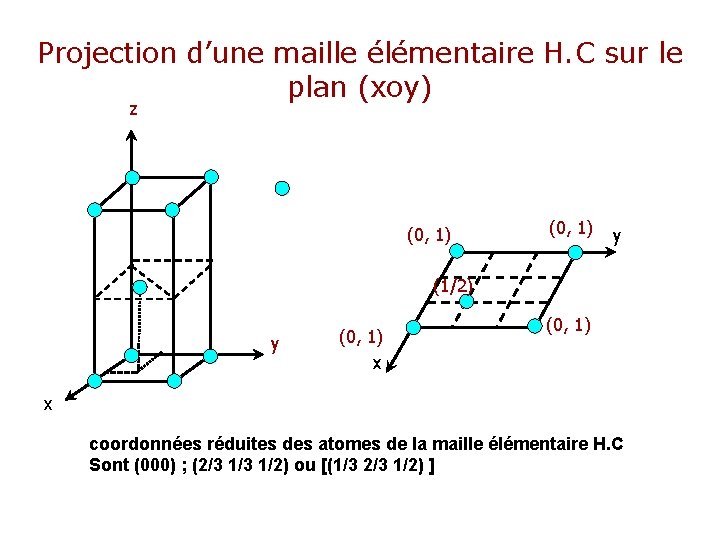
Projection d’une maille élémentaire H. C sur le plan (xoy) z (0, 1) y (1/2) y (0, 1) x coordonnées réduites des atomes de la maille élémentaire H. C Sont (000) ; (2/3 1/2) ou [(1/3 2/3 1/2) ]

Compacité de la maille H. C • Le volume de la maille H. C est : • V = a 2. c. sin 120° avec a = 2 r , et n = 2 • Le volume total des sphères de rayon r sur le volume de la maille élémentaire est avec La compacité est Soit C=0. 74

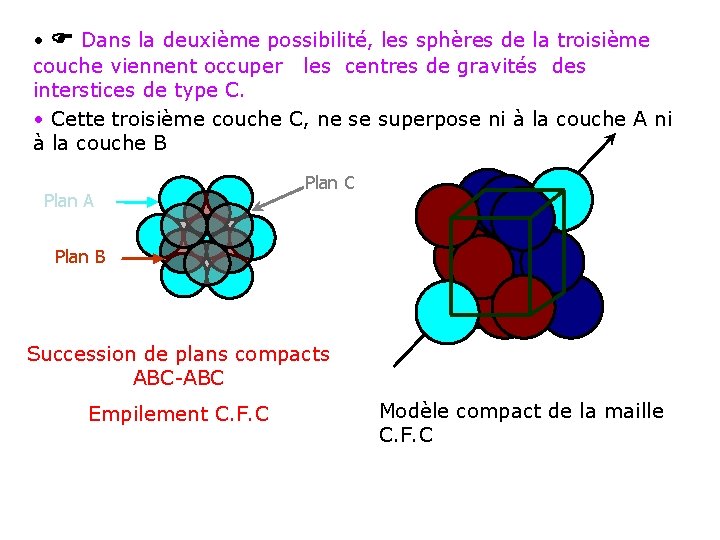
• Dans la deuxième possibilité, les sphères de la troisième couche viennent occuper les centres de gravités des interstices de type C. • Cette troisième couche C, ne se superpose ni à la couche A ni à la couche B Plan A Plan C Plan B Succession de plans compacts ABC-ABC Empilement C. F. C Modèle compact de la maille C. F. C

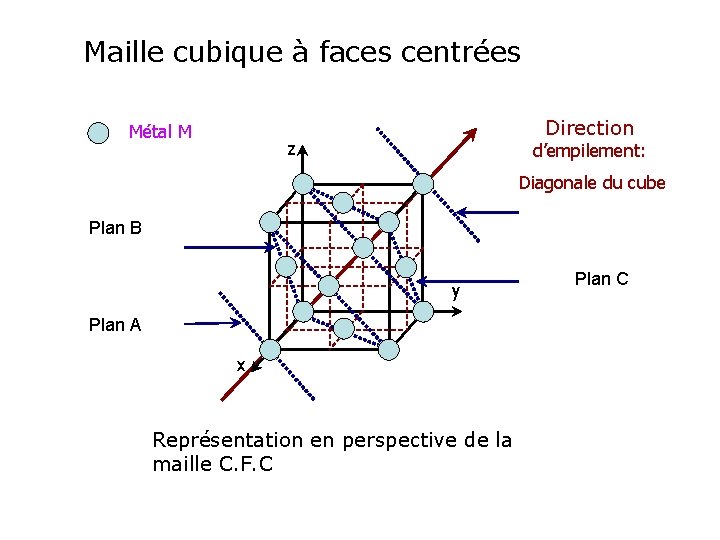
Maille cubique à faces centrées Métal M Direction z d’empilement: Diagonale du cube Plan A Plan B y Plan A x Représentation en perspective de la maille C. F. C Plan C

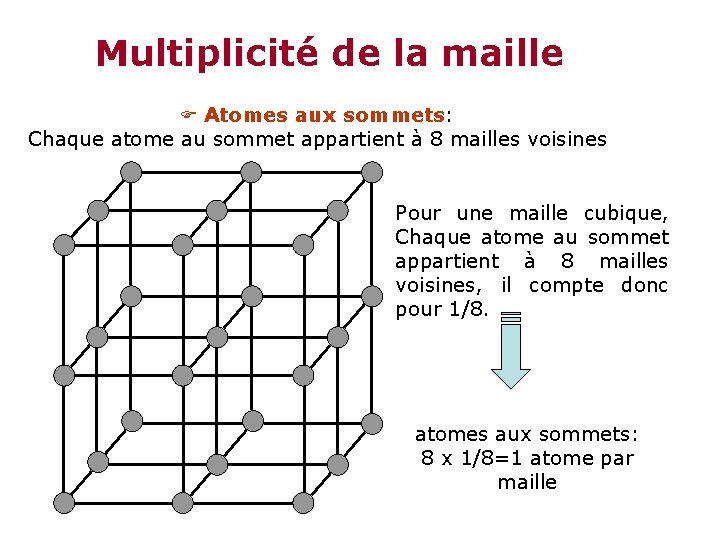
Multiplicité de la maille Atomes aux sommets: Chaque atome au sommet appartient à 8 mailles voisines Pour une maille cubique, Chaque atome au sommet appartient à 8 mailles voisines, il compte donc pour 1/8. atomes aux sommets: 8 x 1/8=1 atome par maille

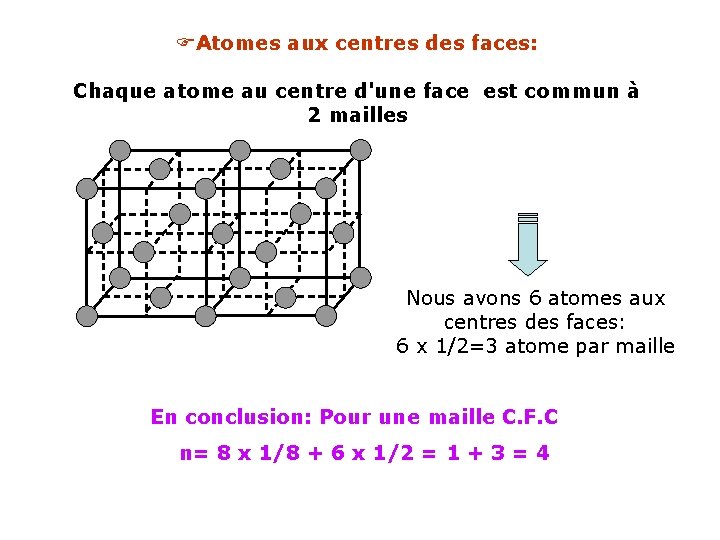
Atomes aux centres des faces: Chaque atome au centre d'une face est commun à 2 mailles Nous avons 6 atomes aux centres des faces: 6 x 1/2=3 atome par maille En conclusion: Pour une maille C. F. C n= 8 x 1/8 + 6 x 1/2 = 1 + 3 = 4

Coordonnées réduites des atomes de la maille élémentaire • Une maille cubique à faces centrées Contient des atomes aux • 8 sommets du cube de coordonnée réduite (000). • 6 centres des faces de coordonnées réduites: (1/2 0), (1/2 0 1/2), (0 1/2),

La coordinence Dans les deux types d’empilements compacts, chaque sphère est entourée de 12 sphères voisines 6 dans le même plan , 3 dans le plan inférieur et 3 dans le plan supérieur La coordinence est donc = 12 Plan C Plan B Plan A Plan C

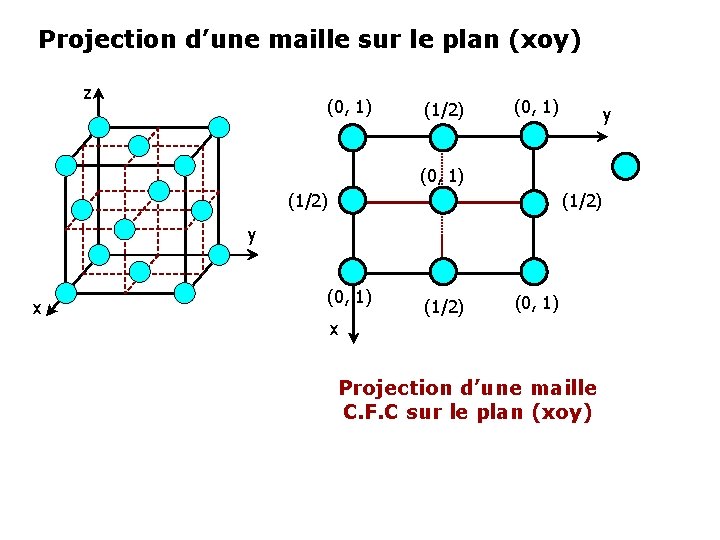
Projection d’une maille sur le plan (xoy) z (0, 1) (1/2) (0, 1) y (0, 1) (1/2) y x (0, 1) (1/2) (0, 1) x Projection d’une maille C. F. C sur le plan (xoy)

Compacité Le volume de la maille C. F. C est : a 3 avec n=4 et Le volume total des sphères de rayon r sur le volume de la maille élémentaire est : • L’empilement compact est la façon la plus efficace de remplir l’espace avec des sphères identiques. • Elles occupent 74% du volume. • Le taux de compacité de l’empilement est 74%. r. Soit exactement la même valeur que dans le système H. C C = 0. 74

Exemple de métaux cristallisant dans les structures H. C et C. F. C Structure Hexagonal compact • Le réseau hexagonal compact regroupe une vingtaine de métaux parmi lesquels : Li, Be, Mg, Y, Tc, Re, Ru, l Os, Sc, Ti, Zr, Hf, Mo, Co, Ni, Cd, Tl, He, …. Structure cubique à faces centrées. • Cette structure regroupe une vingtaine de métaux : Al, Ca, Sr, et certains métaux de transition (Fe , Co, Ni, Cu, Pd, Ag, Yb, Au, Pt…) et les gaz rares (sauf l’hélium) à l’état solide. • N. B Co , Ni, , …présentent deux variétés allotropiques HC et CFC Les structures HC et CFC sont très proches. Allotropie

Empilements non- compacts • Dans cette structure, les sphères d’un même plan sont disposées de sorte que leurs centres constituent les sommets d’un carré de côté a Un second plan est obtenu en plaçant une sphère dans chaque espace libre laissé par les sphères du premier plan; en donnant la succession AB, AB. . A B

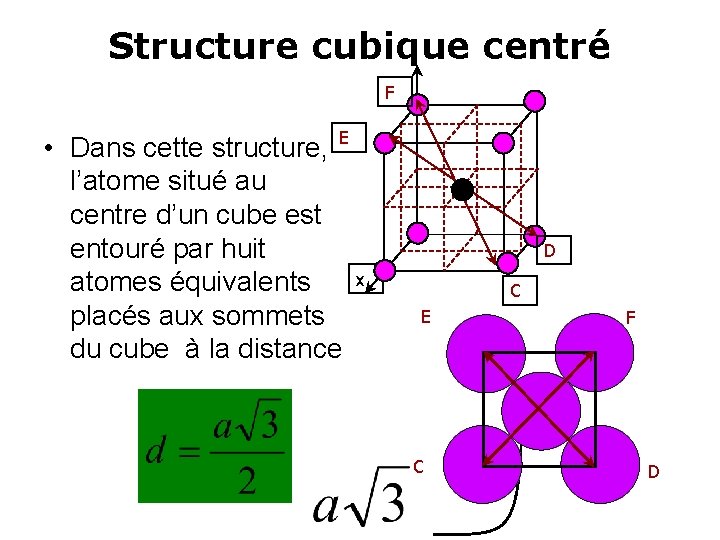
Structure cubique centré F • Dans cette structure, E l’atome situé au centre d’un cube est entouré par huit atomes équivalents x placés aux sommets du cube à la distance D C E C F D

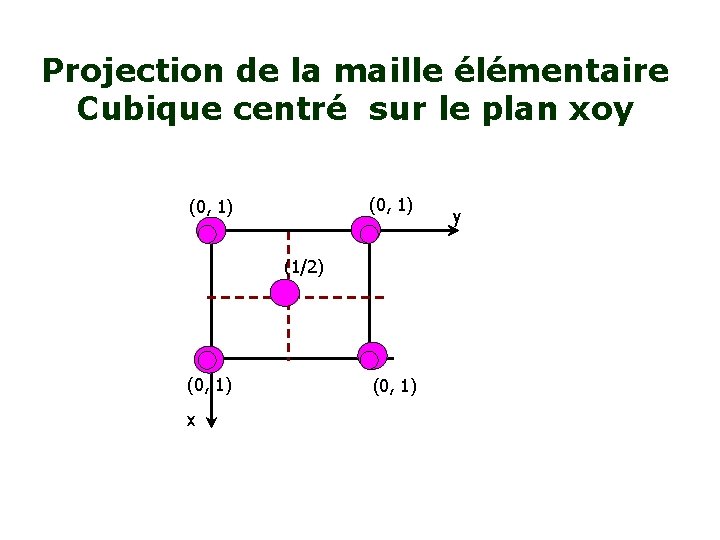
Projection de la maille élémentaire Cubique centré sur le plan xoy (0, 1) (1/2) (0, 1) x (0, 1) y
![La coordinence Dans cette empilement la coordinence est X 8 • La coordinence • Dans cette empilement la coordinence est [X] = [8]](https://slidetodoc.com/presentation_image_h/bd113677267e9e1b67301f52bc1bfc07/image-33.jpg)
• La coordinence • Dans cette empilement la coordinence est [X] = [8] • La multiplicité de la maille : 8 x 1/8 +1 =2 • Les coordonnées réduites les coordonnées réduites nécessaires pour décrire l’ensembles des positions atomiques dans un réseau C. C sont (000), (1/2, 1/2). • Compacité: La compacité de cette structure est inférieure à celle de HC et CFC Ex de structure CC: Li, Na, Cs, Ba, Feα, Mo, Zn, W…

Insertion dans les réseaux • L’existence d’interstices vides dans les cristaux métalliques permet d’envisager l’insertion d’atomes plus petits : on obtient ainsi des composés d’insertion comme les alliages métalliques. Ex. l’acier Fer- carbone. L’insertion du carbone permet de modifier les propriétés mécaniques du fer. • Étude des conditions d’insertion dans les empilements compacts CFC et HC. • Sites cristallographiques • Sites octaédriques. Le polyèdre de référence est l’octaèdre, polyèdre à 6 sommets dont les 8 faces sont des triangles équilatéraux. Le centre de cet octaèdre correspond au site octaédrique ce qui implique une coordinence 6 ]

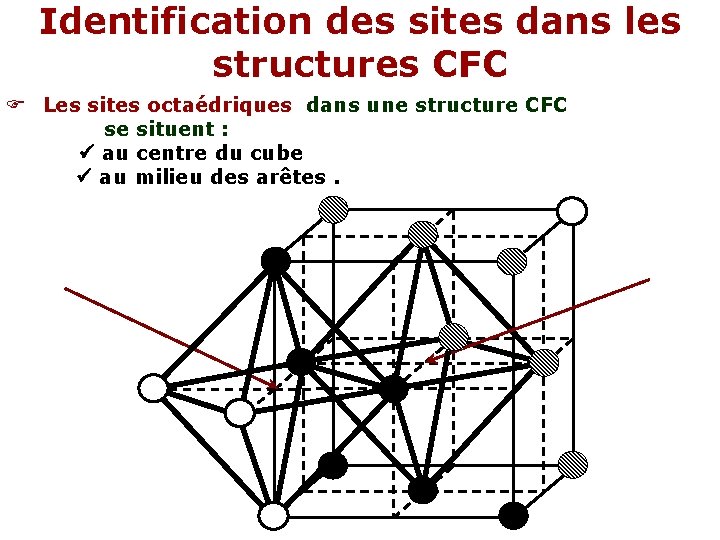
Identification des sites dans les structures CFC Les sites octaédriques dans une structure CFC se situent : au centre du cube au milieu des arêtes.

Le nombre des sites octaédriques est : (1 x 1) + (12 x ¼) = 4 Le nombre de sites octaédriques est égal au nombre de motifs/Maille. Coordonnées réduites des sites octaédriques (1/2, 1/2); (1/2, 0, 0); (0, 1/2, 0)et (0, 0, 1/2) Le rayon maximum ro d’une sphère susceptible d’être introduite en site octaédrique ; sans que soit déformé le réseau, est tel que : 2(R + ro) = a a = 2 R 2 = 2 2 R Ce qui donne : 4 R=

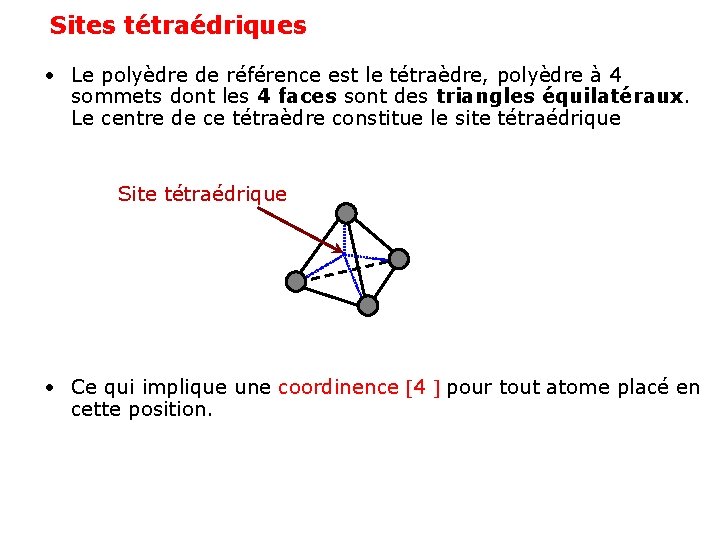
Sites tétraédriques • Le polyèdre de référence est le tétraèdre, polyèdre à 4 sommets dont les 4 faces sont des triangles équilatéraux. Le centre de ce tétraèdre constitue le site tétraédrique Site tétraédrique • Ce qui implique une coordinence 4 pour tout atome placé en cette position.

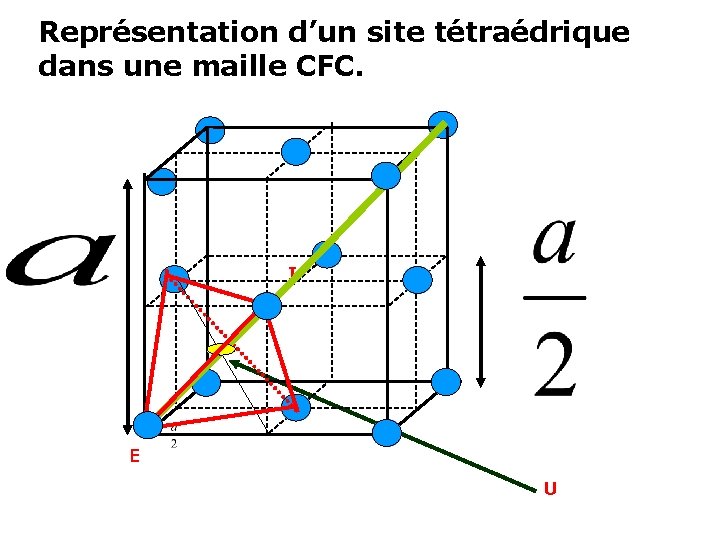
Représentation d’un site tétraédrique dans une maille CFC. I E U

• La maille CFC est formée de 8 petits cubes élémentaires d’arête a/2 portant 4 atomes. • Ces quatre atomes constituent un site tétraédrique, dont le centre U est à mi-chemin entre le point E pris comme origine , donc de coordonnées réduites (0, 0, 0) et le point I, centre de la maille de coordonnées réduites (1/2, 1/2). • Le point U a alors comme coordonnées (3/4, 1/4; 1/4). Il se situe donc au quart de la diagonale du cube issue de E. Comme tous les sites sont internes à la maille. Il en résulte l’existence de : T = 8 • Les coordonnées réduites des autres sites tétraédriques sont: : (1/4, 1/4 ); (3/4, 1/4) (1/4, 3/4, 1/4) (3/4, 1/4) (1/4, 3/4); (3/4, 1/4, 3/4 ) (1/4, 3/4) (3/4, 3/4)

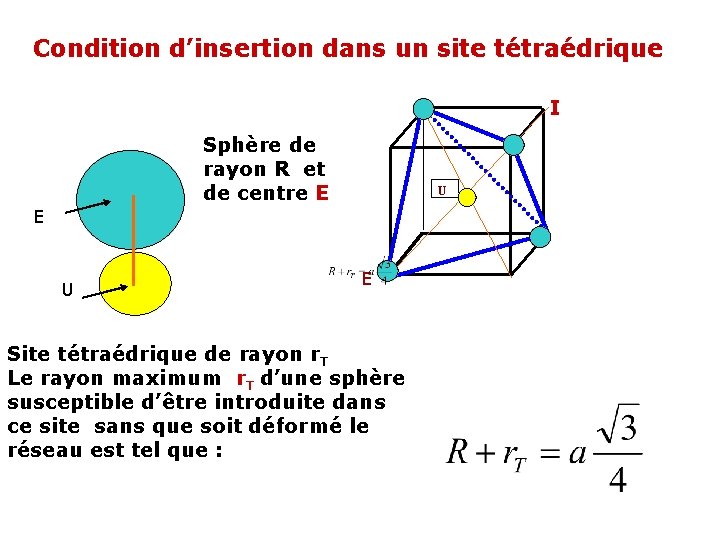
Condition d’insertion dans un site tétraédrique I Sphère de rayon R et de centre E U E Site tétraédrique de rayon r. T Le rayon maximum r. T d’une sphère susceptible d’être introduite dans ce site sans que soit déformé le réseau est tel que :

• En remplaçant a par sa valeur, on obtient : R + r. T = a ( 3)/4) = 2 R 2 ( 3)/4) = R 3/ 2 • r. T/R = ( 3/ 2) - 1 = 0. 225 • Ce qui donne : r. T = 0. 225 R • Un site T ne pourra donc être occupé que par un atome plus petit que celui qui s’insère dans un site octaédrique.

En Conclusion • la condition d’insertion dans un CFC • En site Octaédrique ro / R = 2 -1 = 0, 414 • En site tétraédrique r. T/R = ( 3/ 2) -1 = 0. 225

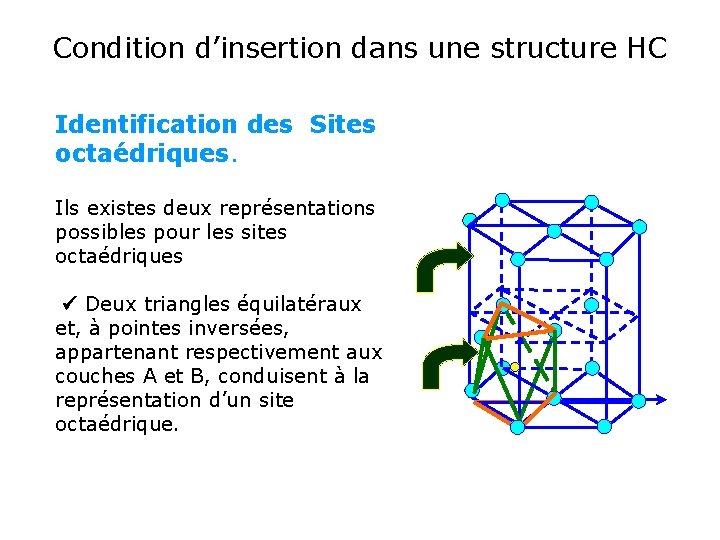
Condition d’insertion dans une structure HC Identification des Sites octaédriques. Ils existes deux représentations possibles pour les sites octaédriques Deux triangles équilatéraux et, à pointes inversées, appartenant respectivement aux couches A et B, conduisent à la représentation d’un site octaédrique.

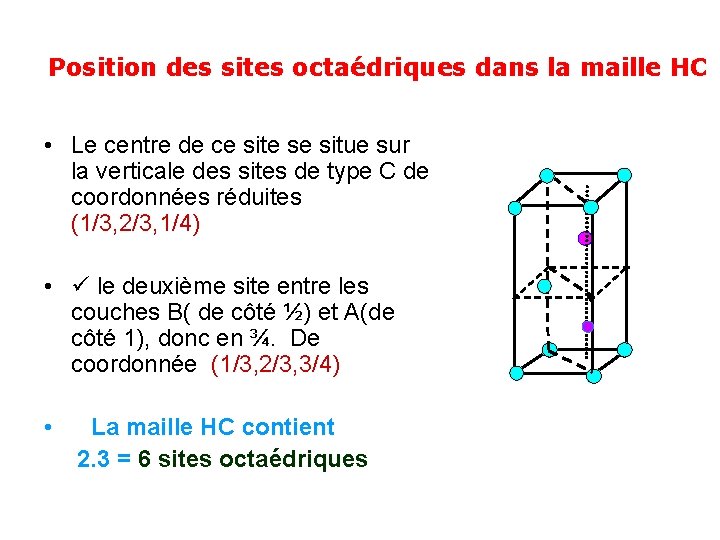
Position des sites octaédriques dans la maille HC • Le centre de ce site se situe sur la verticale des sites de type C de coordonnées réduites (1/3, 2/3, 1/4) • le deuxième site entre les couches B( de côté ½) et A(de côté 1), donc en ¾. De coordonnée (1/3, 2/3, 3/4) • La maille HC contient 2. 3 = 6 sites octaédriques

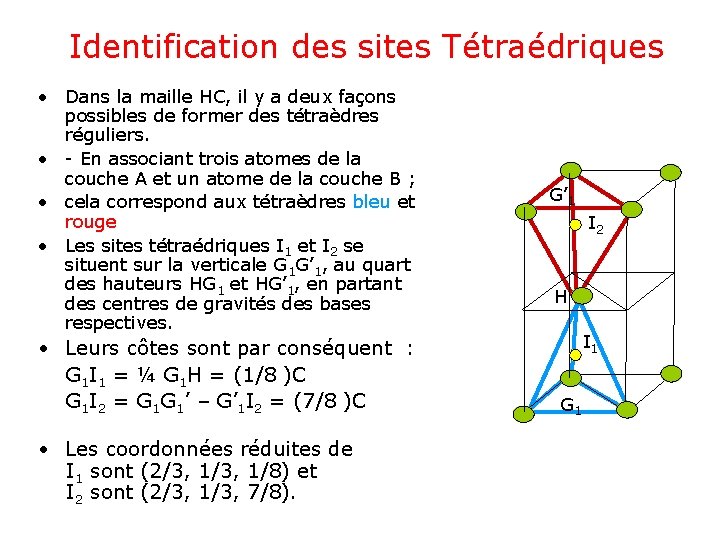
Identification des sites Tétraédriques • Dans la maille HC, il y a deux façons possibles de former des tétraèdres réguliers. • - En associant trois atomes de la couche A et un atome de la couche B ; • cela correspond aux tétraèdres bleu et rouge • Les sites tétraédriques I 1 et I 2 se situent sur la verticale G 1 G’ 1, au quart des hauteurs HG 1 et HG’ 1, en partant des centres de gravités des bases respectives. • Leurs côtes sont par conséquent : G 1 I 1 = ¼ G 1 H = (1/8 )C G 1 I 2 = G 1 G 1’ – G’ 1 I 2 = (7/8 )C • Les coordonnées réduites de I 1 sont (2/3, 1/8) et I 2 sont (2/3, 1/3, 7/8). G’ 1 I 2 H I 1 G 1

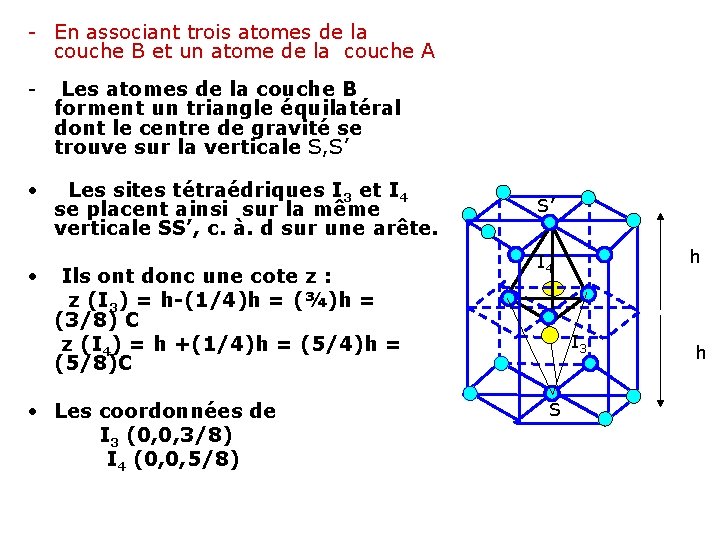
- En associant trois atomes de la couche B et un atome de la couche A - Les atomes de la couche B forment un triangle équilatéral dont le centre de gravité se trouve sur la verticale S, S’ • Les sites tétraédriques I 3 et I 4 se placent ainsi sur la même verticale SS’, c. à. d sur une arête. • Ils ont donc une cote z : z (I 3) = h-(1/4)h = (¾)h = (3/8) C z (I 4) = h +(1/4)h = (5/8)C • Les coordonnées de I 3 (0, 0, 3/8) I 4 (0, 0, 5/8) S’ h I 4 I 3 S h

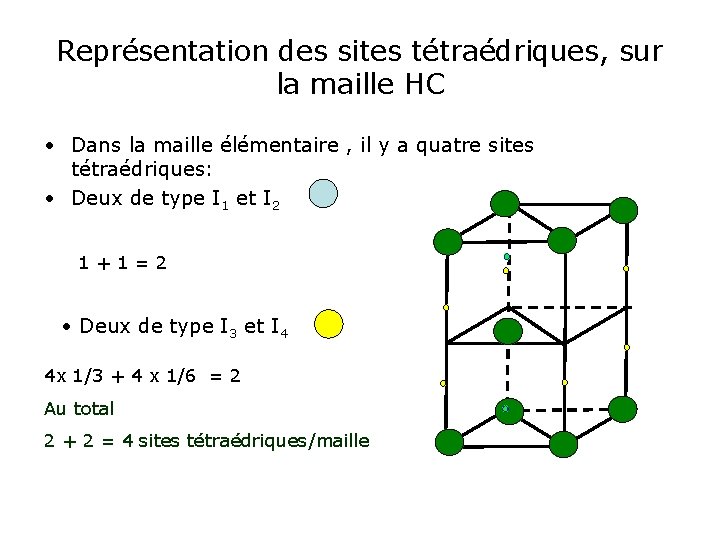
Représentation des sites tétraédriques, sur la maille HC • Dans la maille élémentaire , il y a quatre sites tétraédriques: • Deux de type I 1 et I 2 1 + 1 = 2 • Deux de type I 3 et I 4 4 x 1/3 + 4 x 1/6 = 2 Au total 2 + 2 = 4 sites tétraédriques/maille

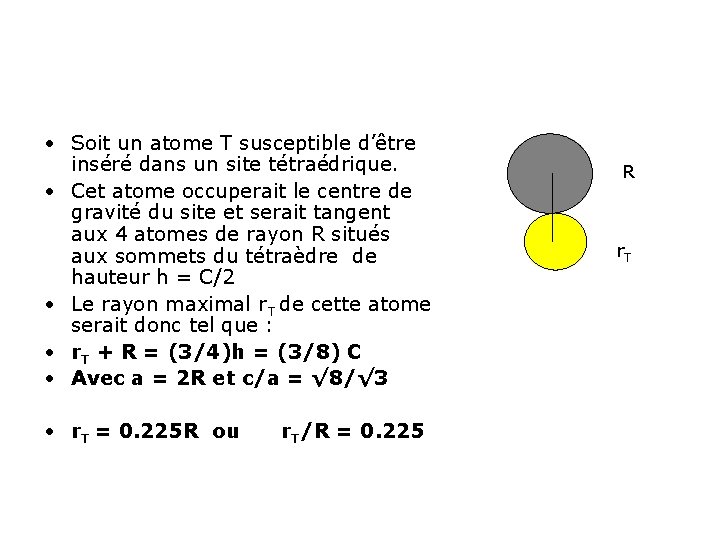
• Soit un atome T susceptible d’être inséré dans un site tétraédrique. • Cet atome occuperait le centre de gravité du site et serait tangent aux 4 atomes de rayon R situés aux sommets du tétraèdre de hauteur h = C/2 • Le rayon maximal r. T de cette atome serait donc tel que : • r. T + R = (3/4)h = (3/8) C • Avec a = 2 R et c/a = √ 8/√ 3 • r. T = 0. 225 R ou r. T/R = 0. 225 R r. T

• De même si un atome O peut s’insérer dans un site octaédrique sans déformer la structure, il occuperait le centre de gravité du site càd le centre du carré de côté a délimité par les atomes formant un octaèdre • Le rayon maximal ro de l’atome à insérer doit être au maximum tel que: • ro+ R = a√ 2/2 avec a =2 R • ro /R = 0. 414 • NB : les conditions d’insertion sont les mêmes pour les deux types de structures CFC et HC

Relation entre les paramètres a et c F A B E D C a