CHAPITRE 8 Hybridation Dfinition Une autre manire dinterprter

CHAPITRE 8 Hybridation

Définition Une autre manière d'interpréter la structure moléculaire est l'utilisation du concept d'hybridation. Pour respecter la symétrie géométrique de la molécule formée, on considère que certaines orbitales atomiques des électrons de valence se combinent linéairement entre elles pour former de nouvelles orbitales atomiques dites orbitales hybrides, notées ti, dont les directions sont celle du squelette s de la molécule. Les orbitales restantes sont dites pures c'est à dire elles gardent leur direction initiale. Remarque: Le concept d'hybridation, largement utilisé en chimie, a pour principale faiblesse le fait qu'il utilise à priori la symétrie moléculaire. Il n'est pas la consécration d'une opération réelle mais Il n'est qu'une conséquence mathématique de la linéarité de l'équation de Schrödinger.
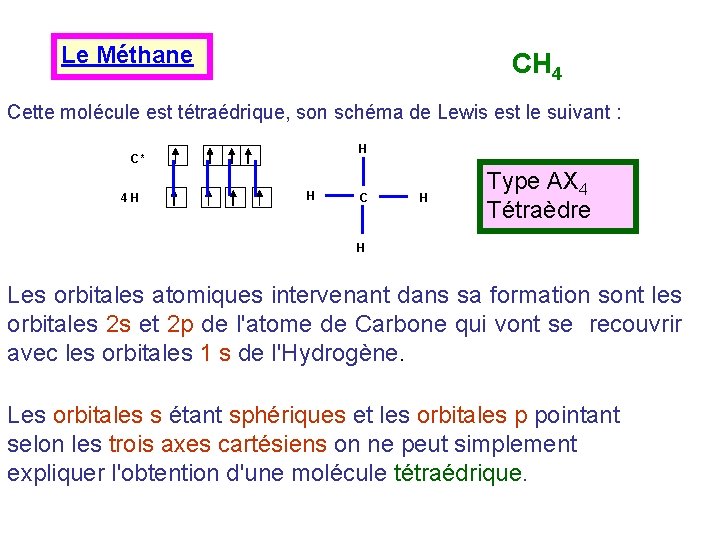
Le Méthane CH 4 Cette molécule est tétraédrique, son schéma de Lewis est le suivant : H C* 4 H H C H Type AX 4 Tétraèdre H Les orbitales atomiques intervenant dans sa formation sont les orbitales 2 s et 2 p de l'atome de Carbone qui vont se recouvrir avec les orbitales 1 s de l'Hydrogène. Les orbitales s étant sphériques et les orbitales p pointant selon les trois axes cartésiens on ne peut simplement expliquer l'obtention d'une molécule tétraédrique.
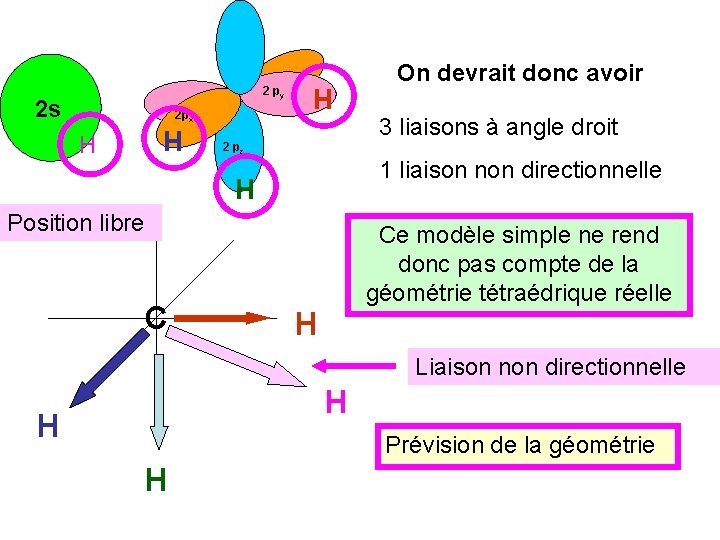
2 py 2 s 2 px H H H 2 pz H Position libre C H H On devrait donc avoir 3 liaisons à angle droit H H 1 liaison non directionnelle Ce modèle simple ne rend donc pas compte de la géométrie tétraédrique réelle H Liaison non directionnelle H H Prévision de la géométrie H

On va donc faire appel à des orbitales atomiques hybrides de l'atome de carbone possédant une géométrie tétraédrique, il en faudra quatre identiques. Ces orbitales atomiques hybrides sont des combinaisons linéaires des 4 orbitales atomiques normales du carbone. sp 3 = a 2 s + b 2 px + c 2 py + d 2 pz Ces quatre orbitales hybrides sont nommées orbitales hybride sp 3, elles sont identiques entre elles et sont dirigées selon les directions d'un tétraèdre centré sur l'atome de Carbone. On peut calculer les divers coefficients a, b, c et d pour obtenir une telle géométrie.
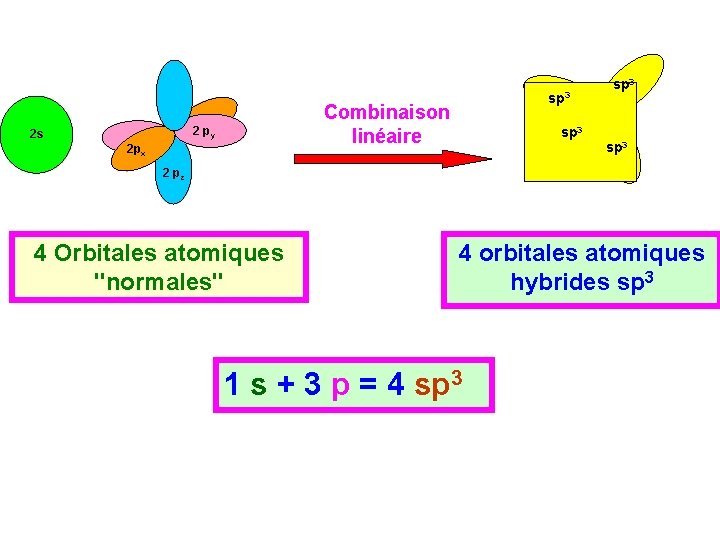
Combinaison linéaire 2 py 2 s sp 3 2 px sp 3 2 pz 4 Orbitales atomiques "normales" 4 orbitales atomiques hybrides sp 3 1 s + 3 p = 4 sp 3
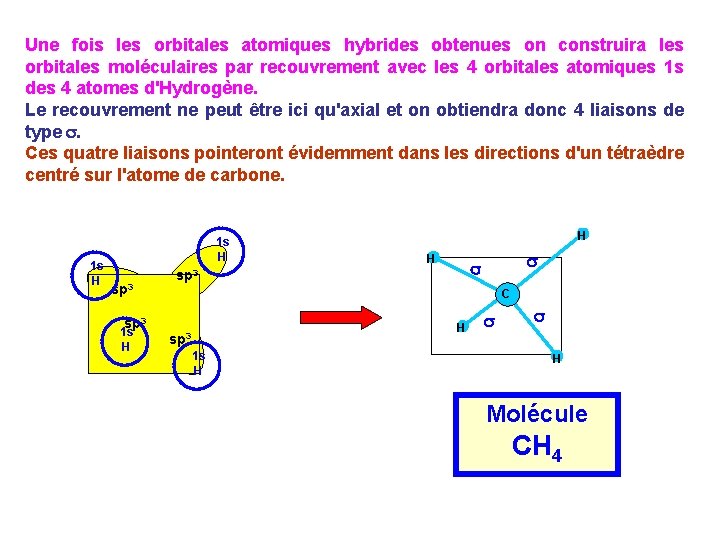
Une fois les orbitales atomiques hybrides obtenues on construira les orbitales moléculaires par recouvrement avec les 4 orbitales atomiques 1 s des 4 atomes d'Hydrogène. Le recouvrement ne peut être ici qu'axial et on obtiendra donc 4 liaisons de type s. Ces quatre liaisons pointeront évidemment dans les directions d'un tétraèdre centré sur l'atome de carbone. 1 s H sp 3 1 s H H H s s sp 3 C H sp 3 1 s H s s H Molécule CH 4
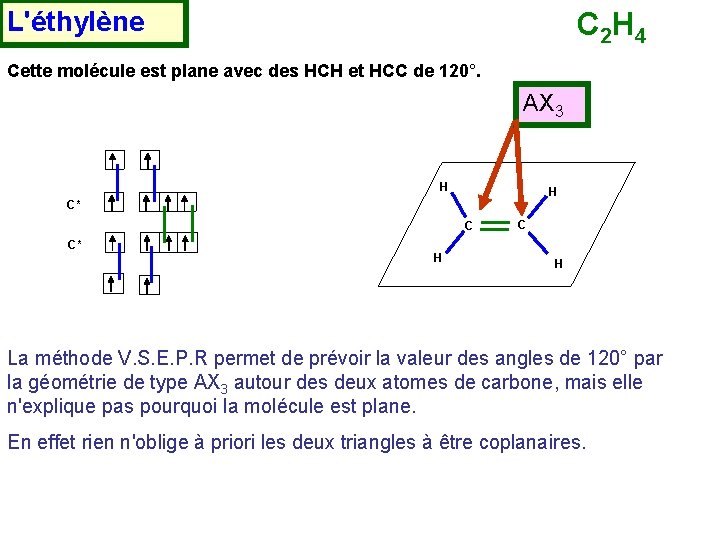
L'éthylène C 2 H 4 Cette molécule est plane avec des HCH et HCC de 120°. AX 3 H H C* C C* H C H La méthode V. S. E. P. R permet de prévoir la valeur des angles de 120° par la géométrie de type AX 3 autour des deux atomes de carbone, mais elle n'explique pas pourquoi la molécule est plane. En effet rien n'oblige à priori les deux triangles à être coplanaires.

Pour décrire cette molécule l'hybridation, de type sp 3 ne convient pas, nous allons faire appel à une hybridation de type sp 2. L'exposant 2 indique ici que seules deux orbitales p seront combinées avec l'orbitale s pour obtenir ce type d'orbitales hybrides. Il restera donc une orbitale p sur chaque atome de carbone. 1 s + 3 p = 3 sp 2 + 1 p Ces orbitales hybrides sp 2 pointeront dans les directions d ’un triangle équilatéral centré sur l ’atome de Carbone.
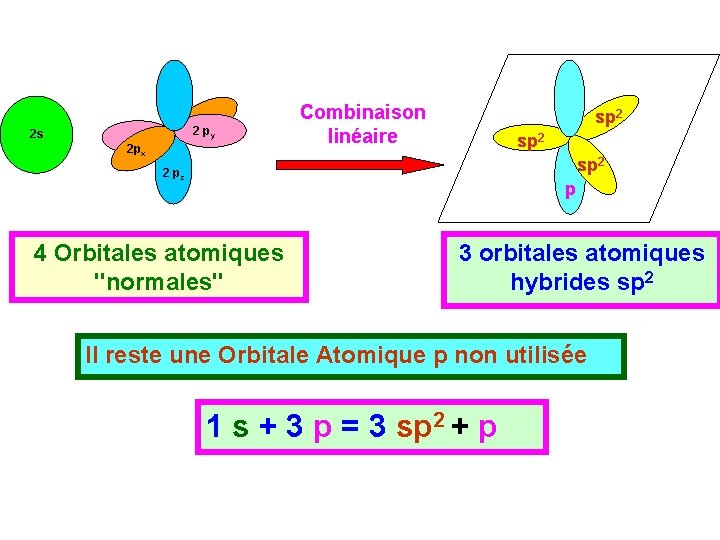
2 py 2 s 2 px Combinaison linéaire sp 2 2 pz p 4 Orbitales atomiques "normales" 3 orbitales atomiques hybrides sp 2 Il reste une Orbitale Atomique p non utilisée 1 s + 3 p = 3 sp 2 + p
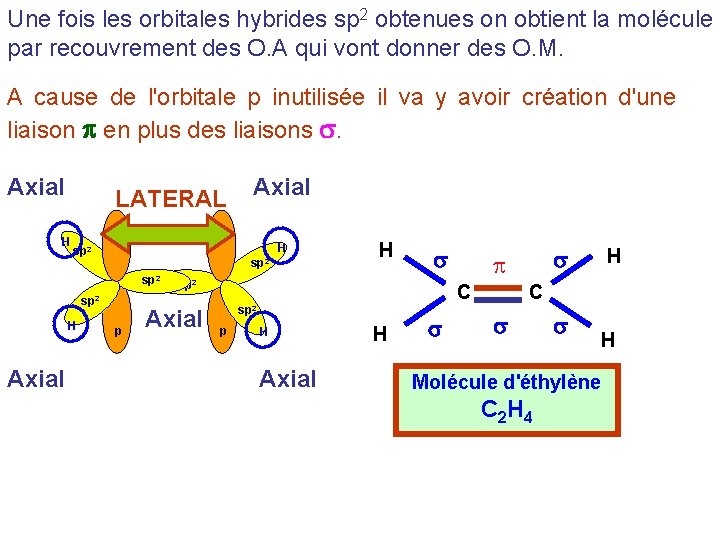
Une fois les orbitales hybrides sp 2 obtenues on obtient la molécule par recouvrement des O. A qui vont donner des O. M. A cause de l'orbitale p inutilisée il va y avoir création d'une liaison p en plus des liaisons s. Axial LATERAL H H sp 2 H Axial p H s sp 2 Axial C sp 2 p H Axial H s s p H C s s H Molécule d'éthylène C 2 H 4
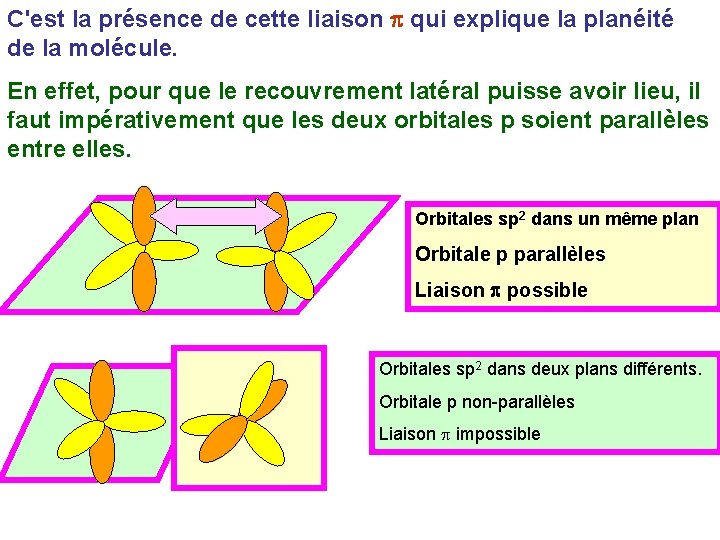
C'est la présence de cette liaison p qui explique la planéité de la molécule. En effet, pour que le recouvrement latéral puisse avoir lieu, il faut impérativement que les deux orbitales p soient parallèles entre elles. Orbitales sp 2 dans un même plan Orbitale p parallèles Liaison p possible Orbitales sp 2 dans deux plans différents. Orbitale p non-parallèles Liaison p impossible
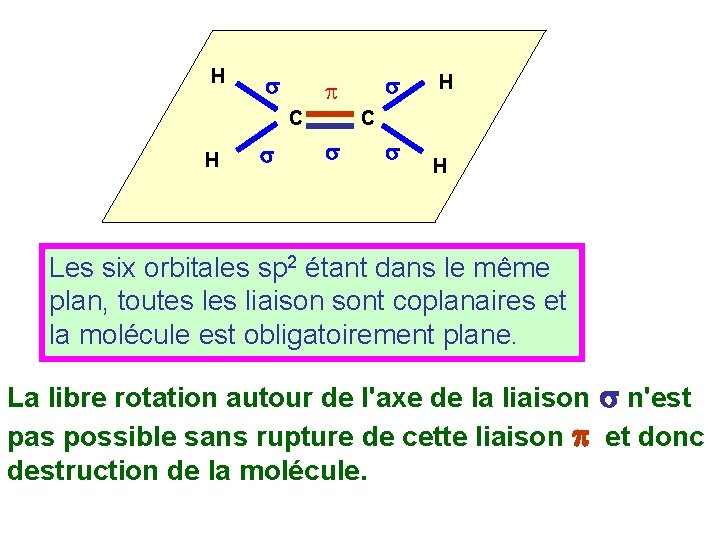
H s C H s s p H C s s H Les six orbitales sp 2 étant dans le même plan, toutes liaison sont coplanaires et la molécule est obligatoirement plane. La libre rotation autour de l'axe de la liaison s n'est pas possible sans rupture de cette liaison p et donc destruction de la molécule.
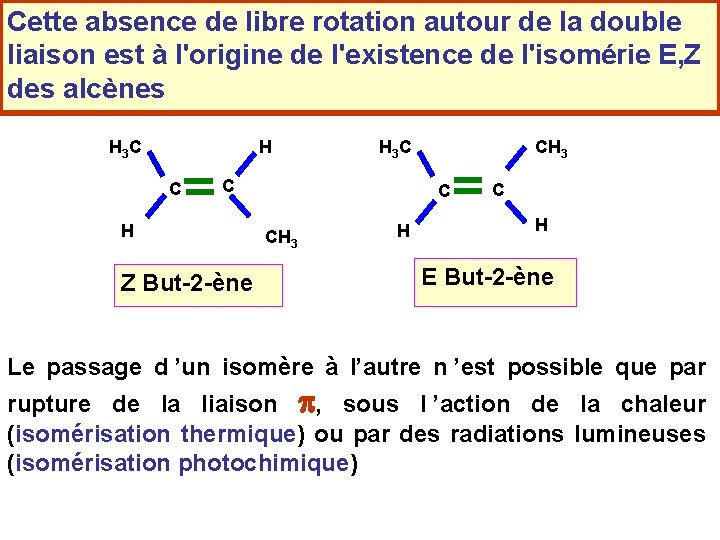
Cette absence de libre rotation autour de la double liaison est à l'origine de l'existence de l'isomérie E, Z des alcènes H 3 C C H Z But-2 -ène CH 3 C CH 3 H C H E But-2 -ène Le passage d ’un isomère à l’autre n ’est possible que par rupture de la liaison p, sous l ’action de la chaleur (isomérisation thermique) ou par des radiations lumineuses (isomérisation photochimique)
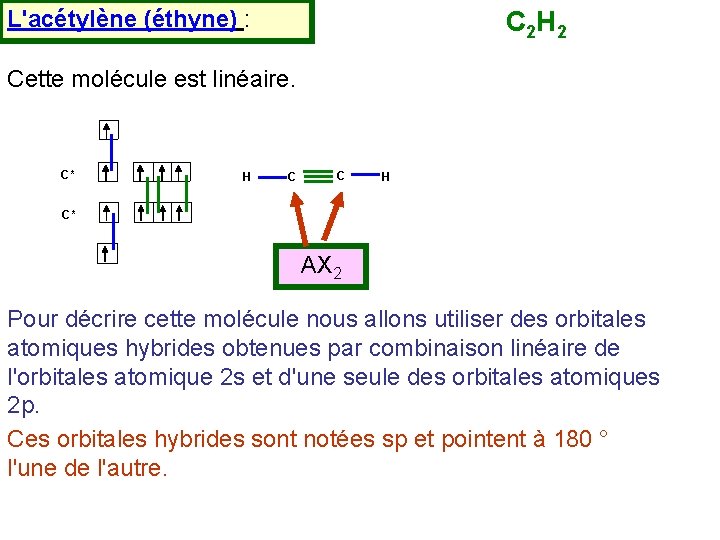
L'acétylène (éthyne) : C 2 H 2 Cette molécule est linéaire. C* H C C H C* AX 2 Pour décrire cette molécule nous allons utiliser des orbitales atomiques hybrides obtenues par combinaison linéaire de l'orbitales atomique 2 s et d'une seule des orbitales atomiques 2 p. Ces orbitales hybrides sont notées sp et pointent à 180 ° l'une de l'autre.
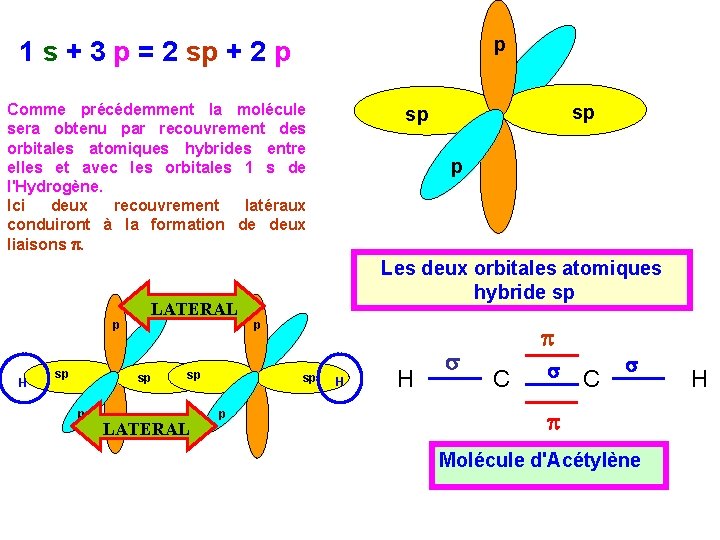
p 1 s + 3 p = 2 sp + 2 p Comme précédemment la molécule sera obtenu par recouvrement des orbitales atomiques hybrides entre elles et avec les orbitales 1 s de l'Hydrogène. Ici deux recouvrement latéraux conduiront à la formation de deux liaisons p. p H sp LATERAL sp p sp LATERAL p Les deux orbitales atomiques hybride sp p sp sp H H s p C s p Molécule d'Acétylène H

Méthode générale Pour retrouver d'une manière systématique l'hybridation on doit opérer selon les étapes suivantes: 1ère étape: Trouver le nombre L de liguants X autour de l'atome central A. Il est égal au nombre de liaisons simples contractées par l'atome central. 2ème étape: Écrire la configuration électronique des électrons de valence de l'état fondamental de l'atome central et en déduire sa valence minimale vmin. Il est nécessaire d'utiliser la notation avec les cases quantiques ou en différenciant les orbitales "équivalentes" (npx, npy et npz par exemple)

3ème étape: Deux cas se présentent: *1 er cas : L ≤ vmin. On passe à la 4éme étape. *2ème cas: L> vmin. On dégèle des doublets libres pour permettre aux électrons d'occuper de nouvelles orbitales atomiques. On s'arrêtera quand le nombre d'électrons célibataires est supérieur ou égal à L. On notera K le nombre total d'orbitales occupées par des doublets ou par des électrons célibataires. 4ème étape: Préciser le nombre P de liaison π contractées par l'atome central et le nombre D de doublets libres restants. Calculer alors le nombre N d'orbitales à hybrider suivant la formule: N=. K-P. Ces N orbitales serviront à former le squelette s de l'entité moléculaire, à contenir les D doublets libres ou dans certains cas les électrons restants célibataires pour les composés radicalaires. 5ème étape: Nommer l'hybridation de l'atome central en indiquant par un exposant à droite le nombre d'orbitales hybridé d'un même

L' hybridation dsp 3 L' exemple sera illustré par la molécule de pentachlorure de phosphore, de formule PCl 5. Voilà une molécule qui n' existe pas si l' on s' en tient au modèle de LEWIS: la règle de l' octet n' est pas satisfaite puisque le phosphore est entouré de 10 électrons de valence, et non pas de huit (cf "octet"). Et pourtant, elle existe bel et bien. . Le phosphore P (Z = 15) a la structure électronique suivante, pris dans son état fondamental: [Ne] 3 s 2 3 p 3

Le chlore Cl (Z = 17) a la structure électronique suivante, pris dans son état fondamental: [Ne] 3 s 2 3 p 5 Afin d' expliquer la valence 5 du phosphore il est alors imaginé de réarranger les électrons des sous-couches 3 s et 3 p du phosphore, en les combinant, le plus arbitrairement qui soit, mais en tenant compte d' énergies voisines de ces différentes sous-couches, avec une partie de la sous-couche 3 d. On aura alors comme structure électronique de l' atome de phosphore la structure suivante: [Ne] 3 s 1 3 p 3 3 d 1 On aura alors : 1 orbitale 3 s + 3 orbitales 3 p + 1 orbitale 3 d 5 orbitales atomiques hybrides "dsp 3 " ou " sp 3 d "
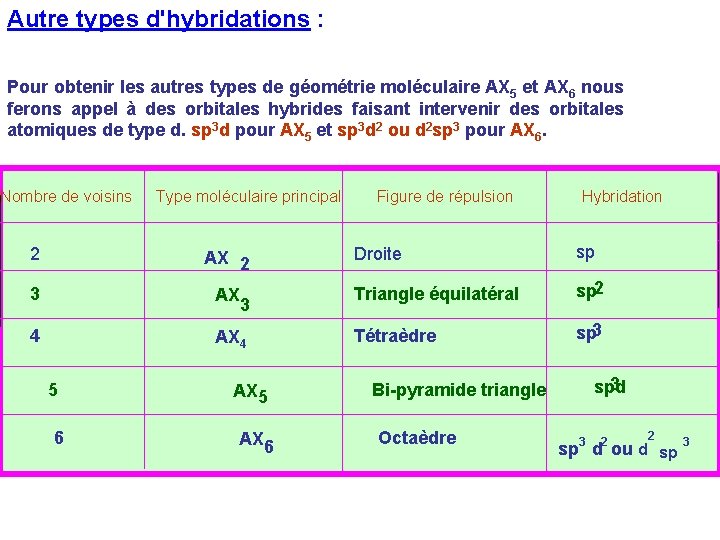
Autre types d'hybridations : Pour obtenir les autres types de géométrie moléculaire AX 5 et AX 6 nous ferons appel à des orbitales hybrides faisant intervenir des orbitales atomiques de type d. sp 3 d pour AX 5 et sp 3 d 2 ou d 2 sp 3 pour AX 6. Nombre de voisins Type moléculaire principal 2 AX 2 3 AX 4 5 6 3 AX 5 AX 6 Figure de répulsion Hybridation Droite sp Triangle équilatéral sp 2 Tétraèdre sp 3 Bi-pyramide triangle Octaèdre sp 3 d 2 3 sp d ou d sp
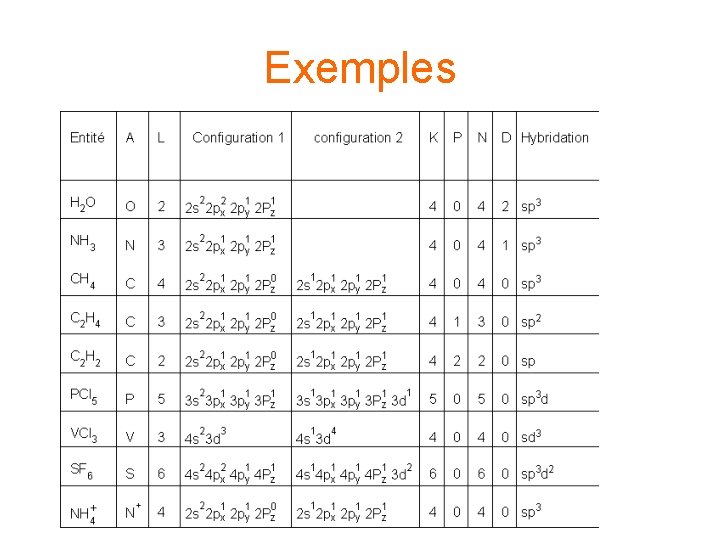
Exemples
- Slides: 22