Chapitre 6 Constante dacidit dun couple acide base

Chapitre 6 : Constante d’acidité d’un couple acide / base Introduction Ecritures de K dans le cas particulier des réactions acidobasiques 1. Produit ionique de l’eau 2. Constante d’acidité Ka 3. Comportement des acides et des bases en solution 4. Diagrammes de prédominance et de distribution

Chapitre 6 : Constante d’acidité d’un couple acide / base 1. Produit ionique de l’eau Eau pure : p. H = 7, 0 [H 3 O+] = 10 -7 mol/L Comment se fait-il qu’il y ait des ions H 3 O+? H 3 O+(aq) / H 2 O(l) / OH-(aq) H 2 O(l)+ H 2 O(l) = H 3 O+(aq) + OH-(aq) Autoprotolyse de l’eau Le taux d’avancement de cette réaction est très faible. Expression de la constante d’équilibre K = [H 3 O+]*[OH-](aq)

Chapitre 6 : Constante d’acidité d’un couple acide / base 1. Produit ionique de l’eau Ke La constante d’équilibre de la réaction d’autoprotolyse de l’eau est appelée « produit ionique de l’eau » et est notée K e. Ke = [H 3 O+]*[OH-] -log. Ke = -log[H 3 O+]-log[OH-] p. Ke = p. H -log[OH-] À 25°C Ke = 1, 0. 10 -14 p. Ke = 14, 0 p. Ke e = -log. Ke p. K Ke = [H 3 O+]*[OH-] p. H = p. Ke + log[OH-] = 10(p. H-p. Ke)
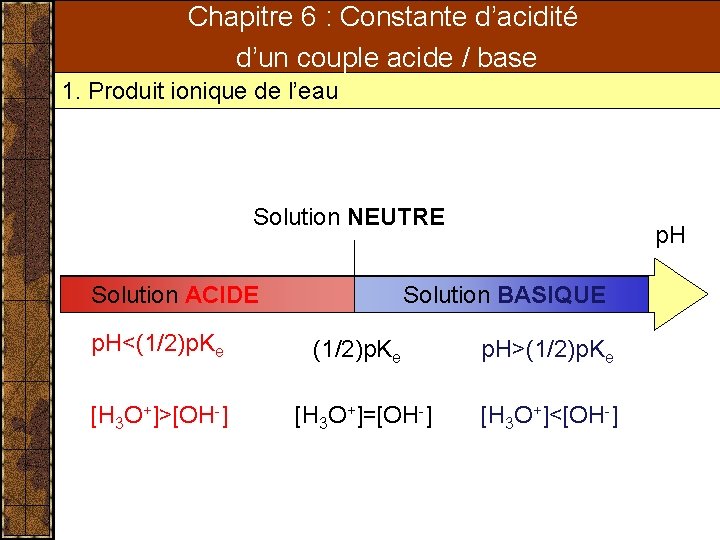
Chapitre 6 : Constante d’acidité d’un couple acide / base 1. Produit ionique de l’eau Solution NEUTRE Solution ACIDE p. H Solution BASIQUE p. H<(1/2)p. Ke p. H>(1/2)p. Ke [H 3 O+]>[OH-] [H 3 O+]=[OH-] [H 3 O+]<[OH-]
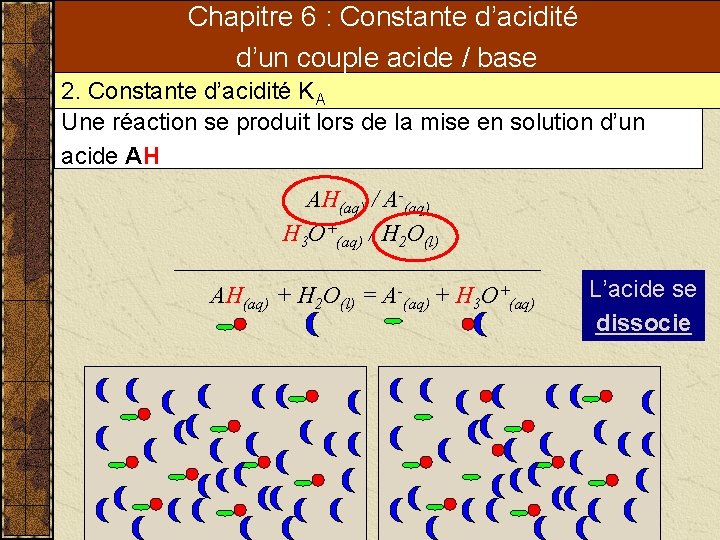
Chapitre 6 : Constante d’acidité d’un couple acide / base 2. Constante d’acidité KA Une réaction se produit lors de la mise en solution d’un acide AH AH(aq) / A-(aq) H 3 O+(aq) / H 2 O(l) AH(aq) + H 2 O(l) = A-(aq) + H 3 O+(aq) L’acide se dissocie

Chapitre 6 : Constante d’acidité d’un couple acide / base 2. Constante d’acidité KA La constante d’équilibre de cette réaction est appelée constante d’acidité et est notée KA. Elle ne dépend que de la température. KA = [A-]eq. [H 3 O+]eq [AH]eq p. KA = -log. KA p. H = p. KA + log( [A-]eq/[AH]eq )
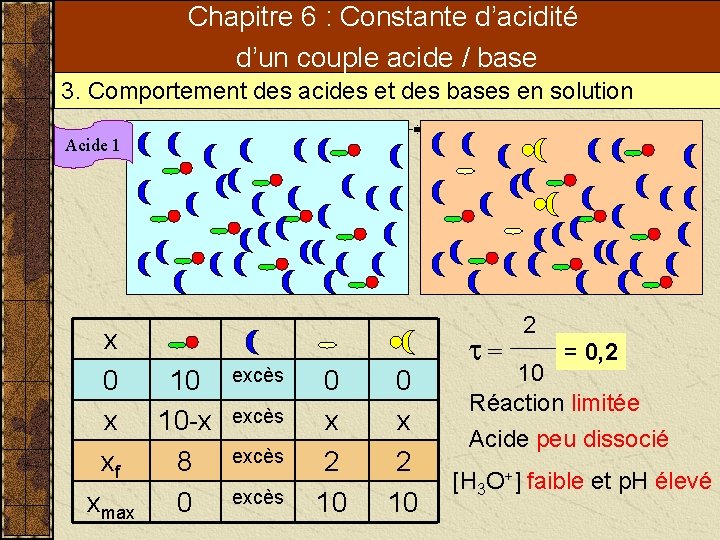
Chapitre 6 : Constante d’acidité d’un couple acide / base 3. Comportement des acides et des bases en solution Acide 1 x 0 x xf xmax 10 10 -x 8 0 excès 0 x 2 10 t= 2 = 0, 2 10 Réaction limitée Acide peu dissocié [H 3 O+] faible et p. H élevé
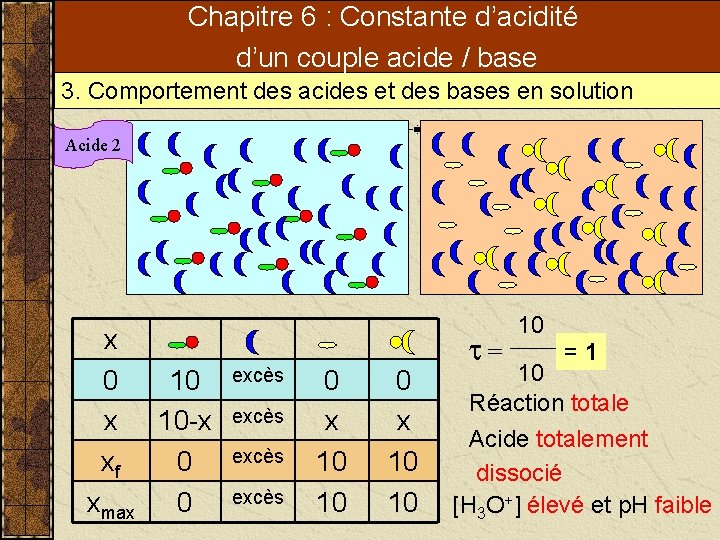
Chapitre 6 : Constante d’acidité d’un couple acide / base 3. Comportement des acides et des bases en solution Acide 2 x 0 x xf xmax 10 10 -x 0 0 excès 0 x 10 10 t= 10 = 1 10 Réaction totale Acide totalement dissocié [H 3 O+] élevé et p. H faible

Chapitre 6 : Constante d’acidité d’un couple acide / base 3. Comportement des acides et des bases en solution Acide 1 Acide 2 Pour des solutions de même concentrations apportées: • le p. H est d’autant plus faible • le taux d’avancement est d’autant plus élevé • l’acide est d’autant plus dissocié que l’acide est fort (que son KA est élevé et son p. KA faible).

Chapitre 6 : Constante d’acidité d’un couple acide / base 3. Comportement des acides et des bases en solution De la même façon, pour des solutions de bases Pour des solutions de même concentrations apportées: • le p. H est d’autant plus élevé • le taux d’avancement est d’autant plus élevé • la base est d’autant plus protonée que la base est forte (que son KA est faible et son p. KA élevé).
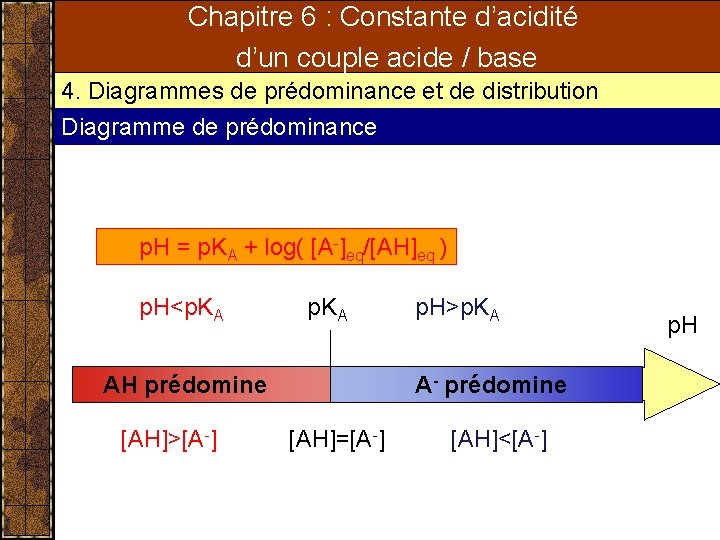
Chapitre 6 : Constante d’acidité d’un couple acide / base 4. Diagrammes de prédominance et de distribution Diagramme de prédominance p. H = p. KA + log( [A-]eq/[AH]eq ) p. H<p. KA AH prédomine [AH]>[A-] p. H>p. KA A- prédomine [AH]=[A-] [AH]<[A-] p. H
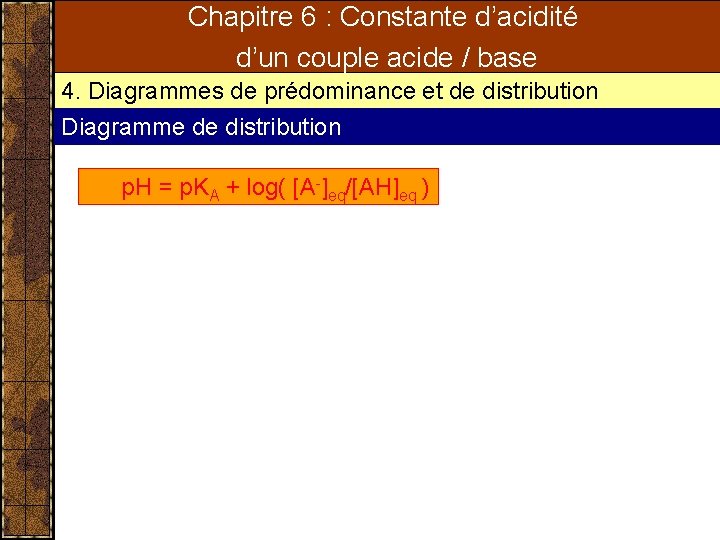
Chapitre 6 : Constante d’acidité d’un couple acide / base 4. Diagrammes de prédominance et de distribution Diagramme de distribution p. H = p. KA + log( [A-]eq/[AH]eq )

Chapitre 6 : Constante d’acidité d’un couple acide / base 4. Diagrammes de prédominance et de distribution Indicateurs colorés HInd / Ind. Les indicateurs colorés de p. H sont constitués par des couples acido-basiques dont les espèces conjuguées ont des teintes différentes. Exemple: Bleu de Bromothymol (BBT) HInd(aq)+ H 2 O(l) = H 3 O+(aq) + Ind-(aq) p. Ka-1 p. Ka+1 6, 3 8, 3 Zone de virage p. H
Chapitre 6 : Constante d’acidité d’un couple acide / base 5. Détermination expérimentale d’un KA Voir TP
Chapitre 6 : Constante d’acidité d’un couple acide / base Objectif BAC Autoprotolyse de l’eau Produit ionique de l’eau Constante d’acidité KA / p. KA Acide faible / Acide Fort Acide dissocié Diagramme de prédominance Diagramme de distribution Indicateur coloré Objectif BAC expérimental Conductimétrie p. H-métrie
- Slides: 15