CHAPITRE 3 QUILIBRES DE PRCIPITATION 1 INTRODUCTION Exemples

CHAPITRE 3 ÉQUILIBRES DE PRÉCIPITATION
1 ) INTRODUCTION Exemples. Entartrage : Ca. CO 3 (s) 1 2 Ca 2+ (aq) + CO 32 - (aq) sens 1 : sens direct : dissolution du carbonate de calcium sens 2 : sens inverse : précipitation du carbonate de calcium Dosage des ions chlorure par une solution de nitrate d ’argent Cl- (aq) + Ag+ (aq) = Ag. Cl (s)

2 ) SOLUBILITÉ D ’UN COMPOSÉ IONIQUE 2. 1 ) Solubilité : définition. Soit une solution saturée d ’un composé peu soluble A , Ba. F 2 , par exemple : La solubilité de A, notée s, est le quotient de la quantité de A qu ’il a fallu dissoudre pour obtenir cette solution saturée, par le volume V de solution à une température donnée. Elle s’exprime généralement en mol. L-1 : mol. L-1 L Elle peut aussi s ’exprimer en g. L-1 g g. L-1 L

exemples : dissolution de Ag. Cl : Ag. Cl (s) = Ag+ + Cl. E. I. n 0 équilibre (mol) équilibre (mol. L-1) - - n 0 - n n n - s s [Ag+] = [Cl-] dissolution de Ba. F 2 : Ba. F 2 (s) = Ba 2+ + 2 FE. I. n 0 - - équilibre (mol) n 0 - n n 2 n équilibre (mol. L-1 ) - s 2 s [Ba 2+] = Remarque : dans l ’équilibre ci-dessus , la réaction de l ’eau avec les ions fluorure a été négligée.

2. 2 ) Produit de solubilité Ks. Soit une solution saturée en chlorure d ’argent : le système est le siège de l ’équilibre : Ag. Cl (s) = Ag+ + Cléquilibre hétérogène Cet équilibre est caractérisé par une constante d ’équilibre thermodynamique appelée produit de solubilité et notée Ks. La constante d ’équilibre relie entre elles activités des espèces participant à l ’équilibre. • activité ai d ’un soluté idéal : C 0 : concentration de référence = 1, 00 mol. L-1 • activité a du solvant ou d ’un solide seul dans sa phase : 1 Ks = [Ag+] [Cl-] = 2, 0 10 -10 à 25°C KS n ’a pas d ’unité et ne dépend que de la température
![Ba. F 2 (s) = Ba 2+ + 2 FKS = [Ba 2+] [F-]2 Ba. F 2 (s) = Ba 2+ + 2 FKS = [Ba 2+] [F-]2](http://slidetodoc.com/presentation_image_h/d25a1147cc04f1792805ddf58e3cb937/image-6.jpg)
Ba. F 2 (s) = Ba 2+ + 2 FKS = [Ba 2+] [F-]2 p. Ks = 6, 0 d ’où Plus le composé est soluble plus KS est KS = 1, 0 10 -6 est grand et plus p. Ks est pks = - log(Ks) petit 2. 3 ) Calculs de solubilité La connaissance du produit de solubilité permet de calculer la solubilité s d ’un composé peu soluble. exemple 1 : solubilité du chlorure d ’argent Ag. Cl (s) = Ag+ + Cléquilibre mol. L-1 - d ’où Ks = s 2 s Ks = [Ag+] [Cl-] = 2, 0 10 -10 s et s = (Ks)1/2 = 1, 4 10 -5 mol. L-1

exemple 2 : solubilité du fluorure de baryum Ba. F 2 (s) = Ba 2+ + 2 Féquilibre (mol. L-1) - d ’où Ks = s s (2 s)2 = Ks = [Ba 2+] [F-]2 = 1, 0 10 -6 2 s 4 s 3 et s = 6, 3 10 -3 mol. L-1

2. 4 ) Condition de précipitation • Soit une solution saturée de chlorure d ’argent : les trois espèces , Ag+, Cl- et Ag. Cl (s) coexistent : le système est en équilibre. et vérifient : Ks = [Ag+] [Cl-] • Si la solution n ’est pas saturée , il n ’y a pas de solide et le système est hors d ’équilibre chimique. • On mélange une solution contenant des ions Ag+ et une solution contenant des ions Cl-. Soient et les concentrations apportées dans le mélange, y a-t-il précipitation ou non ? Soit le produit ionique ou quotient de réaction défini par Q = [Ag+]0 [Cl-]0 Q = Ks la solution est saturée ou à la limite de la saturation Q Q < Ks pas de précipité Q > Ks le précipité se forme jusqu’à ce que Q = Ks

Condition de précipitation : il y a précipitation si le produit ionique ou quotient réactionnel est supérieur ou égal au produit de solubilité : la formation du précipité se poursuit jusqu’à ce que le quotient réactionnel devienne égal au produit de solubilité. Il y a précipitation si P. I. (ou Q) KS Application : y a-t-il précipitation quand on mélange 100 cm 3 d’une solution de dichlorure de zinc (C = 2, 0 10 -4 mol. L-1) et 150 cm 3 de solution d’hydroxyde de sodium (C = 2, 0 10 -4 mol. L-1) ? Donnée : Zn(OH)2 ; p. Ks = 17, 0. Il y a précipitation si Q Ks Expression du quotient réactionnel : Zn(OH)2 (s) = Zn 2+ + 2 OHQ = [Zn 2+]0 [OH-]02 Calcul des concentrations apportées : KS = [Zn 2+]éq [OH-]éq 2 = 1, 0 10 -17

dissolutions : n H 2 O Zn(Cl 2) (s) = Zn 2+ + 2 Cl. E. I. E. F. (mol) C V 1 - - - C V 1 2 C V 1 n H 2 O Na. OH (s) = Na+ + OHE. I. E. F. (mol) C V 2 - - C V 2 [Zn 2+]0 = 8, 0 10 -5 mol. L-1 [OH-]0 = 1, 2 10 -4 mol. L-1 Q = [Zn 2+]0 [OH-]02 = Conclusion : Q > KS 1, 15 10 -12 Il y a précipitation V 1 = 100 cm 3 V 2 = 150 cm 3

2. 5 ) Effet d ’ion commun. définition : il y a effet d ’ion commun : • quand un composé ionique est dissous dans une solution contenant déjà l ’un des ions qui constituent le composé : par exemple dissolution du chlorure d ’argent dans une solution contenant des ions Ag+ ou Cl • quand on ajoute à une solution d ’un composé ionique, une solution contenant l ’un des ions qui constituent le composé ionique : par exemple ajout d ’une solution d ’ions chlorure à une solution de chlorure d ’argent. L ’effet d ’ion commun diminue la solubilité Application : déterminer la solubilité du sulfate d ’argent : a) dans l ’eau pure ; b) dans une solution de sulfate de sodium de concentration C = 1, 0 mol. L-1. Donnée : p. KS (Ag 2 SO 4) = 4, 8. Remarque : la réaction des ions sulfate avec l ’eau est négligée.

a ) solubilité s dans l ’eau pure équilibre de dissolution : Ks = Ag 2 SO 4 (s) = 2 Ag+ + équilibre (mol. L-1) - 2 s KS = 4 s 2 s = 4 s 3 1, 58 10 -5 s d ’où s = 1, 6 10 -2 mol. L-1 b ) solubilité s ’ dans une solution de sulfate de sodium de concentration C = 1, 0 mol. L-1. Le sulfate de sodium est un électrolyte fort qui se dissout totalement. E. F. (mol. L-1) Na 2 SO 4 (s) = 2 Na+ + - 2 C C équilibre de dissolution du sulfate d ’argent : Ag 2 SO 4 (s) = 2 Ag+ + E. I. - 0 C équilibre (mol. L-1) - 2 s ’ C + s ’

équilibre de dissolution du sulfate d ’argent : KS = 1, 58 10 -5 Ag 2 SO 4 (s) = 2 Ag+ + E. I. - 0 C équilibre (mol. L-1) - 2 s ’ C + s ’ donc s ’ << C d ’où KS = 4 s ’ 2 (C + s ’ ) Hypothèse : KS << 1 KS 4 s ’ 2 C et s ’ = C + s ’ C 2, 0 10 -3 mol. L-1 l ’hypothèse est valide et s’ est inférieure à s (1, 6 10 -2 mol. L-1 ).
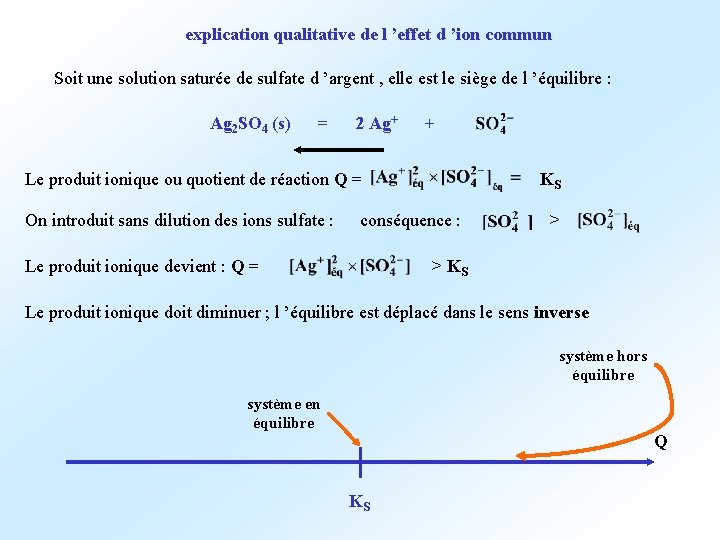
explication qualitative de l ’effet d ’ion commun Soit une solution saturée de sulfate d ’argent , elle est le siège de l ’équilibre : Ag 2 SO 4 (s) = 2 Ag+ + Le produit ionique ou quotient de réaction Q = On introduit sans dilution des ions sulfate : KS conséquence : Le produit ionique devient : Q = > > KS Le produit ionique doit diminuer ; l ’équilibre est déplacé dans le sens inverse système hors équilibre système en équilibre Q KS

2. 6 ) Effet du p. H : solubilité des composés ioniques peu solubles à anion basique. exemple : chromate de baryum ; Ba. Cr. O 4 données : p. KS(Ba. Cr. O 4) = 10, 0 ; p. KA(HCr. O 4 -/Cr. O 42 -) = 6, 4 Question : calculer la solubilité s du chromate de baryum dans l ’eau pure : la réaction des ions chromate avec l ’eau est négligée. équilibre : (1) Ba. Cr. O 4 (s) = Ba 2+ + équil. (mol/L) - s Ks = s 2 d’où s = A. N. : s = 1, 0 10 -5 mol/L si on trace la courbe s = f(p. H) KS = s 1, 0 10 -10
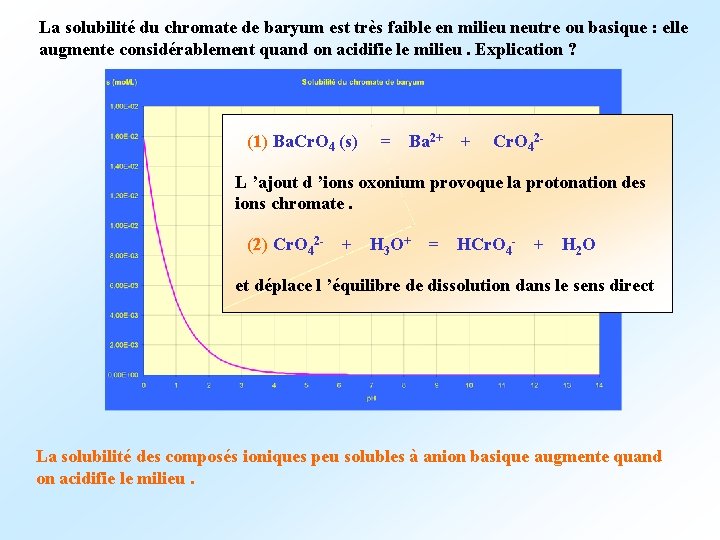
La solubilité du chromate de baryum est très faible en milieu neutre ou basique : elle augmente considérablement quand on acidifie le milieu. Explication ? (1) Ba. Cr. O 4 (s) = Ba 2+ + Cr. O 42 L ’ajout d ’ions oxonium provoque la protonation des ions chromate. (2) Cr. O 42 - + H 3 O+ = HCr. O 4 - + H 2 O et déplace l ’équilibre de dissolution dans le sens direct La solubilité des composés ioniques peu solubles à anion basique augmente quand on acidifie le milieu.

Expression de la solubilité du chromate de baryum . exp. simp données : p. KS(Ba. Cr. O 4) = 10, 0 ; p. KA(HCr. O 4 -/Cr. O 42 -) = 6, 4 Objectif : établir la solubilité s du chromate de baryum en fonction de KS , KA et [H 3 O+]. équilibres : (1) Ba. Cr. O 4 (s) = Ba 2+ + KS = (3) Cr. O 42 - + H 2 O = HCr. O 4 - + OH- K 0 = KB 0 = 1, 0 10 -10 2, 5 10 -8 Ba. Cr. O 4 peut se dissoudre suivant l ’équation (1) mais aussi suivant l ’équation (2) : (2) Ba. Cr. O 4 (s) + H 2 O = Ba 2+ + HCr. O 4 - + OH- 2, 5 10 -18

(R 1) Ba. Cr. O 4 (s) = Ba 2+ + équilibre (mol. L-1) - s 1 + s 2 s 1 (R 2) Ba. Cr. O 4 (s) + H 2 O = Ba 2+ + HCr. O 4 - + OHéquilibre (mol. L-1) - s 2 + s 1 s 2 Expression de s : ( nombre de mol de Ba. Cr. O 4 ) qui passent en solution par litre de solution. [Ba 2+] = s s = [Ba 2+] = s 1 + s 2 = = s (2) d ’où [Cr. O 42 -] = d ’où [HCr. O 4 -] = (2) (1) d ’où s 2 =
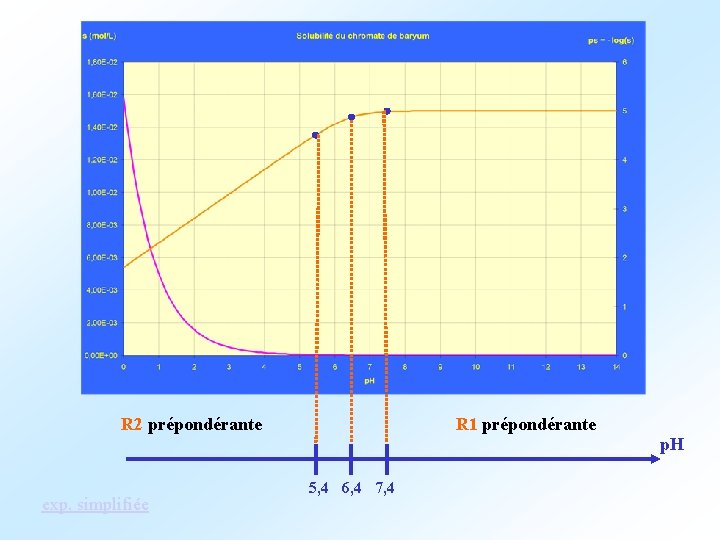
R 2 prépondérante exp. simplifiée R 1 prépondérante 5, 4 6, 4 7, 4 p. H

Expression générale de la solubilité : Question : on peut, dans des domaines de p. H à préciser, simplifier l ’expression précédente : donner ces expressions simplifiées. si p. H > 7, 4 , la réaction prépondérante est graphique constante R 2 R 1 : (R 1) Ba. Cr. O 4 (s) = Ba 2+ + équilibre (mol. L-1) d ’où Ks = - s s 2 et s = s s = 1, 0 10 -5 mol. L-1 et ps = 5, 0 si p. H < 5, 4 , la réaction prépondérante est R 2 : (R 2) Ba. Cr. O 4 (s) + H 2 O = Ba 2+ + HCr. O 4 - + OHéquilibre (mol. L-1) d ’où s 2 = - s et ps = s

2. 7 ) Précipitation des hydroxydes métalliques. De très nombreux cations métalliques donnent un précipité en présence d ’ions hydroxyde : Al 3+, Zn 2+, Ca 2+, Cu 2+, Fe 2+, . . . exemple : Mg 2+ + 2 OH- = Mg(OH)2 (s) K 0 = Question : soit C, la concentration des ions Mg 2+, déterminer le p. H pour lequel on observe l ’apparition du précipité. p. Ks = 10, 8 condition de précipitation : soit : la précipitation commence quand le produit ionique (ou quotient réactionnel Q) devient égal à KS [Mg 2+] [OH-]2 = KS C [OH-]2 = KS d ’où h 2 = soit p. H = A. N. : C = 1, 0 10 -2 mol. L-1 : p. H = 9, 6 Mg(OH)2 (s) 9, 6 domaine d ’existence du précipité p. H


Application ; calculer le p. H de précipitation de Al(OH)3 : p. KS = 32 Remarque ; quand on ajoute une solution d ’hydroxyde de sodium à une solution contenant des ions Al 3+, on observe d ’abord la formation du précipité Al(OH)3 puis la redissolution du précipité. Interprétation. Al 3+ + 3 OH- = Al(OH)3 (s) K 0 = Al(OH)3 (s) + OH- = [Al(OH)4]- 1, 0 1032 K 0 = Al(OH)3 est un hydroxyde amphotère. Al(OH)3 (s) + 3 H 3 O+ = Al 3+ + 6 H 2 O Al(OH)3 (s) + OH- = [Al(OH)4]-

Exercice ; calculer la solubilité du sulfure de manganèse dans une solution tampon p. H = 6 : p. Ks (Mn. S) = 12, 6 : H 2 S/HS- ; p. KA 1 = 7, 0 : HS-/S 2 - ; p. KA 2 = 13, 0.
- Slides: 24