Chapitre 3 Lquilibre chimique 1 Lien avec les

Chapitre 3 L’équilibre chimique 1
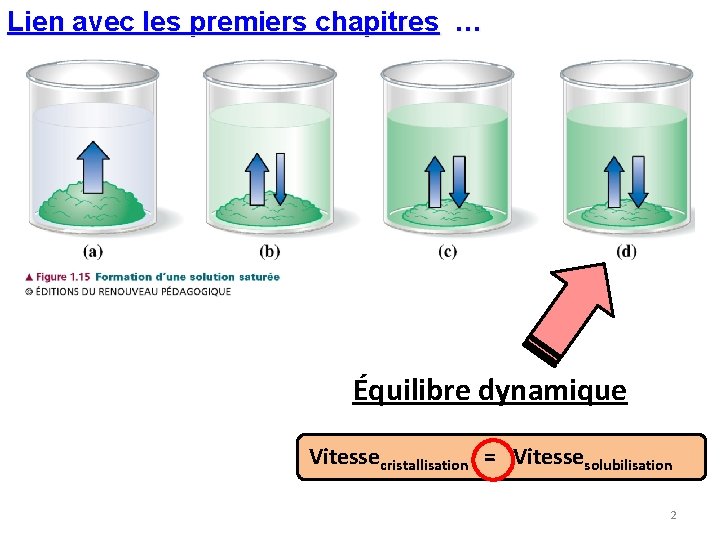
Lien avec les premiers chapitres … Équilibre dynamique Vitessecristallisation = Vitessesolubilisation 2

Sections à voir üSection 3. 1 Le caractère dynamique de l’équilibre. üSection 3. 2 L’expression de la constante d’équilibre. üSection 3. 3 Les modifications des expressions des constantes d’équilibre. üSection 3. 4 Le traitement qualitatif de l’équilibre: principe de Le. Chatelier / labo 6. üSection 3. 5 Quelques exemples de problèmes d’équilibre. 3
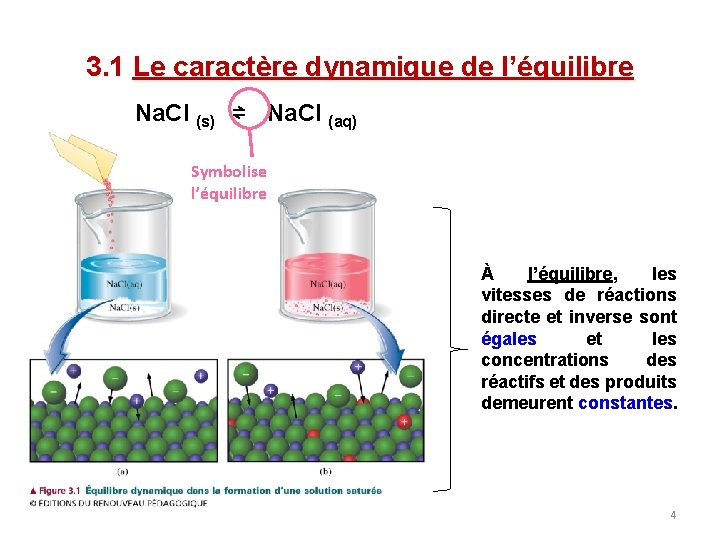
3. 1 Le caractère dynamique de l’équilibre Na. Cl (s) ⇌ Na. Cl (aq) Symbolise l’équilibre À l’équilibre, les vitesses de réactions directe et inverse sont égales et les concentrations des réactifs et des produits demeurent constantes. 4
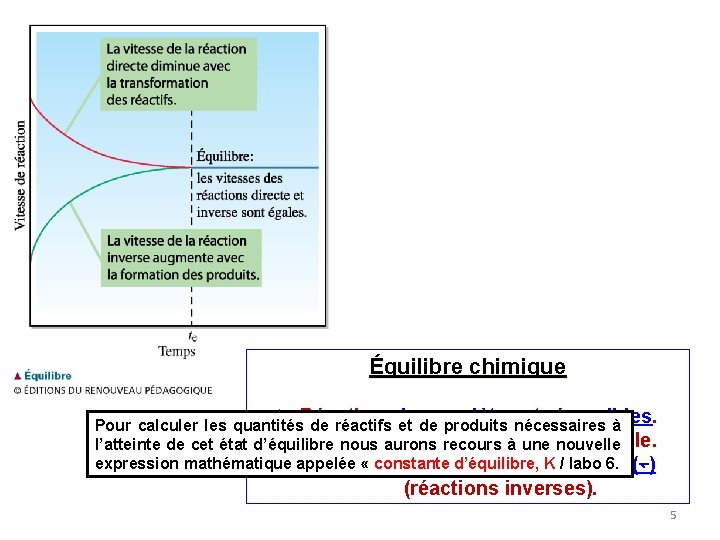
Équilibre chimique Ø Réactions incomplètes et réversibles. Pour calculer les quantités de réactifs et de produits nécessaires à Ø Atteinte état d’équilibre variable. l’atteinte de cet état d’équilibre nous d’un aurons recours à une nouvelle expression mathématique « constante d’équilibre, K / labo 6. Øappelée Réactions directes (⇀) et indirectes(↽) (réactions inverses). 5
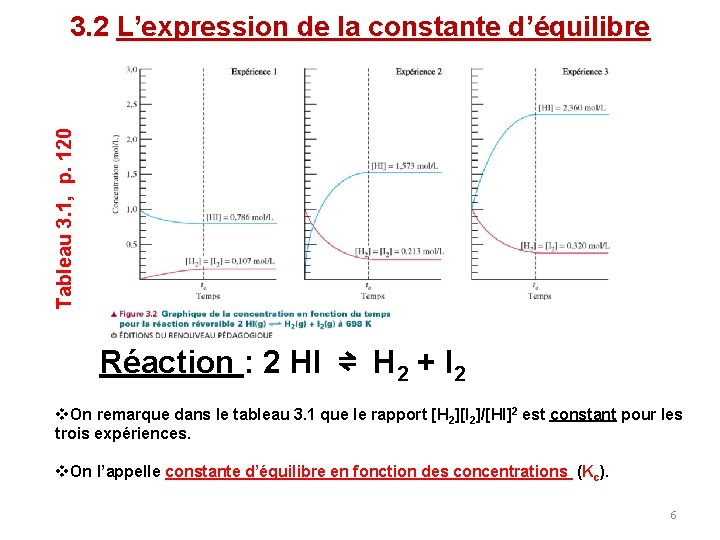
Tableau 3. 1, p. 120 3. 2 L’expression de la constante d’équilibre Réaction : 2 HI ⇌ H 2 + I 2 v. On remarque dans le tableau 3. 1 que le rapport [H 2][I 2]/[HI]2 est constant pour les trois expériences. v. On l’appelle constante d’équilibre en fonction des concentrations (Kc). 6
![Généralisation dans l’expression d’une constante d’équilibre Kc = [produits] [réactifs] à une To constante Généralisation dans l’expression d’une constante d’équilibre Kc = [produits] [réactifs] à une To constante](http://slidetodoc.com/presentation_image_h/b1e3209cb489aedd1f99edd6d90826fd/image-7.jpg)
Généralisation dans l’expression d’une constante d’équilibre Kc = [produits] [réactifs] à une To constante a. A+b. B ⇌ c. C+d. D Kc = [C]c [D]d / [A]a [B]b Concentrations molaires volumiques Valeur de Kc sans unité
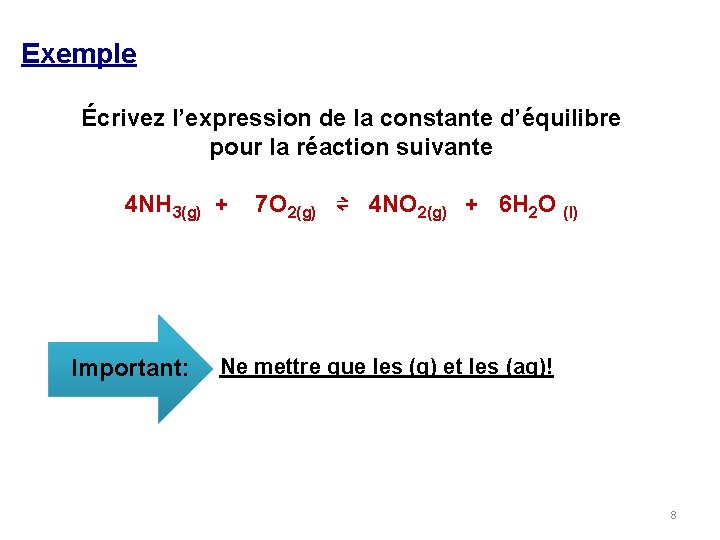
Exemple Écrivez l’expression de la constante d’équilibre pour la réaction suivante 4 NH 3(g) + Important: 7 O 2(g) ⇌ 4 NO 2(g) + 6 H 2 O (l) Ne mettre que les (g) et les (aq)! 8

3. 3 Les modifications des expressions des constantes d’équilibre Il faut parfois modifier l’expression d’une constante d’équilibre pour l’adapter: ü ü modification de l’équation chimique réaction globale équilibre des gaz équilibre des solides et des liquides purs Exemples 9

1) Modification de l’équation chimique Équilibre 1: formation de NO 2 Équilibre 2: décomposition de NO 2 2 NO(g) + O 2(g) ⇌ 2 NO(g) + O 2(g) Kform = [NO 2]2 = 4, 67 x 1013 [NO]2 [O 2] Kdécom = [NO]2 [O 2] = 2, 14 x 10 -14 [NO 2]2 Kdécom = 1 Kform 4, 67 x 1013 = 2, 14 x 10 -14 Constante d’équilibre de la réaction inverse est la réciproque de la constante d’équilibre de la réaction directe. 10

2) Réaction globale On peut combiner les équations de réactions individuelles afin d’obtenir une équation globale, en appliquant la loi de Hess. Soit l’équation suivante, dont la valeur de Kc est inconnue (à 298 K). (1) N 2 O (g) + 3/2 O 2 (g) ⇌ 2 NO 2 (g) équation globale Si on connaît les réactions élémentaires ((2) et (3) à 298 K) on peut les additionner afin d’obtenir la réaction globale (1). (2) N 2 O(g) + ½O 2 (g) ⇌ 2 NO (g) (3) 2 NO(g) + O 2 (g) ⇌ 2 NO 2 (g) Kc (2) = 1, 7 x 10 -13 Kc (3) = 4, 67 x 10 13 (1) N 2 O (g) + 3/2 O 2 (g) ⇌ 2 NO 2 (g) Kc (1) = ? Suite 11
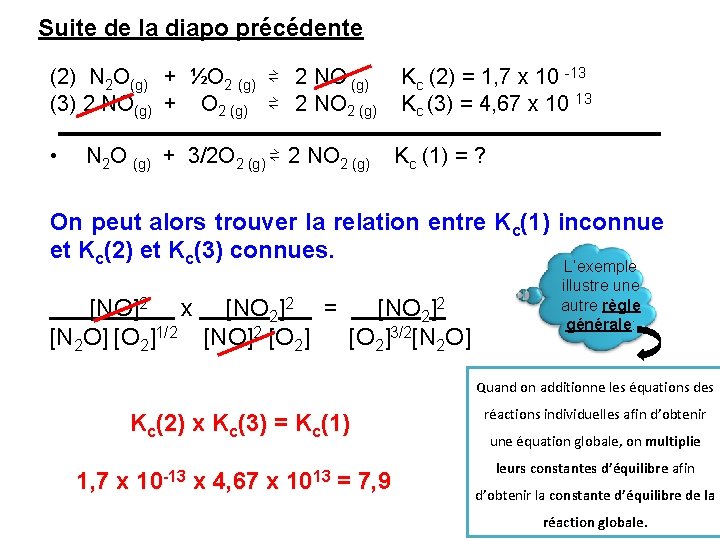
Suite de la diapo précédente (2) N 2 O(g) + ½O 2 (g) ⇌ 2 NO (g) (3) 2 NO(g) + O 2 (g) ⇌ 2 NO 2 (g) • N 2 O (g) + 3/2 O 2 (g) ⇌ 2 NO 2 (g) Kc (2) = 1, 7 x 10 -13 Kc (3) = 4, 67 x 10 13 Kc (1) = ? On peut alors trouver la relation entre Kc(1) inconnue et Kc(2) et Kc(3) connues. [NO]2 x [NO 2]2 = [NO 2]2 [N 2 O] [O 2]1/2 [NO]2 [O 2]3/2[N 2 O] L’exemple illustre une autre règle générale: Quand on additionne les équations des Kc(2) x Kc(3) = Kc(1) 1, 7 x 10 -13 x 4, 67 x 1013 = 7, 9 réactions individuelles afin d’obtenir une équation globale, on multiplie leurs constantes d’équilibre afin d’obtenir la constante d’équilibre de la réaction globale.

3) Les équilibres des gaz Dans l’étude des réactions des gaz, il est souvent plus pratique de mesurer les pressions partielles (p) plutôt que les concentrations molaires volumiques. Soit la réaction suivante en phase gazeuse a A (g) + b B (g) ⇌ c C (g) + d D (g) Kp = (PC)c (PD)d (PA)a (PB)b à une To donnée Constante d’équilibre en fonction des pressions partielles Suite 13
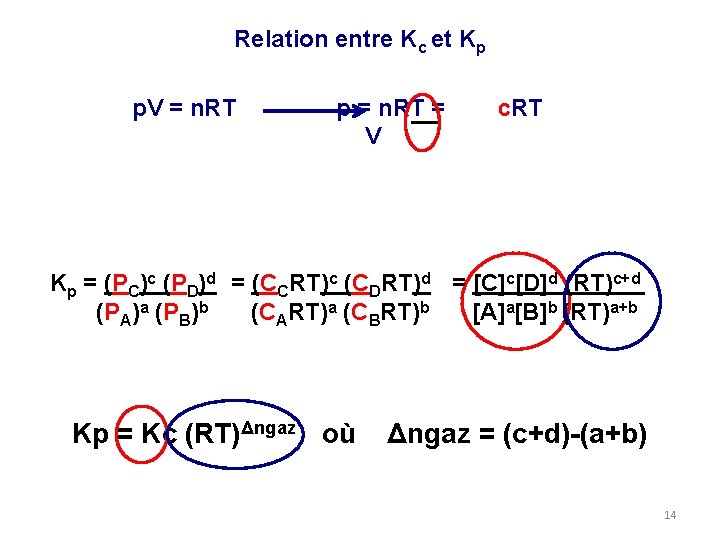
Relation entre Kc et Kp p. V = n. RT p = n. RT = V c. RT Kp = (PC)c (PD)d = (CCRT)c (CDRT)d = [C]c[D]d (RT)c+d (PA)a (PB)b (CART)a (CBRT)b [A]a[B]b (RT)a+b Kp = Kc (RT)Δngaz où Δngaz = (c+d)-(a+b) 14

Faire exemple 3. 3 p. 126! 15
4) Les équilibres des solides et des liquides purs Les concentrations des solides et des liquides purs n’apparaissent pas dans l’expression de la constante d’équilibre d’une réaction hétérogène, parce qu’elles ne varient pas au cours d’une réaction. Bien que les quantités de solides et de liquides purs varient durant une réaction, ces phases demeurent pures et leurs concentrations demeurent constantes. 16

Avant de faire des bilans: le quotient réactionnel Prédiction du sens d’une transformation nette 17

3. 4 Le principe de Le Chatelier (labo 6) Quand on impose une contrainte à un équilibre, le système réagit pour atteindre un nouvel équilibre qui minimise l’influence de la contrainte. 1) modification des espèces réagissantes 2) modification de la pression externe ou du volume 3) modification de la température 4) ajout d’un catalyseur 5) ajout d’un gaz inerte 18
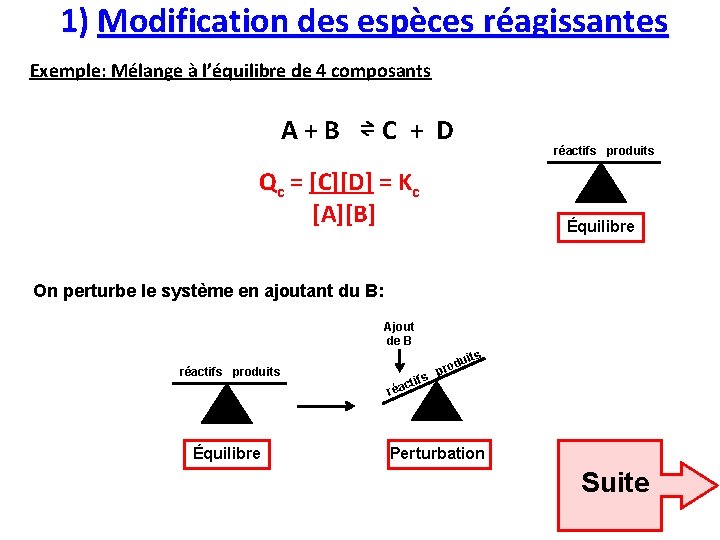
1) Modification des espèces réagissantes Exemple: Mélange à l’équilibre de 4 composants A + B ⇌ C + D Qc = [C][D] = Kc [A][B] réactifs produits Équilibre On perturbe le système en ajoutant du B: Ajout de B réactifs produits Équilibre tifs uits d o pr c réa Perturbation Suite
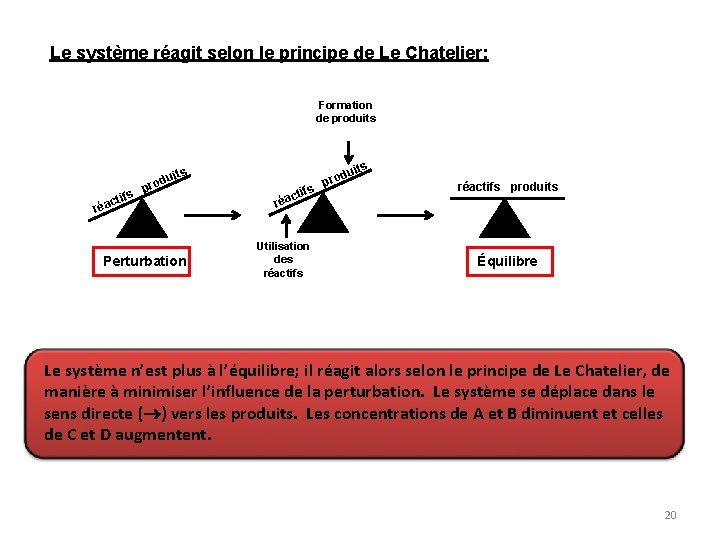
Le système réagit selon le principe de Le Chatelier: Formation de produits ifs act its odu pr ré Perturbation ifs ct réa Utilisation des réactifs uits d o pr réactifs produits Équilibre Le système n’est plus à l’équilibre; il réagit alors selon le principe de Le Chatelier, de manière à minimiser l’influence de la perturbation. Le système se déplace dans le sens directe ( ) vers les produits. Les concentrations de A et B diminuent et celles de C et D augmentent. 20
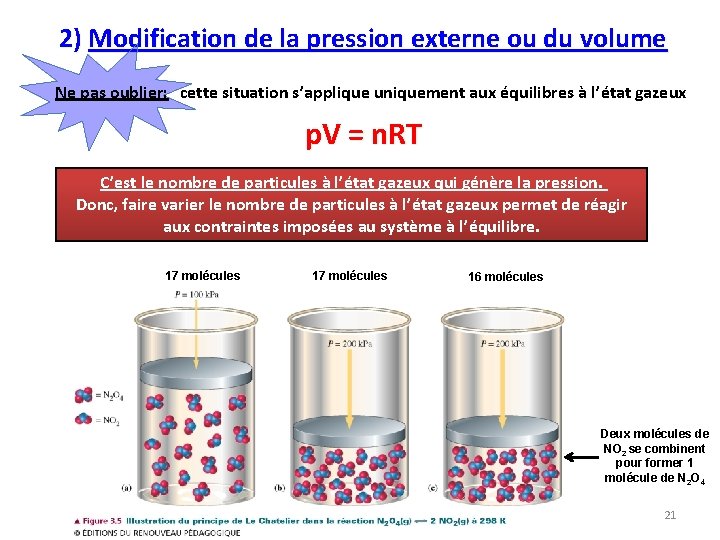
2) Modification de la pression externe ou du volume Ne pas oublier: cette situation s’applique uniquement aux équilibres à l’état gazeux p. V = n. RT C’est le nombre de particules à l’état gazeux qui génère la pression. Donc, faire varier le nombre de particules à l’état gazeux permet de réagir aux contraintes imposées au système à l’équilibre. 17 molécules 16 molécules Deux molécules de NO 2 se combinent pour former 1 molécule de N 2 O 4 21
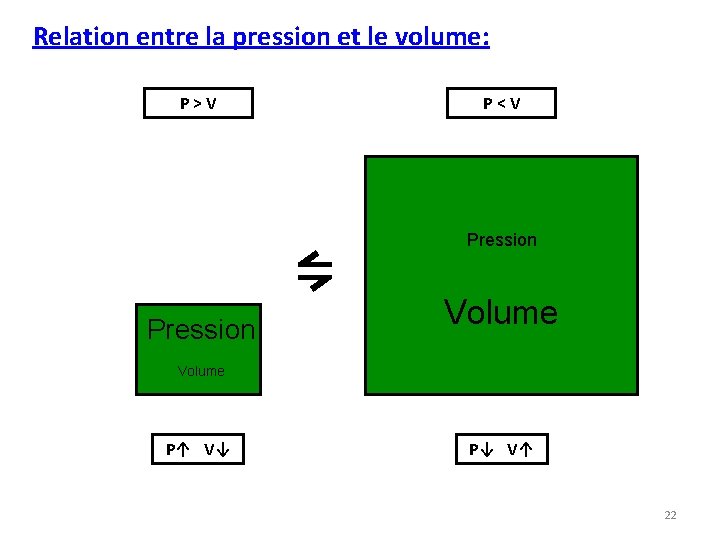
Relation entre la pression et le volume: P > V P < V ⇋ Pression Volume P↑ V↓ P↓ V↑ 22

⇌ N 2 O 4(g) 2 NO 2 (g) 2 NO 2(g) (brun) 1 N 2 O 4(g) (incolore) De manière générale ü Si P ou V : il faut prendre le moins d’espace possible. On va alors du côté de l’équilibre qui génère le moins de molécules à l’état gazeux ( )…plus pâle! ü Si P ou V : il faut prendre le plus d’espace possible. On va alors du côté de l’équilibre qui génère le plus grand nombre de molécules à l’état gazeux ( )…plus foncé! 23

3 ) Modification de la température Système à l’équilibre Endothermique ⇌ Exothermique À chaque système à l’équilibre correspond un ∆H (variation d’enthalpie) Ø Si ∆H valeur positive : réaction endothermique valeur négative : réaction exothermique Pour voir de quelle manière une modification de la température affecte le système à l’équilibre, il faut considérer la variation de température comme un constituant de l’équilibre. Ø Si ∆H R P valeur positive : considéré comme un réactif valeur négative : considéré comme un produit Exemples

Pour résoudre un problème faisant intervenir une variation de température, il faut: 1) Placer la quantité d’énergie dans l’équilibre 2) Utiliser la même démarche que lors de modifications des quantités Exemples: Pour un équilibre du type endothermique A + B ⇌ C + D où ∆ H = positif (endothermique) 1) A + B + chaleur ⇌ C + D R P Pour un équilibre du type exothermique 1) A + B ⇌ C + D où ∆ H = négatif (exothermique) R P 2) A + B ⇌ C + D + chaleur 25

⇌ N 2 O 4(g) 2 NO 2 (g) 2 NO 2(g) (brun) N 2 O 4(g) (incolore) 2 NO 2 (g) ⇌ N 2 O 4(g) + Chaleur ∆H: -57 k. J/mol
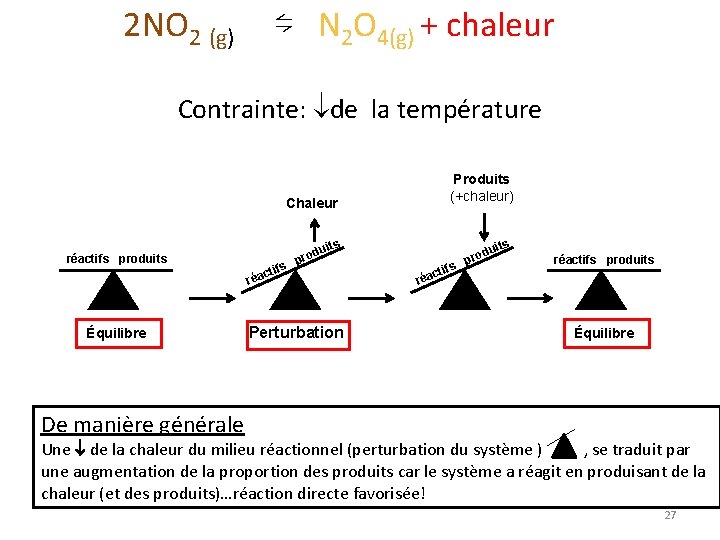
2 NO 2 (g) ⇋ N 2 O 4(g) + chaleur Contrainte: de la température Produits (+chaleur) Chaleur réactifs produits ifs act ts dui o r p ré Équilibre Perturbation uits ré ifs act d pro réactifs produits Équilibre De manière générale Une de la chaleur du milieu réactionnel (perturbation du système ) , se traduit par une augmentation de la proportion des produits car le système a réagit en produisant de la chaleur (et des produits)…réaction directe favorisée! 27

4) Ajout d’un catalyseur Augmente la vitesse de la réaction directe, mais aussi celle de la réaction inverse donc les concentrations demeurent inchangées. 28

5) Ajout d’un gaz inerte Pour simplifier, considérons que cette perturbation n’influence pas un système d’équilibre. 29

Exercice La réaction suivante est une réaction utilisée pour la production commerciale de l’hydrogène. Comment se comportera ce système fermé à l’équilibre dans chacune des cinq condition suivantes? CO(g) + H 2 O(g) ⇌ CO 2 (g) + H 2 (g) • On élimine du gaz carbonique Réaction directe est favorisée/déplacement de l’équilibre vers la droite. • On ajoute de la vapeur d’eau Réaction directe est favorisée/déplacement de l’équilibre vers la droite. c) On augmente la pression par l’addition d’hélium Aucune influence. d) On augmente la température (la réaction est exothermique) Réaction inverse favorisée/déplacement de l’équilibre vers la gauche (plus de réactifs). e) On augmente la pression en diminuant le volume Aucune influence.

3. 5 Quelques exemples de problèmes d’équilibre Deux types de problèmes d’équilibre fondamentaux 1) Trouver K à partir de données expérimentales 2) Trouver des quantités à l’équilibre à partir de K Bilan réactionnel

1) Détermination des valeurs des constantes d’équilibre à partir de données expérimentales (exemple 3. 11, p. 141)

2) Calcul des quantités à l’équilibre à partir des valeurs de Kc et de Kp (exemples 3. 12, 3. 13, 3. 14 et 3. 15)
- Slides: 33