CHAPITRE 2 Objectif 6 OCTOBRE 2011 1 Molcule

CHAPITRE 2 Objectif 6 OCTOBRE 2011

1 - Molécule : Substance qui est formé de deux atomes ou plus Retour à la table des matières Q u i t t e r . : : Amer Hanna: : . . : : Samer Fawaz: :

2 - Lorsqu’un atome gagne ou perd des électrons il devient un ion Retour à la table des matières Q u i t t e r . : : Amer Hanna: : . . : : Samer Fawaz: :


- Tous les éléments qui sont dans la famille: Famille 1 perd 1 électron Famille 2 perd 2électrons Famille 3 perd 3électrons
Tous les éléments qui sont dans la famille: Famille 5 gagne 3 électrons Famille 6 gagne 2électrons Famille 7 gagne 1électron

Ion positif Lorsqu’un atome perd des électrons , il devient un ion positif. Sa charge est égale au nombre d’électrons perdus. Exemple: B+3

Ion négatif Lorsqu’un atome gagne des électrons , il devient un ion négatif. Sa charge est égale au nombre d’électrons gagnés. Exemple: O-2

C ’est un type de liaison qui se forme entre un élément donneur d’électrons (métal) et un élément receveur d’électrons (non-métal) Exemple Métal avec Non-métal
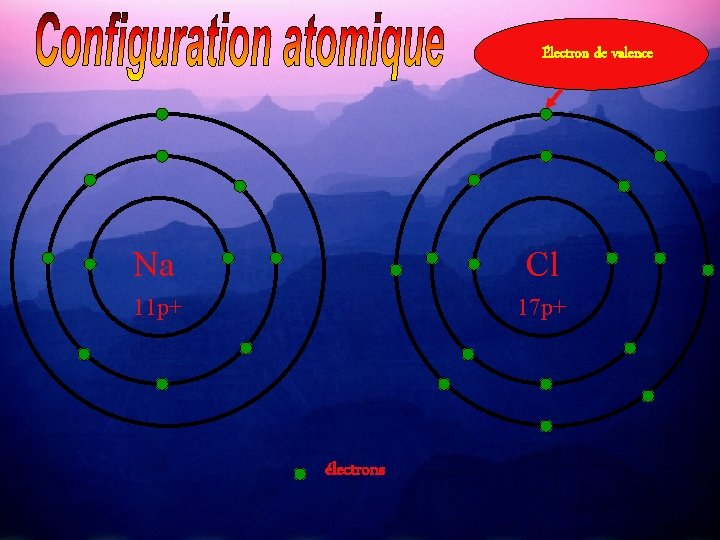
Électron de valence Na Cl 11 p+ 17 p+ électrons
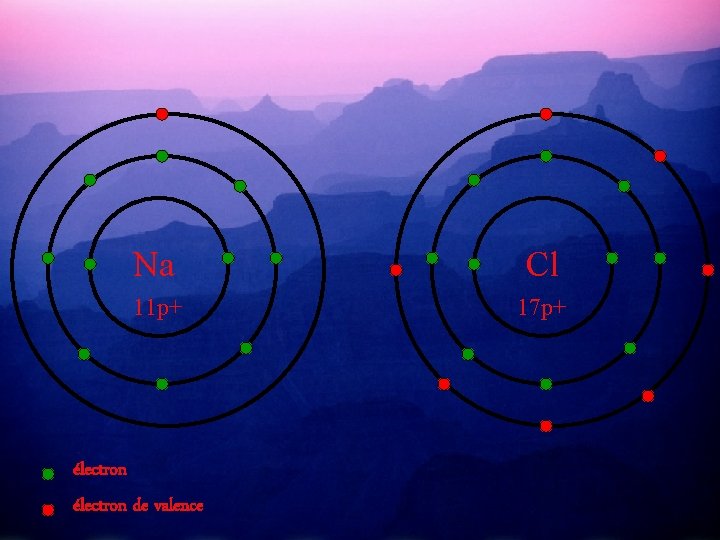
Na Cl 11 p+ 17 p+ électron de valence
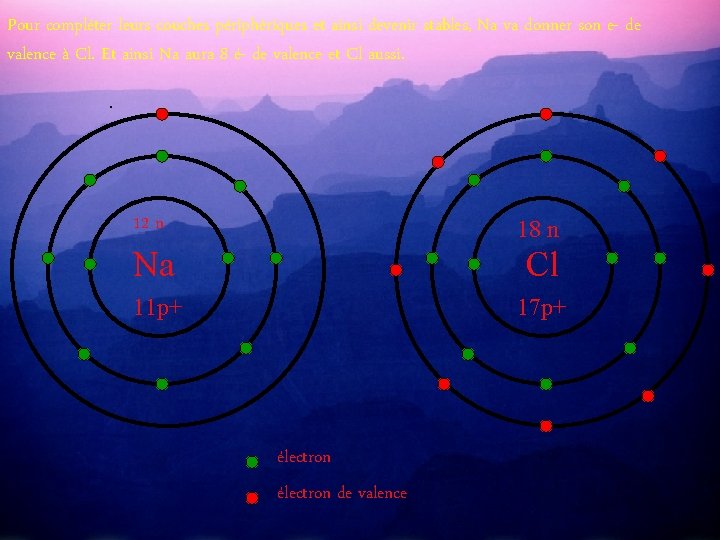
Pour compléter leurs couches périphériques et ainsi devenir stables, Na va donner son e- de valence à Cl. Et ainsi Na aura 8 é- de valence et Cl aussi. . 12 n 18 n Na Cl 11 p+ 17 p+ électron de valence
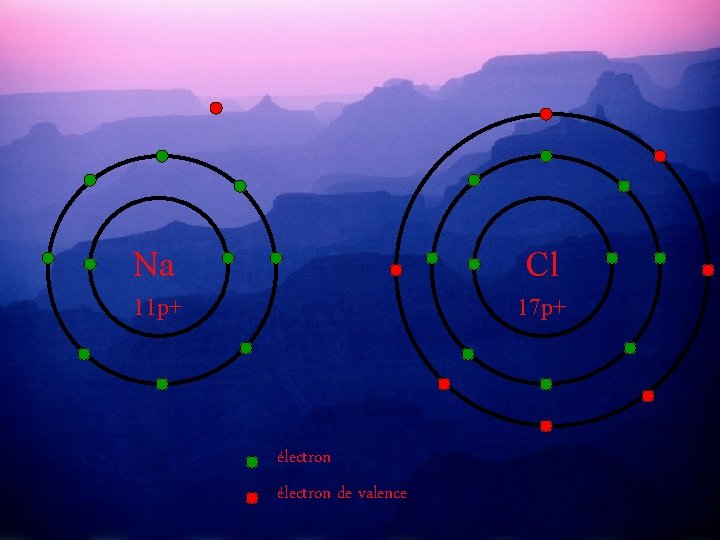
Na Cl 11 p+ 17 p+ électron de valence
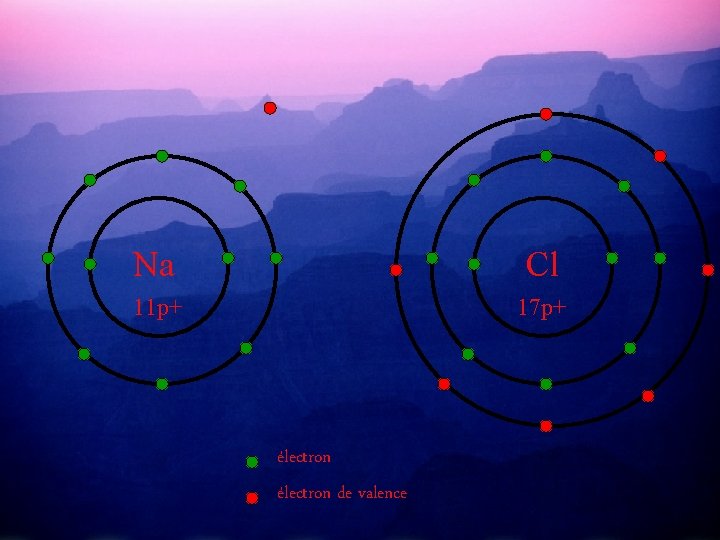
Na Cl 11 p+ 17 p+ électron de valence
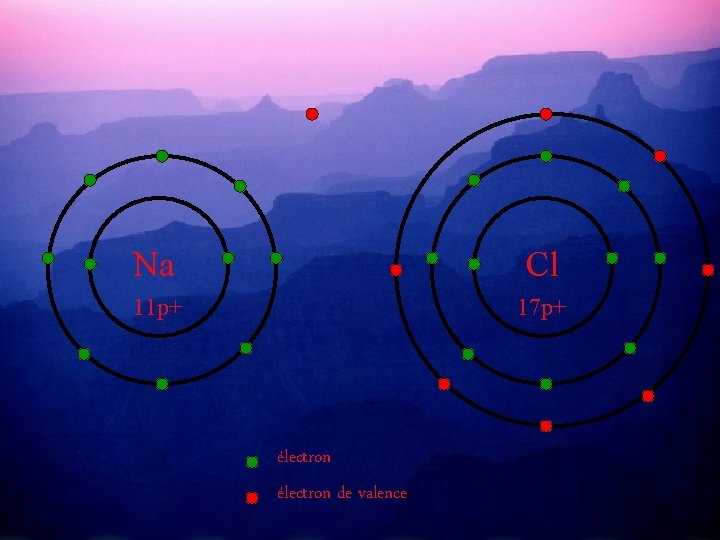
Na Cl 11 p+ 17 p+ électron de valence
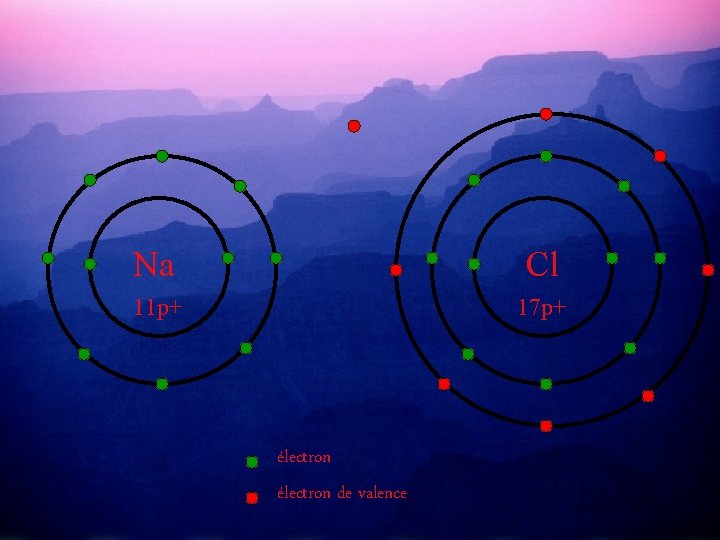
Na Cl 11 p+ 17 p+ électron de valence
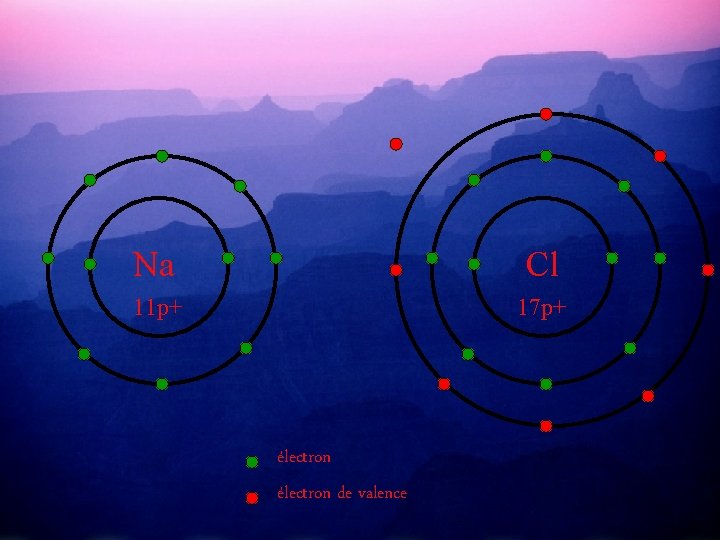
Na Cl 11 p+ 17 p+ électron de valence
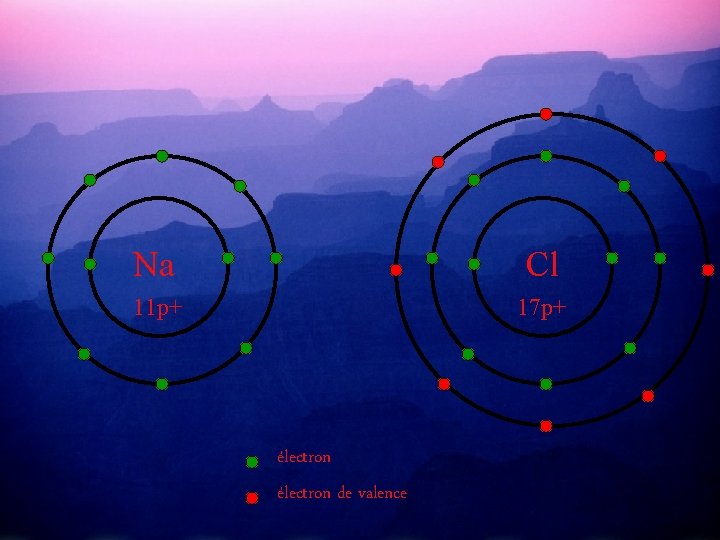
Na Cl 11 p+ 17 p+ électron de valence
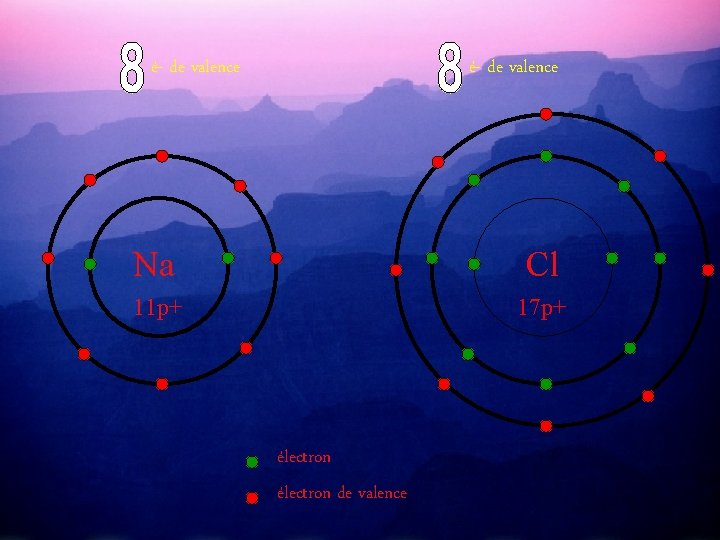
é- de valence Na Cl 11 p+ 17 p+ électron de valence


Selon la règle de l’octet, les éléments cherchent à gagner ou perdre un é- de valence pour obtenir la configuration électronique du gaz inerte(8 électrons de valence) et deviennent stable.

La règle de l ’octet ne s’applique pas toujours. Il y a, en effet, deux exceptions: L’hydrogène L’hélium


A) Les Solutions: Les solutions sont des mélanges homogènes formés d’un soluté et d’un solvant. 1) Le solvant est la substance qui reçoit le soluté Remarque Lorsque le solvant est de l’eau, nous sommes en présence d’une solution aqueuse

2) Le soluté est la substance qui est dissoute dans le solvant. Mettre le soluté dans le solvant s’appelle la solubilité Le soluté peut être solide (sucre dans l’eau), liquide (alcool dans le vin) ou gazeux (dioxygène dans l’eau de l’aquarium).

B) 1 - La Concentration: C= m V m: masse du soluté(en g) V: Volume de la solution(en L) C: la concentration (en g/L)
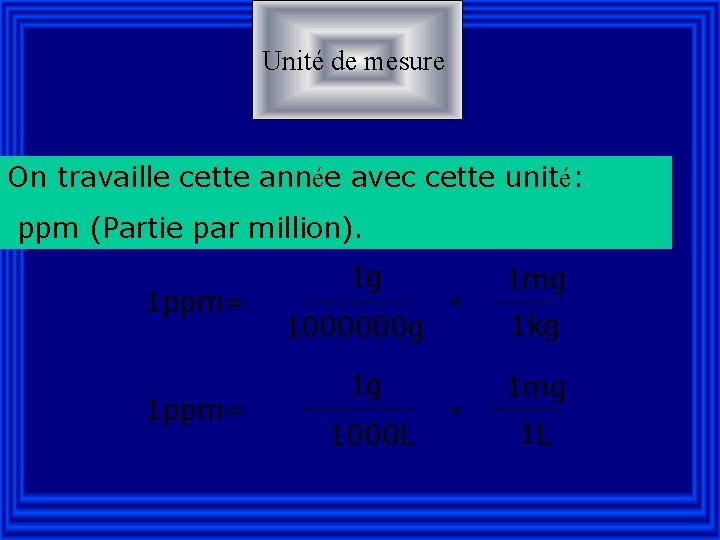
Unité de mesure On travaille cette année avec cette unité: ppm (Partie par million). 1 ppm= 1 g 1000000 g 1 g 1000 L = = 1 mg 1 kg 1 mg 1 L

C) Dilution Diluer = ajouter de l’eau à la solution initiale

En résumé: L’équation à utiliser lors d’une Dilution: C au début x. V au début =C OU ENCORE C 1 V 1 = C 2 V 2 à la fin x. V à la fin

ÉLECTROLYTES Définition: Un électrolyte est une substance qui, dissoute dans l’eau, conduit du courant. ÆCette solution est appelée Solution électrolytique

Dissociation électrolytique C’est la séparation de la substance dissoute en deux ions de signes opposées. Ex : Dissociation Électrolytique Non électrolytique
TYPES D’ÉLECTROLYTES Électrolyte Acide, base ou sel

IDENTIFICATION DES COMPOSÉS ÆAcide Définition: Substance qui libère des ions H+ en solution aqueuse. CARACTÉRISTIQUES ü ü Solution aqueuse dont le p. H est inférieur à 7. A un goût aigre. Conduit l'électricité Réagit avec des métaux en libérant du dihydrogène. ü Fait rougir le papier de tournesol bleu. ü Neutralise les bases.
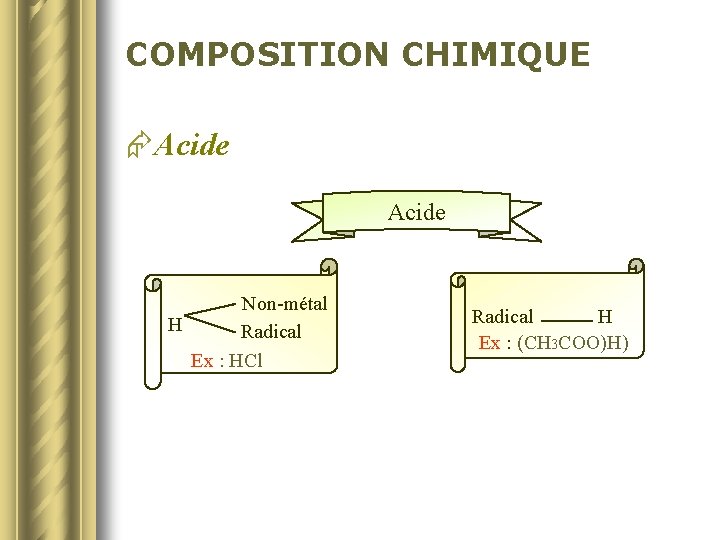
COMPOSITION CHIMIQUE ÆAcide Non-métal H Radical Ex : HCl Radical H Ex : (CH 3 COO)H)

IDENTIFICATION DES COMPOSÉS ÆBase: substance qui libère des ion 0 H- en solution aqueuse. ÆCARACTÉRISTIQUES ü ü ü Solution aqueuse dont le p. H est supérieur à 7. A un goût amer. Visqueuse au toucher. Fait bleuir le papier de tournesol rouge. Neutralise les acides.
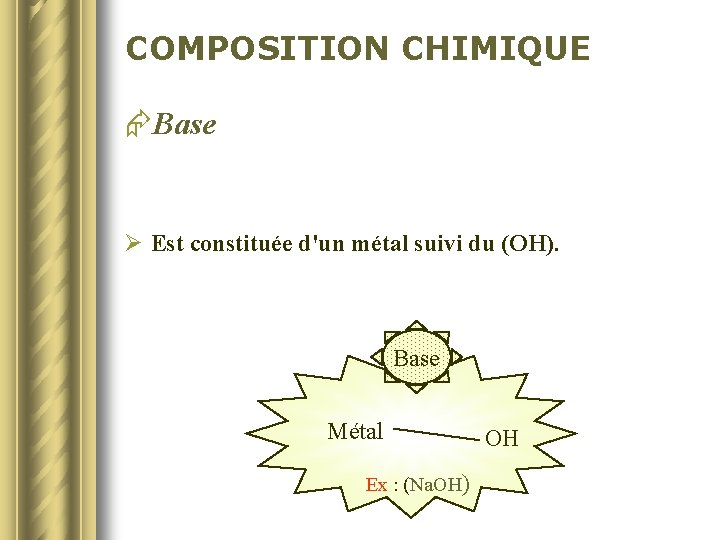
COMPOSITION CHIMIQUE ÆBase Ø Est constituée d'un métal suivi du (OH). Base Métal Ex : (Na. OH) OH

IDENTIFICATION DES COMPOSÉS Æ Sel Substance provenant de la liaison entre un métal et un non-métal. CARACTÉRISTIQUES ü ü Est un solide cristallin. A un goût salé. Conduit l'électricité lorsqu'il est en solution aqueuse. N'a aucun effet sur le papier de tournesol. Composition chimique : D'un métal suivi d'un non-métal.
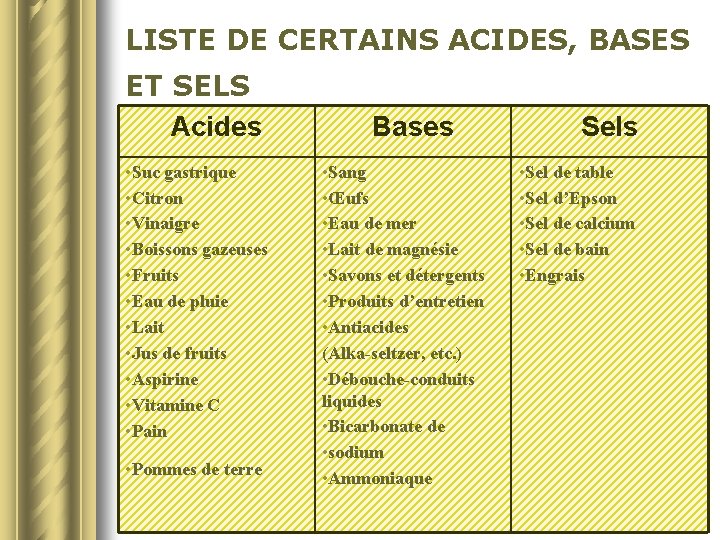
LISTE DE CERTAINS ACIDES, BASES ET SELS Acides • Suc gastrique • Citron • Vinaigre • Boissons gazeuses • Fruits • Eau de pluie • Lait • Jus de fruits • Aspirine • Vitamine C • Pain • Pommes de terre Bases • Sang • Œufs • Eau de mer • Lait de magnésie • Savons et détergents • Produits d’entretien • Antiacides (Alka-seltzer, etc. ) • Débouche-conduits liquides • Bicarbonate de • sodium • Ammoniaque Sels • Sel de table • Sel d’Epson • Sel de calcium • Sel de bain • Engrais
- Slides: 38