Chapitre 11 Sucres et polysaccharides 1 Les monosaccharides


















- Slides: 42

Chapitre 11 Sucres et polysaccharides 1. Les monosaccharides A. Classification B. Configurations et conformations C. Dérivés de sucres

2. Les polysaccharides A. Les disaccharides B. Polysaccharides de structure: la cellulose et la chitine C. Polysaccharides de réserve: l'amidon et le glycogène D. Glycosaminoglycanes 3. Les glycoprotéines A. Protéoglycanes


Glucides - Classe prépondérante (en masse) des molécules organiques - Molécules partiellement réduites, souvent solubles dans l’eau, et remplissant de multiples fonctions - Réservoir d’énergie (glucose, glycogène, amidon, saccharose) Rôle structurel (chitine, cellulose) Point de départ pour la synthèse d’autres constituants Intervenant dans la structure de ADN et ARN Garnissant certaines protéines ou lipides

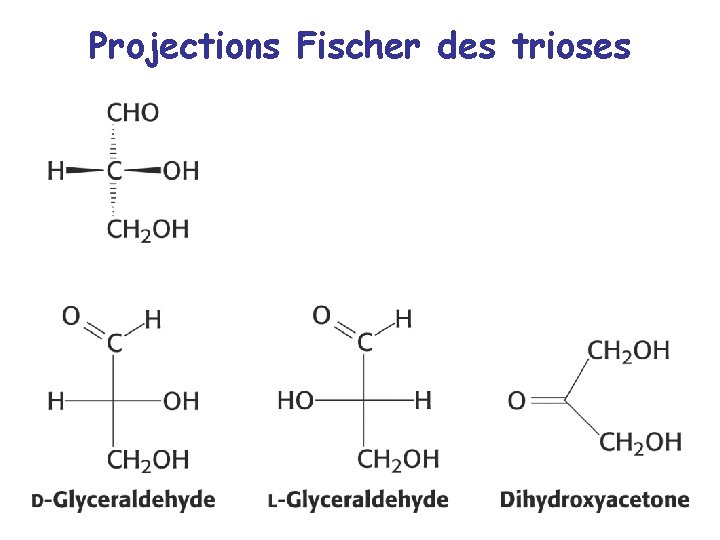
Monosaccharides - Aldose et cétose - Projection de Fischer - stéréoisomères, énantiomères, diastéréisomères, épimères - triose, tétrose, pentose, hexose, heptose - aldoses et cétoses physiologiquement importants - hémiacétal, pyranose, furanose, configurations anomériques - conformations


Projections Fischer des trioses

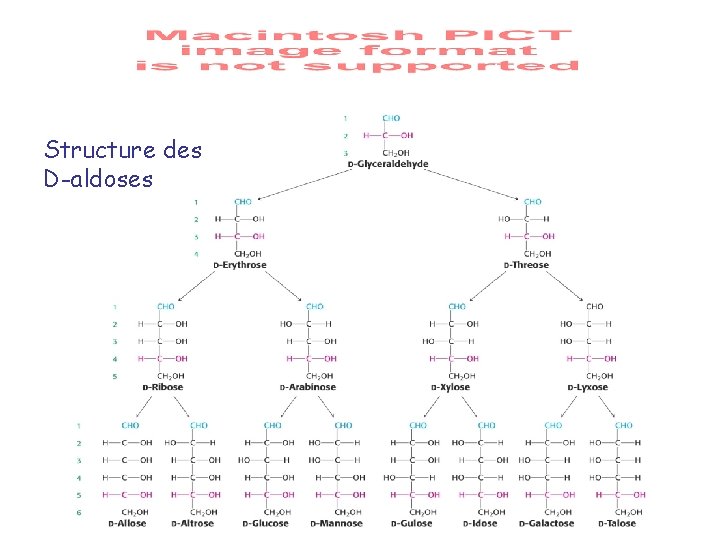
Structure des D-aldoses

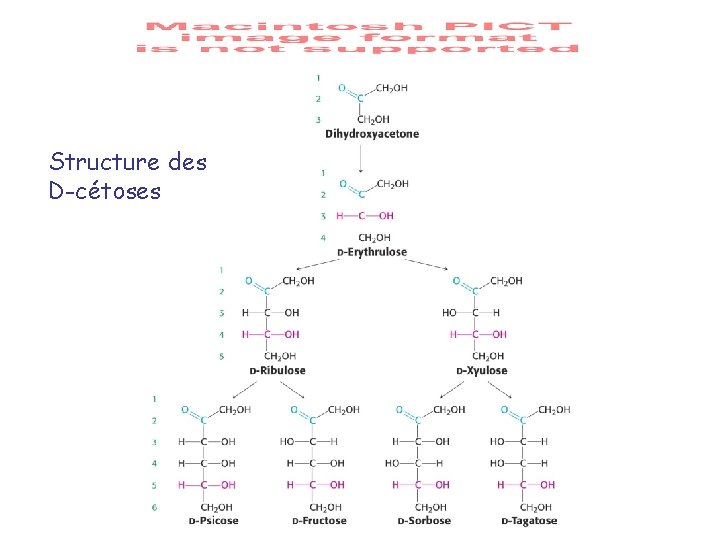
Structure des D-cétoses

Stéréoisomères : isomères différant par la disposition dans l’espace des substituants (configuration) autour d’au moins un carbone chiral Enantiomères : stéréoisomères qui sont des images en miroir l’un de l’autre exemple : D-glucose et L-glucose Diastéréoisomères : stéréoisomères non-énantiomériques exemple : D-glucose et L-galactose Epimères : stéréoisomères différant l’un de l’autre au niveau d’un seul carbone chiral exemple : D-glucose et D-galactose, D-glucose et D-mannose Anomères : stéréoisomères différant par la configuration du carbone anomérique

Aldoses et cétoses les plus importants Aldose Cétose Triose D-glycéraldéhyde* Dihydroxyacétone* Tétrose Erythrose* Pentose Ribose* Ribulose* Xylulose* Hexose Glucose Mannose Galactose Fructose *Formes phosphorylées sont importantes

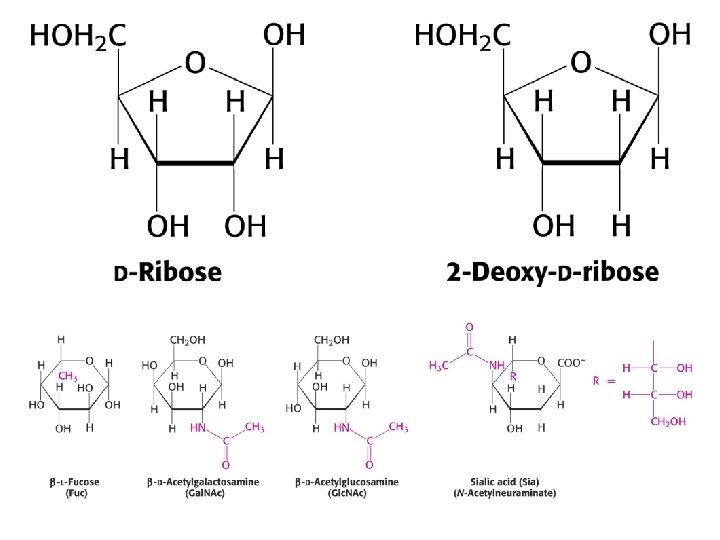
Aldoses et cétoses les plus importants D-ribose : tous les OH du côté droit D-ribulose : cétose correspondant au ribose D-xylulose : épimère en C 3 du D-ribulose D-mannose : épimère en C 2 du glucose D-galactose : épimère en C 4 du glucose D-fructose : cétose correspondant au glucose (et au mannose)

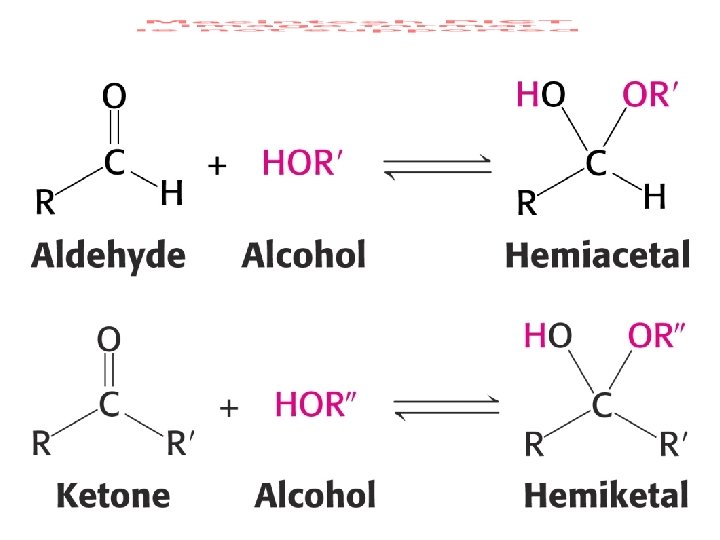
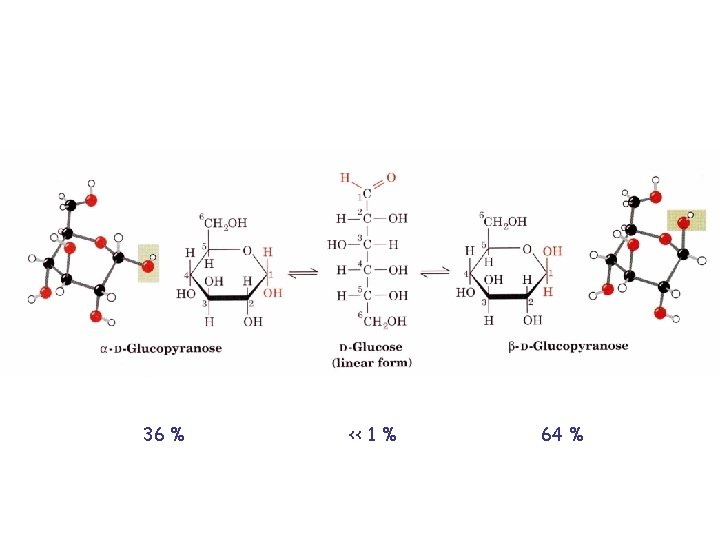
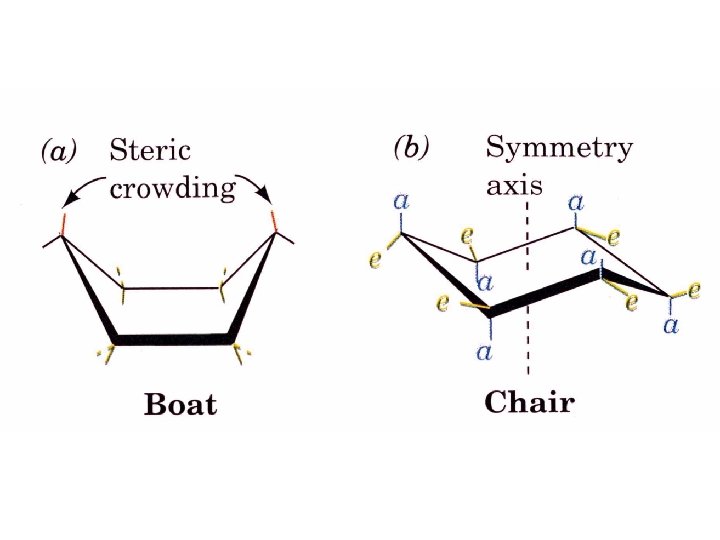
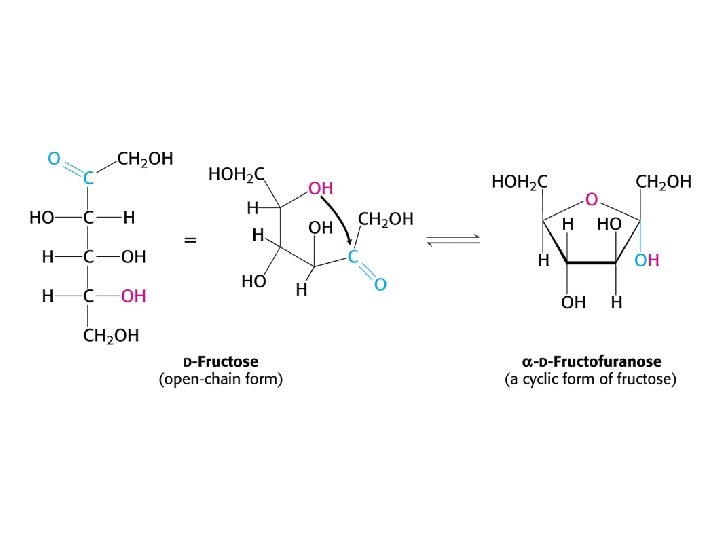
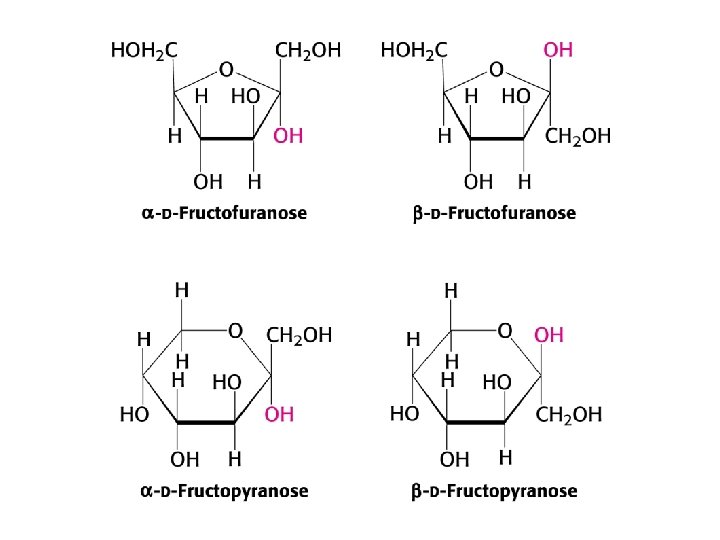
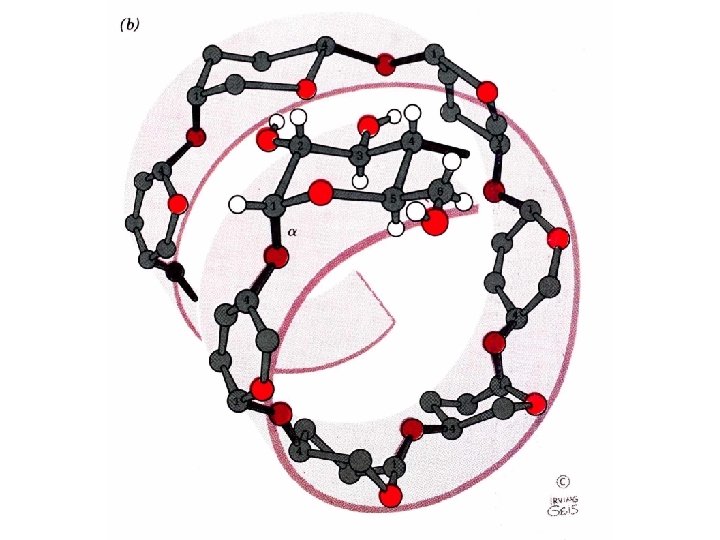
Hémiacétalisation et ses conséquences - Possibilité de former hémiacétal (aldose) ou hémicétal (cétose) - Cycle à 6 atomes (pyranose) ou à 5 atomes (furanose) - Création d’un carbone asymétrique supplémentaire : carbone anomérique - Deux configurations anomériques supplémentaires Alpha = OH en-dessous du cycle (pour sucre série D) Bêta = OH au-dessus du cycle (pour sucre série D) Interconversion spontanée ± lente - Projection de Haworth - Conformations - chaise (substituants axial et équatorial) et bateau (pyranose) - enveloppe et tordue (furanose)




Anomérisation Conversion d’un anomère en un autre anomère (jusqu’à atteindre équilibre thermodynamique) Passe par la forme ouverte S’accompagne d’un changement du pouvoir rotatoire (aussi appelée “mutarotation”) Impossible si liaison osidique (acétalique)


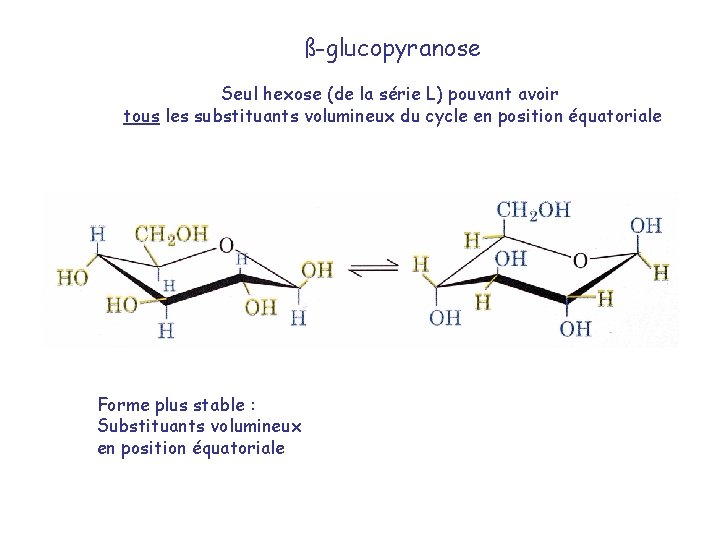
ß-glucopyranose Seul hexose (de la série L) pouvant avoir tous les substituants volumineux du cycle en position équatoriale Forme plus stable : Substituants volumineux en position équatoriale



Dérivés de monosaccharides 1. Esters phosphoriques : le plus souvent carbone extrême glucose-6 -phosphate, fructose-6 -phosphate 1. 2. Acides aldoniques : carbone 1 oxydé gluconate, mannonate (acide gluconique, acide mannonique) 3. Acides uroniques : dernier carbone oxydé glucuronate, L-iduronate (acide glucuronique, …) 4. Sucres aminés glucosamine (2 -amino-2 -désoxyglucose) dérivé : N-acétyl-glucosamine 5. Sucres désoxy 2 -désoxyribose 6. Polyols : glycérol, ribitol (ribose réduit), sorbitol (glucose réduit), inositol (polyol cyclique)


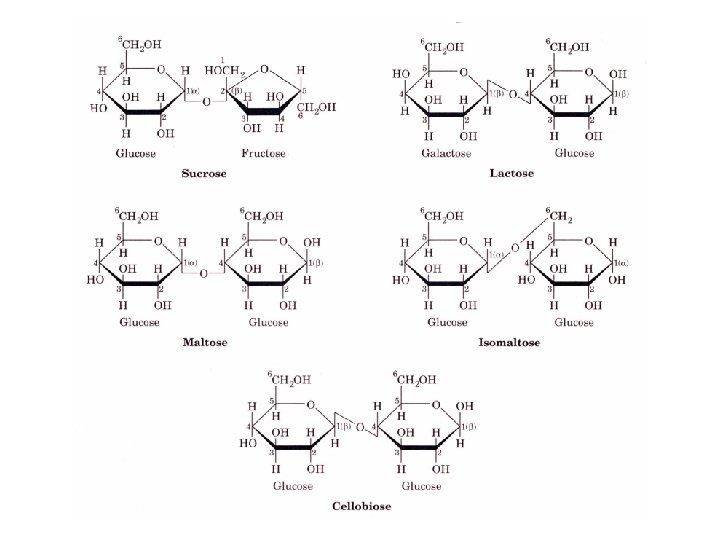
Quelques disaccharides Maltose : deux glucoses unis par liaison alpha 1, 4 (produit de dégradation de l’amidon) Lactose : galactose uni à glucose par liaison alpha 1, 4 (sucre du lait) Isomaltose : deux glucoses unis par liaison alpha 1, 6 (produit de dégradation de l’amylopectine et du glycogène) Cellobiose : deux glucoses unis par liaison ß 1, 4 (produit de dégradation de la cellulose) Saccharose : glucose uni au fructose par les carbones anomériques (alpha-1 ß-2); (sucre transporté dans la sève des plantes et stocké dans la betterave et la canne à sucre) NB : A l’exception du saccharose, tous ces disaccharides ont une extrémité réductrice.


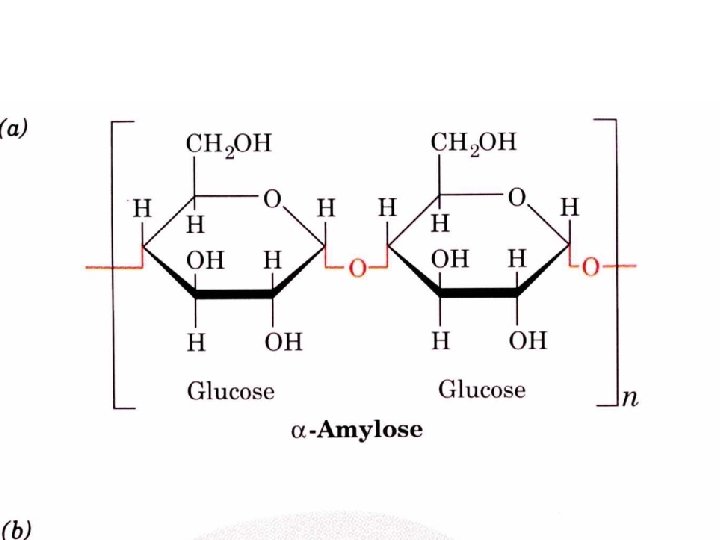
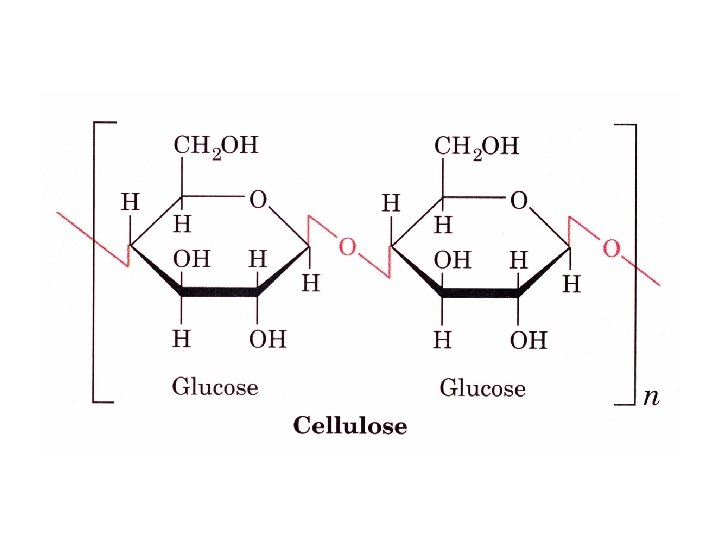
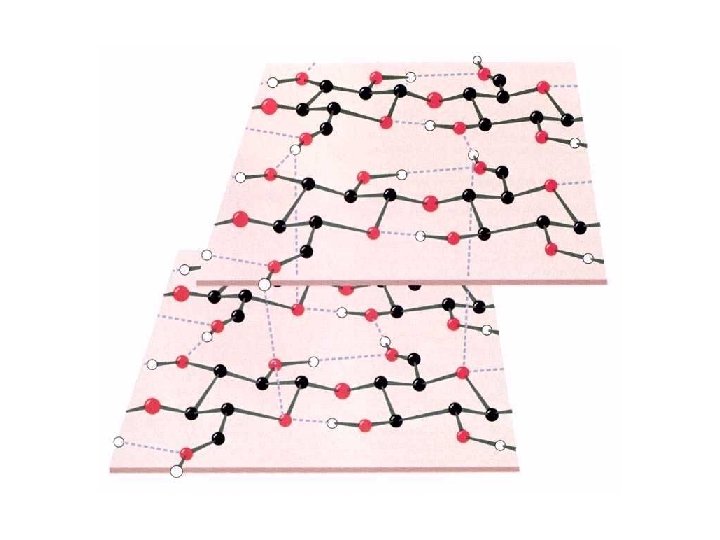
Polysaccharides Longs polymères de résidus monosaccharidiques Homopolysaccharides : un seul type de monosaccharides Hétéropolysaccharides : au moins deux types de résidus mono saccharidiques Polysaccharides de structure (cellulose, chitine) - insoluble - extracellulaire Polysaccharides de réserve (glycogène, amidon) - généralement soluble - intracellulaire Polysaccharides linéaires (amylose, cellulose) ou ramifiés (glycogène, amylopectine) Extrémités « réductrice » et non-réductrice

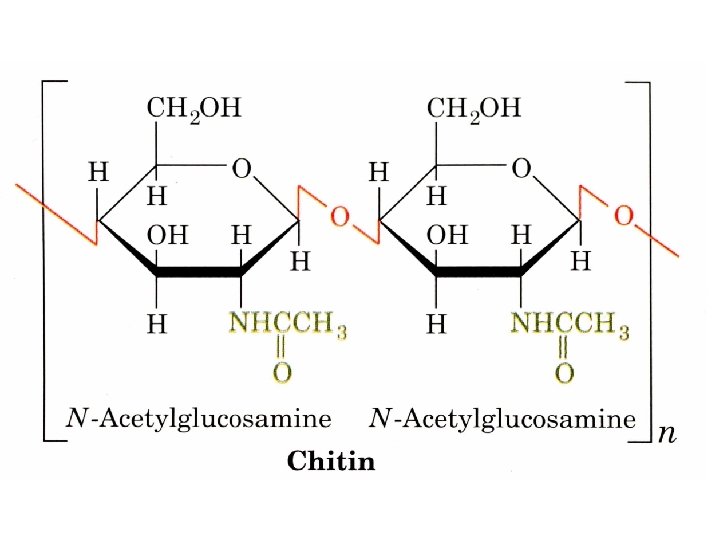
Homopolysaccharides Amylose (amidon) Réserve Amylopectine (amidon) Réserve Glycogène Cellulose Chitine Réserve Structure Bois, coton Structure Exosquelette Glucose N-acetylglucosamine Linéaire Alpha 1 -4 Branché Alpha 1, 4 Alpha 1, 6 (24 -30) Branché Alpha 1, 4 Alpha 1, 6 (812) Linéaire Bêta 1, 4 ≈1000 à 500 000 résidus Jusqu’à 106 résidus Plusieurs millions Jusqu’à 15 000 ? Très grand







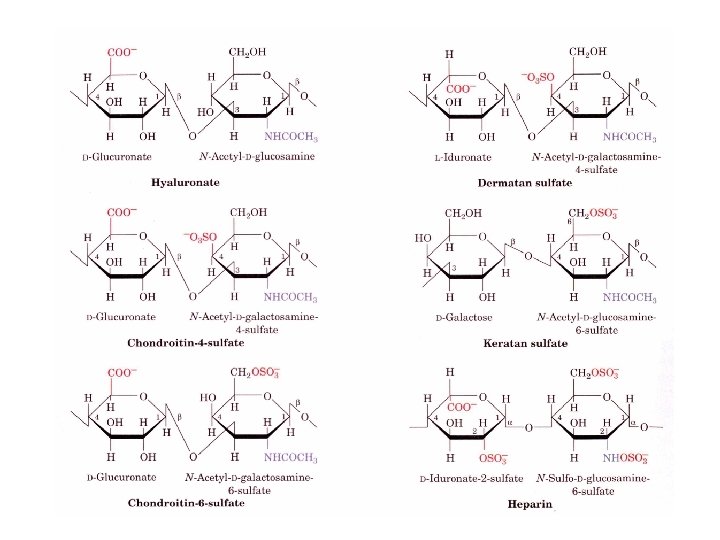
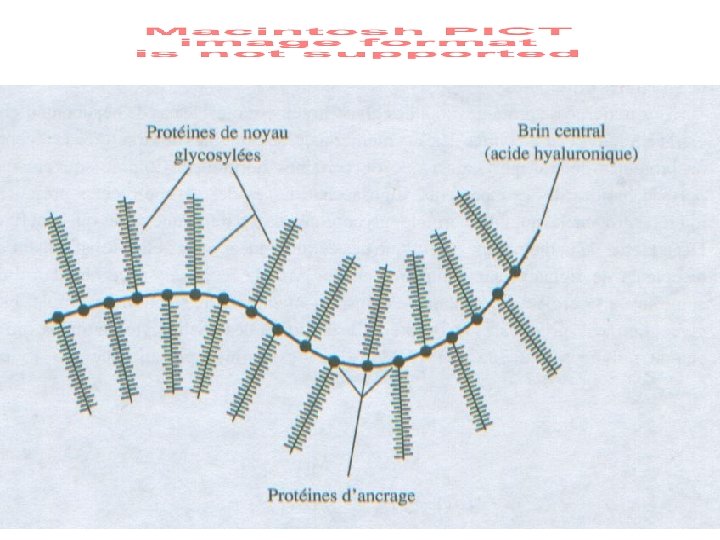
Hétéropolysaccharides Glycosaminoglycans = mucopolysaccharides (substance fondamentale) Polysaccharides linéaires anioniques (gpts carboxyliques ou sulfates) constitués de la répétition d’une unité disaccharidique Acide hyaluronique : Acide glucuronique (Glc. A) et N-acétylglucosamine (NAG) ß-Glc. A-(1 -3)-ß-NAG-(1 -4)- ß-Glc. A etc… Chondroïtine sulfate Dermatan sulfate Keratan sulfate Héparine


Glycoprotéines - Très grande variabilité de structure; - sucres impliqués : -Galactose, glucose, mannose, -N-acétylglucosamine, N-acétylgalactosamine, -N-acétylneuraminate (chargé), appelé aussi “acide sialique” -L-fucose, -xylose. -Concerne le plus souvent des protéines sécrétées, ou du réticulum endoplasmique, du Golgi, des lysosomes

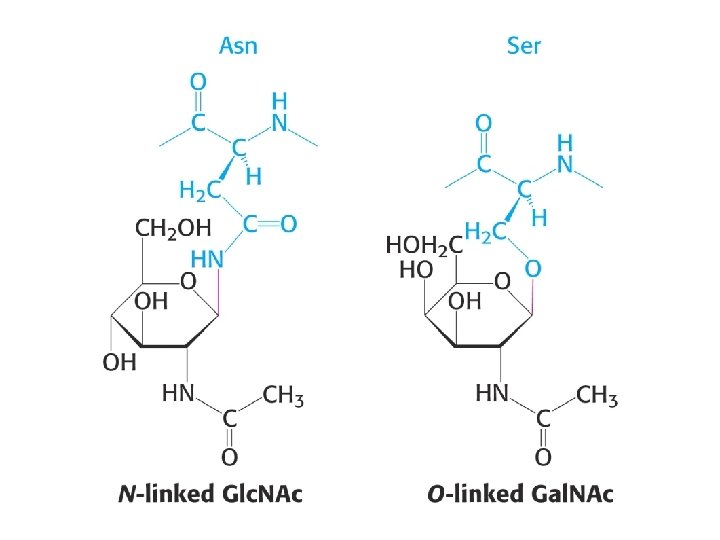
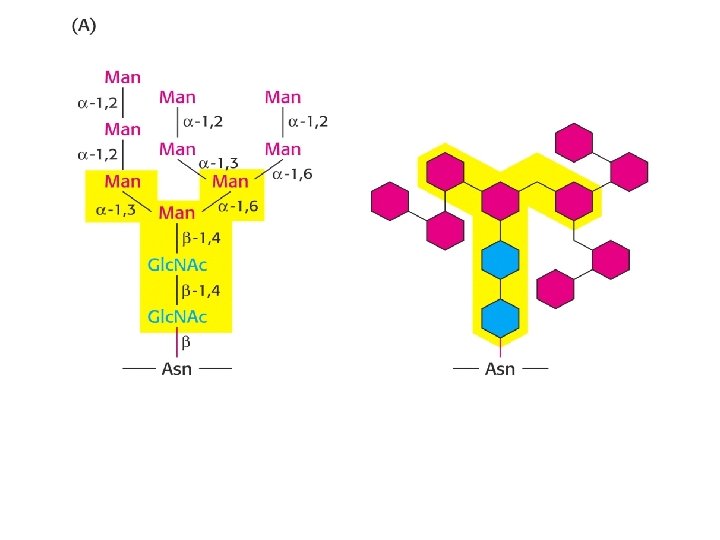
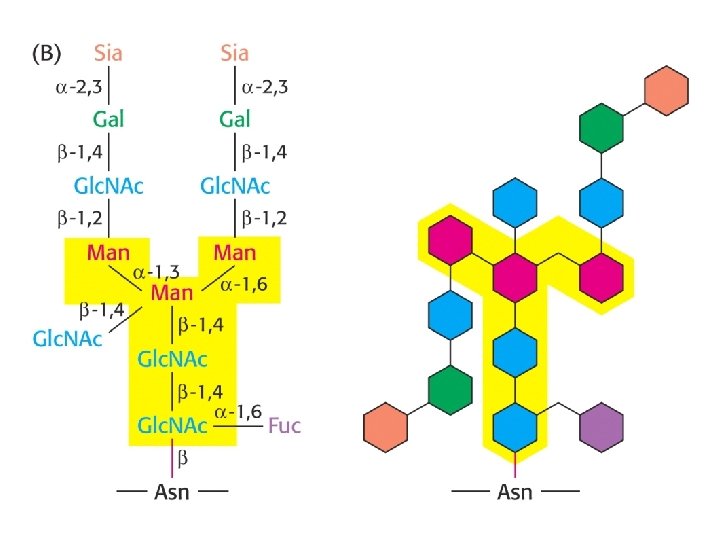
Glycoprotéines Mode d’attachement : O-glycosylation Liaison à sérine ou thréonine Liaison à hydroxylysine - par Gal. NAc - Glc. Nac isolé (protéines cytosol, noyau) - Gal (collagène) N-glycosylation* Liaison à asparagine - oligosaccharide branché, comportant 2 Glc. Nac et 3 Man à sa base *Indispensable pour le repliement correct ou le fonctionnement de certains protéines




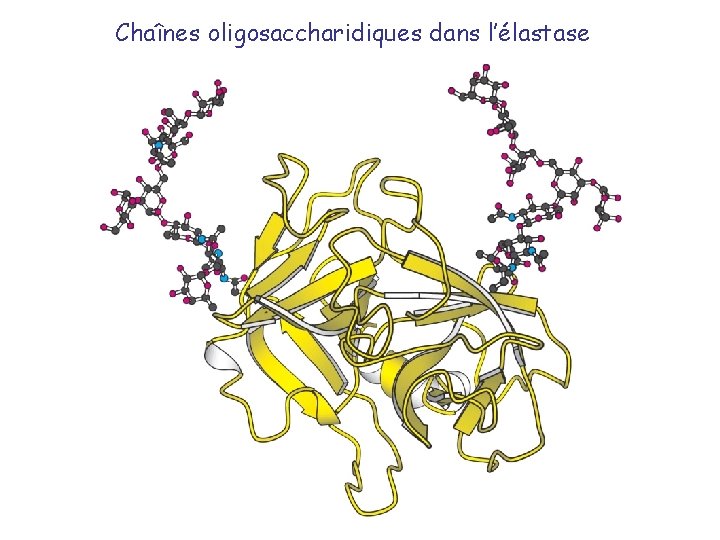
Chaînes oligosaccharidiques dans l’élastase
