Chapitre 10 LHmoglobine Relations structurefonction 1 Fonction de

Chapitre 10 L'Hémoglobine: Relations structure-fonction 1. Fonction de l'hémoglobine A. L'hème B. Liaison d'O 2 C. Transport de CO 2 et effet Bohr D. Influence du BPG sur la liaison d'O 2

2. Structure et mécanisme A. Structure de la myoglobine B. Structure de l'hémoglobine C. Mécanisme coopératif de la liaison de l'O 2 D. Base structurale de la liaison du BPG 3. Hémoglobines anormales 4. Régulation allostérique et modèles de coopérativité

L'hémoglobine Sa couleur, son abondance et sa facilité d'isolement en ont fait un objet de recherche depuis les temps anciens • Observation de cristaux pour la première fois en 1840 par Friedrich Hünefeld • Une des premières protéines dont la masse moléculaire a été déterminée avec précision • Première protéine à être caractérisée par ultracentrifugation • Première protéine a être associée à une fonction • Première protéine qui permet de démontrer qu'une mutation ponctuelle provoque une maladie • Une des premières protéines dont la structure a été déterminée par rayons X (Max Perutz, 1968)

1 FONCTION DE L'HEMOGLOBINE L'hémoglobine (Hb) est un héterotétramère, (dimère de protomères ). Les sous-unités et sont apparentée à la myoglobine (Mb) L'Hb transporte l'O 2 des poumons vers le tissus pour leur respiration. La Mb facilite le transport d'O 2 dans les muscles A. L'hème La Mb et chacune des 4 sous-unités de l'Hb lient un seul groupement hème de façon non-covalente L'hème dérive d'une porphyrine formée de 4 noyaux pyrrole reliées par des ponts méthène
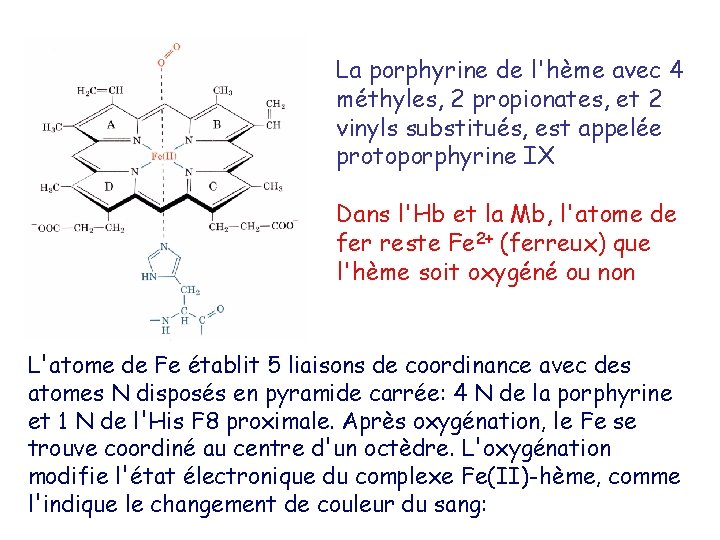
La porphyrine de l'hème avec 4 méthyles, 2 propionates, et 2 vinyls substitués, est appelée protoporphyrine IX Dans l'Hb et la Mb, l'atome de fer reste Fe 2+ (ferreux) que l'hème soit oxygéné ou non L'atome de Fe établit 5 liaisons de coordinance avec des atomes N disposés en pyramide carrée: 4 N de la porphyrine et 1 N de l'His F 8 proximale. Après oxygénation, le Fe se trouve coordiné au centre d'un octèdre. L'oxygénation modifie l'état électronique du complexe Fe(II)-hème, comme l'indique le changement de couleur du sang:
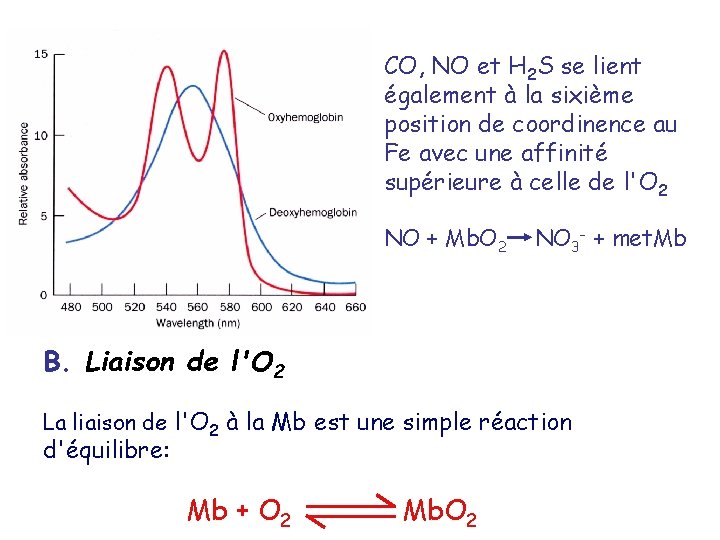
CO, NO et H 2 S se lient également à la sixième position de coordinence au Fe avec une affinité supérieure à celle de l'O 2 NO + Mb. O 2 NO 3 - + met. Mb B. Liaison de l'O 2 La liaison de l'O 2 à la Mb est une simple réaction d'équilibre: Mb + O 2 Mb. O 2

où Kd est une constante de dissociation La dissociation de l'O 2 de la Mb peur être caractérisée par sa saturation partielle, YO 2, définie comme la fraction des sites de liaison d'oxygène occupés par l'O 2: L'O 2 étant un gaz, on exprime sa concentration par sa pression partielle, p 02 (aussi appelée la tension en oxygène):

P 50 est la valeur de p 02 pour laquelle YO 2 = 50%, ce qui signifie que la moitié des sites de liaison de l'O 2 de la Mb sont occupés a. L'Hb lie l'O 2 de manière coopérative La courbe de saturation de la Mb suit une hyperbole; sa P 50 est égale à 2, 8 torr (760 torr = 1 atm). La Mb est donc presque saturée pour les valeurs physiologiques de p 02 dans le sang artériel (100 torr) et le sang veineux (30 torr). Par contre la courbe de dissociation de l'Hb est sigmoïdale et sa P 50 est égale à 26 torr. Par conséquent, la Hb libère une partie de son O 2 à la Mb à la pression veineuse de 30 torr dans des tissus:
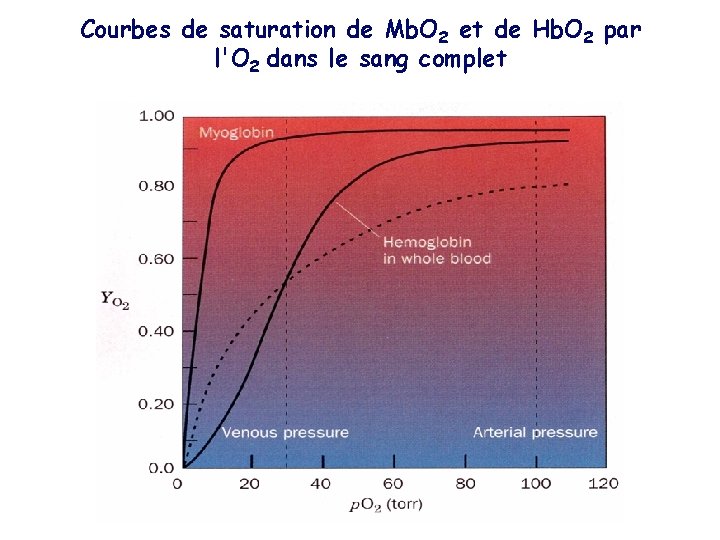
Courbes de saturation de Mb. O 2 et de Hb. O 2 par l'O 2 dans le sang complet

Une courbe de dissociation sigmoïdale est une indication d'interaction coopérative entre les sites de liaison d'une protéine pour un ligand. La liaison de l'O 2 augmente l'affinité de l'Hb pour la liaison de molécules d'O 2 supplémentaires (coopérativité positive de fixation d'O 2) b. L'équation de Hill A. V. Hill a caractérisé le comportement coopératif des enzymes oligomériques en 1910 E + n. S ESn E = enzyme, S = ligand, n= n° sous-unités

L'équation de Hill La valeur de n, la constante de Hill, augmente avec le degré de coopérativité de fixation du ligand Si n = 1, la liaison du ligand est non coopérative, et la courbe de saturation est celle d'une hyperbole comme pour la Mb Quand n > 1, la liaison est à coopérativité positive
![Représentation de Hill v = Vmax log [S]n S 0. 5 n + [S]n Représentation de Hill v = Vmax log [S]n S 0. 5 n + [S]n](http://slidetodoc.com/presentation_image_h2/e7d07f64d62f844580ad8ddf94719a3f/image-12.jpg)
Représentation de Hill v = Vmax log [S]n S 0. 5 n + [S]n log v = n. log [S] - n. log S 0. 5 Vmax- v v Vmax- v 0 Pente = n log[S]
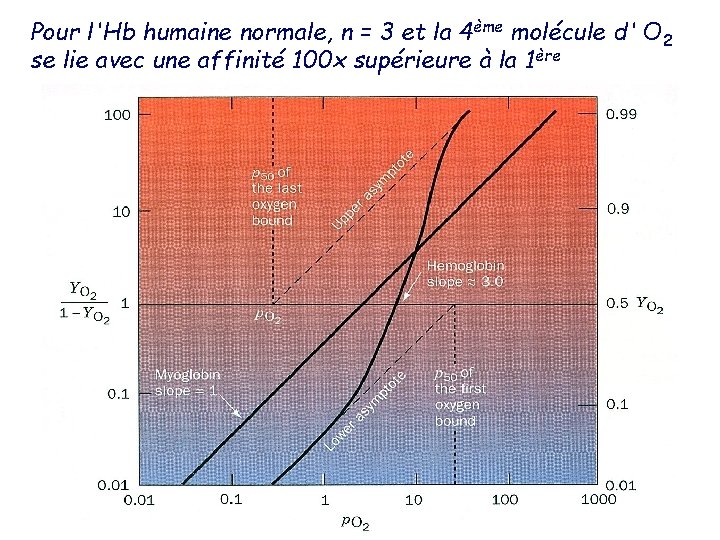
Pour l'Hb humaine normale, n = 3 et la 4ème molécule d' O 2 se lie avec une affinité 100 x supérieure à la 1ère
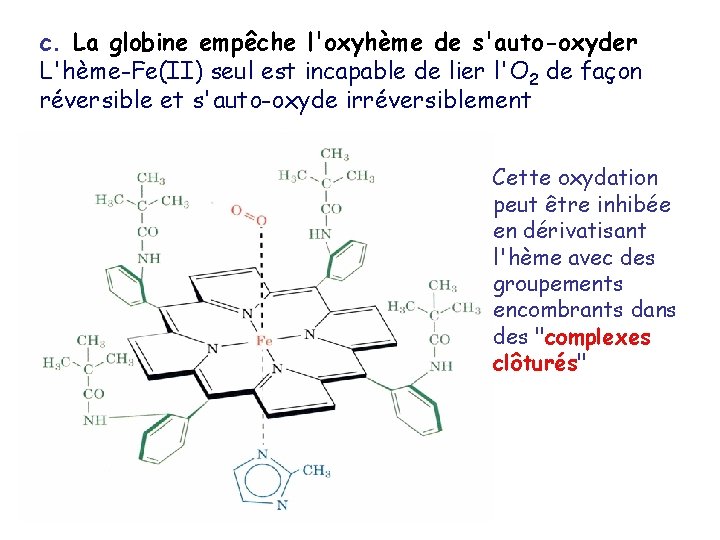
c. La globine empêche l'oxyhème de s'auto-oxyder L'hème-Fe(II) seul est incapable de lier l'O 2 de façon réversible et s'auto-oxyde irréversiblement Cette oxydation peut être inhibée en dérivatisant l'hème avec des groupements encombrants dans des "complexes clôturés"

C. Transport du dioxyde de carbone et effet Bohr a. L'effet Bohr facilite le transport de l'O 2 CO 2 + H 2 O H+ + HCO 3 - Dans les tissus où la p 02 est basse, les H+ issus de la formation du bicarbonate sont captés par l'Hb qui libère son O 2. Ces protons captés facilitent le transport du CO 2 en stimulant la formation du bicarbonate. Dans les poumons, où la p 02 est élevée, la liaison de l'O 2 par l'Hb libère les protons captés précédemment, ce qui provoque le départ du CO 2
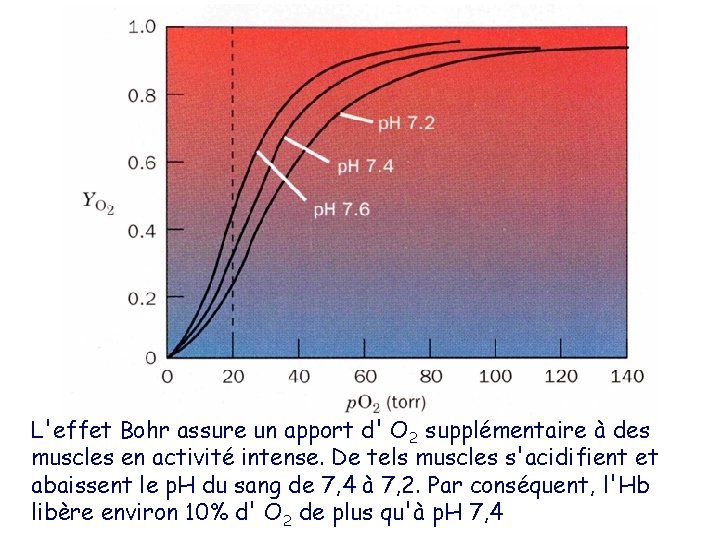
L'effet Bohr assure un apport d' O 2 supplémentaire à des muscles en activité intense. De tels muscles s'acidifient et abaissent le p. H du sang de 7, 4 à 7, 2. Par conséquent, l'Hb libère environ 10% d' O 2 de plus qu'à p. H 7, 4
b. Une quantité de CO 2 est transporté par l'Hb et le CO 2 module l'affinité de l'Hb pour l'O 2 Le CO 2 module la liaison de l'O 2 et se combine réversiblement aux groupements N-terminaux libres des protéines sanguines pour former des carbamates: Prot-NH 2 + CO 2 Prot-NH-COO- + H+ La désoxy. Hb fixe davantage de CO 2 sous forme de carbamate que l'oxy. Hb D. Influence du BPG sur la liaison d'O 2 L'Hb purifiée (nue) a une affinité plus grande pour l'O 2 que l'Hb du sang complet. La présence du D-2, 3 -bisphoglycérate (BPG) diminue l'affinité de l'Hb pour l'O 2
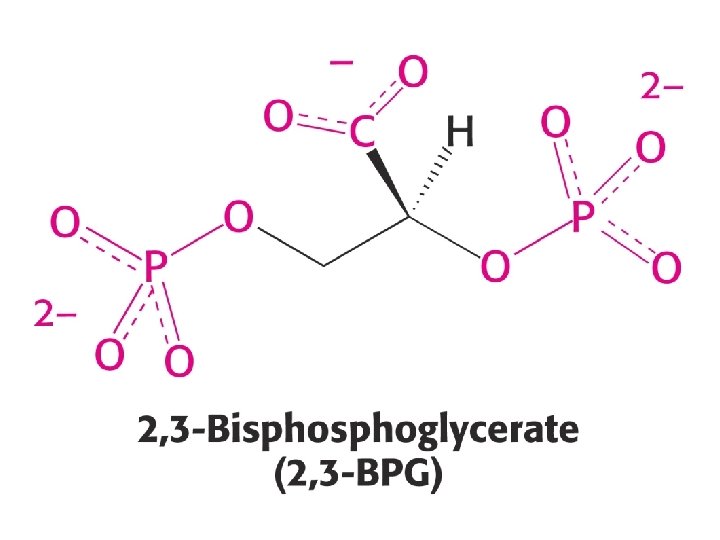
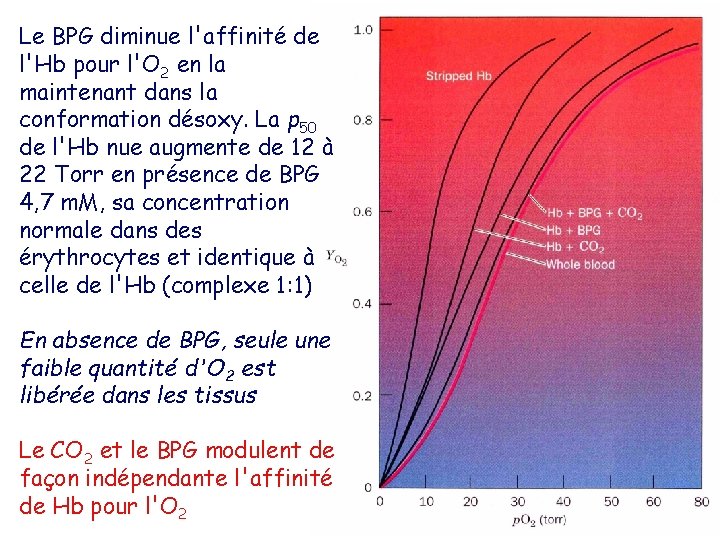
Le BPG diminue l'affinité de l'Hb pour l'O 2 en la maintenant dans la conformation désoxy. La p 50 de l'Hb nue augmente de 12 à 22 Torr en présence de BPG 4, 7 m. M, sa concentration normale dans des érythrocytes et identique à celle de l'Hb (complexe 1: 1) En absence de BPG, seule une faible quantité d'O 2 est libérée dans les tissus Le CO 2 et le BPG modulent de façon indépendante l'affinité de Hb pour l'O 2
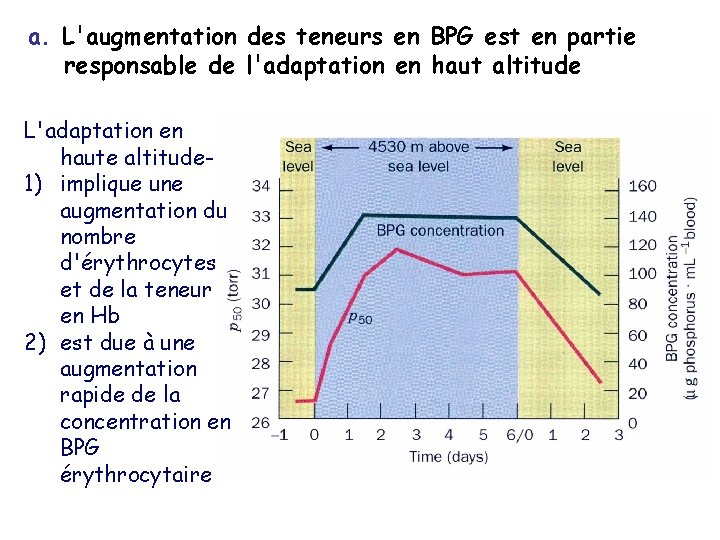
a. L'augmentation des teneurs en BPG est en partie responsable de l'adaptation en haut altitude L'adaptation en haute altitude 1) implique une augmentation du nombre d'érythrocytes et de la teneur en Hb 2) est due à une augmentation rapide de la concentration en BPG érythrocytaire
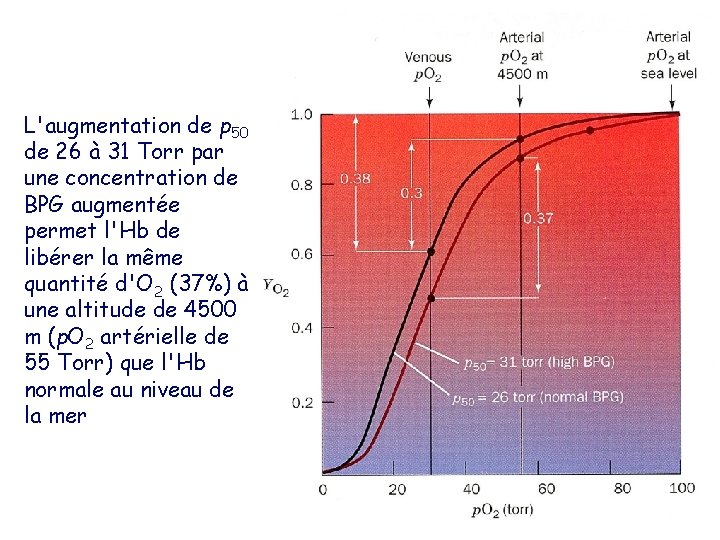
L'augmentation de p 50 de 26 à 31 Torr par une concentration de BPG augmentée permet l'Hb de libérer la même quantité d'O 2 (37%) à une altitude de 4500 m (p. O 2 artérielle de 55 Torr) que l'Hb normale au niveau de la mer

b. L'Hb foetale a une faible affinité pour le BPG -le BPG se lie avec moins d'affinité a la désoxy Hb. F ( 2 2) que à la désoxy Hb. A maternelle 2 STRUCTURE ET MECANISME Les déterminations des premières structures de protéines par rayons X, celles de la Mb de cachalot (John Kendrew, 1959) et de l'Hb de cheval (Max Perutz, 1968) a provoqué une révolution dans la manière de penser biochimique qui a rénové notre compréhension de la chimie de la vie

Première structure de protéines par rayons X • Myoglobine de cachalot par John Kendrew en 1959 • Pli 75% hélice - 155 acides aminés, ~ 17 k. Da

Premier complexe protéique • Hémoglobine • Deux copies de chaque sous-unité & • Déterminé par Max Perutz en 1968

A. Structure de la myoglobine Myoglobine - Protéine de 157 acides aminés - De ≈ 4, 5 x 2, 5 nm - Comportant 8 hélices alpha (désignées A-H) reliées entre elles par des boucles (résidus désignés en fonction de leur position dans hélices ou dans boucles) - Comportant un groupement prosthétique : hème, - pris en sandwich entre hélices E et F - Fer lié à His F 8 (histidine proximale) - groupements propionates affleurant à la surface - O 2 (si présent) - lié à Fe et à His E 7 (histidine distale) - modifie distribution électronique de l’hème (coloration rouge vif)
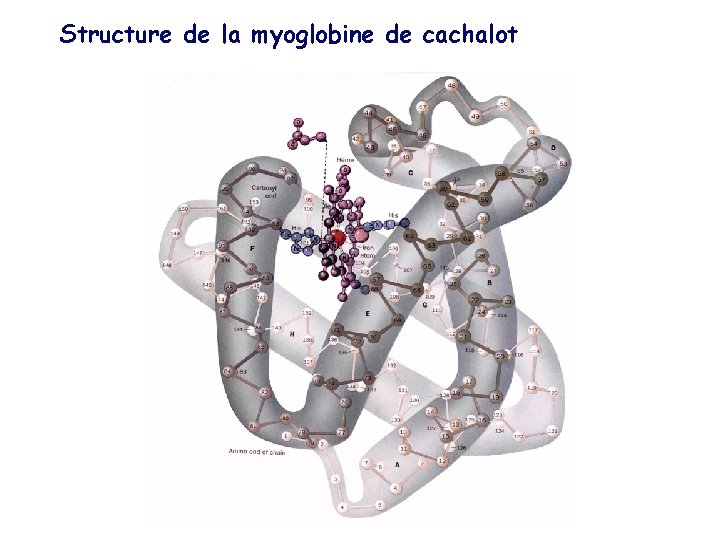
Structure de la myoglobine de cachalot
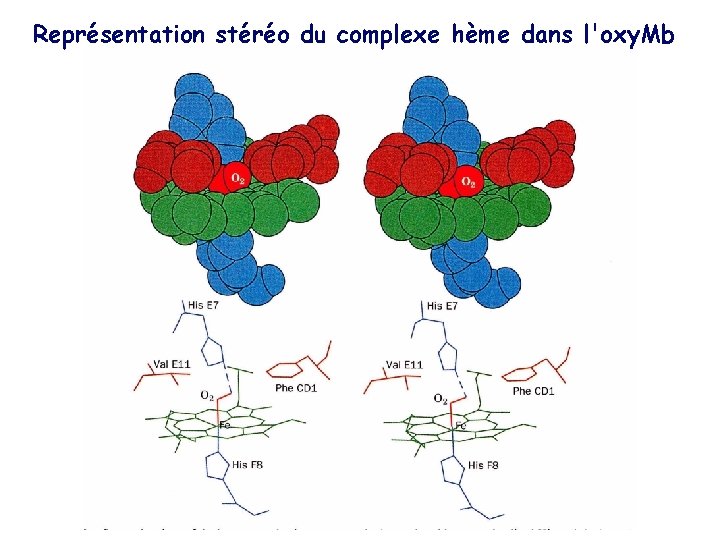
Représentation stéréo du complexe hème dans l'oxy. Mb

B. Structure de l'hémoglobine Tétramère constitués de 2 sous-unités alpha + 2 sous-unité ß (quasi homotétramère) Sous-unités alpha et ß = homologues de la myoglobine - 18 % d’identités - présence de résidus invariants (par ex. His. E 7, His. F 8, Phe. CD 1) Chaque sous-unité possède un hème et est donc capable de fixer un O 2 (4 O 2 au total) Arrangement des sous-unités: dimères de dimères contacts : 1 -ß 1 ou 2 -ß 2: 35 résidus 1 -ß 2 ou 2 -ß 1: 19 résidus 1 - 2 ou ß 1 -B: guère d’interactions 1 1 2 2
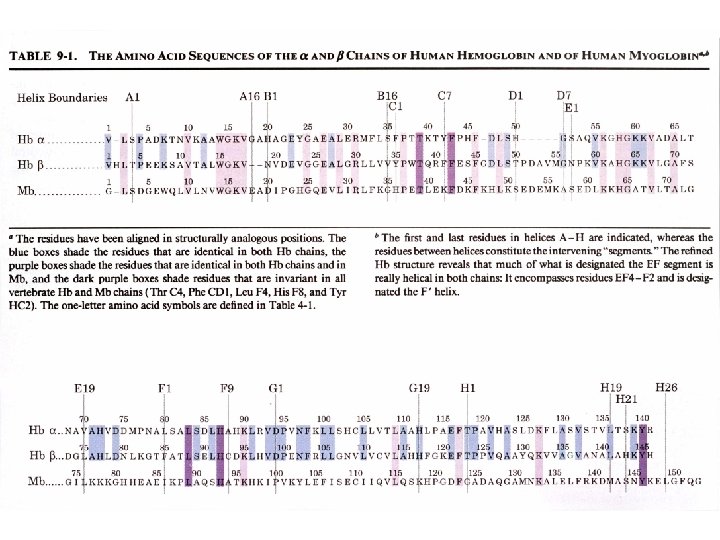
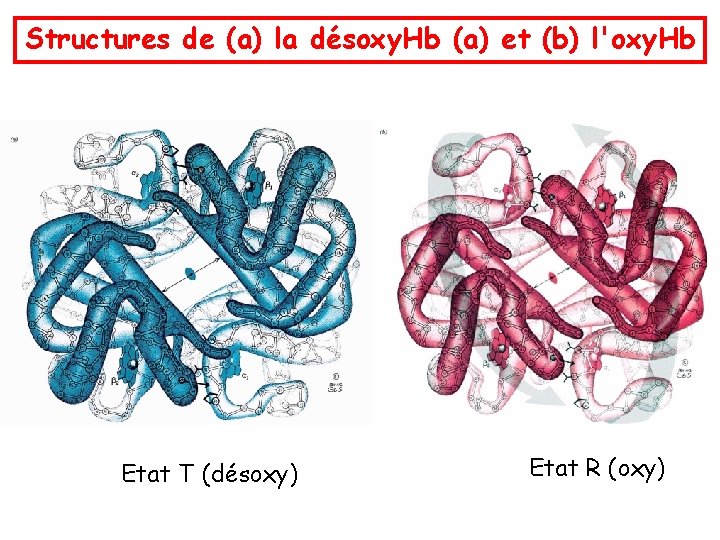
Structures de (a) la désoxy. Hb (a) et (b) l'oxy. Hb Etat T (désoxy) Etat R (oxy)
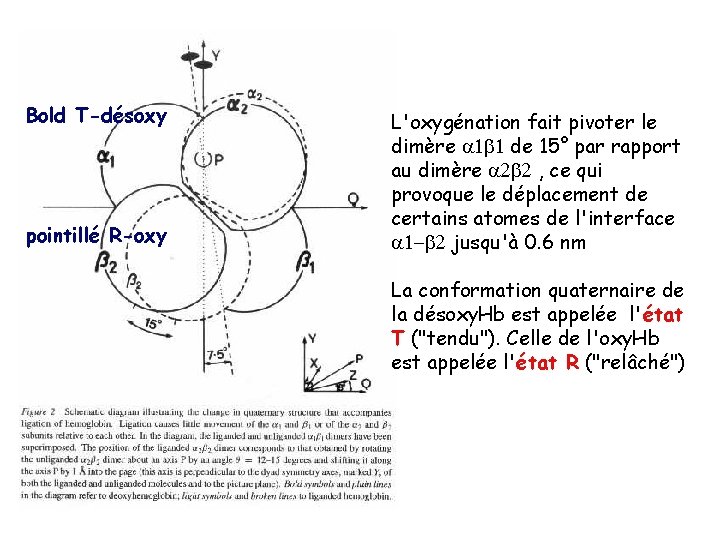
Bold T-désoxy pointillé R-oxy L'oxygénation fait pivoter le dimère de 15° par rapport au dimère , ce qui provoque le déplacement de certains atomes de l'interface jusqu'à 0. 6 nm La conformation quaternaire de la désoxy. Hb est appelée l'état T ("tendu"). Celle de l'oxy. Hb est appelée l'état R ("relâché")
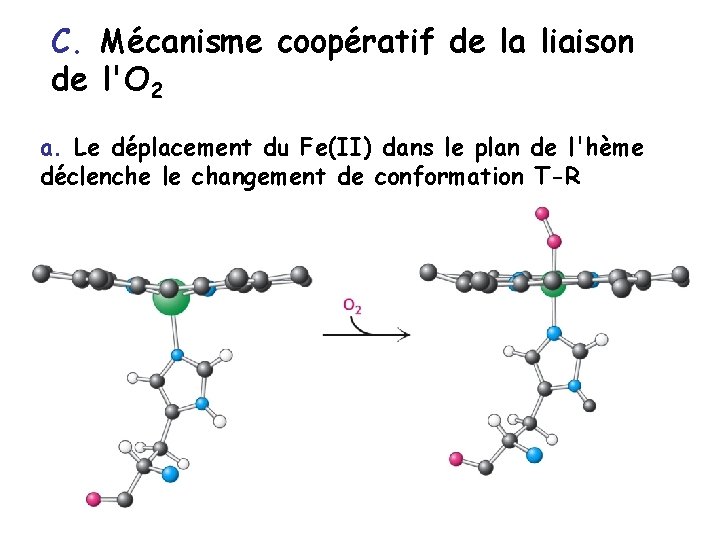
C. Mécanisme coopératif de la liaison de l'O 2 a. Le déplacement du Fe(II) dans le plan de l'hème déclenche le changement de conformation T-R
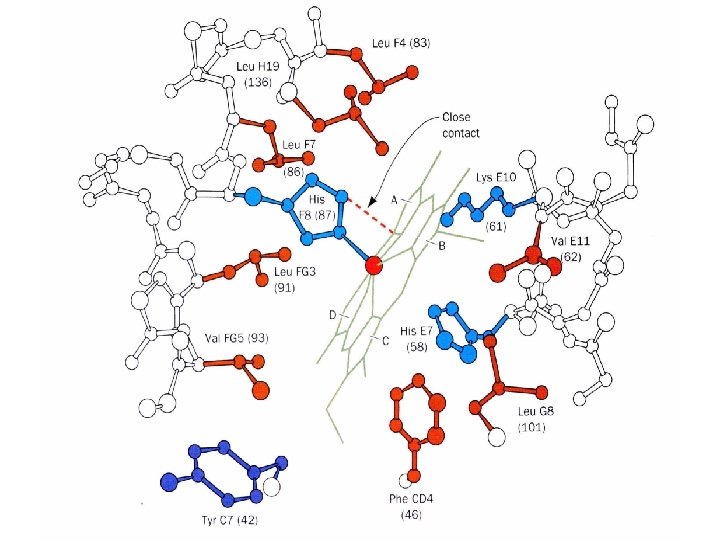
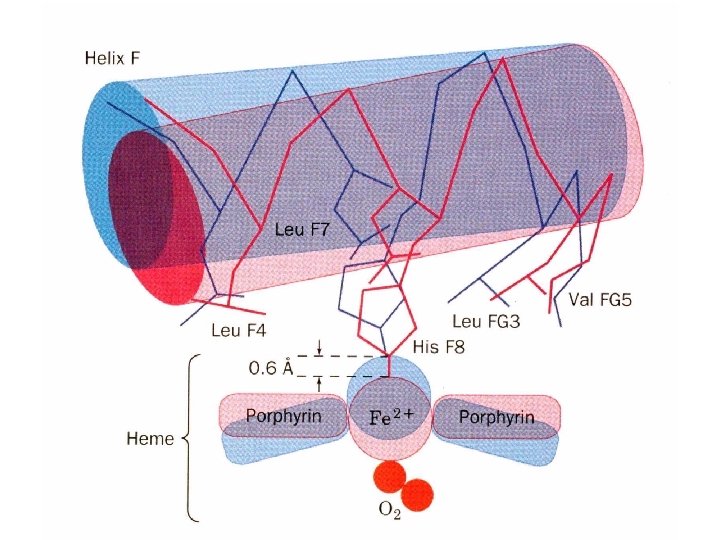
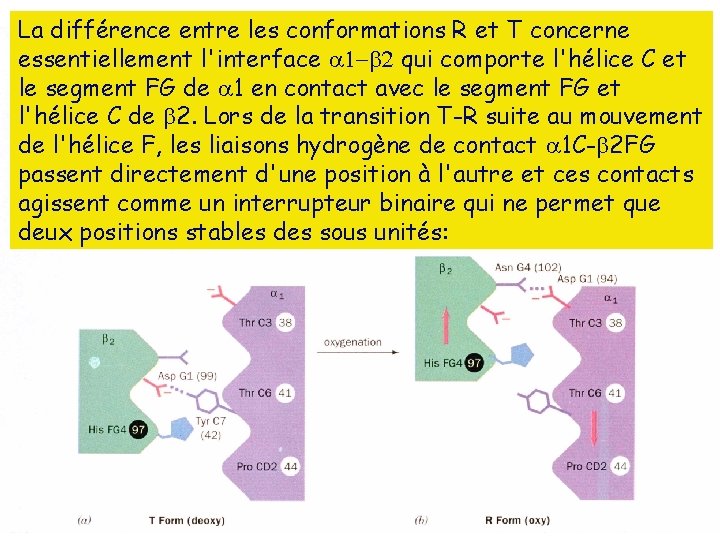
La différence entre les conformations R et T concerne essentiellement l'interface qui comporte l'hélice C et le segment FG de 1 en contact avec le segment FG et l'hélice C de 2. Lors de la transition T-R suite au mouvement de l'hélice F, les liaisons hydrogène de contact 1 C- 2 FG passent directement d'une position à l'autre et ces contacts agissent comme un interrupteur binaire qui ne permet que deux positions stables des sous unités:
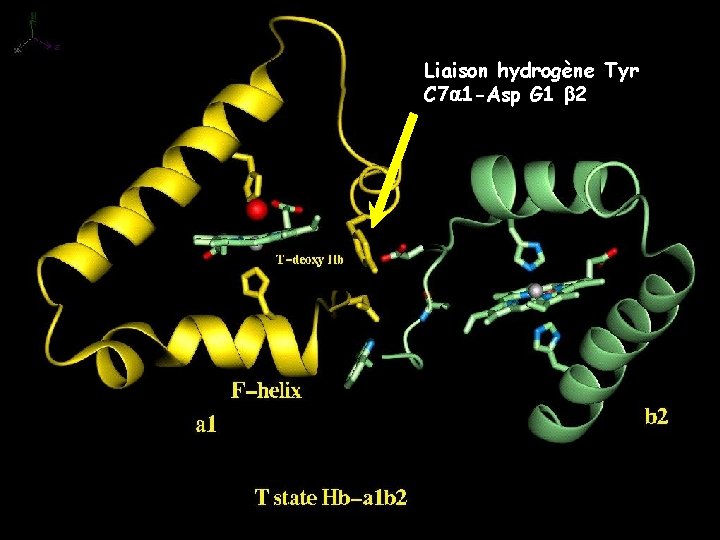
Liaison hydrogène Tyr C 7 1 -Asp G 1 2
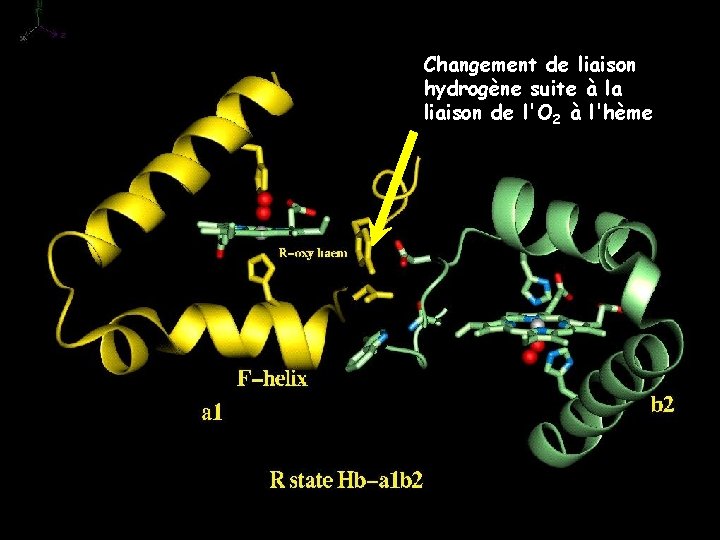
Changement de liaison hydrogène suite à la liaison de l'O 2 à l'hème
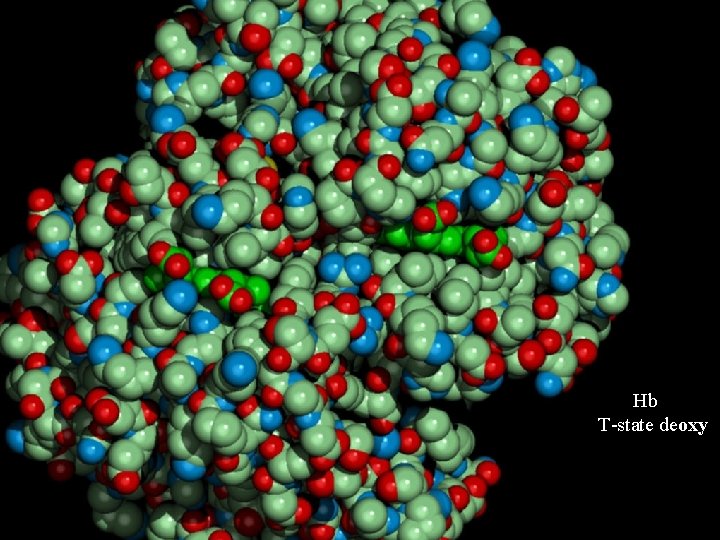
Hb T-state deoxy
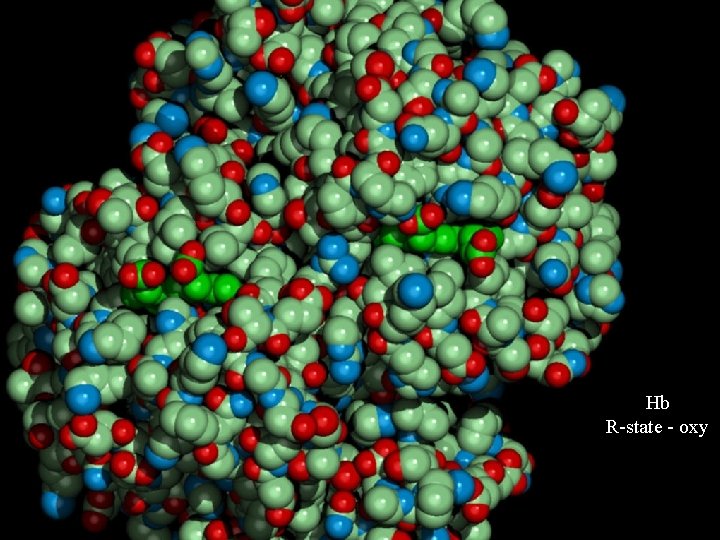
Hb R-state - oxy
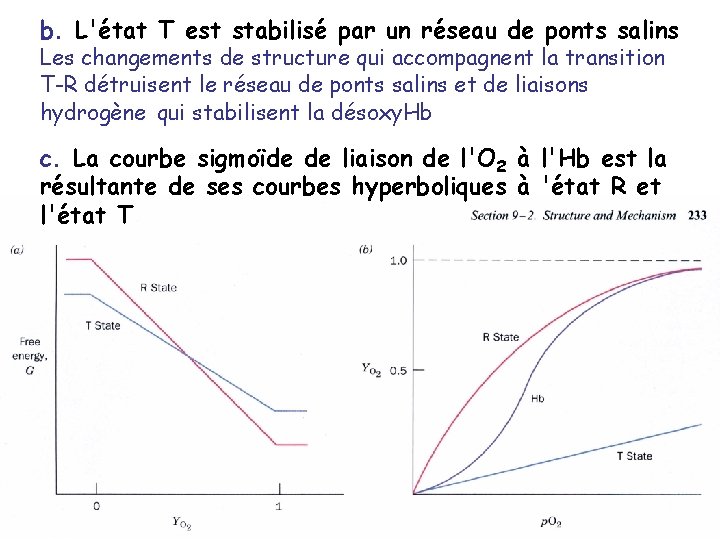
b. L'état T est stabilisé par un réseau de ponts salins Les changements de structure qui accompagnent la transition T-R détruisent le réseau de ponts salins et de liaisons hydrogène qui stabilisent la désoxy. Hb c. La courbe sigmoïde de liaison de l'O 2 à l'Hb est la résultante de ses courbes hyperboliques à 'état R et l'état T
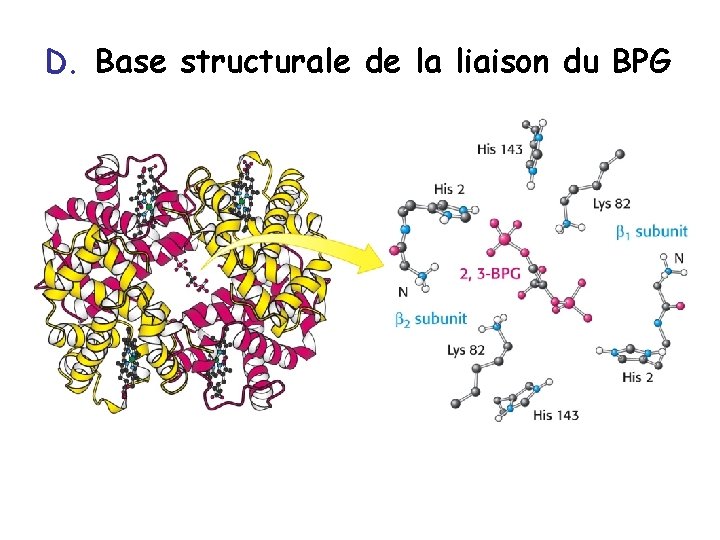
D. Base structurale de la liaison du BPG
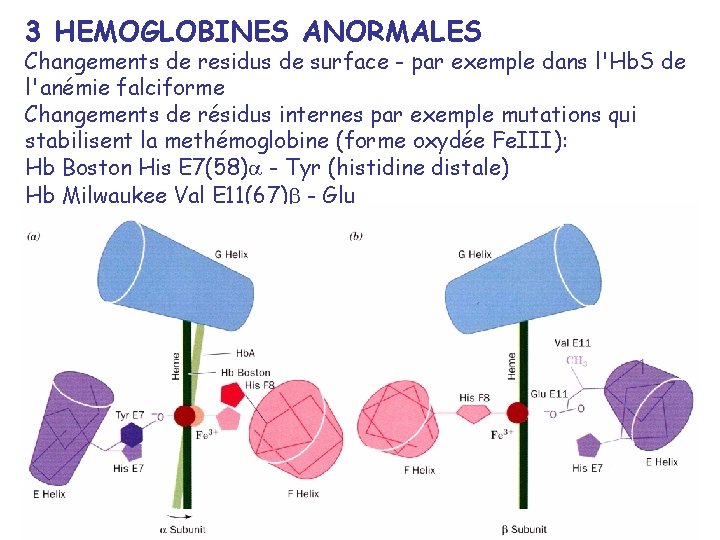
3 HEMOGLOBINES ANORMALES Changements de residus de surface - par exemple dans l'Hb. S de l'anémie falciforme Changements de résidus internes par exemple mutations qui stabilisent la methémoglobine (forme oxydée Fe. III): Hb Boston His E 7(58) - Tyr (histidine distale) Hb Milwaukee Val E 11(67) - Glu

4 REGULATION ALLOSTERIQUE Allos: autre; stereos: solide (forme dans l’espace) Régulation (principalement d’activités enzymatiques) - faisant intervenir des modifications de conformation d’une protéine et - permettant de rendre compte de l’effet d’effecteurs allostériques - et de phénomènes de coopérativité Effecteur allostérique: molécule se liant à distance du site catalytique (au niveau d’un site allostérique), agissant comme activateur ou comme inhibiteur Coopérativité positive ou négative: effet d’un ligand d’une protéine de faciliter ou de défavoriser la fixation d’un autre ligand Effet homotrope: effet coopératif d’un ligand sur sa propre fixation Effet hétérotrope: effet coopératif d’un ligand sur la fixation d’un autre ligand
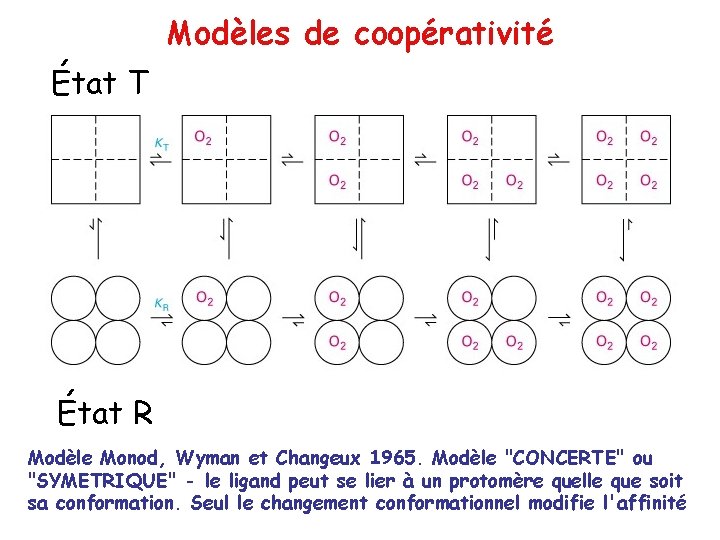
Modèles de coopérativité État T État R Modèle Monod, Wyman et Changeux 1965. Modèle "CONCERTE" ou "SYMETRIQUE" - le ligand peut se lier à un protomère quelle que soit sa conformation. Seul le changement conformationnel modifie l'affinité
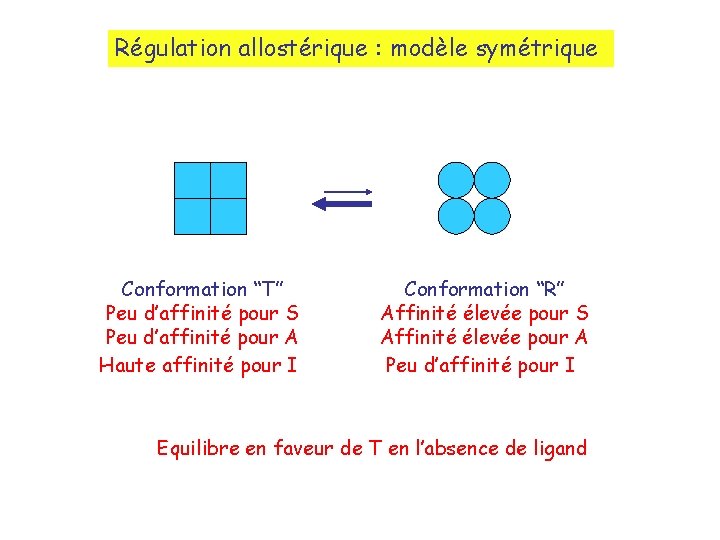
Régulation allostérique : modèle symétrique Conformation “T” Peu d’affinité pour S Peu d’affinité pour A Haute affinité pour I Conformation “R” Affinité élevée pour S Affinité élevée pour A Peu d’affinité pour I Equilibre en faveur de T en l’absence de ligand
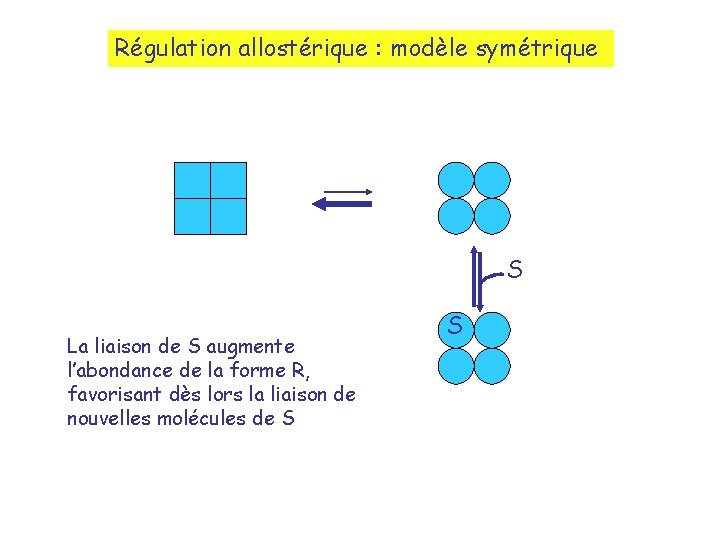
Régulation allostérique : modèle symétrique S La liaison de S augmente l’abondance de la forme R, favorisant dès lors la liaison de nouvelles molécules de S S
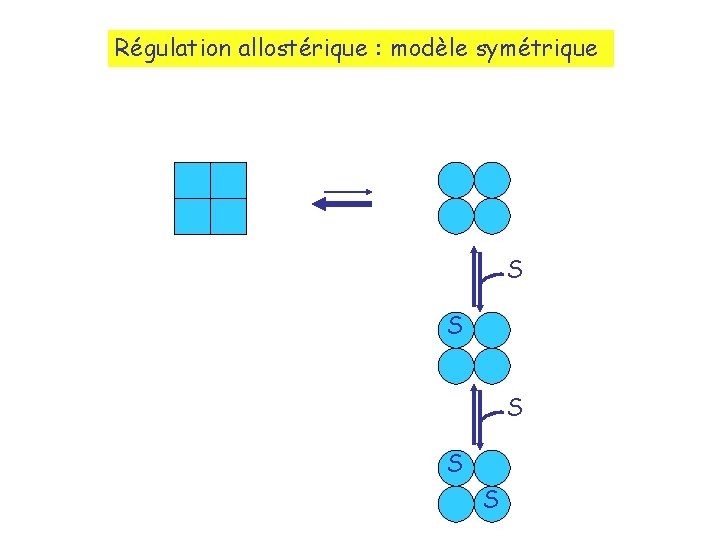
Régulation allostérique : modèle symétrique S S S
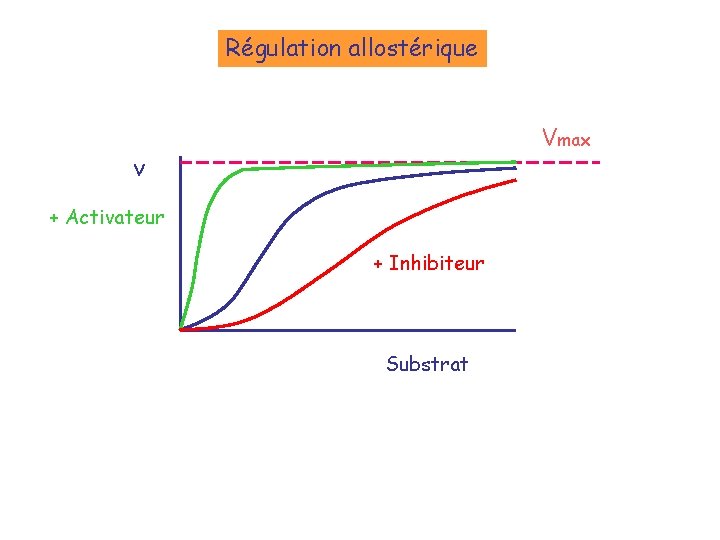
Régulation allostérique Vmax v + Activateur + Inhibiteur Substrat
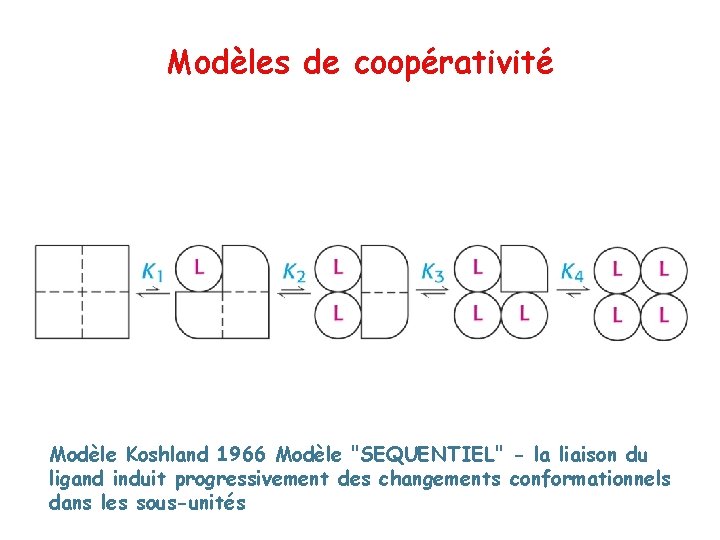
Modèles de coopérativité Modèle Koshland 1966 Modèle "SEQUENTIEL" - la liaison du ligand induit progressivement des changements conformationnels dans les sous-unités
- Slides: 49