Chap 5 Les acides et les bases Lgende

Chap 5 Les acides et les bases

Légende! Écoutez, comprenez, votre attention est nécessaire, votre crayon est facultatif Si je vole votre cahier de notes, je devrais voir textuellement ces parties Exercices, questions ou raisonnements Notez-en à votre discrétion

A) Retour et définitions (pp. 223 -224) � Définition d’Arrhénius ◦ Acide: donneur de protons (H+) ◦ Base: donneur d’hydroxyde (OH-) Le tout en milieu aqueux seulement. Pourtant, il existe plusieurs bases ne possédant pas de groupements hydroxydes…
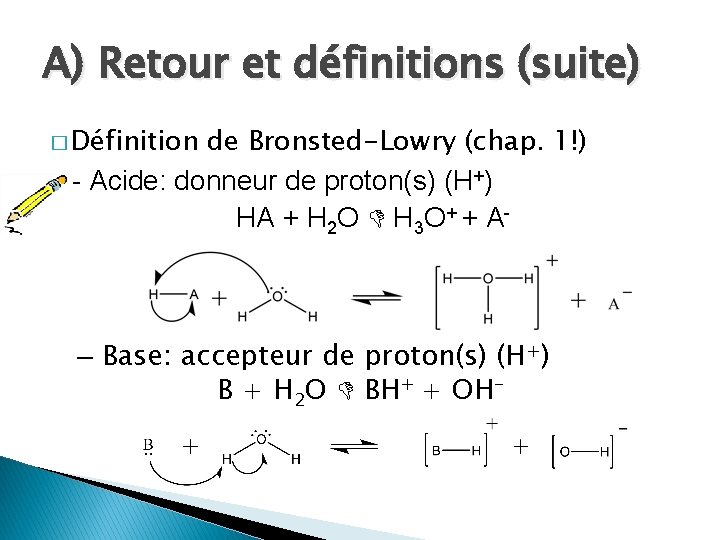
A) Retour et définitions (suite) � Définition de Bronsted-Lowry (chap. 1!) - Acide: donneur de proton(s) (H+) HA + H 2 O H 3 O+ + A- – Base: accepteur de proton(s) (H+) B + H 2 O BH+ + OH-
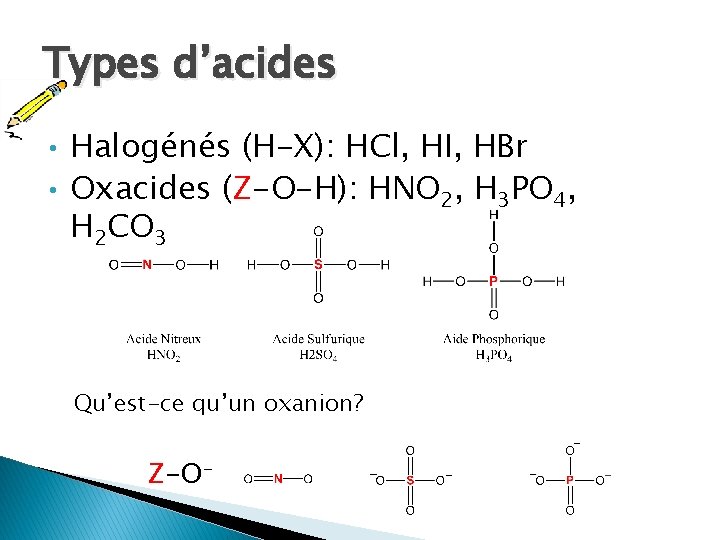
Types d’acides • Halogénés (H-X): HCl, HI, HBr • Oxacides (Z-O-H): HNO 2, H 3 PO 4, H 2 CO 3 Qu’est-ce qu’un oxanion? Z-O-
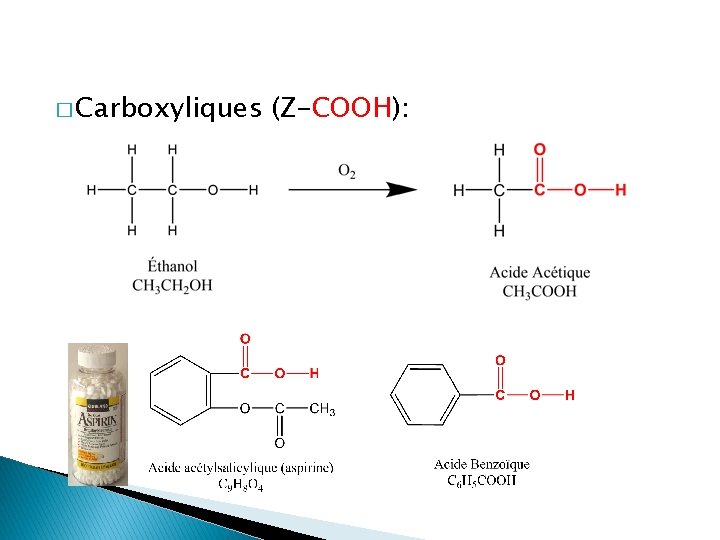
� Carboxyliques (Z-COOH):
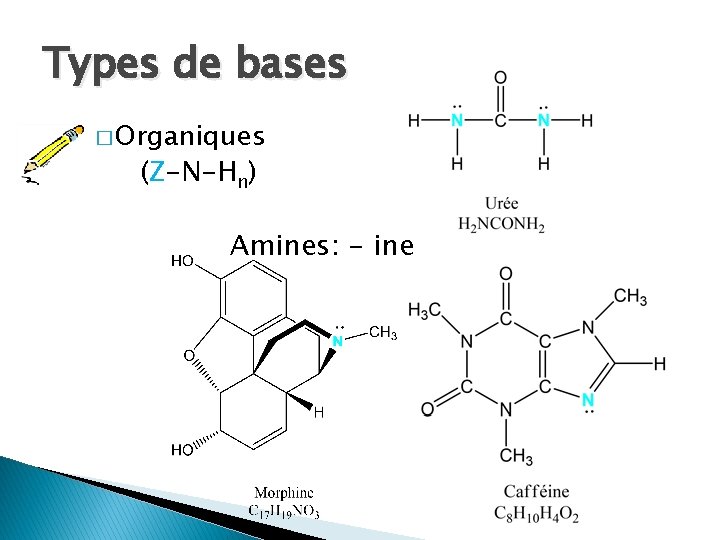
Types de bases � Organiques (Z-N-Hn) Amines: - ine
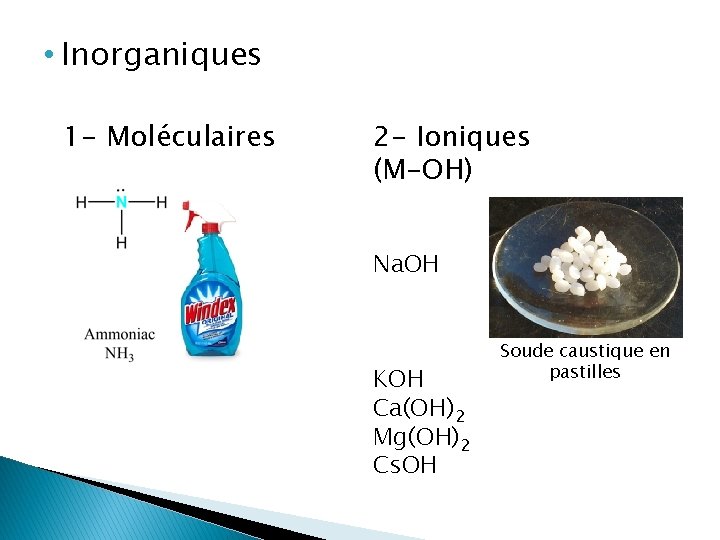
• Inorganiques 1 - Moléculaires 2 - Ioniques (M-OH) Na. OH KOH Ca(OH)2 Mg(OH)2 Cs. OH Soude caustique en pastilles

Concept de conjugué Reprenant la définition de Bronstead-Lowry, dans l’équation générale d’un acide + + AHA + H O + 2 3 H O + A HA + 3 A- H 2 O serait un accepteur de proton (une base) H 3 O+ serait un donneur de protons (un acide) D’où A- est la base conjuguée de l’acide HA. H 3 O+ est l’acide conjugué de la « base » H 2 O.
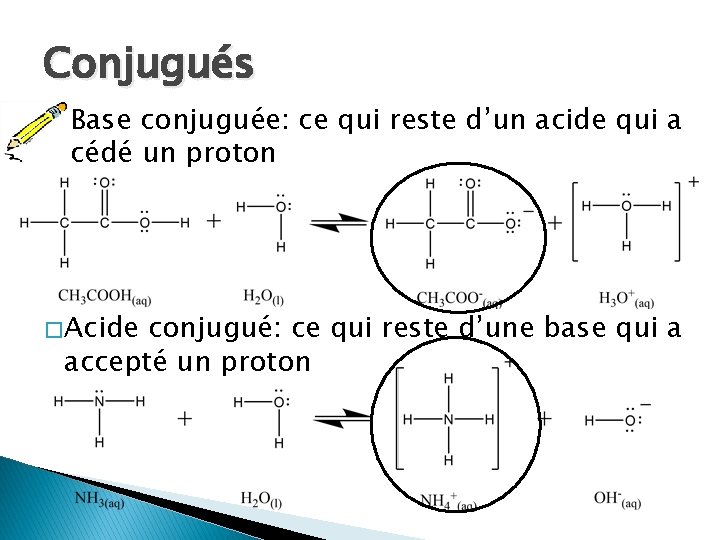
Conjugués � Base conjuguée: ce qui reste d’un acide qui a cédé un proton � Acide conjugué: ce qui reste d’une base qui a accepté un proton
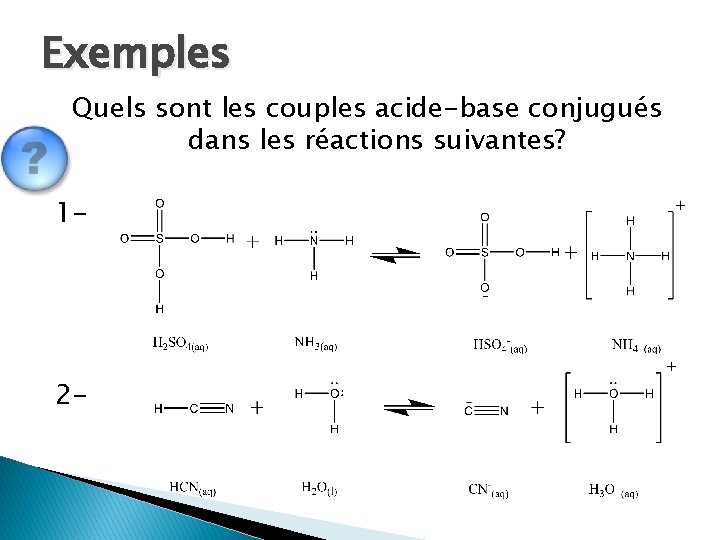
Exemples Quels sont les couples acide-base conjugués dans les réactions suivantes? 1 - 2 -
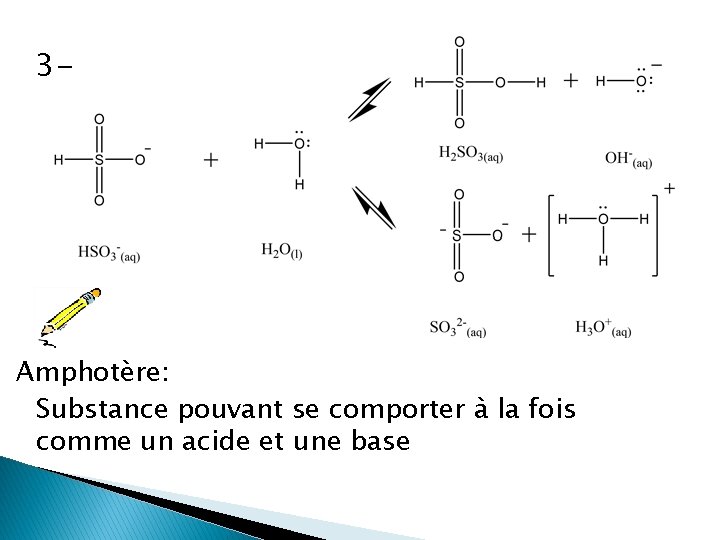
3 - Amphotère: Substance pouvant se comporter à la fois comme un acide et une base

Réponses 12 - 3 - CH 3 COO- est la base conjuguée H 3 O+ est l’acide conjugué NH 4+ est l’acide conjugué OH- est la base conjuguée HSO 3 - étant amphotère, H 2 SO 3 et H 3 O+ = acides conjugués OH- et SO 32 - = bases conjuguées
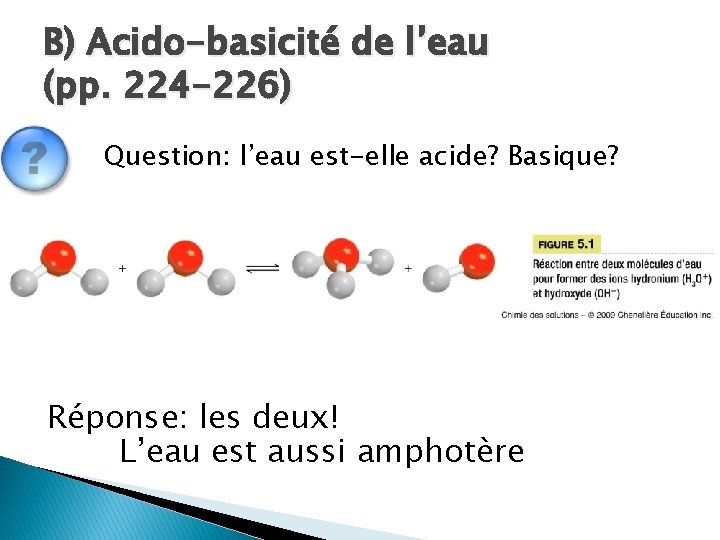
B) Acido-basicité de l’eau (pp. 224 -226) Question: l’eau est-elle acide? Basique? Réponse: les deux! L’eau est aussi amphotère
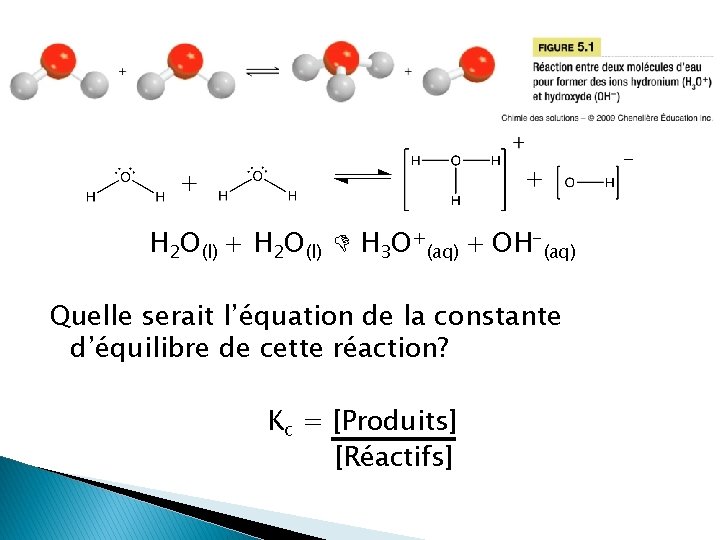
H 2 O(l) + H 2 O(l) H 3 O+(aq) + OH-(aq) Quelle serait l’équation de la constante d’équilibre de cette réaction? Kc = [Produits] [Réactifs]
![Keau Constante d’équilibre de l’auto-ionisation de l’eau: Keau = [H 3 O+][OH-] Dans l’eau Keau Constante d’équilibre de l’auto-ionisation de l’eau: Keau = [H 3 O+][OH-] Dans l’eau](http://slidetodoc.com/presentation_image_h/8929c72e257b29927d1bc0cc7ea9af92/image-16.jpg)
Keau Constante d’équilibre de l’auto-ionisation de l’eau: Keau = [H 3 O+][OH-] Dans l’eau pure à 25 °C, [H 3 O+]= [OH-] = 1, 0 x 10 -7 mol/L D’où Keau = (1, 0 x 10 -7) Keau = 1, 0 x 10 -14

C) p. H: le degré d’acidité (pp. 227 -231) Dans un milieu aqueux, les concentrations d’ions H 3 O+ et OH- sont habituellement très faibles, avec des exposants négatifs de 10. Pour faire plus pratique, Sørensen inventa l’échelle de p. H = - log [H 3 O+] Avec laquelle on travaille avec des nombres oscillant généralement entre 1 et 14.
![Solutions acides: [H 3 O+] >1, 0 x 10 -7 mol/L, p. H < Solutions acides: [H 3 O+] >1, 0 x 10 -7 mol/L, p. H <](http://slidetodoc.com/presentation_image_h/8929c72e257b29927d1bc0cc7ea9af92/image-18.jpg)
Solutions acides: [H 3 O+] >1, 0 x 10 -7 mol/L, p. H < 7 Solutions neutres: [H 3 O+] =1, 0 x 10 -7 mol/L, p. H = 7 Solutions basiques: [H 3 O+]<1, 0 x 10 -7 mol/L, p. H > 7 On peut aussi en faire l’équation inverse: [H 3 O+] = 10 -p. H

Même chose pour OHSi on recherche une mesure du degré de basicité: p. OH = - log [OH-] La même équation inverse est possible: [OH-] = 10 -p. OH En généralisant: p de quelque chose = -log (quelque chose)

Calculs de p. H simples La règle pour les chiffres significatifs des calculs des p. H est simple: On utilise autant de décimales que de chiffres significatifs dans le nombre principal. 1. [H 3 O+] = 1, 0 x 10 -6 mol/L 2 ch. s 2. [H 3 O+] = 4, 54 x 10 -3 mol/L 3 ch. s p. H = -log (1, 0 x 10 -6) p. H = -log (4, 54 x 10 -3) 2 déc. p. H = 6, 00 3 déc. p. H = 2, 343

La magie commence… Rappelons-nous de l’équation de la constante d’équilibre de l’auto-ionisation de l’eau Keau = [H 3 O+][OH-] = 1, 0 x 10 -14 Si on prend le log naturel négatif de chaque côté, - log [H 3 O+] - log [OH-] = - log (1, 0 x 10 -14) ou p. H + p. OH = 14, 00
- Slides: 21