Chang Kap 9 Kjemisk Binding Del I Kovalent

Chang Kap 9 Kjemisk Binding Del I Kovalent Binding • • • Atomer bygges opp av kjernepartikler (protoner og nøytroner) og elektroner Elektronene som er i det ytterste skallet deltar i bindinger mellom atomene ved å dele et eller flere elektronpar Disse elektronene kalles valenselektroner Valenselektronene representeres vha Lewis struktur Valenselektronene danner kovalente bindinger Kovalente bindinger kan være enkelbindinger, dobbeltbindinger eller trippelbindinger Lewis struktur kan også vise alene par av elektroner (lone pairs) som ikke deltar i de kovalente bindingene Resonans struktur er representasjon av flere mulige Lewis strukturer hvor en bestemt Lewis struktur ikke kan gi et nøyaktig bilde av molekylet De kjemiske bindingene i et legemiddel er viktig for dets egenskaper og virkemåte Kjennskap til de kjemiske bindingene kan hjelpe oss i å forutsi egenskapene til et legemiddel 1

Kjemisk Binding: Oktett Regelen – Oktett regelen • Atomer danner bindinger for oppnå elektron konfigurasjonen til en edelgass, som er en stabil elektron konfigurasjon • For de fleste atomer skjer dette ved deling av tilsammen 8 elektroner, bortsett fra de som er nær helium hvor 2 elektroner deles • Atomer kan danne enten ioniske eller kovalente bindinger for å oppfylle oktett regelen 2

Kap 9. 1 Lewis struktur • • Det periodiske system gir oss mulighet til å si hvor mange valenselektroner et atom har Atomer kombinerer sine valenselektroner slik at en mer stabil elektron konfigurasjon oppnås (Oktett regelen), helst edelgass konfigurasjon Valenselektronene holdes orden på vha Lewis strukturer • Se Fig. 9. 1 for valens strukturer • 3

Kap 9. 2 Kovalent Binding • • • Kjemisk binding skjer ved å dele elektroner Når to elektroner deles i en binding dannes det en kovalent binding som bygger opp kovalente forbindelser Symbolet for dette er en rett strek – Eks. HCl Elektronkonfigurasjoner: H: 1 s 1 (et valenselektron) og Cl: 1 s 22 p 63 s 23 p 5 (5 valenselektroner) NB ! Kun 2 elektroner deltar og de andre kalles alene par som ikke deltar i kovalente bindingen 4

Kap 9. 2 Kovalent Binding • Eks. H 2 O • Eks. Cl 2 • Det dannes kovalente bindinger når det ikke er nok elektroner for hvert individuelt atom for å oppnå oktett regelen. Ved å dele elektroner og danne kovalente bindinger kan de enkelte atomene fylle opp sine 5 ytterste skal og oktett regelen oppnås

Kap 9. 2 Kovalent Binding • Vi har nå sett hvordan kovalente enkelt bindinger dannes. Tilsvarende dannes dobbelt og trippel bindinger. For disse bindingene deler man to eller tre elektronpar • Eks. N 2 • Eks. C 2 Cl 4 6
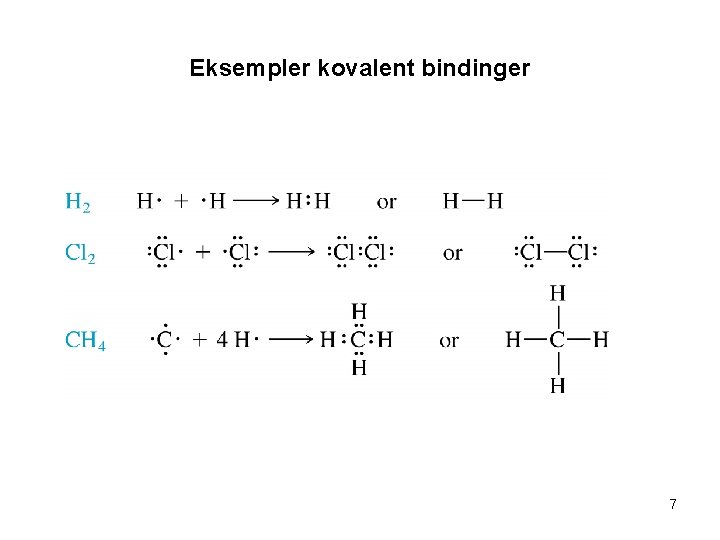
Eksempler kovalent bindinger 7

Kap. 9. 3 Elektronegativitets verdier • • For HCl viser det seg eksperimentelt at elektronene tilbringer mer tid ved Cl enn ved H. Dette skyldes at Cl har høyere elektronegativitet enn H. Det dannes da en polar kovalent binding For å se om vi har en polar kovalent binding bruker vi elektronegativitet, som er et mål på evnen et atom har til å trekke på elektronene i en binding. Atomer som F, O, N, S, Cl og Br har høy elektronegativitets verdi og trekker sterkt på elektronene. Det dannes en polarisering av valens elektronene • Se Fig. 9. 4 for elektronegativitets verdier • Generelt dannes det en ionebinding når forskjellen i elektronegativitets verdi er større enn 2 ! 8
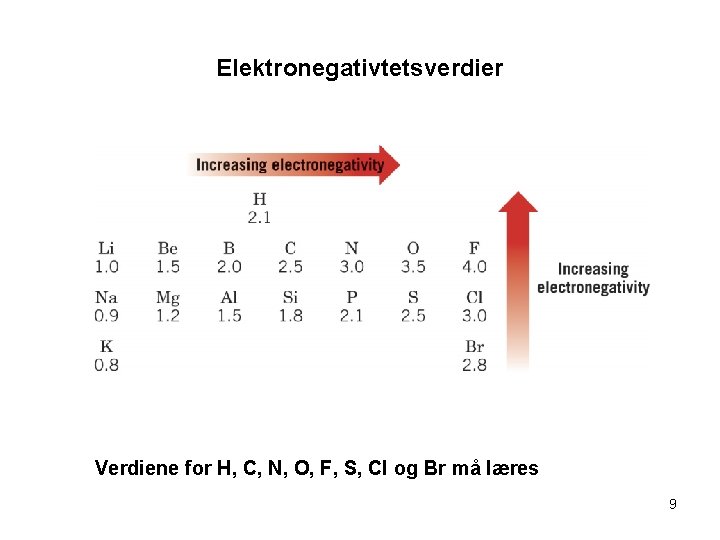
Elektronegativtetsverdier Verdiene for H, C, N, O, F, S, Cl og Br må læres 9

Ioniske bindinger – Ionisk binding • Når ioniske bindinger dannes får man eller taper man elektroner for å oppnå edelgass konfigurasjon – Det dannes ioner i denne prosessen med motsatte ladninger – Skjer for atomer med stor forskjell i elektronegativitets verdi • Eks. – Li taper et elektron og får positiv ladning Li+ – F får et elektron og blir negativ ladet FDet dannes da en sterk binding mellom Li+ og F- 10
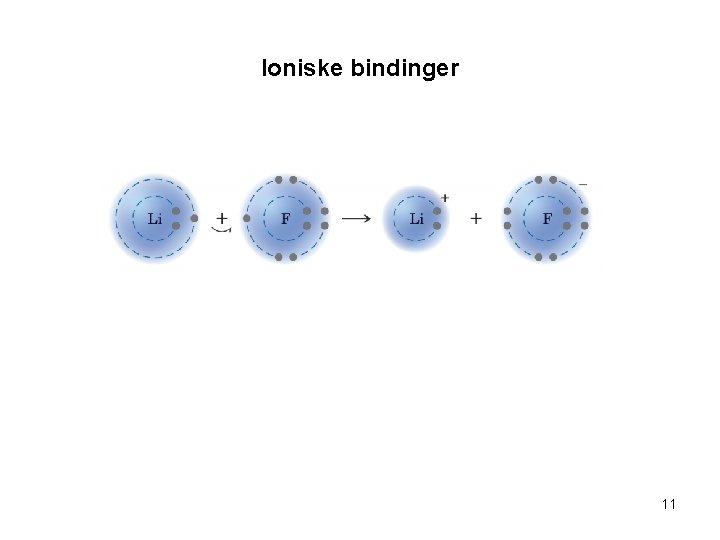
Ioniske bindinger 11

Hydrogenbindinger • • Dannes Hydrogen bindinger mellom H-atomet og et elektronegativ atom som X= F, N og O Skyldes at vi har en polar binding mellom H og X Er en relativ sterk binding og er meget viktig innen kjemi, biokjemi og biologi Er viktig for interaksjoner mellom reseptorer-enzymer og legemidler for at legemiddelene skal virke Eks. : 12

Kap. 9. 4 Mer om Lewis struktur Regler for Lewis strukturer 1) Start med molekylets skjellett hvor atomet med minst elektronegativitets verdi er sentral atom 2) Tell antall valenselektroner og legg til valenselektroner for negative ladninger og trekk fra valenselektroner for positivt ladninger 3) Tegn inn en enkelt kovalent binding mellom sentral atomet og de andre atomene. Sjekk antall valenselektroner som er brukt 4) Hvis oktettregelen ikke er oppfylt for sentral atomet tegner man inn dobbelt og trippelbindinger mellom sentral atomet og de andre atomene vha alene parene Eksempler: O 2, CH 3 Cl, Cl. O 3 -, CO 32 - 13

Eksempel CO 32 - 14

Kap. 9. 6 Resonans • • Vi så at for CO 32 - kunne vi ha tre alternative måter å presentere Lewis strukturen på Men eksperimentelt har man bestemt bindingene i har eksakt lik bindingslengde. Vi løser dette problemet ved å bruke alle Lewis strukturene og hver av disse kalles en resonans struktur Resonans struktur er to eller flere Lewis strukturer for å representere et bestemt molekyl Resonans er ikke reelle molekyl strukturer men er en hypotetisk måte å presentere Lewis strukturer Vi har kun endret valenselektronenes posisjon Vi får da en mellomting eller hybrid (gjennomsnitt) av de to resonans bidragene Bruker en dobbeltpil mellom de ulike resonansformene for å illustrere resonans NB ! Må ikke forveksles med en likevekt 15
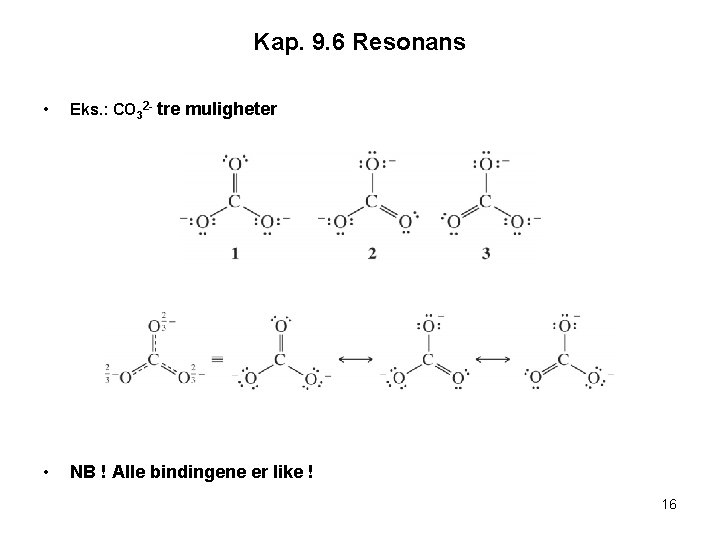
Kap. 9. 6 Resonans • Eks. : CO 32 - tre muligheter • NB ! Alle bindingene er like ! 16
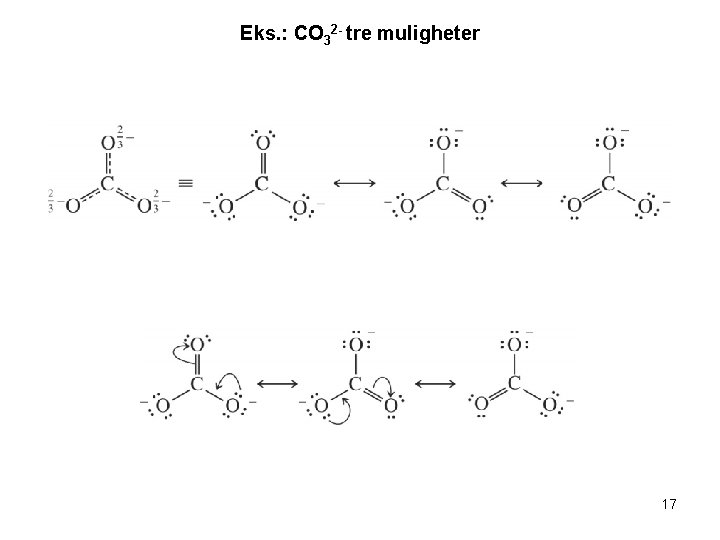
Eks. : CO 32 - tre muligheter 17
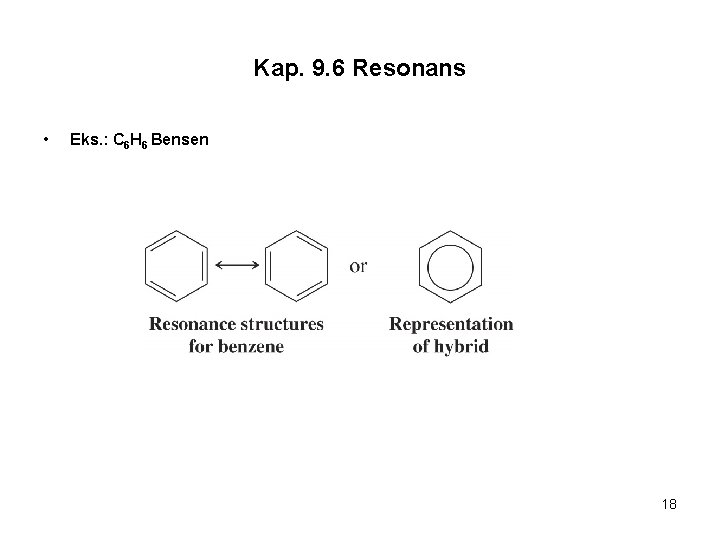
Kap. 9. 6 Resonans • Eks. : C 6 H 6 Bensen 18

Kap 9. 6 Resonans Regler for resonans: 1) 2) 3) 4) 5) 6) 7) 8) 9) Resonans eksisterer kun på papiret og vi bruker en dobbeltpil Kun lov til å flytte på elektroner Alle resonans strukturene må være ekte Lewis strukturer Energien til molekylet er lavere enn for hver individuell struktur Likeverdige resonans strukturer bidrar like mye til hybrid strukturen Jo mer stabil den enkelte resonans strukturen er, jo større er bidraget til hybrid strukturen Jo flere kovalente bindinger et molekyl har, jo mer stabilt er molekylet, spesielt for de som har fulle valens skall Separering av ladninger minker stabiliteten Negativ ladning på elektronegative atomer, dvs atomer med høy elektronegativitetsverdi, er gunstig 19

Pensum for Bindinger Del I • Kap 9. 1 tom 9. 4 og kap. 9. 6 i boken R. Chang General Chemistry, The Essential Concepts • Kap 1. 1 tom 1. 5 og kap 1. 8 i Solomons og Fryhle 20

R. Chang Kap 10. Kjemisk Binding Del II • • Molekylær geometri er den tredimensjonale strukturen til atomene i molekylet som bestemmes vha VSEPR teorien Dipol moment i et diatomisk molekyl dannes der forskjellen i elektronegativitets verdi er høy for de to atomene For treatomige molekyler vil også molekylets geometri bestemme om vi har et dipolmoment Dipolmoment er sentralt for å bestemme reaktiviteten og fysikalskkjemiske egenskaper til molekyler 21

Kap 10. 1 • Molekyl Geometri: Valens skall elektron repulsjons teorien • Forenklet teori men gir en indikasjon på geometrien til molekyler • Valenselektronene er sentrale, både bindende elektronpar i enkelt og dobbeltbindiger, men også frie elektroner i ikkebindende elektronpar • Antar at elektronene vil være lengst mulig fra hverandre i rommet pga samme negative ladning • Ikke bindende elektroner vil frastøte hverandre enda mer • Geometrien til molekylet bestemmes av antall sett av elektroner og bindigene • Geometrien til et molekyl påvirker de fysikalsk-kjemiske egenskapene til molekylet 22

VSEPR • Molekyler med formel ABx, X = 1 tom 6, kun se på X = 1 tom 4 • AB dvs X = 1 vil være linære • AB 2 dvs X = 2 vil også være linære • AB 3 dvs X = 3 vil være trigonal plant • AB 4 dvs X = 4 vil tetraedrisk • Eksempler Se Tab 10. 1 23

VSEPR • Molekyler med formel ABx. Ey, X = 2 og 3, Y = 1 og 2 • AB 2 E vil være bøyd • AB 3 E vil være tetraedrisk • AB 2 E 2 vil tetraedrisk • Eksempler Se Tab 10. 2 24

Regler for VSEPR 1) 2) 3) 4) Skriv Lewis struktur for molekylet hvor elektroner kun ved sentralatomet tas med i betraktning Tell antall elektronpar for sentralatomet hvor alle bindinger telles som enkelt bindinger Bruk Tab. 10. 1 og 10. 2 og bestem geometrien Husk at alene par vil ha sterkere frastøtning enn bindende elektroner slik at avvik fra valensvinkelen kan skje Eks. OF 2 25
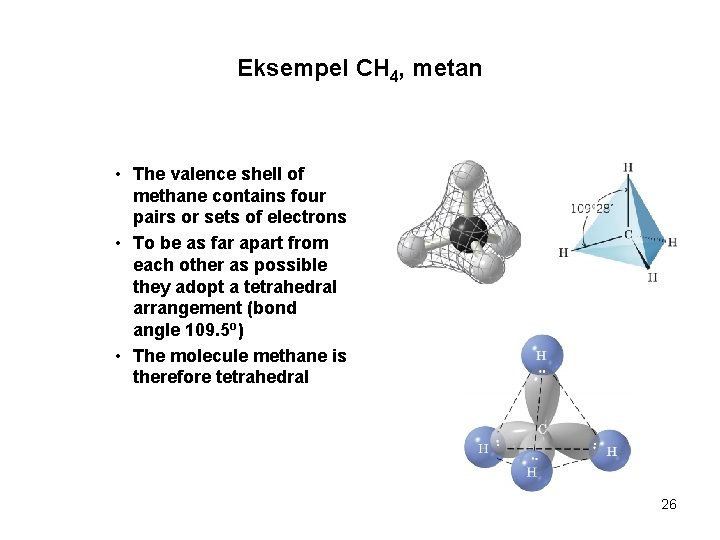
Eksempel CH 4, metan • The valence shell of methane contains four pairs or sets of electrons • To be as far apart from each other as possible they adopt a tetrahedral arrangement (bond angle 109. 5 o) • The molecule methane is therefore tetrahedral 26

Eksempel amoniakk, NH 3 • When the bonding and nonbonding electrons are considered there are 4 sets of electrons • The molecule is essentially tetrahedral but the actual shape of the bonded atoms is considered to be trigonal planar • The bond angles are about 107 o and not 109. 5 o because the non-bonding electrons in effect are larger and compress the nitrogen-hydrogen bond 27

Eksempel vann H 2 O • There are four sets of electrons including 2 bonding pairs and 2 non-bonding pairs • Again the geometry is essentially tetrahedral but the actual shape of the atoms is considered to be an angular arrangement • The bond angle is about 105 o because the two “larger” nonbonding pairs compress the electrons in the oxygenhydrogen bonds 28
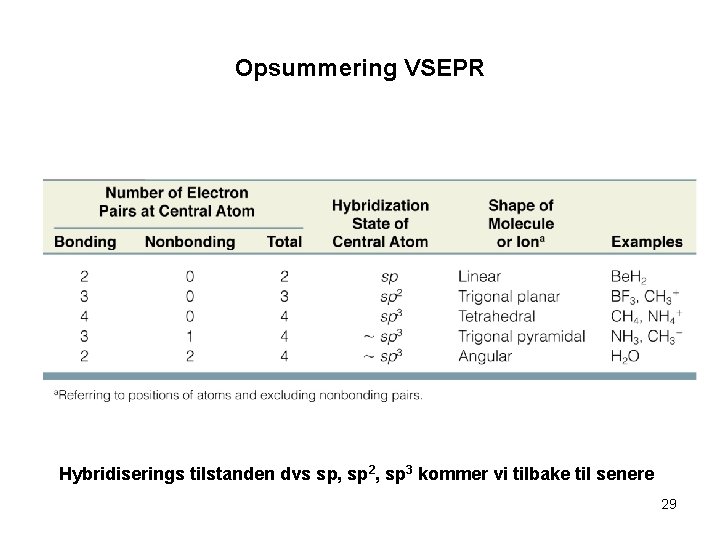
Opsummering VSEPR Hybridiserings tilstanden dvs sp, sp 2, sp 3 kommer vi tilbake til senere 29

Kap 10. 2 Dipol moment • • Dipol moment dannes i molekyler med polar kovalente bindinger Elektrontettheten endres fra et atom til et annet atom som har høyere elektronegativitet • Eks. H-Cl • For treatomige molekyler vil molekyl geometrien også spille en rolle • Eks. : SO 2 30

Pensum for Bindinger Del II • Kap 10. 1 tom 10. 3 i boken R. Chang General Chemistry, The Essential Concepts • Kap 1. 16 i Solomons og Fryhle • Resten av kap 10, dvs 10. 4 og 10. 5 i Chang og kap 1. 10, 1. 12 -1. 14 og 1. 17 gjennomgås mandag 20. 9 -04 • Kap 9. 5, 9. 7 og 10. 6 i boken R. Chang General Chemistry, The Essential Concepts er IKKE PENSUM • Kap 1. 6, 1. 7 og 1. 9 i Solomons og Fryhle er IKKE PENSUM 31
- Slides: 31