Chane respiratoire et oxydation phosphorylante La chane respiratoire















- Slides: 38

Chaîne respiratoire et oxydation phosphorylante La chaîne respiratoire Les composants de la chaîne La théorie chimiosmotique Structure et fonction de l’ATPase mitochondriale Systèmes navette de NAD/NADH Agents découplants

Formation de NADH et FADH 2

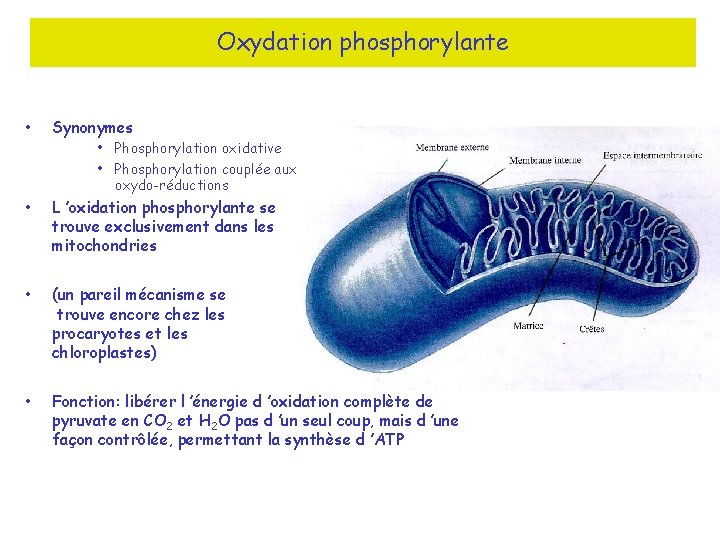
Oxydation phosphorylante • Synonymes • L ’oxidation phosphorylante se trouve exclusivement dans les mitochondries • (un pareil mécanisme se trouve encore chez les procaryotes et les chloroplastes) • Fonction: libérer l ’énergie d ’oxidation complète de pyruvate en CO 2 et H 2 O pas d ’un seul coup, mais d ’une façon contrôlée, permettant la synthèse d ’ATP • Phosphorylation oxidative • Phosphorylation couplée aux oxydo-réductions

Mitochondries • Le nombre de mitochondrie par cellule varie énormément: • • • Trypanosome: Levure: Muscle blanc: Muscle rouge: Foie: • Dimensions: 1 1 -10 peu (glycolyse) nombreuses (oxidation phoshorylante) 5000 • diamètre de 0. 2 -0. 8 µm • longueur de 0. 5 -1. 5 µm • Constituants: • • • membrane externe membrane interne espace intermembranaire crêtes matrice

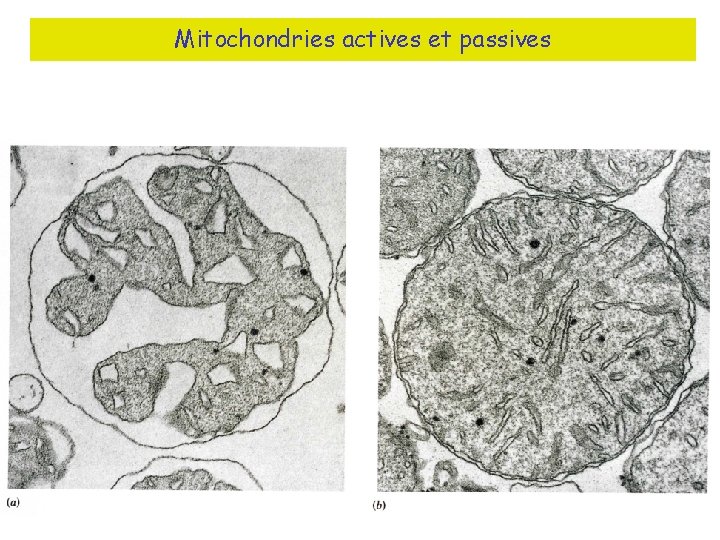
Mitochondries actives et passives

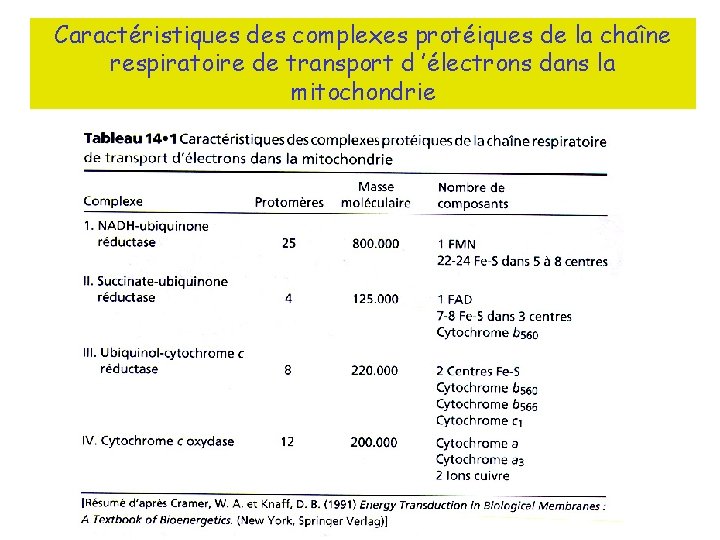
Caractéristiques des complexes protéiques de la chaîne respiratoire de transport d ’électrons dans la mitochondrie

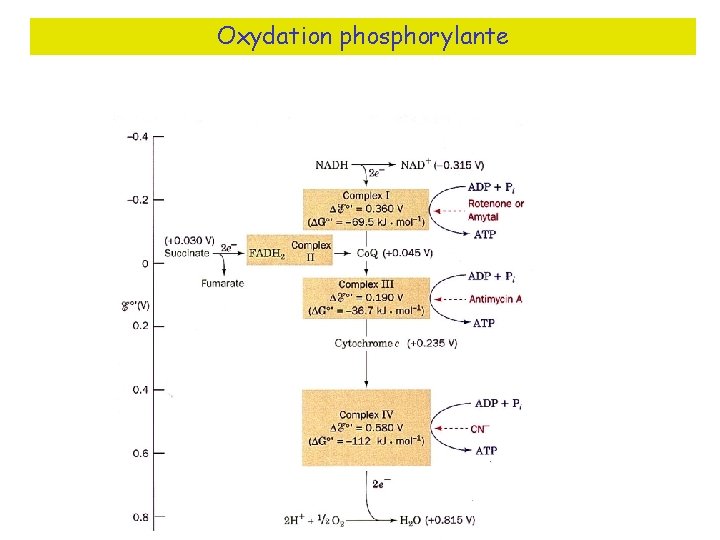
Oxydation phosphorylante

Composants de la chaîne respiratoire • • Protéines avec un ou deux centres fer-soufre Protéines à FMN Ubiquinone Cytochromes

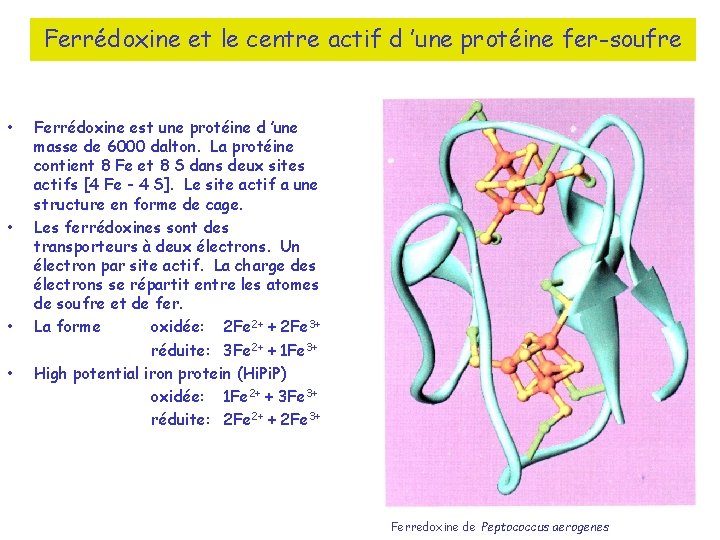
Ferrédoxine et le centre actif d ’une protéine fer-soufre • • Ferrédoxine est une protéine d ’une masse de 6000 dalton. La protéine contient 8 Fe et 8 S dans deux sites actifs [4 Fe - 4 S]. Le site actif a une structure en forme de cage. Les ferrédoxines sont des transporteurs à deux électrons. Un électron par site actif. La charge des électrons se répartit entre les atomes de soufre et de fer. La forme oxidée: 2 Fe 2+ + 2 Fe 3+ réduite: 3 Fe 2+ + 1 Fe 3+ High potential iron protein (Hi. P) oxidée: 1 Fe 2+ + 3 Fe 3+ réduite: 2 Fe 2+ + 2 Fe 3+ Ferredoxine de Peptococcus aerogenes

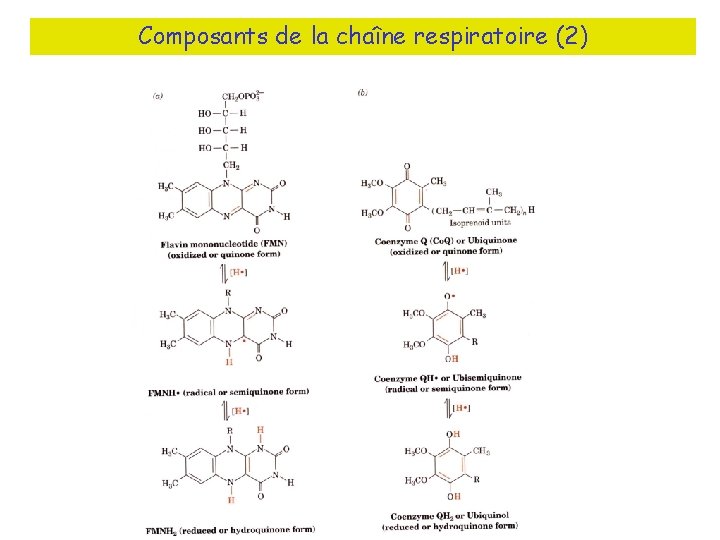
Composants de la chaîne respiratoire (2)

Composants de la chaîne respiratoire (3) • Les cytochromes – Cytochrome b (560 nm) – Cytochrome c (550 nm) – Cytochrome c 1 (553 nm, complex III) – Cytochrome a (600 nm, complex IV ou cytochrome oxidase) – Cytochrome a 3 (600 nm, complex IV ou cytochrome oxidase)

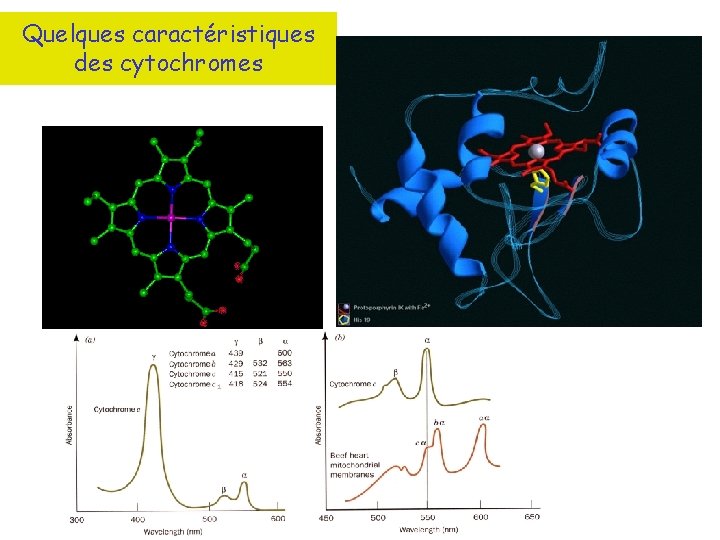
Quelques caractéristiques des cytochromes

Dans la chaîne respiratoire les porteurs d ’hydrogène et d ’électrons alternent • • Porteurs d ’hydrogène porteur + 2 H porteur -H 2 Porteurs d ’électrons porteur - Fe 3+ + H porteur -Fe 2+ + H+ Quand des porteurs d ’électrons sont réduits par des porteurs d ’hydrogène, des protons sont libérés Par contre, pendant la réduction des porteurs d ’hydrogènes par des porteurs d ’électrons, des protons sont utilisés

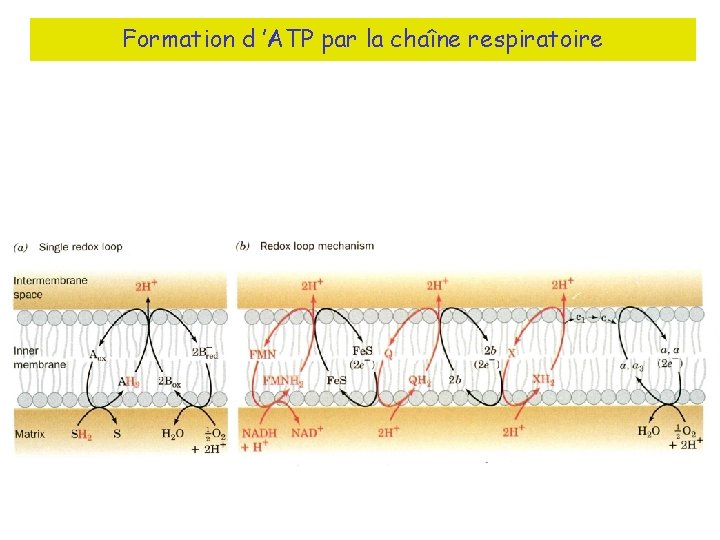
Formation d ’ATP par la chaîne respiratoire

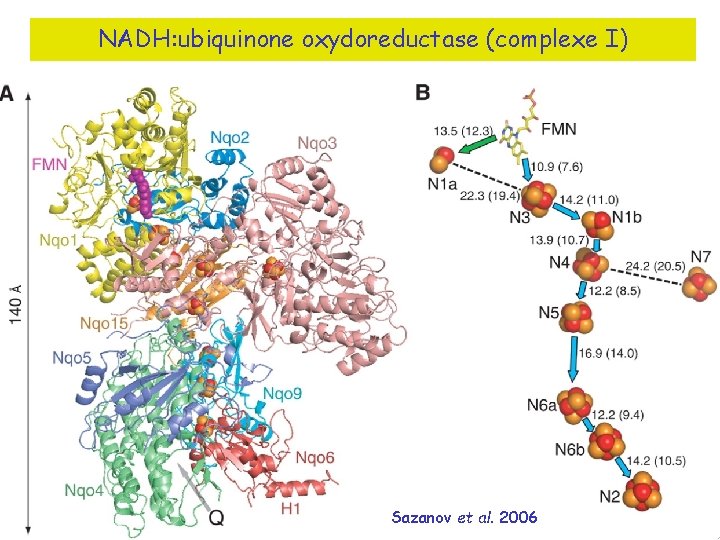
NADH: ubiquinone oxydoreductase (complexe I) Sazanov et al. 2006

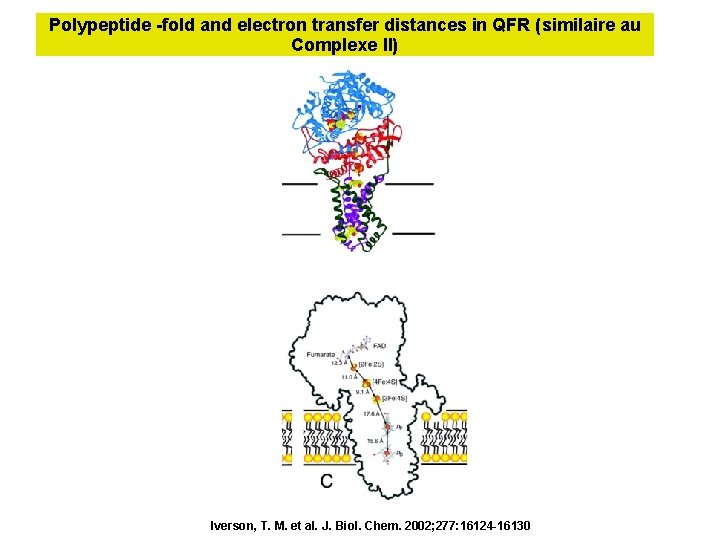
Polypeptide -fold and electron transfer distances in QFR (similaire au Complexe II) Iverson, T. M. et al. J. Biol. Chem. 2002; 277: 16124 -16130

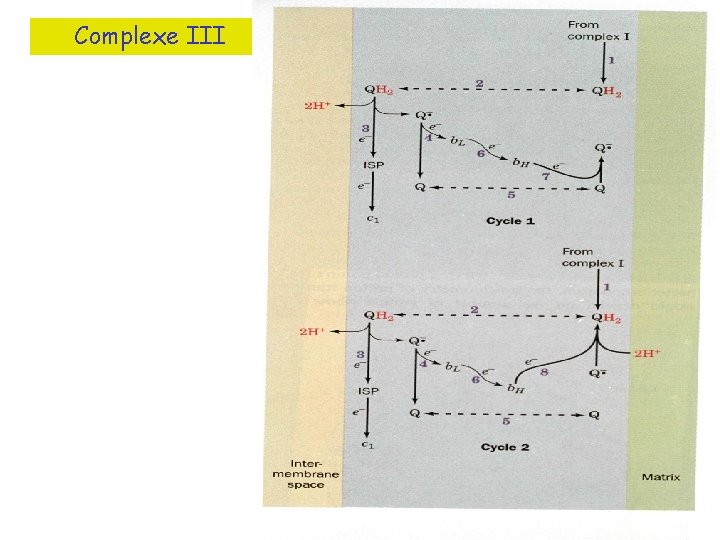
Complexe III

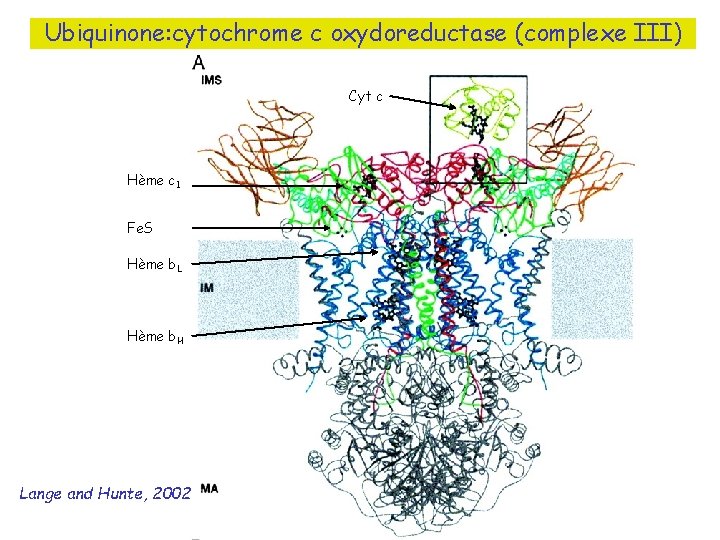
Ubiquinone: cytochrome c oxydoreductase (complexe III) Cyt c Hème c 1 Fe. S Hème b. L Hème b. H Lange and Hunte, 2002

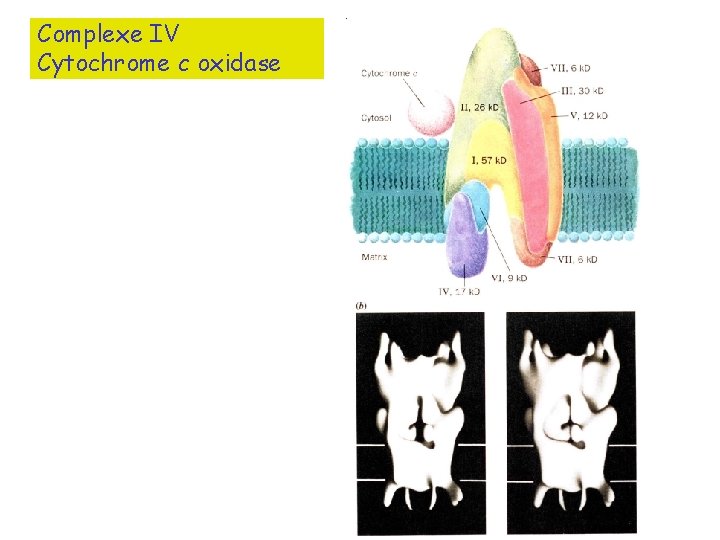
Complexe IV Cytochrome c oxidase

Le potentiel de réduction • Aréd • Box + 2 e • Aréd + Box Aox + 2 e. Bréd Aox + Bréd • ∆G°’ = -n. F∆E°’ • ∆E°’ = -2, 3 RT log Kéq Equation de Nernst n. F • ∆E = ∆E°’ -2, 3 RT log [Aox] [Bréd ] n. F • ∆E = ∆E°’ 0, 059 log. Q n [Aréd] [Box]

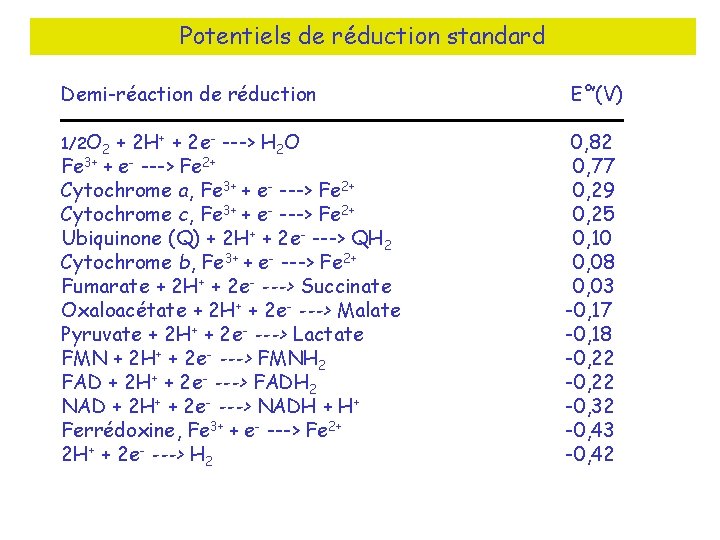
Potentiels de réduction standard Demi-réaction de réduction 1/2 O 2 + 2 H+ + 2 e- ---> H 2 O Fe 3+ + e- ---> Fe 2+ Cytochrome a, Fe 3+ + e- ---> Fe 2+ Cytochrome c, Fe 3+ + e- ---> Fe 2+ Ubiquinone (Q) + 2 H+ + 2 e- ---> QH 2 Cytochrome b, Fe 3+ + e- ---> Fe 2+ Fumarate + 2 H+ + 2 e- ---> Succinate Oxaloacétate + 2 H+ + 2 e- ---> Malate Pyruvate + 2 H+ + 2 e- ---> Lactate FMN + 2 H+ + 2 e- ---> FMNH 2 FAD + 2 H+ + 2 e- ---> FADH 2 NAD + 2 H+ + 2 e- ---> NADH + H+ Ferrédoxine, Fe 3+ + e- ---> Fe 2+ 2 H+ + 2 e- ---> H 2 E°’(V) 0, 82 0, 77 0, 29 0, 25 0, 10 0, 08 0, 03 -0, 17 -0, 18 -0, 22 -0, 32 -0, 43 -0, 42

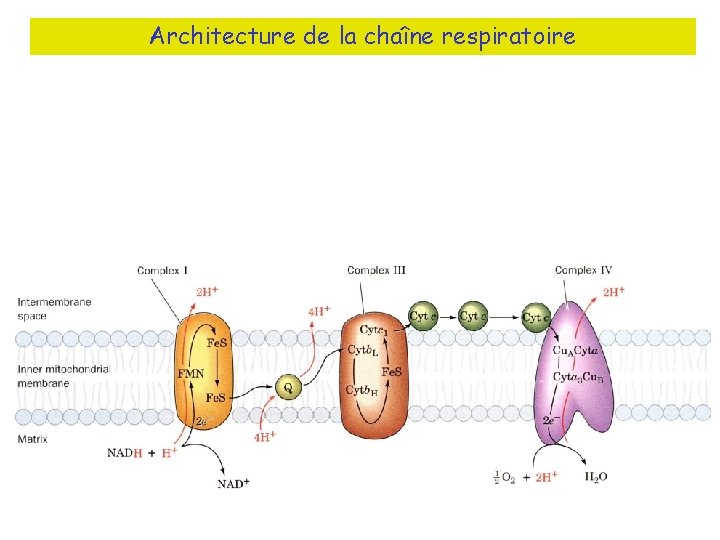
Architecture de la chaîne respiratoire

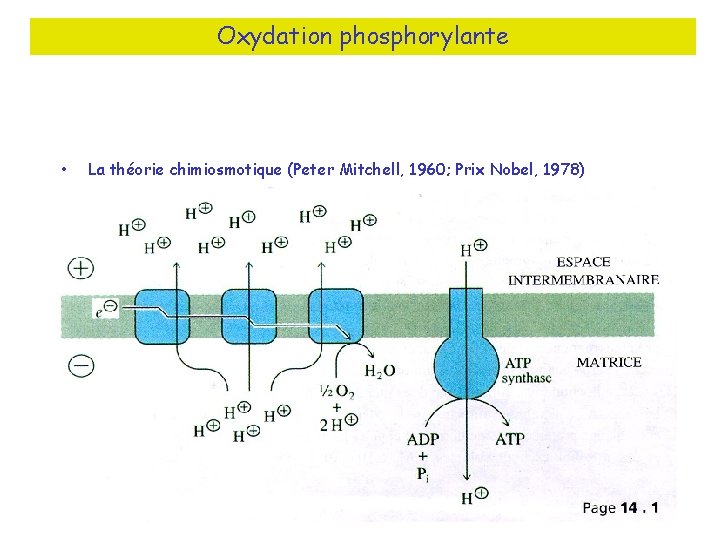
Oxydation phosphorylante • La théorie chimiosmotique (Peter Mitchell, 1960; Prix Nobel, 1978)

La force proton motrice ∆p est exprimé en volt • ∆Gchim = 2. 3 n RT (p. Hint-p. Hext) • ∆Gélec =n F∆ Y • ∆G = ∆ Gchim + ∆Gélec = 2. 3 n RT (∆p. H) + n F∆ Y • ∆G / n F = ∆ Y + (2. 3 RT (∆p. H) / F) • Z = 2. 3 RT /F • ∆p = ∆ Y + Z ∆p. H (Z = 59 m. V à 25°C)

La force proton motrice ∆p • DP consiste de deux composants: • 1. Le potentiel de membrane (Dy) • 2. Le gradient de protons (Dp. H) • Les valeurs typiques pour les mitochondries sont: p. H = 0, 75 Dy = 0, 14 V Dp = Dy + ZDp. H = 0, 14 V + (0, 059 V)x (0, 75) = 0, 18 V = 180 m. V • Chez E. coli (à p. H = 6) p. Hint = 7. 8 Dy = 95 m. V Dp = 200 m. V

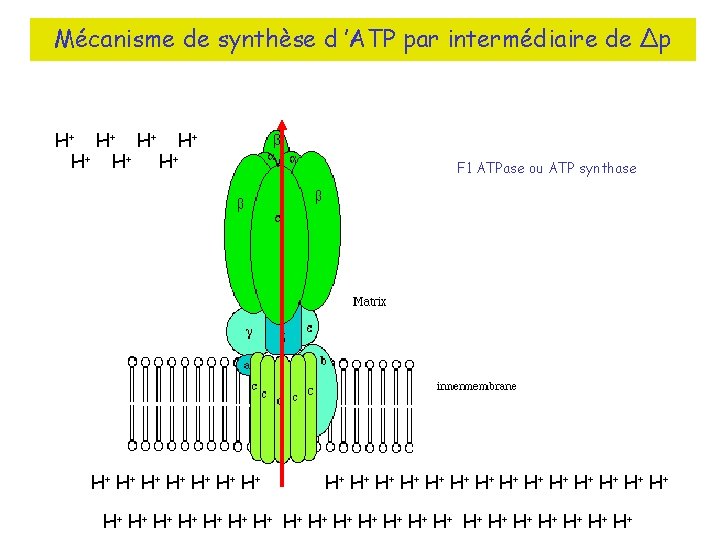
Mécanisme de synthèse d ’ATP par intermédiaire de ∆p H+ H + H + H + H + F 1 ATPase ou ATP synthase H+ H + H + H + H + H + H + H+ H + H + H +

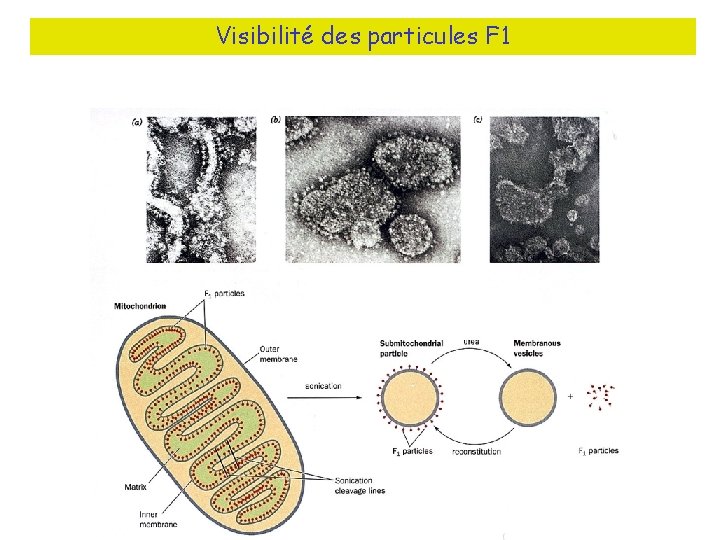
Visibilité des particules F 1

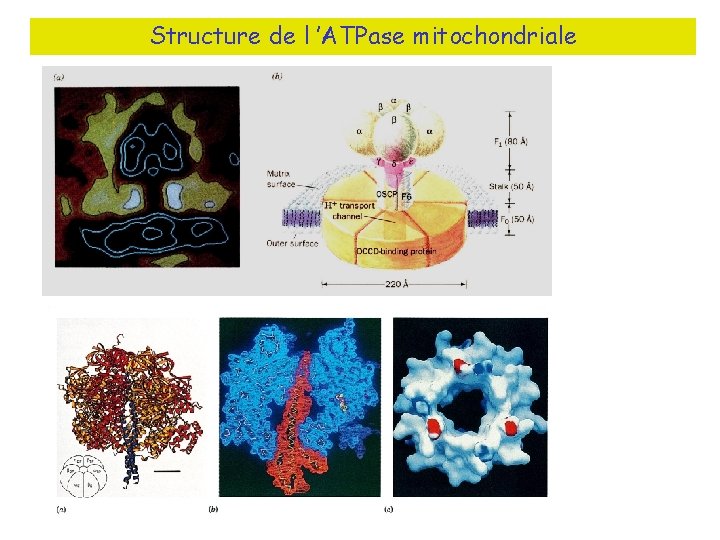
Structure de l ’ATPase mitochondriale

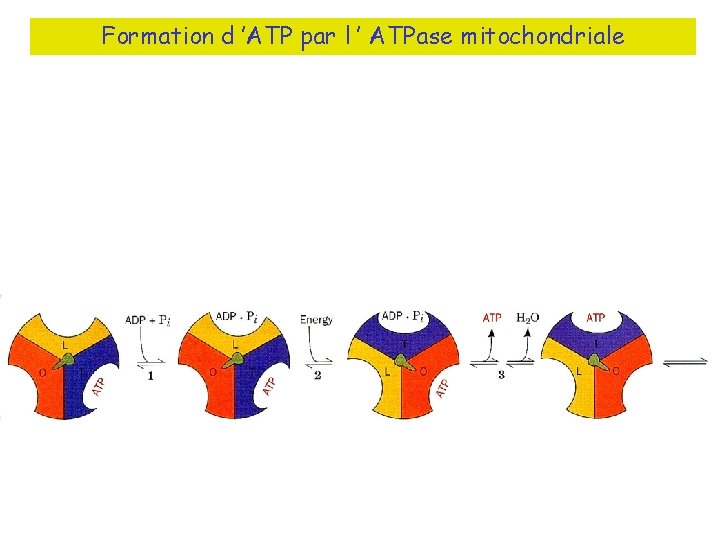
Formation d ’ATP par l ’ ATPase mitochondriale

Moteur moléculaire d’ATPase

An animation showing why the F 1 motor is rotating counter clockwise and how the chemical reaction and the rotation are coordinated by two switches: switch 1 (red) controls the ATP binding; switch 2 (blue) controls the phosphate release.

A perspective view of alpha 3 beta 3 gamma in spacefill display with specular highlights.

A perspective view of alpha 3 beta 3 gamma in cartoon display (frames are generated using Molscript).

GRT video of ATP synthase Available from You. Tube http: //www. youtube. com/watch? v=u. Oo. HKCMAUMc

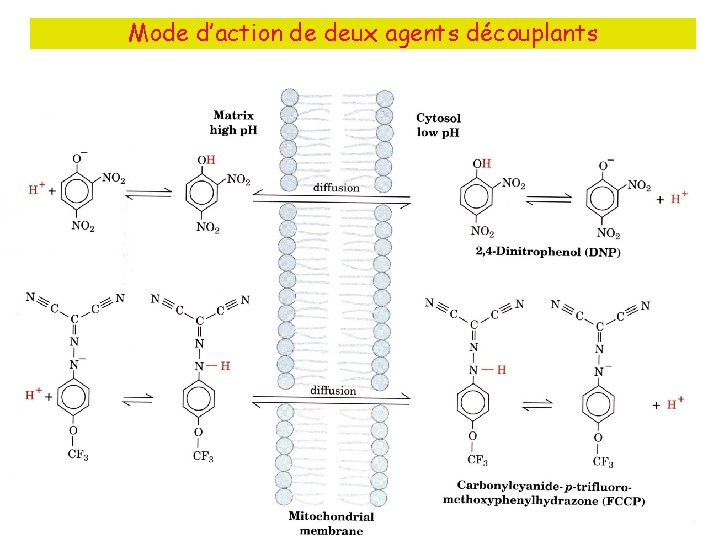
Mode d’action de deux agents découplants • Fig. 4. 12, 4. 13

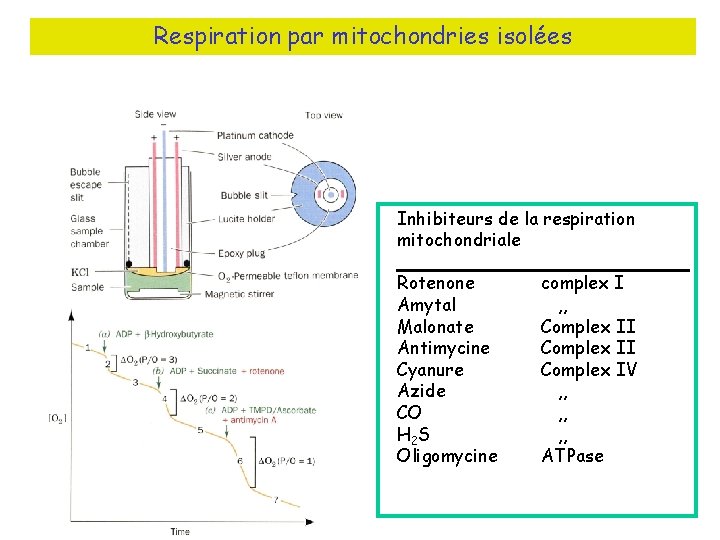
Respiration par mitochondries isolées Inhibiteurs de la respiration mitochondriale Rotenone Amytal Malonate Antimycine Cyanure Azide CO H 2 S Oligomycine complex I , , Complex II Complex IV , , , ATPase

Les systèmes navette assurant l ’oxydation du NADH du cytosol (1)

Les systèmes navette assurant l ’oxydation du NADH du cytosol (2)