Chalkogeny prvky VI A skupiny charakteristika nekovy kyslk



































































- Slides: 72

Chalkogeny – prvky VI. A skupiny • charakteristika: • nekovy: kyslík, síra, polokovy: selen, telur, kov: polonium • p – prvky - valenční elektrony mají v orbitalech s a p a to celkem 6 val. elektronů • elektronegativita jejich atomů roste od polonia ke kyslíku • v přírodě čisté, ale i v minerálech nebo horninách • jejich atomy reaktivní, do oktetu jim chybí pouze 2 elektrony, které získávají od atomu prvku se kterým vstupují do vazby

kyslík (8 O) • výskyt: • nejrozšířenější prvek na Zemi • volný prvek O 2, případně jako ozon O 3 • O 2 v zemské atmosféře tvoří 20, 948 objemových procent • slané, sladké vody • • fotosyntéza u zelených rostlinami začala asi před 2 500 000 let obsah O 2 v atmosféře dosáhl před 800 000 let asi 2% současného stavu a před 580 000 let asi 20% současného obsahu v atmosféře • ve sloučeninách ( jako voda a jako složka většiny hornin, minerálů a půd ) • biogenní prvek – v tělech rostlin a živočichů

• laboratorní příprava: • katalytickým rozkladem peroxidu vodíku pomocí poplatinované niklové folie 2 H 2 O 2 → O 2 + 2 H 2 O, Pt / Ni • tepelným rozkladem některých solí kyslíkatých kyselin 2 KCl. O 3 → 2 KCl + 3 O 2 • reakce probíhá za teploty 400 - 500 °C

• nejlepší metodou pro získání velmi čistého kyslíku je však tepelný rozklad manganistanu draselného ve vakuu • reakce probíhá při 215 až 235 °C • 2 KMn. O 4 → K 2 Mn. O 4 + Mn. O 2 + O 2 • průmyslová výroba: • frakční destilací zkapalněného vzduchu při teplotách okolo -183 °C

• fyzikální vlastnosti: • plyn bez barvy, zápachu a chuti, lehčí než vzduch • tuhý a kapalný kyslík mají modrou barvu • tvoří tři stabilní izotopy z nichž výrazně převládá 16 O, který tvoří více než 99, 73 hmotnostních %, ostatní, velmi vzácné izotopy jsou 17 O a 18 O • dopravuje se podobně jako vodík v ocelových bombách, označených modrým pruhem, stlačený na 15 MPa • existuje i atomární kyslík, vzniká elektrickým výbojem

kapalný kyslík

• chemické vlastnosti: • extrémně reaktivní plyn • přímo oxiduje mnoho prvků, buď při normální nebo při zvýšené teplotě • oxidační čísla v izolovatelných sloučeninách mohou mít hodnoty +1/2, 0, -1/3, -1/2, -1 a -2

ozón • nestálý namodralý plyn s ostrým zápachem, podle kterého byl poprvé zjištěn a podle kterého (z řeckého ozein = čichat, páchnout) jej pojmenoval v roce 1840 C. F. Schőnbein • cítíme jej při koncentraci 0, 003 ppm, při koncentraci vyšší než 0, 15 ppm způsobuje dýchací obtíže • při -111, 9°C kondenzuje na tmavomodrou kapalinu, při -192, 5°C černofialová pevná látka

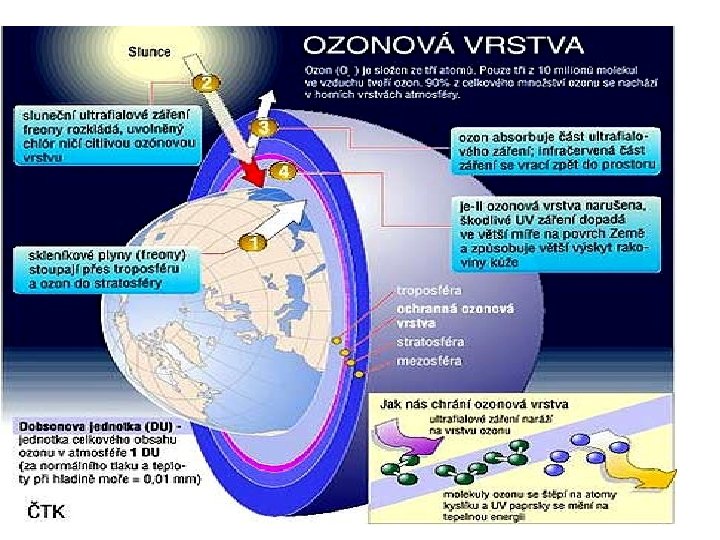
• připravuje se ze stlačeného a zchlazeného vzduchu nebo z kyslíku elektrickým výbojem • užívá se ke sterilizaci potravin a k desinfekci vody, k odstraňování pachů, k bělení papíru • silné oxidační vlastnosti • absorbuje UV záření - chrání povrch Země před intenzivním UV zářením Slunce

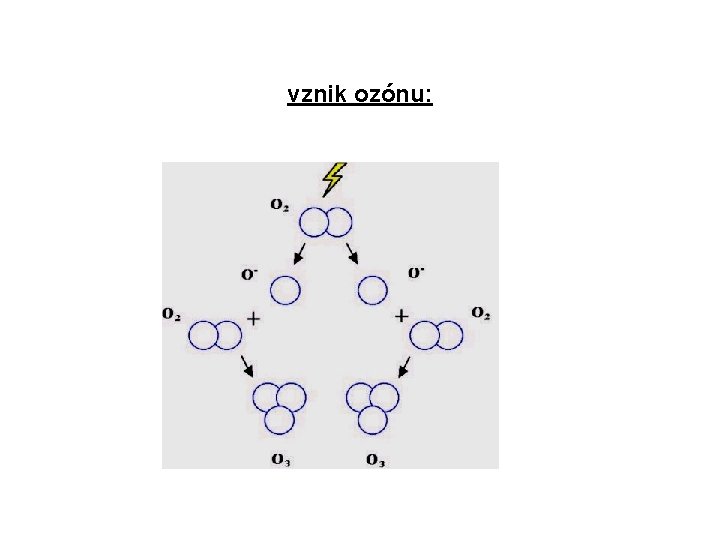
vznik ozónu:

atomární kyslík • příprava - působením elektrického výboje na O 2 za sníženého tlaku • reaktivnější než O 2

• využití dikyslíku: • • • autogenní sváření a řezání kovů dýchací přístroje a kyslíkové stany inhalace při otravách tavení železných a neželezných kovů v kapalném stavu pro pohon raket a kosmických lodí



• sloučeniny: • voda • ve třech skupenstvích, v krystalech ledu a v kapalné vodě jsou molekuly vody vázány vodíkovými můstky, mezi molekulami vodní páry vodík. můstky nejsou • obsažená v hydrátech solí (např. Fe. SO 4· 7 H 2 O, Cu. SO 4· 5 H 2 O)

• polární rozpouštědlo, rozpouští polární látky • bod varu vyšší, než odpovídá molární hmotnosti (způsobeno vodíkovými můstky mezi molekulami vody)

• voda se podle přítomnosti minerálních látek dělí na: a) měkkou – s minimálním obsahem rozpuštěných solí b) tvrdou • rozlišujeme: a) dočasnou tvrdost, která je způsobena hydrogenuhličitanovými anionty, např. hydrogenuhličitanem vápenatým, který se ve vodě rozpouští a dá se odstranit varem, vznikne z něj nerozpustný uhličitan vápenatý – tzv. kotelní kámen • 2(HCO 3)- → (CO 3)2 - + H 2 O + CO 2

• trvalá tvrdost je způsobena sírany hořečnatými a vápenatými, které se ve vodě nerozpouští • dá se odstranit sodou (Na 2 CO 3) nebo pomocí iontoměničů: • Ca 2+ + Na 2 CO 3 → Ca. CO 3↓ + 2 Na+

• peroxid vodíku • • poprvé připraven v roce 1818 J. L. Thenardem reakcí kyseliny sírové s peroxidem barnatým a odpařením nadbytečné vody za sníženého tlaku: Ba. O 2 + H 2 SO 4 → Ba. SO 4↓ + H 2 O 2(aq) průmyslově se vyrábí autooxidací 2 -ethylantrachinolu (30%) • bezbarvá kapalina • méně těkavá než voda • má větší hustotu a viskozitu než voda

peroxid vodíku – 3%, 12%, 30 %

• rozkládá se: 2 H 2 O 2(l) → 2 H 2 O(l) + O 2(g) inhibitor: močovina, kys. fosforečná katalyzátor: oxid manganičitý, stříbro, platina • využití: • oxidační i redukční činidlo, dezinfekce

• oxidy • • s výjimkou vzácných plynů jsou známé oxidy všech prvků periodické tabulky vlastnosti oxidů se mění v širokém rozmezí - od nesnadno kondenzovatelných plynů, jako je např. : oxid uhelnatý (teplota varu 191, 5 °C) až po netěkavé, těžkotavitelné oxidy, např. : oxid zirkoničitý (teplota varu 4850 °C) • z chemického hlediska dělíme oxidy na několik podskupin:

• kyselé: většinou oxidy nekovů (CO 2, SO 2, NO 2), pokud jsou ve vodě rozpustné, tak s ní reagují za vzniku kyselin • bazické: oxidy elektropozitivních prvků (Na 2 O, Ca. O) • amfoterní: oxidy méně elektropozitivních prvků (Be. O, Zn. O, Al 2 O 3) • neutrální: oxidy, které nereagují s vodou ani s vodnými roztoky kyselin nebo hydroxidů (CO, N 2 O)

• z hlediska vodivosti: • výborné isolanty (např. Mg. O) • polovodiče (např. Ni. O) • dobré vodiče (např. Re. O 3)

síra (16 S) • historie: • Síru znali již staří Řekové a Římané, od legendárního zničení Sodomy a Gomory sirným deštěm, až k nedávnému objevu, že síra spolu s kyselinou sírovou je hlavní složkou atmosféry planety Venuše. Egypťané znali síru již od 16. století před naším letopočtem a o použití hořící síry k desinfekci se lze dočíst i v Homérově Odysseji. V roce 1245 objevil Friar Bacon střelný prach, který se skládal z ledku, práškovitého dřevěného uhlí a síry. Poprvé byl použit v bitvě u Kresčaku. V roce 1746 zavedl John Roebuck výrobu kyseliny sírové v Anglii.

• výskyt: • čistá síra v sirných dolech (USA, Mexiko) • sulfan v ropě, zemním plynu • sulfidické minerály např. : pyrit, galenit, sfalerit, rumělka, sádrovec

krystaly kosočtverečné síry

nosiči síry - Indonésie

síra - Vesuv

• průmyslová výroba: • v první polovině 20. století – metodou vyvinutou H. Fraschem – vháněním přehřáté vodní páry do ložisek síry a vytlačováním zkapalněné síry horkým vzduchem na povrch • ze zemního plynu, který obsahuje 15 - 20% sulfanu a z ropy

• fyzikální vlastnosti: • • • síra má 4 stabilní izotopy 32 S, 33 S, 34 S a 36 S žlutá látka nerozpustná ve vodě dobře rozpustná např. v ethanolu dobrý tepelný a elektrický izolant vyskytuje se v několika formách:

• kosočtverečná síra, která je stálá při laboratorní teplotě • jednoklonná síra, která vzniká z kosočtverečné síry při teplotě 95 C • obě tyto formy mají v krystalech cyklické osmiatomové molekuly • zahříváním jednoklonné síry nad 119°C připravíme tzv. kapalnou síru (hustá, viskózní kapalina), jejímž dalším zahříváním vznikají hnědé páry síry • prudkým ochlazením těchto par vzniká sirný květ, který má podobu žlutého prášku • při prudkém ochlazení kapalné síry dostaneme síru plastickou, která však není stálá a postupně přechází na modifikaci kosočtverečnou molekuly plastické síry vytvářejí dlouhé polymerní řetězce, které jsou také příčinnou její plastičnosti •

• chemické vlastnosti: • síra hoří na vzduchu modrým plamenem za vzniku oxidu siřičitého a v malém množství i oxidu sírového • reaguje s kyselinami, které mají oxidační vlastnosti: S + 2 HNO 3 → H 2 SO 4 + 2 NO • reakcí s hydroxidy vzniká thiosíran a sulfid: 4 S + 6 KOH → K 2 S 2 O 3 + 2 K 2 S + 3 H 2 O

• využití: • • vulkanizace kaučuku výroba oxidu siřičitého výroba kyseliny sírové insekticidy, fungicidy, léčiva např. na kožní onemocnění

• sloučeniny: • sulfan – bezbarvý, nepříjemně páchnoucí plyn, velmi jedovatý, v sopečných plynech, v minerálních vodách, při rozkladu bílkovin – příprava - působením kyselin na sulfidy: Fe. S + 2 HCl → Fe. Cl 2 + H 2 S

• plynný H 2 S na vzduch hoří namodralým plamenem za vzniku oxidu siřičitého a vody: H 2 S + 3/2 O 2 → SO 2 + H 2 O • sulfan reaguje s vodou za vzniku kyseliny sulfanové • dvojsytná kyselina, která existuje pouze ve vodném roztoku – tvoří dva druhy solí: sulfidy a hydrogensulfidy

• sulfidy alkalických kovů alkalických zemin jsou rozpustné ve vodě, sulfidy těžkých kovů jsou nerozpustné a většinou barevné • oxidy • 13 oxidů síry

oxid siřičitý • vyrábí se spalováním síry nebo sulfanu: S + O 2 → SO 2 H 2 S + 3/2 O 2 → SO 2 + H 2 O • vzniká při spalování uhlí obsahující síru (znečišťování ovzduší) • bezbarvý jedovatý plyn, dusivého zápachu • dobře rozpustný ve vodě, reakcí s vodou vzniká vodný roztok „kyseliny siřičité“ • oxiduje se na oxid sírový: SO 2 + 1/2 O 2 → SO 3 (katalyzátor Pt nebo V 2 O 5)

• využití: – výroba kyseliny sírové – bělící činidlo – např. recyklovaného papíru (výroba novin ) – dezinfekční činidlo (vinařství) – konzervační činidlo v potravinářském průmyslu (výroba marmelád, sušeného ovoce, nealko nápojů)

• oxid sírový • připravuje se oxidací oxidu siřičitého: 2 SO 2 + O 2 → 2 SO 3 ( katalyzátor Pt nebo V 2 O 5 ) • meziprodukt při výrobě kyseliny sírové • s vodou reaguje za vzniku kyseliny sírové, s organickými látkami dochází k extrakci vody a k zuhelnatění organického materiálu

• kyselina siřičitá – příprava - zaváděním oxidu siřičitého do vody: SO 2 + H 2 O → H 2 SO 3 – pouze jako vodný roztok – silné redukční činidlo – tvoří dvě řady solí: siřičitany a hydrogensiřičitany

• kyselina sírová • bezbarvá olejovitá kapalina, neomezeně se mísí s vodou, je oxidačním činidlem, má dehydratační účinky – odebírá látkám vodu, zuhelnaťuje organické látky • má vysokou elektrickou vodivost – způsobenou autoprotolýzou: 2 H 2 SO 4 → (HSO 4)- + (H 3 SO 4)+

• zředěná kyselina oxiduje a rozpouští neušlechtilé kovy za vývoje vodíku: H 2 SO 4 + Zn → Zn. SO 4 + H 2 • horká koncentrovaná kyselina oxiduje a rozpouští některé ušlechtilé kovy: Cu + 2 H 2 SO 4 → Cu. SO 4 + SO 2 + 2 H 2 O • zlato, platina, olovo účinkům konc. H 2 SO 4 odolává

• využití: – výroba hnojiv – elektrolyt do akumulátorů

• tvoří dvě řady solí – sírany – hydrogensírany

• výroba: – kontaktní způsob – spalování síry: • S + O 2 → SO 2 – směs oxidu siřičitého a vzduchu prochází přes oxid vanadičný – žlutočerná pevná látka, která je katalyzátorem, reakce probíhá za teploty cca 450 C: – oxid vanadičný se vratně rozkládá na oxid vanidičitý a na kyslík, který reaguje s oxidem siřičitým: • 2 SO 2 + O 2 → 2 SO 3 – oxid sírový je rozpouštěn v konc. kyselině sírové, vzniká oleum – hustá, dýmavá kapalina, která se ředí vodou na požadovanou koncentraci kyseliny sírové: • SO 3 + konc. H 2 SO 4 → H 2 S 2 O 7

kyselina sírová používaná do akumulátorů v automobilech

oxid vanadičný




likvidace úniku kyseliny sírové

• sírany – příprava • rozpouštěním kovu ve vodném roztoku kyseliny: Fe + H 2 SO 4 → Fe. SO 4 + H 2 • reakcí kyseliny s oxidy nebo hydroxidy kovů: 2 Na. OH + H 2 SO 4 → Na 2 SO 4 + 2 H 2 O Zn. O + H 2 SO 4 → Zn. SO 4 + H 2 O – většina síranů je ve vodě dobře rozpustná, jsou to krystalické látky

• kyselina peroxodisírová – bezbarvá pevná látka – soli: peroxodisírany - oxidační a bělící činidla

• kyselina thiosírová • nestálá látka • soli: thiosírany – silnější oxidační činidla oxidují thiosíran až na hydrogensíran: (S 2 O 3)2 - + 4 Cl 2 + 5 H 2 O → 2(HSO 4)- + 8 HCl – tato reakce se využívá při odstraňování přebytku chlóru z vlákna při průmyslovém bělení • hydratovaný thiosíran sodný (Na 2 S 2 O 3 · 10 H 2 O) – bílá krystalická látka – snadno rozpustná ve vodě

• kyselina peroxosírová (Carova) – silná jednosytná kyselina – bezbarvá krystalická látka

selen (34 Se) • výskyt: • ve formě minerálů, tyto minerály se vyskytují v přírodě společně s minerály obsahujícími síru

• fyzikální vlastnosti: • polokov, pevná krystalická látka, v různých formách, např. šedý, černý nebo červený selen, nerozpustný ve vodě – 3 červené monoklinické polymorfní formy červený selen (alfa, beta, gama), z kruhů Se 8 – šedá „kovová“ - hexagonální krystalická forma – červený amorfní - spirálové poněkud deformované řetězce – sklovitý černý selen - nejdostupnější modifikace, má strukturu složenou z kruhů, které obsahují až tisíc atomů v jednom kruhu

• v roce 1957 zjištěno, že selen má v organizmu lidí a zvířat esenciální význam pro tvorbu enzymu glutathionperoxidázy • tento enzym katalyzuje reakce, ve kterých jsou likvidovány volné radikály různých látek v organismu • volný radikál je atom nebo molekula látky, které obsahují jeden nebo více nespárovaných elektronů • volné radikály látek působí destruktivně např. na membrány buněk v těle apod. • nejvíce selenu obsahují mořské ryby a para ořechy


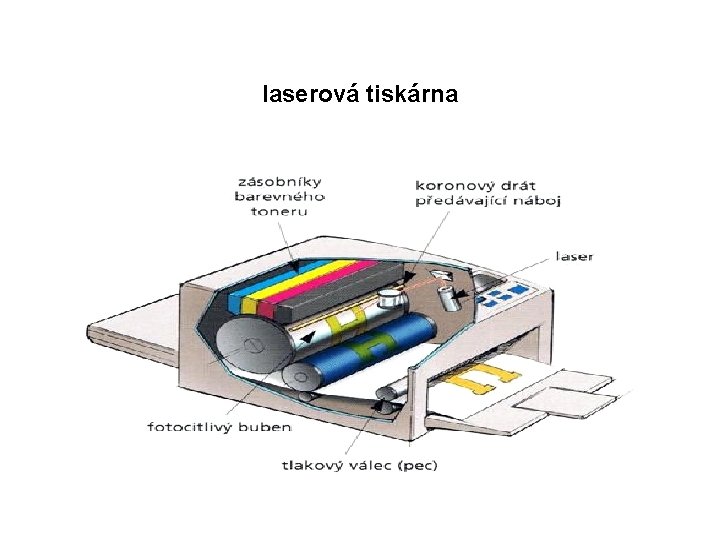
• využití: • výroba fotočlánků – ve fotočlánku jsou atomy selenu schopny uvolňovat elektrony po ozáření viditelným světlem, fotočlánek se tak stává zdrojem el. energie • fotočlánky se využívají v solárních panelech, v kopírkách • selen se také využívá pro výrobu světlocitlivého válce v laserových tiskárnách

Od roku 1998 obíhá na oběžné dráze ve výšce kolem 400 km mezinárodní vědecká stanice ISS .


elektrárna využívající solární panely (Bavorsko)

laserová tiskárna

polonium (84 Po) • historie: • • Marie Curie-Sklodowská v roce 1898 izolovala dva prvky ze smolince, jeden prvek pojmenovala podle své vlasti polonium, druhý podle vlastnosti (radioaktivity) radium za tento objev získala v roce 1911 Nobelovu cenu za chemii • výskyt: • polonium se vzhledem ke svému krátkému poločasu rozpadu v přírodě téměř nevyskytuje • • v přírodě v uranových rudách se vyskytuje pouze izotop 210 Po je těkavé, má krátký poločas rozpadu, takže uranové rudy jej obsahují pouze 0, 1 mg v 1 t rudy

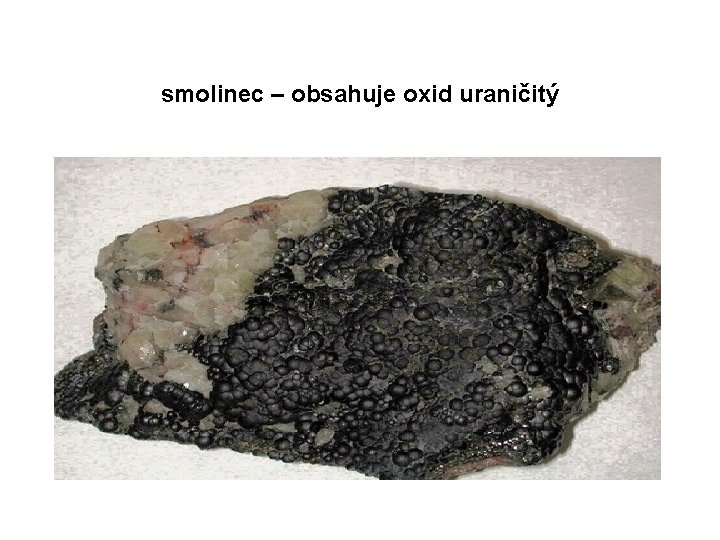
smolinec – obsahuje oxid uraničitý

• průmyslová výroba: • prakticky veškeré znalosti o fyzikálních a chemických vlastnostech tohoto prvku byly získány studiem izotopu 210 Po, který se nejsnadněji připraví v jaderném reaktoru bombardováním 209 Bi neutrony: • 209 Bi(n; γ) → 210 Bi →(β) 210 Po →(α) 206 Pb

• fyzikální vlastnosti: • • kovový prvek tvoří stříbřité bílé krystaly větší elektrická vodivost než u telluru nemá žádný stabilní izotop

vzorek polonia

• chemické vlastnosti: • všechny sloučeniny polonia by měly být považovány za potencionálně toxické • • usazuje se v ledvinách, slezině a játrech a již v nepatrných koncentracích způsobují bolesti hlavy, nevolnosti, zvracení a podráždění sliznic; maximálně povolená dávka nejběžnějšího izotopu 210 Po pro lidské tělo je 7. 10 -12 g koncentrace sloučenin polonia ve vzduchu musí být nižší než 4· 10 -11 mg·m-3
