Chalkogeny Prvky 16 skupiny Obecn charakteristika Nzev Kyslk

Chalkogeny Prvky 16. skupiny
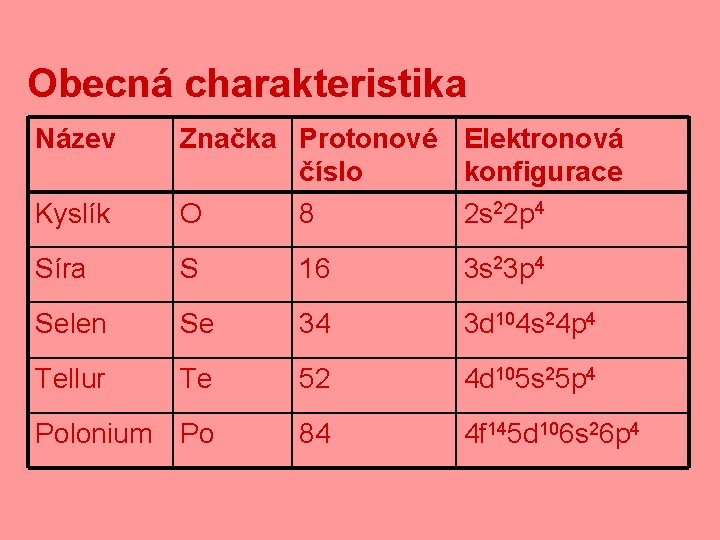
Obecná charakteristika Název Kyslík Značka Protonové Elektronová číslo konfigurace O 8 2 s 22 p 4 Síra S 16 3 s 23 p 4 Selen Se 34 3 d 104 s 24 p 4 Tellur Te 52 4 d 105 s 25 p 4 Polonium Po 84 4 f 145 d 106 s 26 p 4

Kyslík • Nejrozšířenější prvek na zemi • Má 3 izotopy , • Výskyt • V atmosféře-dvouatomové molekuly O 2 nebo trojatomových molekul jako ozon O 3 • Vázaný je součástí anorganických (vody, hornin) a organických (sacharidy, aminokyseliny) sloučenin • Biogenní prvek, nezbytný k dýchání organismů
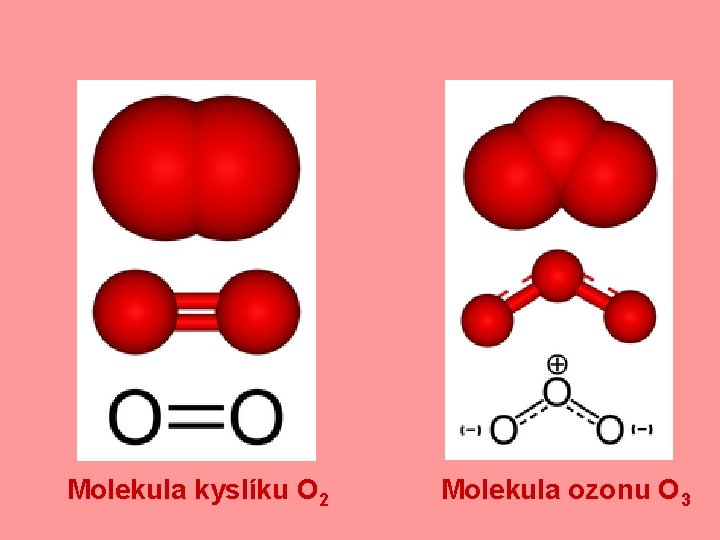
Molekula kyslíku O 2 Molekula ozonu O 3

Vlastnosti • Bezbarvý plyn, bez chuti, zápachu, těžší než vzduch, omezeně rozpustný ve vodě • Molekulový kyslík je velmi reaktivní • Silné oxidační činidlo, oxidační reakce mohou být rychlé (hoření) nebo pomalé (práchnivění dřeva) • Ve sloučeninách nejčastěji dvojvazný • Ozon O 3 je jedovatý plyn modré barvy, má silné oxidační účinky, vzniká účinkem UV záření nebo elektrických výbojů (blesk při bouřce), molekuly O 2 se rozštěpí na O a ty se opět slučují s molekulami O 2

Příprava • Tepelným rozkladem některých kyslíkatých sloučenin 2 KMn. O 4 ------ K 2 Mn. O 4 + Mn. O 2 + O 2 • Elektrolýzou vody, vyloučí se na anodě 4 OH- - 4 e- ------ 2 H 2 O + O 2 • Reakcí burelu s kyselinou sírovou Výroba • Frakční destilací zkapalněného vzduchu • Elektrolýzou vody

Použití • Stlačený vzduch se dodává v ocelových tlak. lahvích označených modrým pruhem • V hutnictví • Při sváření a řezání kovů • V chemické výrobě • Dýchací přístroje v lékařství, pro horníky, letce • Kapalný kyslík je raketové palivo • Ozon se používá k dezinfekci vzduchu a pitné vody (usmrcuje organismy)

Sloučeniny kyslíku Oxidy • Dvouprvkové sloučeniny, ox. číslo –II, • Oxidy přechodných prvků jsou barevné (Cr 2 O 3 zelený, Cu 2 O červený) • Připravují se přímým slučováním prvků C + H 2 O ------ CO + H 2
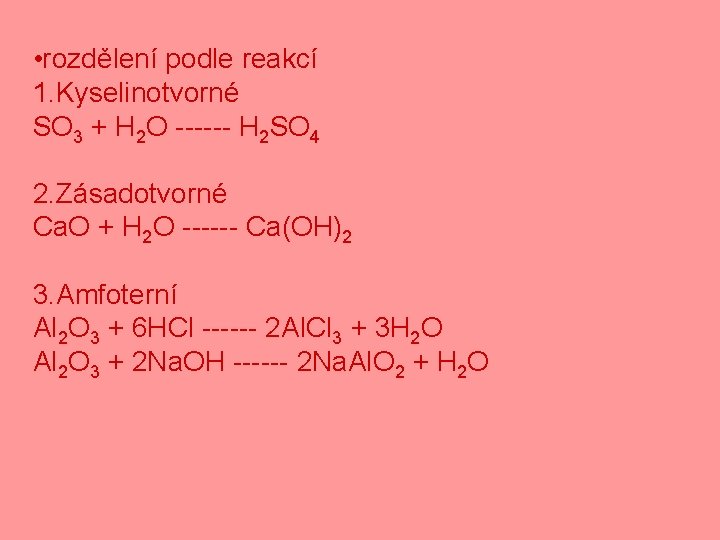
• rozdělení podle reakcí 1. Kyselinotvorné SO 3 + H 2 O ------ H 2 SO 4 2. Zásadotvorné Ca. O + H 2 O ------ Ca(OH)2 3. Amfoterní Al 2 O 3 + 6 HCl ------ 2 Al. Cl 3 + 3 H 2 O Al 2 O 3 + 2 Na. OH ------ 2 Na. Al. O 2 + H 2 O

Peroxid vodíku H 2 O 2 • Patří mezi peroxysloučeniny-látky obsahující 2 atomy kyslíku, z nichž každý má ox. číslo –I • Bezbarvá olejovitá kapalina, v bezvodém stavu výbušná • Polární rozpouštědlo • S vodou neomezeně mísitelný • Jeho 3 % roztok se používá jako bělící a dezinfekční činidlo • Účinkem světla některých látek se snadno rozkládá na H 2 O a O

• Se silnými ox. činidly působí jako redukční činidlo • Ve vodě se chová jako slabá kyselina H 2 O 2 + H 2 O ------ H 3 O+ + OH 2 - (peroxidový aniont)

Síra • Má 4 izotopy • Výskyt • A)Volná-sopečného původu, příměs v uhlí • B)Vázaná ve sloučeninách-anorganické (sulfidy, sírany, sulfan, rumělka), organické (bílkoviny) • Biogenní prvek

Vlastnosti • Žlutá, křehká, krystalická látka, nekov • Nerozpustná ve vodě, rozpustná v nepolárních rozpouštědlech • Vyskytuje se v několika modifikacích: 1. Krystalická-podle uspořádání 8 -atomových molekulkosočtverečná jednoklonná • 2. Amorfní-v podobě sirného květu (rychlé ochlazení jejích par) nebo v podobě plastické síry (rychlé ochlazení její taveniny)

• Za běžné teploty stálá, při vyšších teplotách reaguje s kovy i nekovy S + O 2 ------ SO 2 S + Fe ------ Fe. S • Vyskytuje se v několika modifikacích: 1. Krystalická-podle uspořádání 8 -atomových molekulkosočtverečná jednoklonná • 2. Amorfní-v podobě sirného květu (rychlé ochlazení jejích par) nebo v podobě plastické síry (rychlé ochlazení její taveniny) • Za běžné teploty stálá, při vyšších teplotách reaguje s kovy i nekovy S + O 2 ------ SO 2 S + Fe ------ Fe. S

Příprava a výroba • Těží se • Získává se pražením sulfidů nebo z technických plynů Použití • Při výrobě pryže z kaučuku, zápalek, střelného prachu, pesticidů • Základní surovina k výrobě kyseliny sírové, sulfanu, sulfidů a siřičitanů

Sloučeniny síry Sulfan H 2 S • Dříve sirovodík • Bezbarvý, nepříjemně páchnoucí a prudce jedovatý plyn • Redukční vlastnosti • Zapálením na vzduchu hoří namodralým plamenem za vzniku SO 2 nebo S • Vzniká při rozkladu bílkovin nebo reakcí sulfidů s kyselinami Fe. S + 2 HCl ------ Fe. Cl 2 + H 2 S

• Rozpouštěním sulfanu ve vodě vzniká kys. sirovodíková (sulfanová nebo sirovodíková voda)

Sulfidy • Charakteristicky zbarvené, používají se jako pigmenty • Pražení při výrobě kovů-zahřívání sulfidů na vzduchu vzniká oxid kovu (nebo kov) a SO 2 Oxidy SO 2 • Bezbarvý, jedovatý plyn, podílí se na vzniku kyselých dešťů • Vzniká spalováním síry a vrábí se pražením sulfidů

• Redukční činidlo, používá se k výrobě kys. sírové, odbarvování, při výrobě celulózy SO 3 • Pevná látka (cyklické molekuly) nebo plyn (jednoduché molekuly) • Oxidační činidlo • Vyrábí se oxidací SO 2 • Reaguje s vodou za vzniku kys. sírové

Kyseliny H 2 SO 3 • Slabá kyselina, redukční vlastnosti • Tvoří 2 řady solí-siřičitany SO 3 -2 hydrogensiřičitany HSO 3 -1

H 2 SO 4 • Silná kyselina, mísitelná s vodou za uvolňování tepla (kyselina do vody) • 1. Koncentrovaná-silné oxidační a dehydratační účinky, reaguje se všemi kovy kromě olova, zlata a platiny Cu + H 2 SO 4 ------ Cu. O + SO 2 + H 2 O 2. Zředěná-ox. schopnosti ztrácí a reaguje pouze s méně ušlechtilými kovy Fe + H 2 SO 4 ------ Fe. SO 4 + H 2

• Výroba kontaktnm způsobem S + O 2 ------ SO 2 + O 2 ------ SO 3 + H 2 O ------ H 2 SO 4 • Základní surovina chem. průmyslu, výroba hnojiv, anorg. sloučenin, barviv, léčiv, výbušnin, plastů atd. • Tvoří 2 řady solí-sírany SO 4 -2 hydrogensírany HSO 4 -1

Selen, Tellur, Polonium • Nevýznamné prvky

KONEC Vypracovala: Sandra Šandová
- Slides: 24