CH HIROCACBON KHNG NO III TNH CHT HA

CHỦ ĐỀ HIĐROCACBON KHÔNG NO
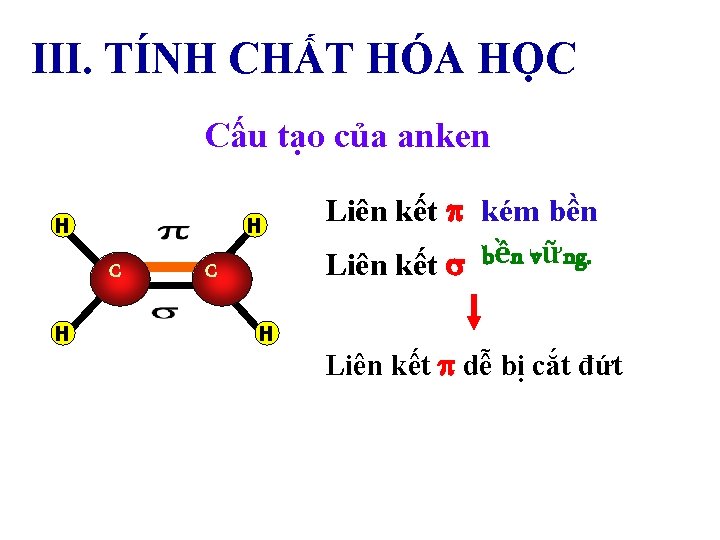
III. TÍNH CHẤT HÓA HỌC Cấu tạo của anken H H C H Liên kết kém bền Liên kết bền vững. Liên kết dễ bị cắt đứt
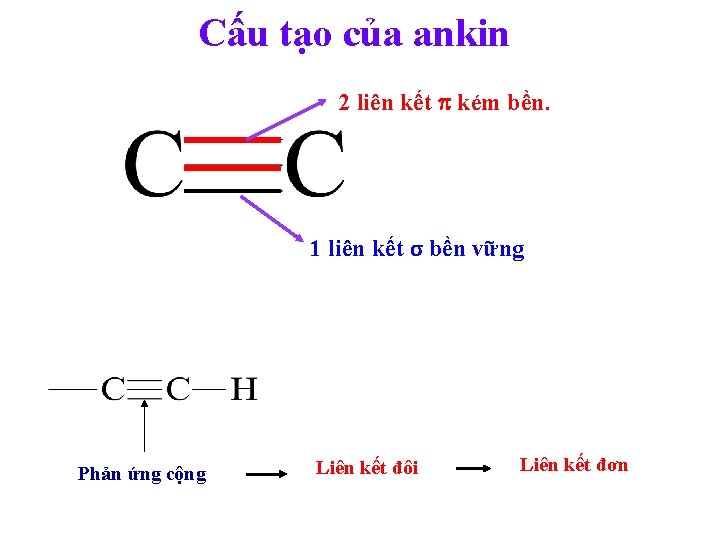
Cấu tạo của ankin 2 liên kết kém bền. 1 liên kết σ bền vững Phản ứng cộng Liên kết đôi Liên kết đơn

Liên kết kém bền nên dễ bị cắt đứt, gây nên tính chất hóa học đặc trưng của hiđrocacbon không no: dễ tham gia phản ứng cộng, tạo thành hợp chất no tương ứng. 1. Phản ứng cộng của anken
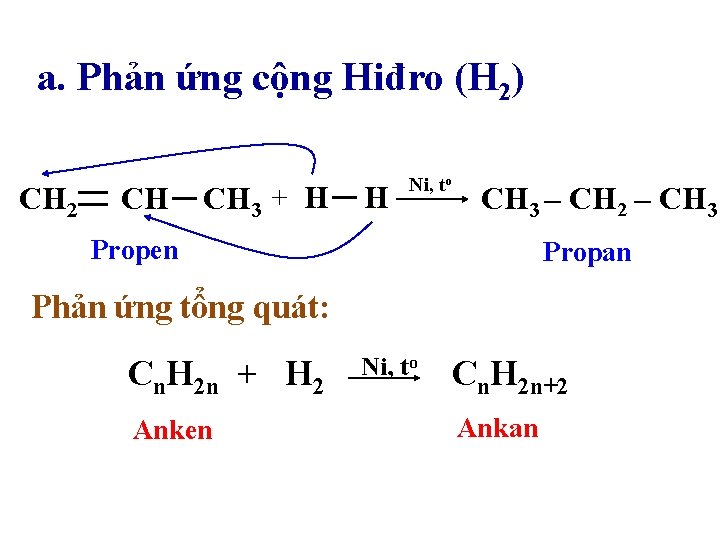
a. Phản ứng cộng Hiđro (H 2) CH 2 CH CH 3 + H H Ni, to CH 3 – CH 2 – CH 3 Propen Propan Phản ứng tổng quát: Cn. H 2 n + H 2 Anken Ni, to Cn. H 2 n+2 Ankan

b. Cộng Halogen (X 2) Thí nghiệm: Hiện tượng: Anken làm mất màu dung dịch brom. Phương trình phản ứng: CH 2 = CH 2 + Br 2 CH 2 Br – CH 2 Br Phản ứng này dùng để nhận biết anken.
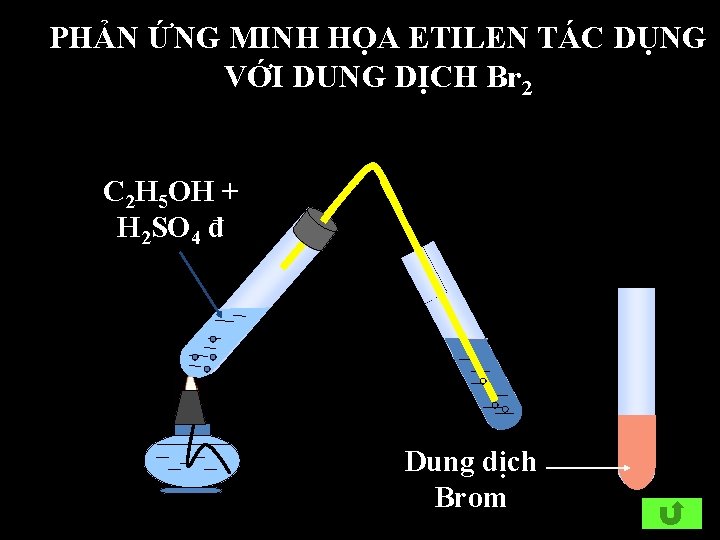
PHẢN ỨNG MINH HỌA ETILEN TÁC DỤNG VỚI DUNG DỊCH Br 2 C 2 H 5 OH + H 2 SO 4 đ Dung dịch Brom

c. Cộng HX ( X là OH, Br, Cl) Các anken cũng tham gia phản ứng cộng với nước (H 2 O), với hiđro halogen (HCl, HBr, HI), với các axit mạnh. Quy tắc cộng Mac-côp-nhi-côp Trong phản ứng cộng HX vào liên kết đôi, nguyên tử H cộng vào nguyên tử cacbon có nhiều H hơn, còn X cộng vào nguyên tử cacbon có ít H hơn.
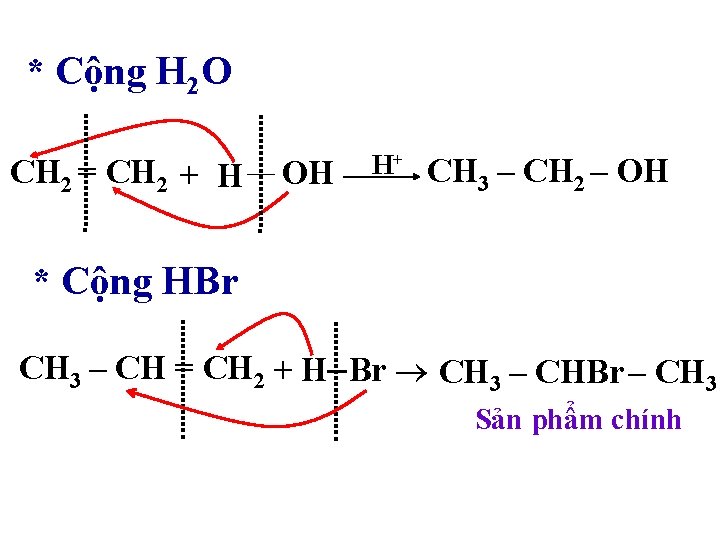
* Cộng H 2 O CH 2 = CH 2 + H OH H+ CH 3 – CH 2 – OH * Cộng HBr CH 3 – CH = CH 2 + H– Br CH 3 – CHBr – CH 3 Sản phẩm chính
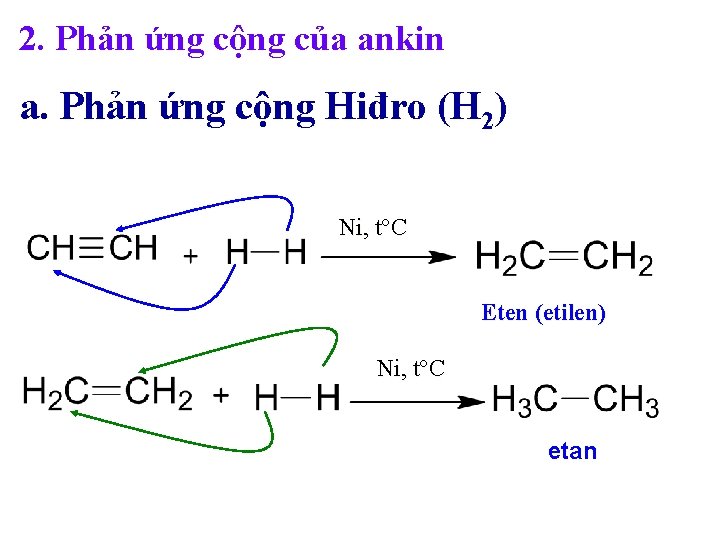
2. Phản ứng cộng của ankin a. Phản ứng cộng Hiđro (H 2) Ni, t°C Eten (etilen) Ni, t°C etan
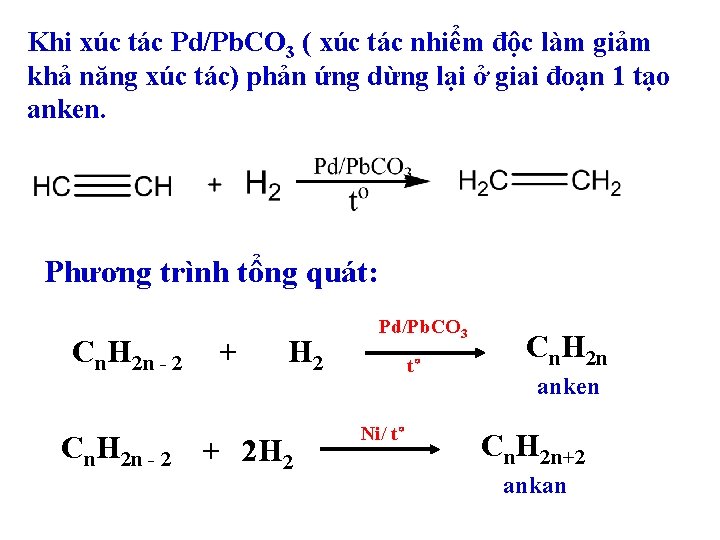
Khi xúc tác Pd/Pb. CO 3 ( xúc tác nhiểm độc làm giảm khả năng xúc tác) phản ứng dừng lại ở giai đoạn 1 tạo anken. Phương trình tổng quát: Cn. H 2 n - 2 + H 2 Cn. H 2 n - 2 + 2 H 2 Pd/Pb. CO 3 t° Ni/ t° Cn. H 2 n anken Cn. H 2 n+2 ankan

b. Phản ứng cộng Brom (Br 2) Thí nghiệm: Dẫn khí axetilen sục vào dung dịch brom.
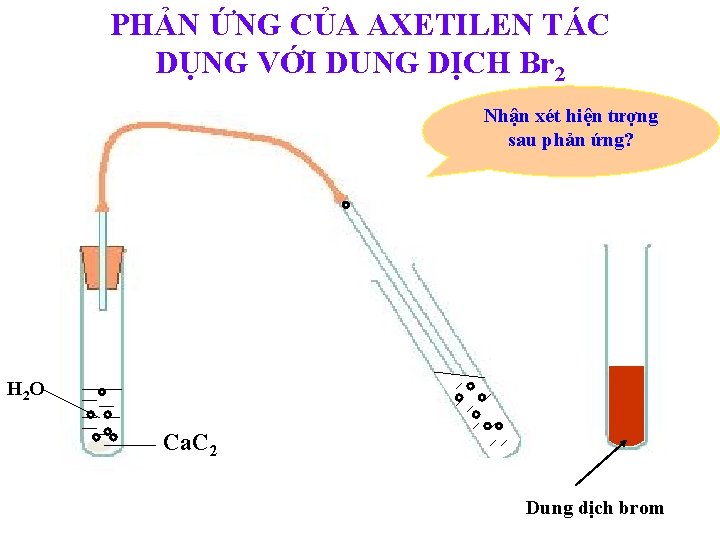
PHẢN ỨNG CỦA AXETILEN TÁC DỤNG VỚI DUNG DỊCH Br 2 Nhận xét hiện tượng sau phản ứng? H 2 O Ca. C 2 Dung dịch brom
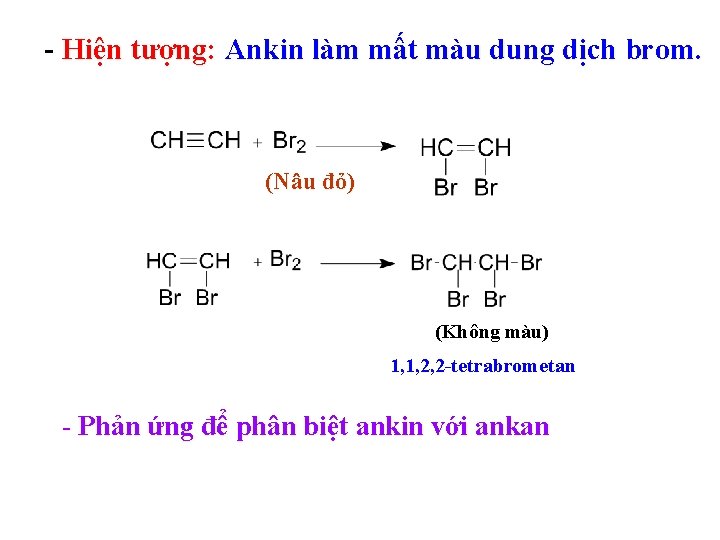
- Hiện tượng: Ankin làm mất màu dung dịch brom. (Nâu đỏ) (Không màu) 1, 1, 2, 2 -tetrabrometan - Phản ứng để phân biệt ankin với ankan
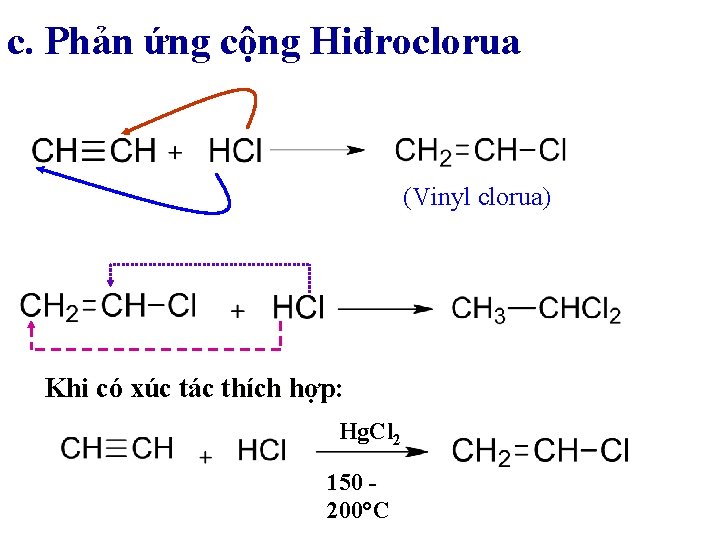
c. Phản ứng cộng Hiđroclorua (Vinyl clorua) Khi có xúc tác thích hợp: Hg. Cl 2 150 200°C
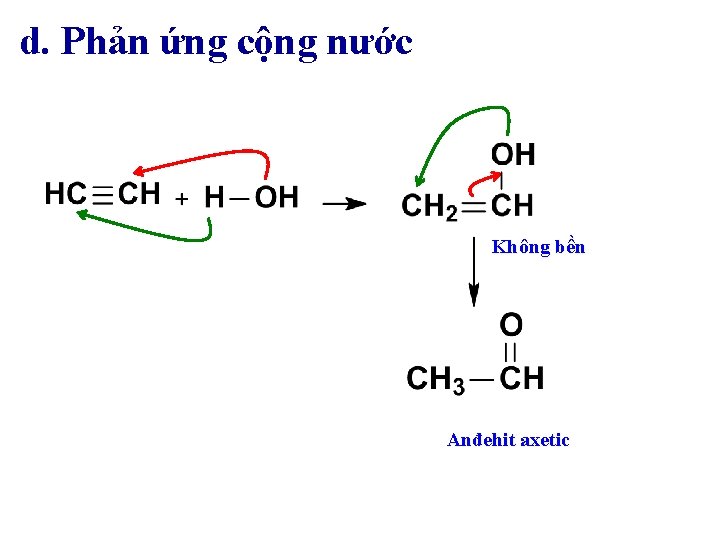
d. Phản ứng cộng nước Không bền Anđehit axetic

3. Phản ứng cộng của ankađien : 1 2 3 4 C=C–C=C Tùy theo nhiệt độ và tỉ lệ mol giữa các chất, Buta-1, 3 -đien cho các sản phẩm cộng khác nhau (theo tỉ lệ mol 1: 1) hoặc sản phẩm cộng vào cả 2 nối đôi (theo tỉ lệ mol 1: 2). a. Cộng hiđro (phản ứng hiđro hóa) CH 2=CH-CH=CH 2 + 2 H 2 Buta-1, 3 -đien PT tổng quát: Cn. H 2 n-2 + 2 H 2 CH 3–CH 2–CH 3 Butan Cn. H 2 n + 2

b. Cộng Brom 4 3 2 1 Cộng 1, 2: CH 2=CH-CH=CH 2 + Br 2 4 3 2 1 Br Br CH 2=CH – CH - CH 2 (Sản phẩm chính) 4 3 2 1 Cộng 1, 4: CH 2=CH-CH=CH 2 + Br 2 4 3 2 CH 2 -CH = CH - CH 2 Br Br (Sản phẩm chính) Cộng đồng thời vào hai liên kết đôi: CH 2=CH-CH=CH 2 + 2 Br 2 1 CH 2 - CH 2 Br Br
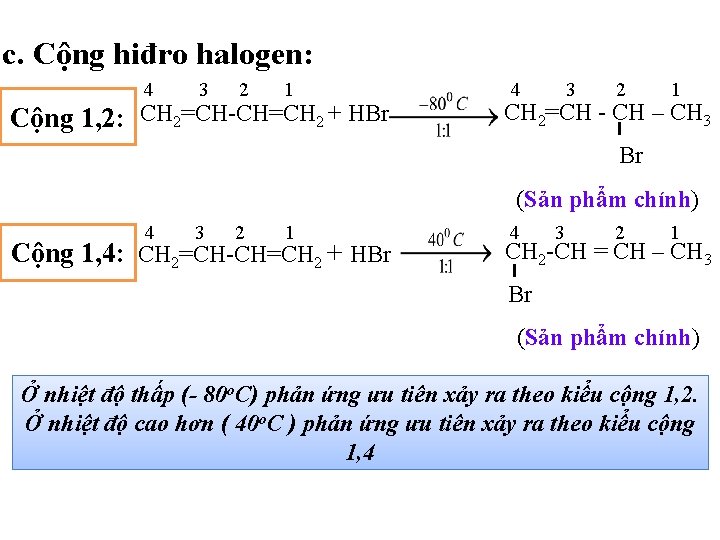
c. Cộng hiđro halogen: 4 3 2 1 Cộng 1, 2: CH 2=CH-CH=CH 2 + HBr 4 3 2 1 CH 2=CH - CH – CH 3 Br (Sản phẩm chính) 4 3 2 1 Cộng 1, 4: CH 2=CH-CH=CH 2 + HBr 4 3 2 1 CH 2 -CH = CH – CH 3 Br (Sản phẩm chính) Ở nhiệt độ thấp (- 80 o. C) phản ứng ưu tiên xảy ra theo kiểu cộng 1, 2. Ở nhiệt độ cao hơn ( 40 o. C ) phản ứng ưu tiên xảy ra theo kiểu cộng 1, 4

4. Phản ứng trùng hợp: a. Phản ứng trùng hợp của anken : Phương trình: n. CH 2 = CH 2 t 0, P, xt CH 2 n Phản ứng trùng hợp là quá trình kết hợp liên tiếp nhiều phân tử nhỏ giống nhau hoặc tương tự nhau tạo thành những phân tử rất lớn (gọi là polime).
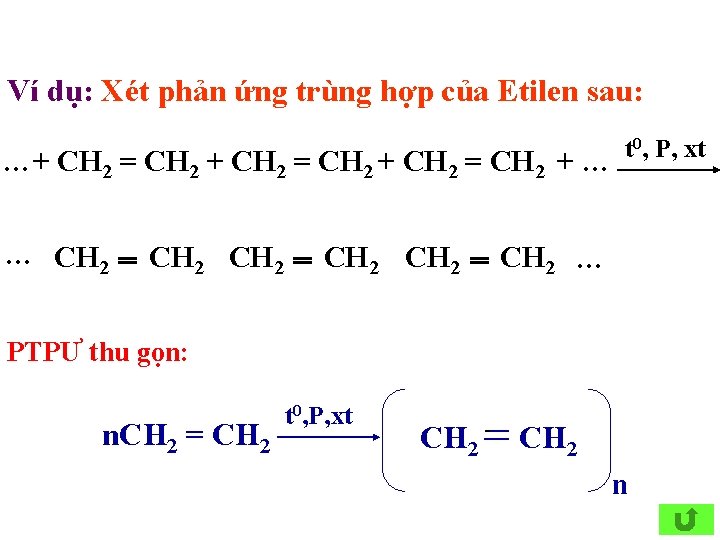
Ví dụ: Xét phản ứng trùng hợp của Etilen sau: …+ CH 2 = CH 2 + … … CH 2 CH 2 t 0, P, xt CH 2 … PTPƯ thu gọn: n. CH 2 = CH 2 t 0, P, xt CH 2 n
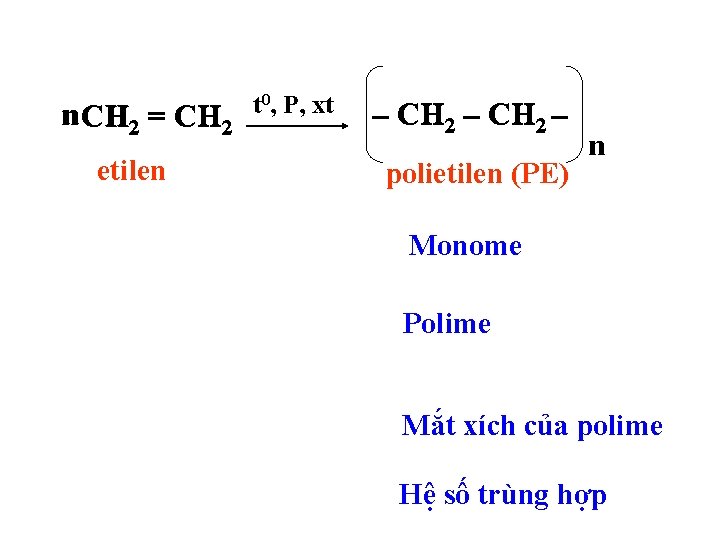
n CH 2 = CH 2 etilen t 0, P, xt – CH 2 – polietilen (PE) n Monome Polime Mắt xích của polime Hệ số trùng hợp
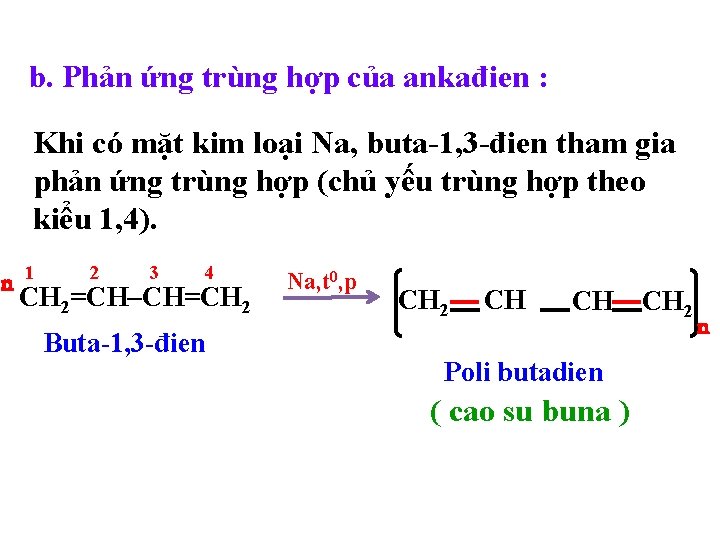
b. Phản ứng trùng hợp của ankađien : Khi có mặt kim loại Na, buta-1, 3 -đien tham gia phản ứng trùng hợp (chủ yếu trùng hợp theo kiểu 1, 4). n 1 2 3 4 CH 2=CH–CH=CH 2 Buta-1, 3 -đien Na, t 0, p CH 2 CH CH Poli butadien ( cao su buna ) CH 2 n
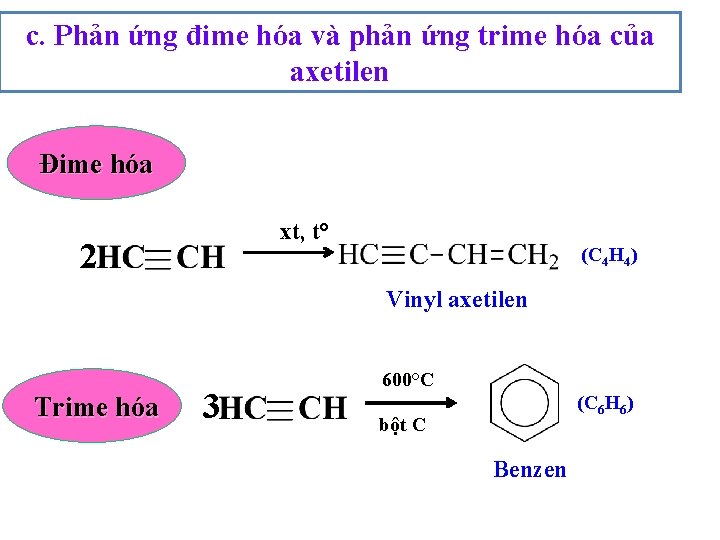
c. Phản ứng đime hóa và phản ứng trime hóa của axetilen Đime hóa xt, t° 2 (C 4 H 4) Vinyl axetilen Trime hóa 3 600°C (C 6 H 6) bột C Benzen

5. Phản ứng thế bằng ion kim loại của ank-1 -in Thí nghiệm: Dẫn khí axetilen sục vào dung dịch bạc nitrat trong amoniac.
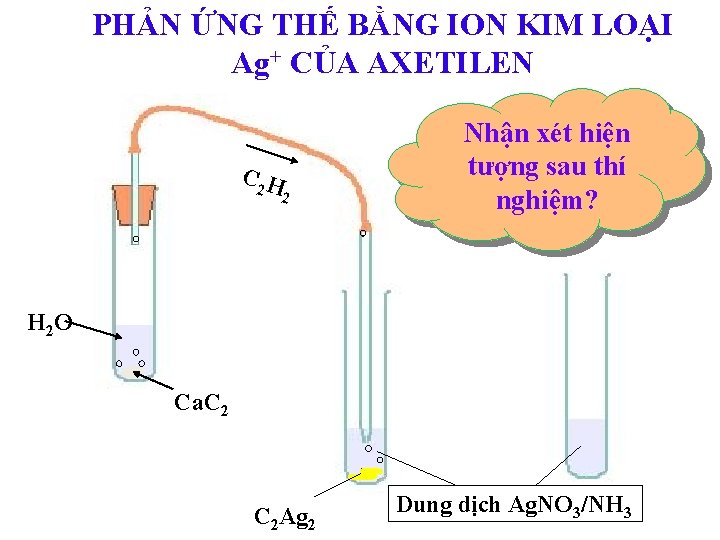
PHẢN ỨNG THẾ BẰNG ION KIM LOẠI Ag+ CỦA AXETILEN C 2 H 2 Nhận xét hiện tượng sau thí nghiệm? H 2 O Ca. C 2 Ag 2 Dung dịch Ag. NO 3/NH 3

Hiện tượng: có kết tủa vàng nhạt xuất hiện. Phương trình phản ứng CH ≡ CH + 2 Ag. NO 3 + H 2 O Ag – C ≡ C – Ag + 2 H 2 O + 2 NH 4 NO 3 kết tủa vàng nhạt Tổng quát: R – C ≡ C – H + Ag. NO 3 + H 2 O R – C ≡ C – Ag + H 2 O + 2 NH 4 NO 3 Chú ý: Chỉ có ank – 1 – in mới có phản ứng này các ankin khác không cho phản ứng này. - Đây là phản ứng phân biệt ank-1 -in (R-C≡ CH) với anken và ankin khác
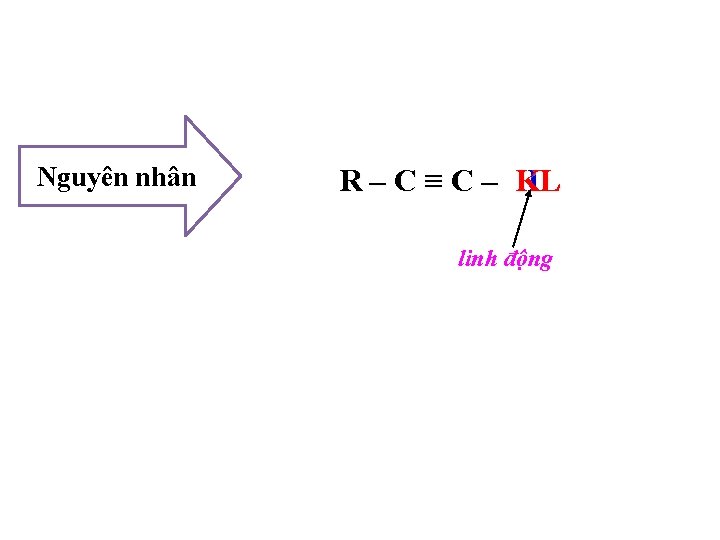
Nguyên nhân R–C≡C– H KL KL linh động

6. Phản ứng oxi hóa a. Phản ứng oxi hóa hoàn toàn của anken Khi bị đốt với oxi, etilen và các đồng đẳng đều cháy và tỏa nhiều nhiệt. Cn. H 2 n + O 2 t 0 n CO 2 + n H 2 O Ví dụ: t 0 C 2 H 4 + 3 O 2 → 2 CO 2 + 2 H 2 O Anken cháy: n. CO 2 = n. H 2 O
Thí nghiệm minh họa Etilen bị đốt cháy C 2 H 5 OH + H 2 SO 4 đ

b. Phản ứng oxi hóa hoàn toàn của ankin Cn. H 2 n – 2 + 3 n – 1 2 Ví dụ: C 2 H 2 + O 2 t 0 n CO 2 + (n – 1) H 2 O t 0 O 2 → 2 CO 2 + H 2 O Ankin cháy: n. CO 2 > n. H 2 O

c. Phản ứng oxi hóa hoàn toàn của ankađien Cn. H 2 n – 2 + 3 n – 1 2 O 2 t 0 n CO 2 + (n – 1) H 2 O Ví dụ: t 0 C 3 H 4 + 4 O 2 → 3 CO 2 + 2 H 2 O Ankađien cháy: n. CO 2 > n. H 2 O

d. Phản ứng oxi hóa không hoàn toàn của anken Thí nghiệm: Hiện tượng: Anken làm mất màu dung dịch KMn. O 4 (thuốc tím) và có kết tủa màu đen của Mn. O 2. Phản ứng dùng để nhận biết anken.

THÍ NGHIỆM ETILEN TÁC DỤNG VỚI DUNG DỊCH KMn. O 4 C 2 H 5 OH + H 2 SO 4đ dd KMn. O 4 Mn. O 2

e. Phản ứng oxi hóa không hoàn toàn của ankin Thí nghiệm: Cho khí axetilen tác dụng với dung dịch KMn. O 4.
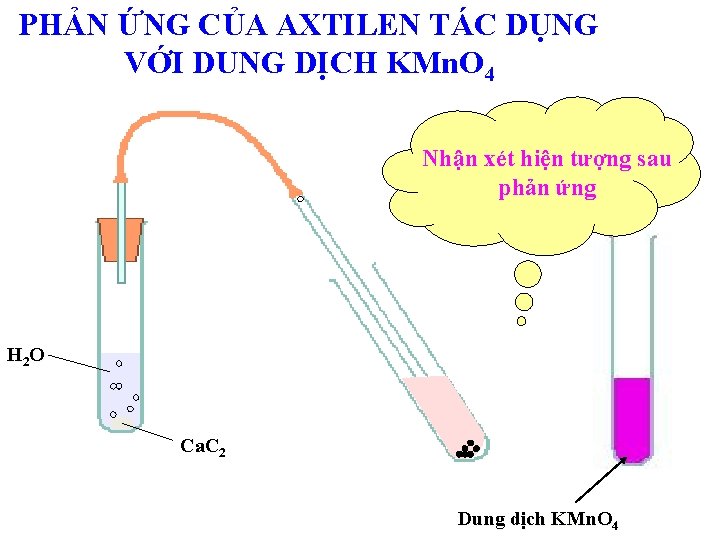
PHẢN ỨNG CỦA AXTILEN TÁC DỤNG VỚI DUNG DỊCH KMn. O 4 Nhận xét hiện tượng sau phản ứng H 2 O Ca. C 2 Dung dịch KMn. O 4

- Hiện tượng: dung dịch KMn. O 4 bị mất màu sau phản ứng. - Phản ứng để phân biệt ankin với ankan f. Oxi hóa không hoàn toàn của ankađien: Ankađien cũng làm mất màu thuốc tím (KMn. O 4) tương tự như anken, ankin.

IV. Điều chế 1. Điều chế anken a. Trong phòng thí nghiệm Etilen được điều chế từ ancol etylic (tách H 2 O): C 2 H 5 OH H 2 SO 4đ, 170 o. C CH 2 = CH 2 + H 2 O b. Trong công nghiệp Anken được điều chế từ ankan (tách H 2): Cn. H 2 n+2 to, p, xt Cn. H 2 n + H 2
2. Điều chế ankin a. Trong phòng thí nghiệm Cho Canxi cacbua Ca. C 2 tác dụng với nước: Ca. C 2 + 2 H 2 O → Ca(OH)2 + C 2 H 2 ↑ b. Trong công nghiệp Axetilen được sản xuất từ metan: 2 CH 4 1500°C Làm lạnh nhanh CH ≡ CH + 3 H 2
V. Ứng dụng Chất dẻo P. E Nhựa PVC ANKEN Rượu Axit axetic (Giấm)
Axit hữu cơ, este Nhựa PVA Axetilen Đèn xì để hàn, cắt kim loại. Nhựa PVC

Ghế salon ANKAĐIEN Nệm Giày dép Lốp xe

CỦNG CỐ Câu 1: Chất làm mất màu dung dịch Brom là chất nào sau đây? A. Butan. B. But-1 -en. C. Cacbon đioxit. D. Metylpropan.

Câu 2: Hidro hóa hoàn toàn buta-1, 3đien thu được A. butan. B. pentan. C. but-1 -en. D. isobutan.

Câu 3: Hiđrocacbon nào sau đây khi bị đốt cháy cho số mol H 2 O lớn hơn số mol CO 2? A. Ankan. B. Anken. C. Ankin. D. Ankađien.

Câu 4: Chất nào không tác dụng với dung dịch bạc nitrat trong amoniac? A. But-1 -in. B. But-2 -in. C. Propin. D. Axetilen.

Câu 5: Cho các chất sau: metan, etilen, buta-1, 3 -đien, but – 2 – in và axetilen. Số chất làm mất màu dung dịch KMn. O 4? A. 1. B. 2. C. 3. D. 4.
- Slides: 47