CENTRO UNIVERSITRIO CATLICA DE SANTA CATARINA JOINVILLE TRABALHO

CENTRO UNIVERSITÁRIO CATÓLICA DE SANTA CATARINA – JOINVILLE TRABALHO DE CONCLUSÃO DE CURSO IV - BIOMEDICINA AS VACINAS PROFILÁTICAS CONTRA O HPV: UMA REVISÃO DA LITERATURA. Acadêmicas: Ane Caroline Costa Santana e Karoline Schmitz Professora Orientadora: Msc. Simone Moreira Professor Coorientador: Drº Dib Ammar Joinville/2015

SUMÁRIO • • • INTRODUÇÃO OBJETIVOS FUNDAMENTAÇÃO TEÓRICA METODOLOGIA CONSIDERAÇÕES REFERÊNCIAS

INTRODUÇÃO • O colo do útero está predisposto a sérias infecções; é um alvo de vírus e carcinógenos que podem levar a um desenvolvimento de carcinoma invasivo. • Há tempos, os dados epidemiológicos vêm delimitando um agente sexualmente transmissível, responsável pela maior causa do câncer de colo do útero: o Vírus Papiloma Humano (HPV). (ROBBINS e COTRAN, 2010) • A vacinação é um método eficaz e de baixo custo benefício, pois previne a doença, promove o combate da disseminação do HPV e as lesões precursoras do Câncer do Colo do Útero (CCU). (ZARDO et al. , 2013)

INTRODUÇÃO • A campanha de vacinação contra o HPV é um método novo de prevenção e espera se que seja eficaz, promovendo no futuro a diminuição do índice de mortalidade que o INCA divulga ano. (INCA, 2014) • Em 2006, a Food and Drug Administration (FDA), aprovou as vacinas profiláticas contra o HPV, e, em seguida, a Agência Nacional de Vigilância Sanitária (ANVISA), também aprovou e regulamentou a comercialização das vacinas. (ZARDO et al. , 2013) • Em 2014, a FDA aprovou a vacina nonavalente, que é composta pelos tipos de HPV constituintes da vacina quadrivalente, acrescidos de cinco tipos de HPVs oncogênicos. (HERRERO et al. , 2015)

SUMÁRIO • • • INTRODUÇÃO OBJETIVOS FUNDAMENTAÇÃO TEÓRICA METODOLOGIA CONSIDERAÇÕES REFERÊNCIAS

OBJETIVO GERAL Caracterizar as vacinas profiláticas contra o Papiloma Vírus Humano descrevendo: Ø Imunogenicidade. Ø Indicações e contraindicações. Ø Eficácia. Ø Segurança.

OBJETIVOS ESPECÍFICOS Ø Compreender a patogênese viral do HPV e sua relação com o CCU. Ø Identificar as vacinas profiláticas disponíveis no mercado, suas indicações e contraindicações. Ø Relatar a eficácia e os efeitos adversos das vacinas profiláticas.

SUMÁRIO • • • INTRODUÇÃO OBJETIVOS FUNDAMENTAÇÃO TEÓRICA METODOLOGIA CONSIDERAÇÕES REFERÊNCIAS

VÍRUS PAPILOMA HUMANO (HPV) Ø Vírus DNA fita dupla Ø Família Papillomaviridae. Ø + 100 tipos diferentes de genótipos. Ø 30 tipos de vírus são potencialmente infectantes para as células da região anogenital. Ø Tipo epiteliotrófico. (BOGLIOLO, 2012)

VÍRUS PAPILOMA HUMANO (HPV) Os HPVs são divididos em: • Alto risco oncogênicos corresponde aos tipos 16, 18, 31, 33, 34, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68 e 70, e, dentre estes, o HPV 16 é o mais prevalente. • Baixo risco oncogênicos são os tipos 6, 11, 42, 43 e 44, e estão associados aos condilomas acuminados. (BOGLIOLO, 2012)

VÍRUS PAPILOMA HUMANO (HPV) • A maioria dos casos de infecção são assintomáticas. • Cerca de 20% dos indivíduos mundialmente estão infectados pelo HPV. • Característica transitória, dificultando a identificação do vírus. • Infecção persistente pode desencadear lesões pré cancerosas levando progressivamente para neoplasia. (ARAÚJO et al. , 2013)

MORFOLOGIA E ESTRUTURA VIRAL • Dupla hélice de DNA circular. • Divido em três regiões: a (LCR) Região Longa de Controle onde ocorre a origem de replicação (ORI) e também a maior parte dos promotores de transcrição. • E a região codificadora é chamada de ORF (Fase de Leitura Aberta), que é

MORFOLOGIA E ESTRUTURA VIRAL • Região precoce (E early) codificação das proteínas envolvidas na replicação do DNA viral e transformação celular= E 1, E 2, E 4, E 5, E 6 e E 7. • Região tardia (L late) codifica as proteínas do capsídeo viral, responsáveis pelas etapas finais da replicação do vírus = L 1 e L 2. (SOUTHERN e HERRINGTON, 1998; BUCK et al. , 2008; ROSA eta al. , 2009)
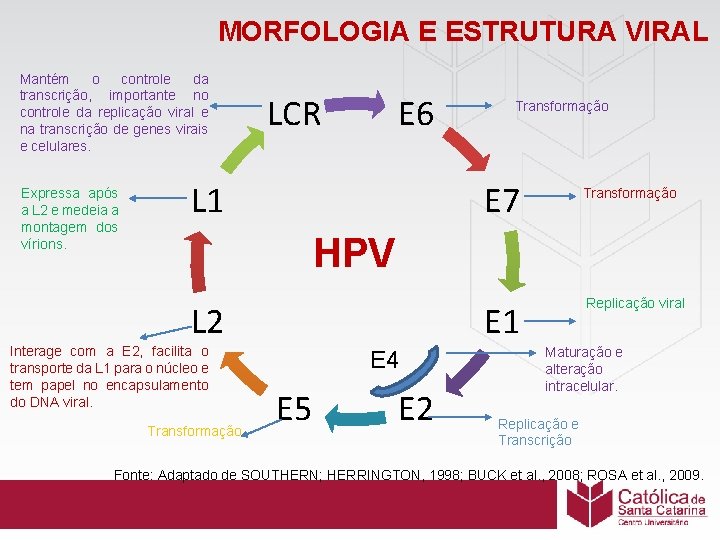
MORFOLOGIA E ESTRUTURA VIRAL Mantém o controle da transcrição, importante no controle da replicação viral e na transcrição de genes virais e celulares. Expressa após a L 2 e medeia a montagem dos vírions. LCR E 6 L 1 Transformação E 7 Transformação HPV L 2 Interage com a E 2, facilita o transporte da L 1 para o núcleo e tem papel no encapsulamento do DNA viral. Transformação Replicação viral E 1 E 4 E 5 E 2 Maturação e alteração intracelular. Replicação e Transcrição Fonte: Adaptado de SOUTHERN; HERRINGTON, 1998; BUCK et al. , 2008; ROSA et al. , 2009.
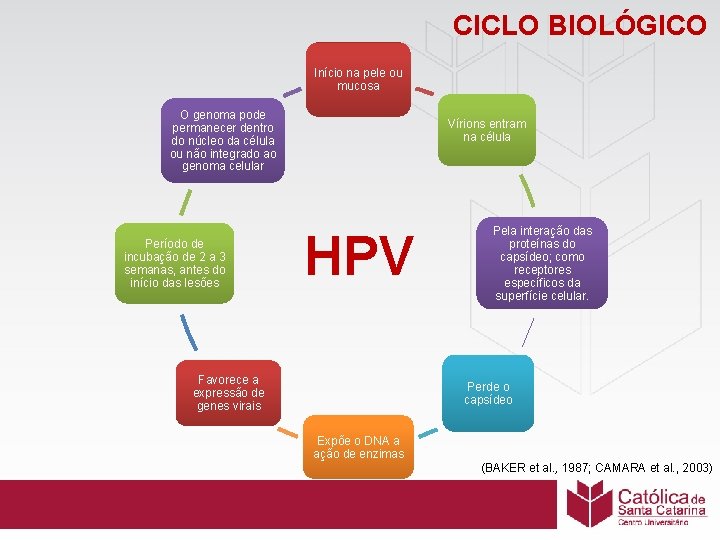
CICLO BIOLÓGICO Início na pele ou mucosa O genoma pode permanecer dentro do núcleo da célula ou não integrado ao genoma celular Período de incubação de 2 a 3 semanas, antes do início das lesões Vírions entram na célula HPV Favorece a expressão de genes virais Pela interação das proteínas do capsídeo; como receptores específicos da superfície celular. Perde o capsídeo Expõe o DNA a ação de enzimas (BAKER et al. , 1987; CAMARA et al. , 2003)
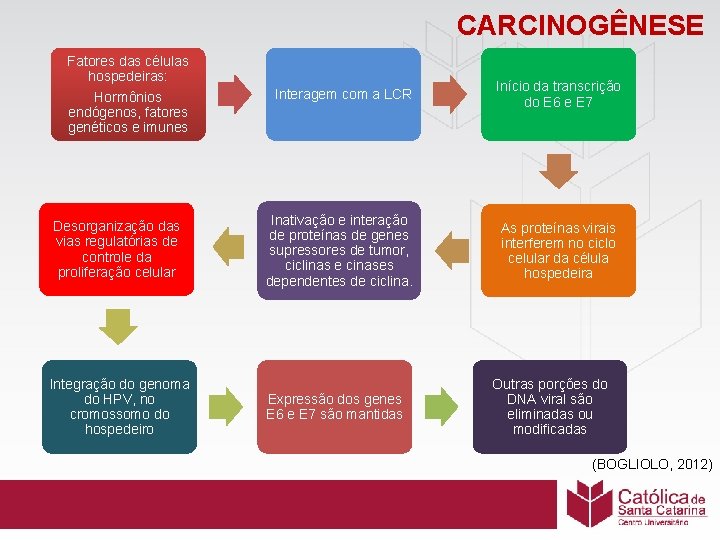
CARCINOGÊNESE Fatores das células hospedeiras: Hormônios endógenos, fatores genéticos e imunes Desorganização das vias regulatórias de controle da proliferação celular Integração do genoma do HPV, no cromossomo do hospedeiro Interagem com a LCR Inativação e interação de proteínas de genes supressores de tumor, ciclinas e cinases dependentes de ciclina. Expressão dos genes E 6 e E 7 são mantidas Início da transcrição do E 6 e E 7 As proteínas virais interferem no ciclo celular da célula hospedeira Outras porções do DNA viral são eliminadas ou modificadas (BOGLIOLO, 2012)
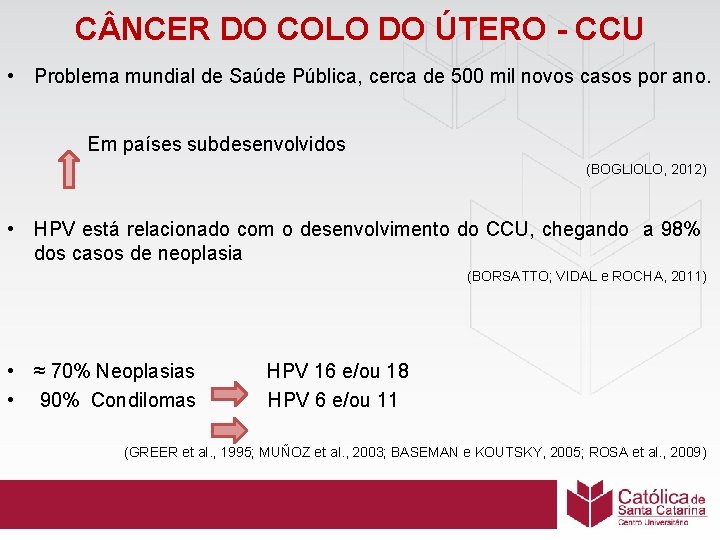
C NCER DO COLO DO ÚTERO - CCU • Problema mundial de Saúde Pública, cerca de 500 mil novos casos por ano. Em países subdesenvolvidos (BOGLIOLO, 2012) • HPV está relacionado com o desenvolvimento do CCU, chegando a 98% dos casos de neoplasia (BORSATTO; VIDAL e ROCHA, 2011) • ≈ 70% Neoplasias • 90% Condilomas HPV 16 e/ou 18 HPV 6 e/ou 11 (GREER et al. , 1995; MUÑOZ et al. , 2003; BASEMAN e KOUTSKY, 2005; ROSA et al. , 2009)

INCIDÊNCIA • Apesar de ser uma doença evitável e tratável, ainda se tem um índice muito alto no número de novos casos por ano. • Justificando isso, o INCA (2014) estimou para o ano de 2014, no Brasil, 15. 590 novos casos.

VACINAS PROFILÁTICAS • As VLP´s são um conjunto de duas proteínas a L 1 e a L 2, que são estruturas semelhantes morfologicamente aos vírus, e não contém material genético viral, por isso são consideradas seguras. (LOWY e SCHILLER, 2006; DERCHAN e SARIAN, 2007) • Proteína L 1 são vírus-like particles (VLP’S), sem o DNA do vírus = VACINAS PROFILÁTICAS. (CHRISTENSEN et al. , 1994; ROSA et al. , 2009) • Vacina: Os anticorpos induzidos pela vacina são liberados na mucosa genital, impedindo precocemente o quadro infeccioso. (MUÑOZ et al. , 2008; SILVA et al. , 2009)

VACINAS PROFILÁTICAS • Estima se que se houver vacinação completa da população, os casos de CCU podem diminuir em até dois terços. (POMFRET, GAGNON, GILCHRIST, 2011; ZARDO et al. , 2014) Tipos de vacinas disponíveis: • Bivalente: VLPs contra os tipos 16 e 18, da Glaxo. Smith. Kline (2009). • Quadrivalente: VLPs contra os tipos 6, 11, 16 e 18, da Merck Sharp e Dohme (2006). (ZARDO et al. , 2014) • Nonavalente: VLPs contra os tipos 6, 11, 16, 18, 31, 33, 45, 52 e 58, da Merck Sharp e Dohme (2014). (HERRERO et al. , 2015)

INDICAÇÃO • Vacina bivalente, tem indicação para as mulheres a partir dos 9 anos, sem restrição de idade máxima. • Vacina quadrivalente é indicada para mulheres e homens na faixa etária dos 9 aos 26 anos. (LINHARES e VILLA, 2006; RODEN e WU, 2006; ZARDO et al. , 2014) • Vacina nonavalente é indicada para mulheres na faixa etária dos 9 aos 26 anos e meninos entre 9 e 15 anos. (MERCK SHARP & DOHME, 2015)

CONTRAINDICAÇÕES • A pacientes que tem hipersensibilidade ao princípio ativo ou outro composto da vacina. • A pacientes que tiveram algum sintoma ou reação grave após a administração de uma dose da vacina. • Não é indicada a gestantes. (DIVE, 2014)
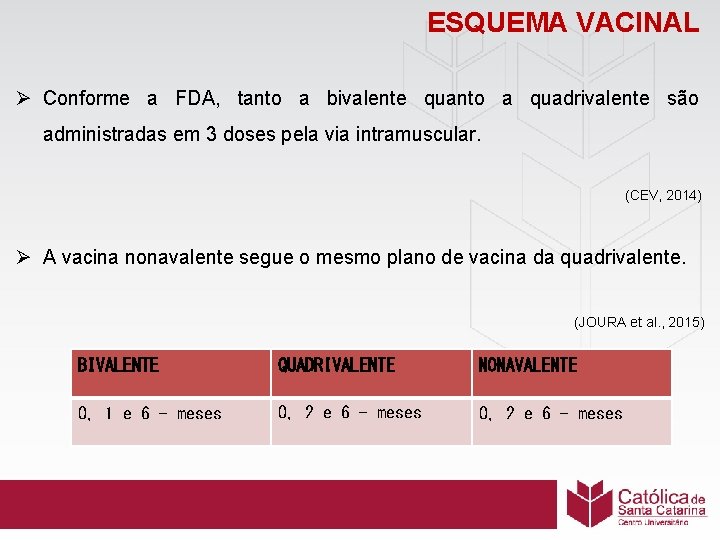
ESQUEMA VACINAL Ø Conforme a FDA, tanto a bivalente quanto a quadrivalente são administradas em 3 doses pela via intramuscular. (CEV, 2014) Ø A vacina nonavalente segue o mesmo plano de vacina da quadrivalente. (JOURA et al. , 2015) BIVALENTE QUADRIVALENTE NONAVALENTE 0, 1 e 6 - meses 0, 2 e 6 - meses

ESQUEMA VACINAL • Estudos com a vacina quadrivalente comprovam que com apenas duas doses a menina já possui imunogenicidade, sendo a terceira dose administrada cinco anos depois da primeira, conferindo uma garantia adicional. (CEV, 2014) • O Ministério da Saúde no Brasil segue as diretrizes do Grupo Técnico Assessor de Imunizações (TAG) da Organização Pan Americana de Saúde (OPAS), que preconiza o esquema vacinal em 0, 6 e 60 meses, e essa decisão foi sustentada após aprovação pelo Comitê Técnico de

EFEITOS ADVERSOS • São classificados em: locais e sistêmicos. • A maioria dos indivíduos vacinados e acompanhados apresentaram tolerância satisfatória e os eventos adversos mais referidos foram os locais. EFEITOS LOCAIS EFEITOS Estão associados a aplicação da vacina: ü ü Inchaço. Dor. Eritema. Prurido. SISTÊMICOS Os efeitos mais observados: ü Cefaleia. ü Náusea. ü Vômito. (LEPIQUE; RABACHINI; VILLA, 2009; BORSATTO et al. , 2011)

ENSAIOS CLÍNICOS • Bivalente e Quadrivalente: Três importantes ensaios clínicos de fase III = Estudos multicêntricos, duplo cegos, randomizados e controlados por placebo. • PApilloma TRIal against Cancer In young Adults (PATRICIA – 2004 a 2009). • Female United to Unilaterally Reduce Endo/Ectocervical Disease Study Group (FUTURE I – 2002 a 2007), (FUTURE II – 2002 a 2007). (LEPIQUE, RABACHINI, VILLA, 2009; BORSATTO et al. , 2011)

ENSAIOS CLÍNICOS PATRICIA (2004 – 2009): • Avaliada depois de ≈ 35 meses após a administração da terceira dose. • Eficácia contra NIC 2 associada aos HPVs 16 e 18 foi de 92, 9%. • Mulheres HPV DNA negativas para 14 tipos oncogênicos e soro negativas para os tipos 16 e 18 com citologia normal, que receberam apenas uma dose da vacina, a eficácia contra NIC 2 associada aos HPVs tipos 16 e 18 foi de 98, 4%. • Total vacinada, independentemente da existência inicial de infecção atual ou prévia por HPV, a eficácia para NIC 2 foi de 30, 4%. (PAAVONEN et al. , 2009; Sociedade Portuguesa de Ginecologia, 2010)

ENSAIOS CLÍNICOS FUTURE II Faixa etária dos participantes 16 24 15 26 Número de parceiros sexuais ≤ 4 Critérios de exclusão Componentes da vacina Gravidez, história prévia de Papanicolau anormal ou verrugas genitais. VLP contra o HPV 6, 11, 16 e 18 Gravidez e história prévia de Papanicolau anormal. VLP contra o HPV 6, 11, 16 e 18 Administração das doses Meses 0, 2 e 6 Frequência do exame citológico A cada 6 meses A cada 12 meses Metas primárias Avaliar a incidência do HPV 6, 11, 16 e 18 associados a verrugas genitais, NIC 1 3, NIVA 1 3, AIS e câncer cervical, vulvar ou vaginal. 100% para o desenvolvimento de lesões intraepiteliais de baixo grau, alto grau e adenocarcinoma. 62% para lesões intraepiteliais de baixo grau, não se mostrando significativa nas lesões de alto grau e adenocarcinoma. 100% contra os vírus 6, 11, 16 e 18 Avaliar a incidência do HPV 16 e 18 com o câncer cervical, NIC 2 3 e AIS. 46% contra o vírus 16 e 76% contra o vírus 18 42% contra o vírus 16 e 79% contra o vírus 18 Eficácia por análise de protocolo referente às lesões Eficácia por intenção de tratar referente às lesões Eficácia por análise de protocolo referente aos tipos virais Eficácia por intenção de tratar referente aos tipos virais 100% para NIC II e 97% para NIC III, não sendo significativo aos valores para adenocarcinoma. 57% para NIC II, 42% para NIC III e 28% para adenocarcinoma. 97% contra o vírus 16 e 100% contra o vírus 18 Fonte: Adaptado de GIRALDO et al. ; 2008; ZARDO et al. ; 2014 e JOURA et al. ; 2015.

ENSAIOS CLÍNICOS • Nonavalente: incluíram seis estudos de Fase III completos. • O principal estudo com a vacina nonavalente foi randomizado, duplo cego, multicêntrico e internacional, sem utilização de placebo, e sim com a utilização da vacina quadrivalente como controle. • Foram incluídas mulheres em idade entre 16 e 26 anos para avaliação da eficácia, imunogenicidade e efeitos colaterais relacionados à vacina. (PARELLADA, 2015)
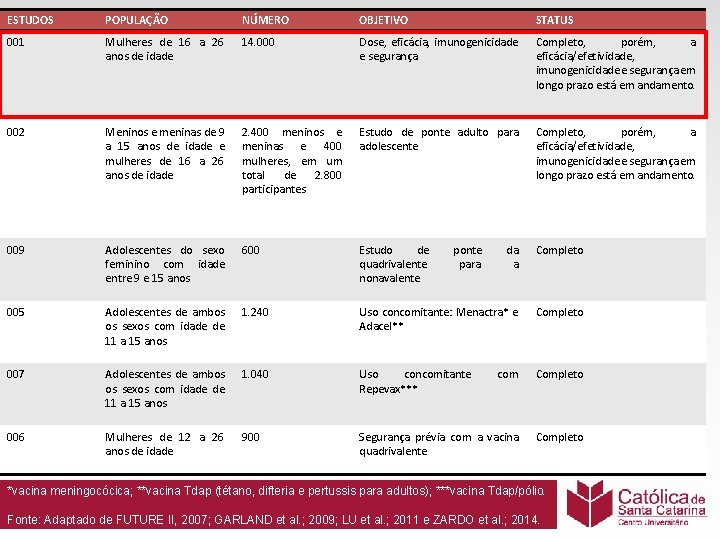
ESTUDOS POPULAÇÃO NÚMERO OBJETIVO STATUS 001 Mulheres de 16 a 26 anos de idade 14. 000 Dose, eficácia, imunogenicidade e segurança Completo, porém, a eficácia/efetividade, imunogenicidade e segurança em longo prazo está em andamento. 002 Meninos e meninas de 9 a 15 anos de idade e mulheres de 16 a 26 anos de idade 2. 400 meninos e meninas e 400 mulheres, em um total de 2. 800 participantes Estudo de ponte adulto para adolescente Completo, porém, a eficácia/efetividade, imunogenicidade e segurança em longo prazo está em andamento. 009 Adolescentes do sexo feminino com idade entre 9 e 15 anos 600 Estudo de quadrivalente nonavalente da a Completo 005 Adolescentes de ambos os sexos com idade de 11 a 15 anos 1. 240 Uso concomitante: Menactra* e Adacel** Completo 007 Adolescentes de ambos os sexos com idade de 11 a 15 anos 1. 040 Uso concomitante Repevax*** com Completo 006 Mulheres de 12 a 26 anos de idade 900 Segurança prévia com a vacina quadrivalente Completo ponte para *vacina meningocócica; **vacina Tdap (tétano, difteria e pertussis para adultos); ***vacina Tdap/pólio. Fonte: Adaptado de FUTURE II, 2007; GARLAND et al. ; 2009; LU et al. ; 2011 e ZARDO et al. ; 2014.
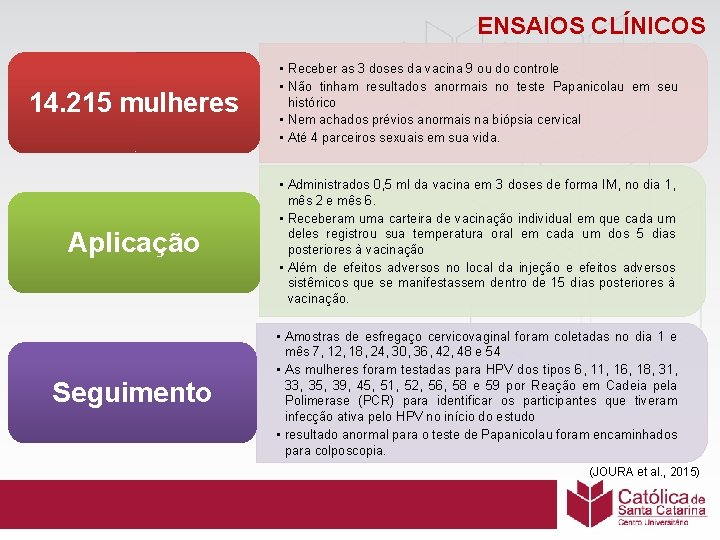
ENSAIOS CLÍNICOS 14. 215 mulheres • Receber as 3 doses da vacina 9 ou do controle • Não tinham resultados anormais no teste Papanicolau em seu histórico • Nem achados prévios anormais na biópsia cervical • Até 4 parceiros sexuais em sua vida. Aplicação • Administrados 0, 5 ml da vacina em 3 doses de forma IM, no dia 1, mês 2 e mês 6. • Receberam uma carteira de vacinação individual em que cada um deles registrou sua temperatura oral em cada um dos 5 dias posteriores à vacinação • Além de efeitos adversos no local da injeção e efeitos adversos sistêmicos que se manifestassem dentro de 15 dias posteriores à vacinação. Seguimento • Amostras de esfregaço cervicovaginal foram coletadas no dia 1 e mês 7, 12, 18, 24, 30, 36, 42, 48 e 54 • As mulheres foram testadas para HPV dos tipos 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 e 59 por Reação em Cadeia pela Polimerase (PCR) para identificar os participantes que tiveram infecção ativa pelo HPV no início do estudo • resultado anormal para o teste de Papanicolau foram encaminhados para colposcopia. (JOURA et al. , 2015)

ENSAIOS CLÍNICOS Ø A incidência de doenças cervicais, vulvar e vaginal de alto grau, entre todos os participantes (independente do resultado do teste de HPV), foi de 14 por 1. 000 pessoas/ano em ambos os grupos de vacina, nonavalente ou quadrivalente. (JOURA et al. , 2015)

ENSAIOS CLÍNICOS RESULTADOS Subgrupo Nonavalente Quadrivalente HPV NEGATIVOS* 2, 4 por 1. 000 pessoas/ano 4, 2 por 1. 000 pessoas/ano HPV POSITIVOS 23, 1 por 1. 000 pessoas/ano 22, 1 por 1. 000 pessoas/ano *Neste subgrupo, a eficácia da vacina para as doenças relacionadas aos tipos de HPV presentes na vacina foi de 100% e a eficácia para as doenças não relacionadas a esses tipos de HPV foi de 19, 7 %. (JOURA et al. , 2015)

ENSAIOS CLÍNICOS • Análises de eficácia com o grupo por protocolo a incidência de doenças de alto grau relacionadas aos HPV 31, 33, 45, 52 e 58 foi de 0, 1 por 1. 000 pessoas/ano no grupo da vacina nonavalente e 1, 6 por 1. 000 pessoas/ano no grupo da vacina quadrivalente. • No mesmo grupo, a incidência de neoplasia cervical epitelial de alto grau, adenocarcinoma in situ e câncer cervical, relacionados aos tipos HPV 31, 33, 45, 52 e 58 foi de 0, 1 por 1. 000 pessoas/ano no grupo da vacina nonavalente e 1, 5 por 1. 000 pessoas/ano no grupo quadrivalente. (JOURA, 2015)

ENSAIOS CLÍNICOS • A incidência de infecção persistente, com duração maior ou igual a seis meses, relacionados aos tipos HPV 31, 33, 45, 52 e 58 na população de análise de eficácia por protocolo foi 2, 1 por 1000 pessoas/ano no grupo da nonavalente e 52, 4 por 1000 pessoas/ano no grupo da quadrivalente. • ≈ 99, 5% dos indivíduos incluídos nas análises imunológicas para cada um dos nove tipos de HPVs constituintes da vacina, tornaram se soropositivos por volta do sétimo mês. • A duração da imunidade após completada a vacinação, ainda não foi estabelecida. As proporções de indivíduos que permaneceram soropositivos para cada tipo de HPV no vigésimo quarto mês, foi

IMUNOGENICIDADE • A resposta de anticorpos após o esquema de vacinação de 3 doses segue o padrão esperado. Após cada dose da vacina quadrivalente, os níveis de anticorpos aumentam até uma concentração de anticorpo, onde o pico é atingido um mês após a terceira dose no esquema primário. (STANLEY, 2010) • Imunogenicidade de um esquema de 2 doses da vacina quadrivalente em 0 a 6 meses em meninas de 9 a 13 anos de idade é estatisticamente não inferior para os HPV 16 e HPV 18 para a imunogenicidade em mulheres que receberam as 3 doses, avaliadas um mês após a dose final. (DOBSON et al. , 2013)

SUMÁRIO • • • INTRODUÇÃO OBJETIVOS FUNDAMENTAÇÃO TEÓRICA METODOLOGIA CONSIDERAÇÕES REFERÊNCIAS

METODOLOGIA • O presente trabalho utilizou como ferramenta metodológica a pesquisa bibliográfica do tipo exploratória, que apresenta um levantamento de bibliografias publicadas, é uma análise crítica, meticulosa e ampla das publicações decorrentes em uma determinada área, que podem ser variadas como livros, revistas, artigos entre outros. (MARCONI; LAKATOS, 2011) • Para a escolha das fontes foram incluídos materiais em meio eletrônico e impresso que abordassem a temática, como o vírus HPV, o câncer do colo do útero, priorizando o tema da vacina contra o HPV. O tempo delimitado para a escolha dos materiais foi de 10 anos (2005 a 2015), a partir do ano de sua publicação, com exceção de alguns conceitos, como em relação ao vírus HPV que tiveram materiais utilizados com mais de 10 anos de sua publicação.

SUMÁRIO • • • INTRODUÇÃO OBJETIVOS FUNDAMENTAÇÃO TEÓRICA METODOLOGIA CONSIDERAÇÕES REFERÊNCIAS

CONSIDERAÇÕES • Compreender a patogênese viral do HPV e sua relação com o CCU. Ø São vírus epiteliotróficos, aderindo a superfície epitelial. Ø Alta mortalidade por CCU, esse que esta diretamente relacionado com o HPV. Ø HPVs de baixo risco – verrugas genitais. Ø HPVs de alto risco – lesões pré cancerosas e câncer.

CONSIDERAÇÕES • Identificar as vacinas profiláticas disponíveis no mercado, suas indicações e contraindicações. Ø Bivalente (16 e 18): indicada a mulheres com idade mínima de 9 anos de idade, sem restrição de idade máxima Ø Quadrivalente (6, 11, 16 e 18): indicada a homens e mulheres entre 9 e 26 anos de idade Ø Nonavalente (6, 11, 16, 18, 31, 33, 45, 52 e 58): indicada a mulheres de 9 a 26 anos de idade e meninos de 9 a 15 anos de idade. Ø Contraindicações: gestantes, hipersensibilidade a alguns componentes pertencentes à ela, principalmente ao Sacharomyces cerevisae.

CONSIDERAÇÕES Relatar a eficácia e os efeitos adversos das vacinas profiláticas. Ø Demonstraram eficácia comprovada, no entanto, é necessário mais tempo de estudo das vacinas, para que se possa comprovar a real eficácia a longo prazo. Ø Bivalente: HPV DNA negativas para 14 tipos oncogênicos e soro negativas para os tipos 16 e 18, que receberam apenas uma dose da vacina, a eficácia contra NIC 2 associada aos HPVs tipos 16 e 18 foi de 98, 4%. Ø Quadrivalente: FUTURE I - 100% contra os vírus 6, 11, 16 e 18; FUTURE II 97% contra o vírus 16 e 100% contra o vírus 18. Ø Nonavalente: Subgrupo HPV negativas eficácia da vacina para as doenças relacionadas aos tipos de HPV presentes na vacina foi de 100% e a eficácia para as doenças não relacionadas a esses tipos de HPV foi de 19, 7 %.

CONSIDERAÇÕES Ø Efeitos colaterais locais e sistêmicos, tendo um relato maior ao local de administração da injeção. Ø Efeitos sistêmicos foram observados mais nenhum de intensidade grave, assim como durante os estudos, tiveram relatos de óbitos, mas nenhum deles associados a vacina.

SUMÁRIO • • • INTRODUÇÃO OBJETIVOS FUNDAMENTAÇÃO TEÓRICA METODOLOGIA CONSIDERAÇÕES REFERÊNCIAS

REFERÊNCIAS • ARAÚJO et. al. Eficácia das vacinas comercialmente disponíveis contra a infecção pelo papilomavírus em mulheres: revisão sistemática e metanálise. Disponível em: <http: //www. scielo. br/pdf/csp/v 29 s 1/a 04. pdf>, acesso em 16/ Nov. 2014 • BACKER CC: Structrural and transcriptional analysis of human papillomavirus type 16 sequences in cervical carcinoma cell lines. J virol 61: 962 971, 1988. • BORSATTO; VIDAL e ROCHA. Vacina contra o HPV e a Prevenção do Câncer do Colo do Útero: Subsídios para a Prática, 2011. Disponível em <http: //www. inca. gov. br/rbc/n_57/v 01/pdf/10_revisao_de_literatura_vacina_hpv_pre vencao_cancer_colo_utero_subsidios. pdf>, acesso em 27 de set. 2014. • BRASIL, Câncer de Colo de Útero: A Vacina Para Prevenção do HPV e o desafio para a Melhoria da Qualidade do Rastreamento no Brasil: BRATS – Boletim Brasileiro de Avaliação de Tecnologias em Saúde. Ano VI, n. 17, acesso em dezembro de 2011. • DERCHAIN, Shopie Francoise Mauricette; SARIAN, Luis, Otávio. Vacinas Profiláticas do HPV. Disponível em: <http: //www. scielo. br/pdf/rbgo/v 29 n 6/a 01 v 29 n 6. pdf>. Acesso em: 12. Set. 2014. • Diretoria de Vigilância Epidemiológica. Disponível em: http: //www. dive. sc. gov. br/conteudos/imunizacao/noticias/2014/Informe_Tec nico_Introducao_vacina_HPV. pdf. Acesso em: 14 de out. de 2014. • DOBSON, Simon R. M. et al. Immunogenicity of 2 Doses of HPV Vaccine in Younger Adolescents vs 3 Doses in Young Women. A Randomized Clinical Trial. The Journal of the American Medical Association 2013. Disponível em: <http: //jamanetwork. com/article. aspx? articleid=1682939>. Acesso em: 07 de set. de 2015. • FILHO, Geraldo Brasileiro; Bogliogo Patologia, 8ª ed. Rio de Janeiro: Guanabara Koogan, 2012. Acesso em: 20, Nov 2015. • GARDASIL® 9 (Papilomavírus Humano 9 valente Vacina Recombinante), MERCK SHARP & DOHME, 2014. Bula de remédio. • GREER CE, Wheeler CM, Ladner MB, Beutner K, Coyne MY, Liang H, et al. Human papillomavirus (HPV) type distribution and serological response to HPV type 6 virus-like particles in patients with genital warts. J Clin Microbiol 1995; 33: 2058 63. Disponível em: http: //www. ncbi. nlm. nih. gov/pmc/articles/PMC 228335/. Acesso em: 20, Nov 2015.

REFERÊNCIAS • HERRERO, Rolando; GONZALEZ, Paula; MARKOWITZ, Lari E. Present status of human papillomavirus vaccine development and implementation. The Lancet Oncology. May 2015. Disponível em: < http: //www. thelancet. com/journals/lanonc/article/PIIS 1470 2045(14)70481 4/abstract>. Acesso em: 07 de set. de 2015. • Instituto Nacional do Câncer – INCA. Disponível em: http: //www 2. inca. gov. br/wps/wcm/connect/acoes_programas/site/home/nobrasil/programa_nacional_controle_cancer_colo_utero/tratame nto. Acesso em: 08 de nov. de 2014. • JOURA, E. A. et al. A 9 -Valent HPV Vaccine against Infection and Intraepithelial Neoplasia in Women. The New England Journal of Medicine. February 2015. Disponível em: http: //www. nejm. org/doi/pdf/10. 1056/NEJMoa 1405044. Acesso em: 07 de set. de 2015. • LEPIQUE AP, Rabachini T, Villa LL. HPV vaccination: the begining of the end of cervical câncer? A Review. Mem Inst Oswaldo Cruz 2009; 104(1): 1 10. Acesso em: 20, Nov 2015. • LINHARES AC, Villa LV. Vaccines against rotavirus and human papillomavirus (HPV). J Pediatr 2006; 82(3): 25 34. • MARCONI, Marina de Andrade; LAKATOS, Eva Maria. Metodologia de Trabalho Científico. 7ª Ed. Atlas: São Paulo, 2011. Acesso em: 20, Nov 2015. • Ministério da Saúde. Vacina contra HPV na prevenção de câncer de colo de útero. Brasília. 2013. Disponível em: <http: //conitec. gov. br/images/Incorporados/Vacina. HPV final. pdf>. Acesso em: 20, Nov 2015. • MUÑOZ N, Franceschi S, Bosetti C, Moreno V, Herrero R, Smith JS, et al. Role of parity and human papillomavirus in cervical cancer: the IARC multicentric case-control study. Lancet 2002; 359: 1085 92. Acesso em: 20, Nov 2015. • PAAVONEN J, Jenkins D, Bosch FX et al. Efficacy of a prophylactic adjuvanted bivalent L 1 virus like particle vaccine against infection with human papillomavirus types 16 and 18 in young women: an interim analysis of a Phase III double blind, randomized controlled trial. Acesso em: 20, Nov 2015.

REFERÊNCIAS • PARELLADA, Cíntia. Desenvolvimento clinico da vacina papilomavírus humano 9 valente (recombinante). Disponível em: < http: //www. sbmf. org. br/pdf_upload/biblioteca/15/6 cintia vacina nonavalente finalsindusfarma. pdf>. Acesso em: 10 de set. de 2015. • POMFRET TC, Gagnon JM, Gilchrist AT. Quadrivalent human papillomavirus (HPV) vaccine: a review of safety, efficacy, and pharmacoeconomics. Journal of clinical pharmacy and therapeutics 2011; 36(1): 1 9. Acesso em: 20, Nov 2015. • ROSA, Maria Inês, et. al, . Papilomavírus humano e neoplasia cervical, 2009. Disponível em < http: //www. scielo. br/scielo. php? script=sci_arttext&pid=S 0102 311 X 2009000500002>Acessado em 25 de janeiro de 2015. • ROBBINS, Stanley Leonard; COTRAN, S. Ramzi; KUMAR, Vinay, Patologia: Base patológica da doença. 8ª. ed. Rio de Janeiro, 2010. • STANLEY, Margaret. HPV – immune response to infection and vaccination. 2010. Disponível em: <http: //www. ncbi. nlm. nih. gov/pmc/articles/PMC 3161350/>. Acesso em: 12, mai 2015. • Secretaria de Estado da Saúde. Vacina contra o papilomavírus humano (HPV). São Paulo. 2014. Disponível em: <http: //www. cve. saude. sp. gov. br/htm/imuni/pdf/HPV 14_INFORME_TECNICO. pdf> Acesso em: 12, mai 2015. • ZARDO, Geisa Picksius et al. Vacina como gente de imunização contra o HPV. Dis ponível em: http: //www. scielosp. org/pdf/csc/v 19 n 9/1413 8123 csc 19 09 3799. pdf. Acesso em: 14 de out. de 2014.

OBRIGADA PELA ATENÇÃO CONTATOS ANE CAROLINE COSTA SANTANA ane. santana@catolicasc. org. br KAROLINE SCHMITZ karoline. schmitz@catolicasc. org. br
- Slides: 48