Cemeg UG CRYNODEB O FONDIO AC ADEILEDDAU N
Cemeg UG CRYNODEB O FONDIO AC ADEILEDDAU . . N H H H
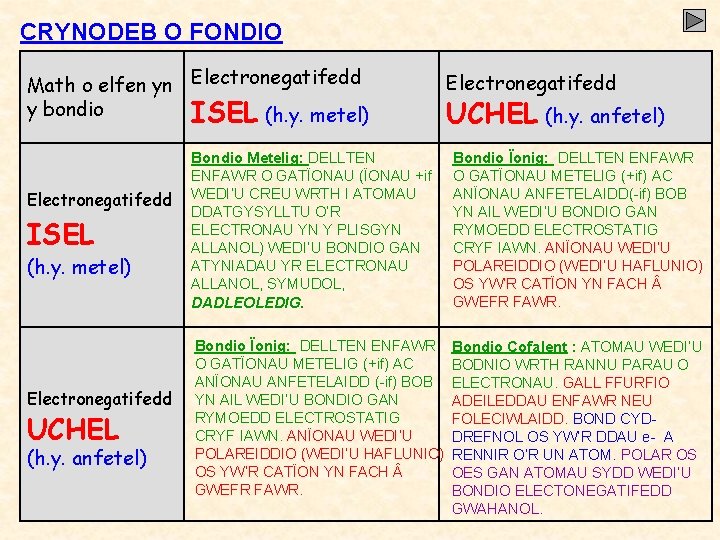
CRYNODEB O FONDIO Math o elfen yn Electronegatifedd y bondio ISEL (h. y. metel) Electronegatifedd UCHEL (h. y. anfetel) Bondio Metelig: DELLTEN ENFAWR O GATÏONAU (ÏONAU +if WEDI’U CREU WRTH I ATOMAU DDATGYSYLLTU O’R ELECTRONAU YN Y PLISGYN ALLANOL) WEDI’U BONDIO GAN ATYNIADAU YR ELECTRONAU ALLANOL, SYMUDOL, DADLEOLEDIG. Bondio Ïonig: DELLTEN ENFAWR O GATÏONAU METELIG (+if) AC ANÏONAU ANFETELAIDD(-if) BOB YN AIL WEDI’U BONDIO GAN RYMOEDD ELECTROSTATIG CRYF IAWN. ANÏONAU WEDI’U POLAREIDDIO (WEDI’U HAFLUNIO) OS YW’R CATÏON YN FACH GWEFR FAWR. Bondio Ïonig: DELLTEN ENFAWR O GATÏONAU METELIG (+if) AC ANÏONAU ANFETELAIDD (-if) BOB YN AIL WEDI’U BONDIO GAN RYMOEDD ELECTROSTATIG CRYF IAWN. ANÏONAU WEDI’U POLAREIDDIO (WEDI’U HAFLUNIO) OS YW’R CATÏON YN FACH GWEFR FAWR. Bondio Cofalent : ATOMAU WEDI’U BODNIO WRTH RANNU PARAU O ELECTRONAU. GALL FFURFIO ADEILEDDAU ENFAWR NEU FOLECIWLAIDD. BOND CYDDREFNOL OS YW’R DDAU e- A RENNIR O’R UN ATOM. POLAR OS OES GAN ATOMAU SYDD WEDI’U BONDIO ELECTONEGATIFEDD GWAHANOL.

NODWEDDION MATHAU O FONDIO: MATH ÏONIG METELIG COFALENT ENFAWR COFALENT MOLECIWLAIDD DIM 1. Van der Waals i bob un 2. Deupol-deupol i foleciwlau polar 3. Bondiau hydrogen ar gyfer H-F, H-N neu H-O Grymoedd rhyngfole -ciwlaidd DIM Ymdoddb wynt UCHEL IAWN – angen llawer o egni i oresgyn atyniadau electrostatig cryf iawn UCHEL IAWN (ac eithrio Hg) – angen llawer o egni i oresgyn atyniadau cryf iawn rhwng catïonau ac electronau dadleoledig UCHEL IAWN – angen llawer o egni i dorri bondiau cofalent cryf UCHEL IAWN oherwydd bod edadleoledig yn symud yn hawdd gyda foltedd. YNYSYDDION – dim gronynnau wedi’u gwefru (ac eithrio graffit edadleoledig). Na, Mg, Al, Cu, Fe ac ati Diemwnt, graffit Si. O 2 SERO oni bai ar ffurf tawdd pan DARGLUD fydd ïonau yn -EDD. symud yn hawdd gyda foltedd. e. e. Na+Cl- , Mg 2+O 2 - ISEL – yn gyffredinol, angen ychydig iawn o egni i oresgyn grymoedd rhyngfoleciwlaidd gwan – ond yn amrywio yn ôl math y grymoedd rhyngfoleciwlaidd a maint moleciwlaidd YNYSYDDION – dim gronynnau wedi’u gwefru. H 2, O 2, N 2, H 2 O, NH 3, Cl 2, Br 2, I 2, HBr, HCl, HF, H 2 S, CH 4 ac ati
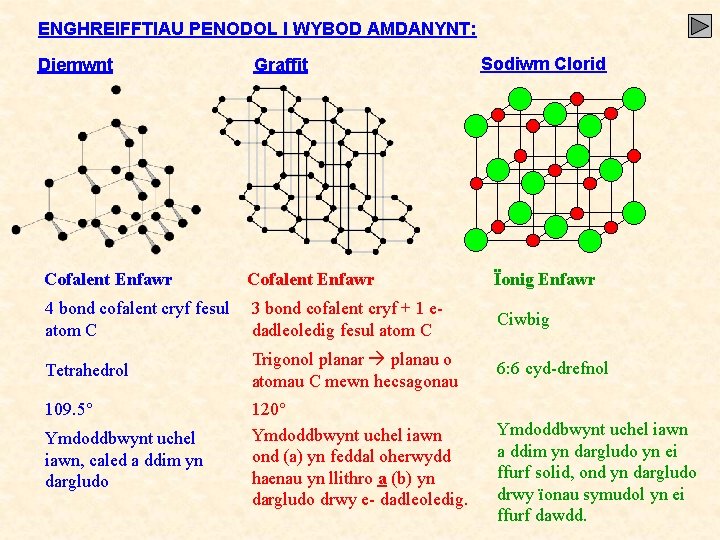
ENGHREIFFTIAU PENODOL I WYBOD AMDANYNT: Diemwnt Graffit Sodiwm Clorid Cofalent Enfawr Ïonig Enfawr 4 bond cofalent cryf fesul atom C 3 bond cofalent cryf + 1 edadleoledig fesul atom C Ciwbig Tetrahedrol Trigonol planar planau o atomau C mewn hecsagonau 6: 6 cyd-drefnol 109. 5° Ymdoddbwynt uchel iawn, caled a ddim yn dargludo 120° Ymdoddbwynt uchel iawn ond (a) yn feddal oherwydd haenau yn llithro a (b) yn dargludo drwy e- dadleoledig. Ymdoddbwynt uchel iawn a ddim yn dargludo yn ei ffurf solid, ond yn dargludo drwy ïonau symudol yn ei ffurf dawdd.
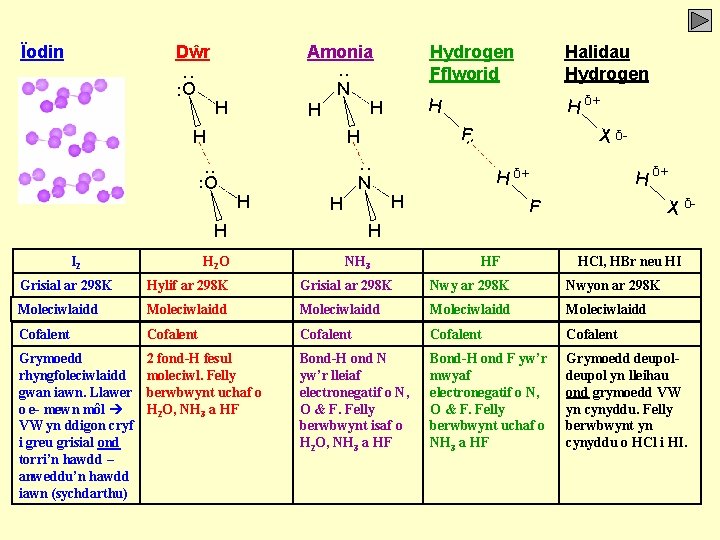
Ïodin Dŵr Amonia O N . . . H H . . N . . O H H 2 O Halidau Hydrogen H H δ+ F. . H . . I 2 H H Hydrogen Fflworid X δH δ+ H X δ- F H NH 3 HF HCl, HBr neu HI Grisial ar 298 K Hylif ar 298 K Grisial ar 298 K Nwyon ar 298 K Moleciwlaidd Moleciwlaidd Cofalent Cofalent Grymoedd rhyngfoleciwlaidd gwan iawn. Llawer o e- mewn môl VW yn ddigon cryf i greu grisial ond torri’n hawdd – anweddu’n hawdd iawn (sychdarthu) 2 fond-H fesul moleciwl. Felly berwbwynt uchaf o H 2 O, NH 3 a HF Bond-H ond N yw’r lleiaf electronegatif o N, O & F. Felly berwbwynt isaf o H 2 O, NH 3 a HF Bond-H ond F yw’r mwyaf electronegatif o N, O & F. Felly berwbwynt uchaf o NH 3 a HF Grymoedd deupol yn lleihau ond grymoedd VW yn cynyddu. Felly berwbwynt yn cynyddu o HCl i HI.
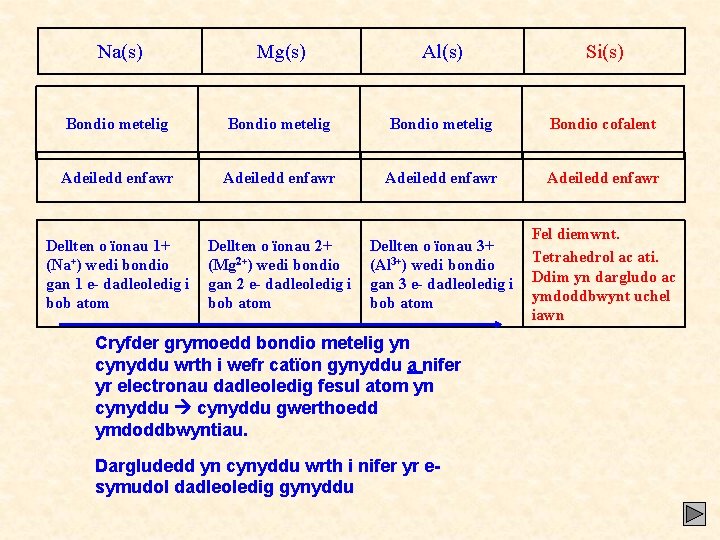
Na(s) Mg(s) Al(s) Si(s) Bondio metelig Bondio cofalent Adeiledd enfawr Dellten o ïonau 1+ (Na+) wedi bondio gan 1 e- dadleoledig i bob atom Dellten o ïonau 2+ (Mg 2+) wedi bondio gan 2 e- dadleoledig i bob atom Dellten o ïonau 3+ (Al 3+) wedi bondio gan 3 e- dadleoledig i bob atom Fel diemwnt. Tetrahedrol ac ati. Ddim yn dargludo ac ymdoddbwynt uchel iawn Cryfder grymoedd bondio metelig yn cynyddu wrth i wefr catïon gynyddu a nifer yr electronau dadleoledig fesul atom yn cynyddu gwerthoedd ymdoddbwyntiau. Dargludedd yn cynyddu wrth i nifer yr esymudol dadleoledig gynyddu
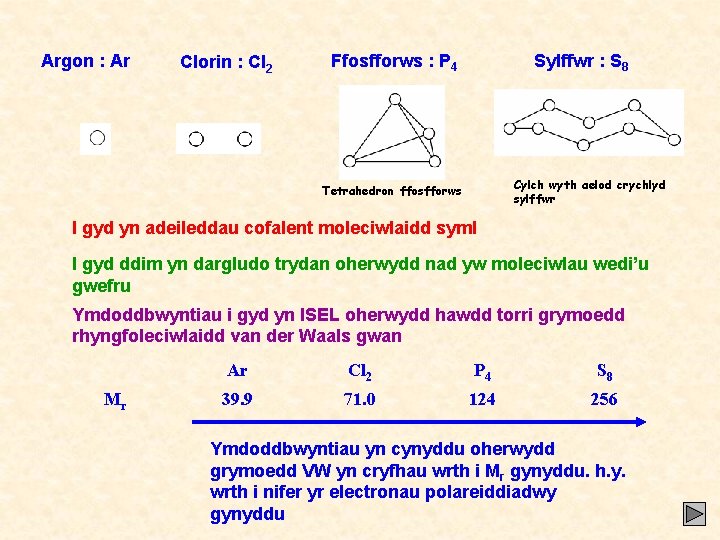
Argon : Ar Clorin : Cl 2 Ffosfforws : P 4 Sylffwr : S 8 Cylch wyth aelod crychlyd sylffwr Tetrahedron ffosfforws I gyd yn adeileddau cofalent moleciwlaidd syml I gyd ddim yn dargludo trydan oherwydd nad yw moleciwlau wedi’u gwefru Ymdoddbwyntiau i gyd yn ISEL oherwydd hawdd torri grymoedd rhyngfoleciwlaidd van der Waals gwan Mr Ar Cl 2 P 4 S 8 39. 9 71. 0 124 256 Ymdoddbwyntiau yn cynyddu oherwydd grymoedd VW yn cryfhau wrth i Mr gynyddu. h. y. wrth i nifer yr electronau polareiddiadwy gynyddu
- Slides: 7