Cellule staminali e cellule staminali tumorali Quali cellule



















- Slides: 48

Cellule staminali e cellule staminali tumorali Quali cellule sono responsabili per la crescita del tumore?

Cellule staminali • Sono cellule che hanno la capacitá di perpetuarsi indefinitamente (“self-renewal”) • Attraverso il differenziamento, esse danno vita alle cellule “mature” • Le cellule differenziate originano dalle cellule staminali del medesimo compartimento • Plasticitá delle cellule staminali: apparentemente, le cellule staminali di un tessuto possono dare origine anche a cellule mature di altri tessuti

Cellule staminali e cellule tumorali • Il tumore è costituito da cellule con una capacità di self-renewal indefinita • La comprensione dei meccanismi di self-renewal delle cellule staminali puó aiutarci a comprendere il tumore

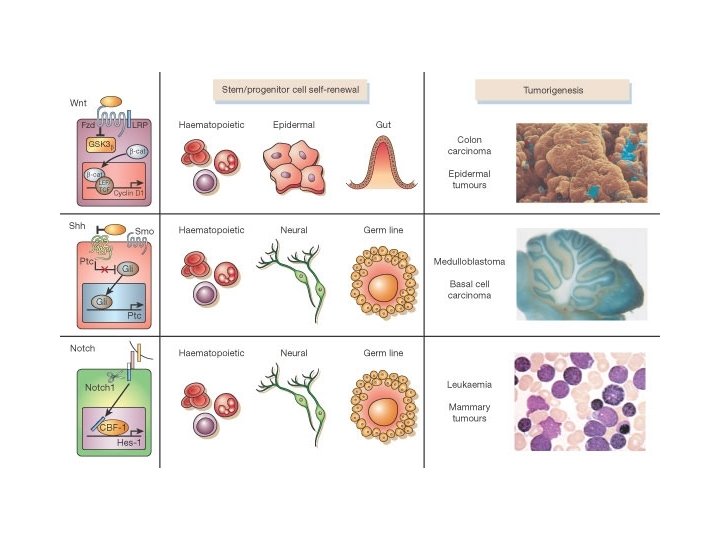
Pathway coinvolti nel selfrenewal e nell’oncogenesi • Ipotesi: le cellule tumorali -capaci di selfrenewal- utilizzano la “machinery” presente nelle cellule staminali • Dimostrazione indiretta di tale ipotesi é il fatto che diversi pathway associati all’oncogenesi sono stati coinvolti nel selfrenewal delle cellule staminali

I pathway di Notch, Shh, Wnt • Notch: l’attivazione di questo pathway é associata ad un aumento del pool delle cellule staminali • Shh: popolazioni arricchite di cellule staminali umane rispondono in vitro a Shh con un aumentato self-renewal • Wnt: la sua attivazione espande il pool di cellule staminali, mentre la sua soppressione inibisce la proliferazione delle cellule staminali


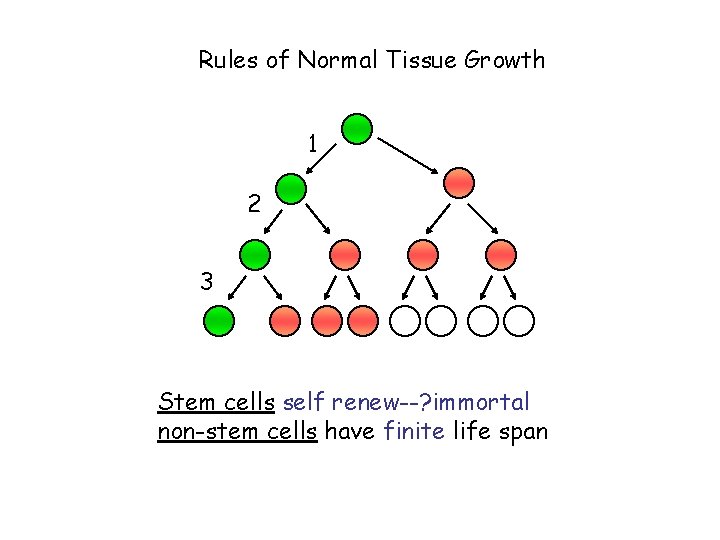
Rules of Normal Tissue Growth 1 2 3 Stem cells self renew--? immortal non-stem cells have finite life span

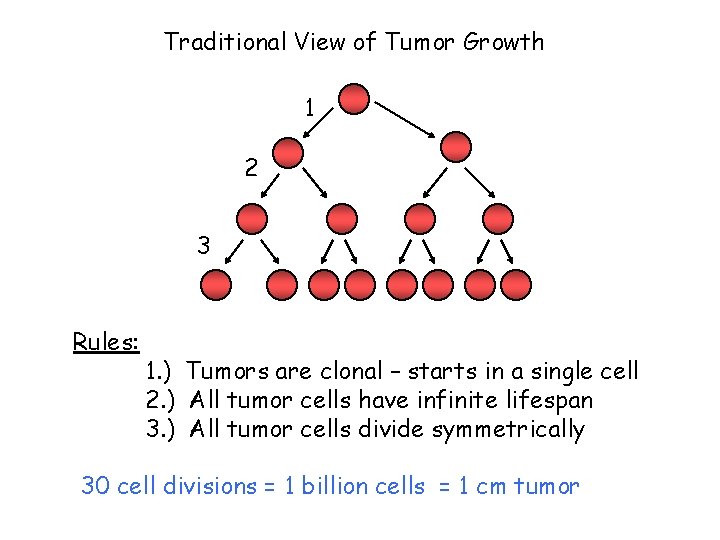
Traditional View of Tumor Growth 1 2 3 Rules: 1. ) Tumors are clonal – starts in a single cell 2. ) All tumor cells have infinite lifespan 3. ) All tumor cells divide symmetrically 30 cell divisions = 1 billion cells = 1 cm tumor

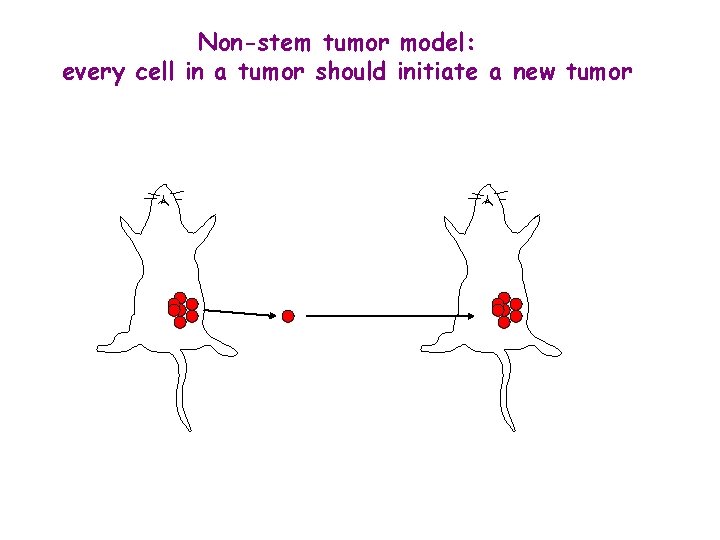
Non-stem tumor model: every cell in a tumor should initiate a new tumor

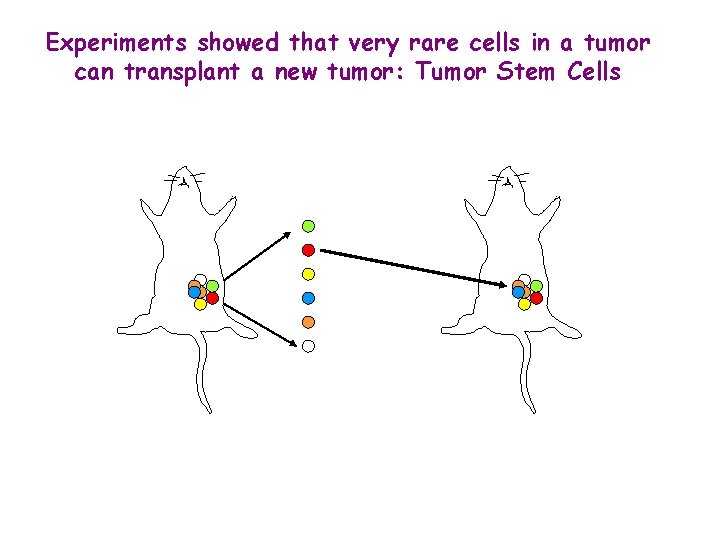
Experiments showed that very rare cells in a tumor can transplant a new tumor: Tumor Stem Cells

Origin of the Theory of Cancer Stem Cells Only a small subset of cancer cells is capable of extensive proliferation Liquid Tumors In vitro colony forming assays: - 1 in 10, 000 to 1 in 100 mouse myeloma cells obtained from ascites could form colonies In vivo transplantation assays: - Only 1 -4% of transplanted leukaemic cells could form spleen colonies Solid Tumors - A large number of cells are required to grow tumors in xenograft models - 1 in 1, 000 to 1 in 5, 000 lung cancer, neuroblastoma cells, ovarian cancer cells, or breast cancer cell from cell lines can form colonies in soft agar or in vivo (fewer with 10 tumor cells)

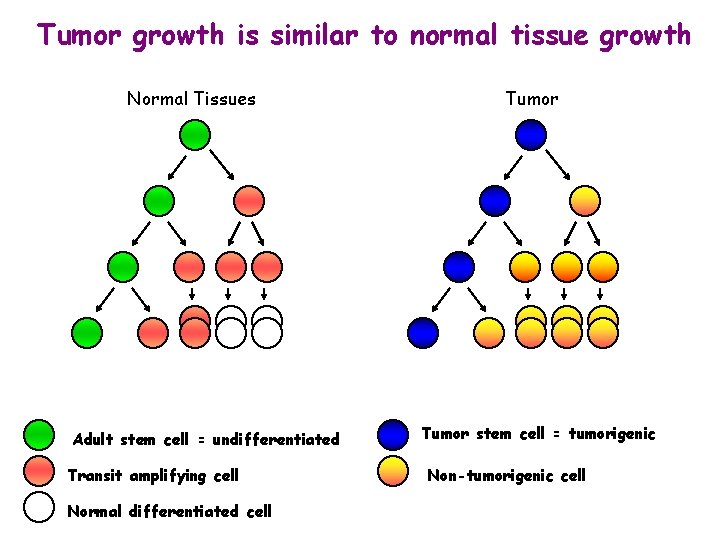
Tumor growth is similar to normal tissue growth Normal Tissues Adult stem cell = undifferentiated Transit amplifying cell Normal differentiated cell Tumor stem cell = tumorigenic Non-tumorigenic cell

Cellule staminali tumorali: organogenesi aberrante • Il tumore puó essere immaginato come un organo aberrante originato da una cellula trasformata che ha acquisito la capacitá di proliferare indefinitamente attraverso varie mutazioni • La popolazione tumorale é eterogenea, e spesso contiene cellule a diversi stadi di differenziamento (seppure anomali): data la clonalitá dei tumori, questo dato implica che la progenie delle cellule tumorali si diversifica (“differenzia”)

Evidenze per la presenza di cellule staminali tumorali

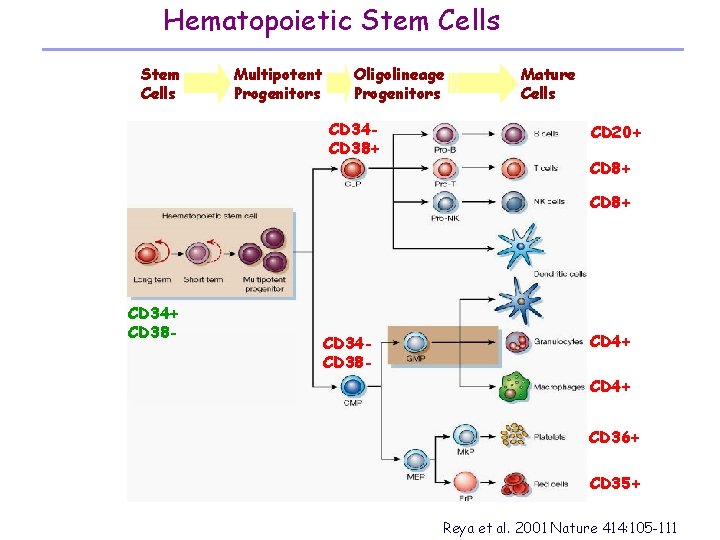
Hematopoietic Stem Cells Multipotent Progenitors Oligolineage Progenitors CD 34 CD 38+ Mature Cells CD 20+ CD 8+ CD 34+ CD 38 - CD 34 CD 38 - CD 4+ CD 36+ CD 35+ Reya et al. 2001 Nature 414: 105 -111

Cellule staminali ematopoietiche • Le cellule caratterizzate con maggiore precisione, grazie ad esperimenti di ripopolamento di topi letalmente irradiati e ricostituiti con popolazioni cellulari altamente purificate a partire dal midollo osseo • Le cellule staminali (0. 05% delle cellule totali del midollo) danno origine ai progenitori ematopoietici che perdono il loro potenziale di self -renewal

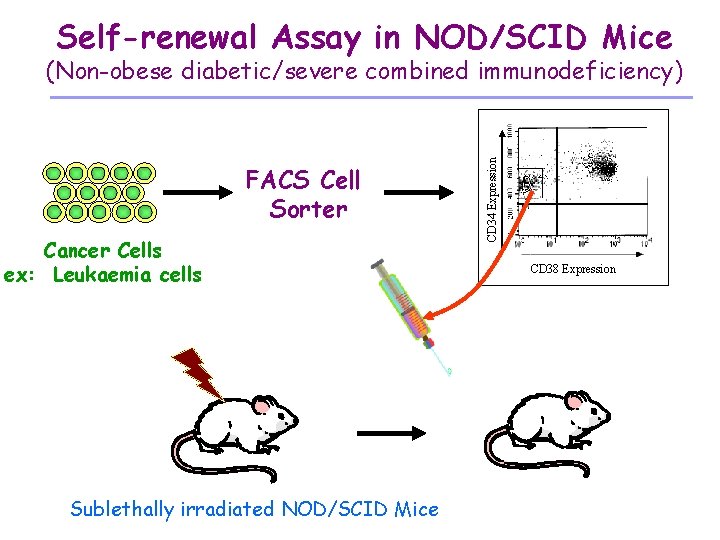
Self-renewal Assay in NOD/SCID Mice FACS Cell Sorter Cancer Cells ex: Leukaemia cells Sublethally irradiated NOD/SCID Mice CD 34 Expression (Non-obese diabetic/severe combined immunodeficiency) CD 38 Expression

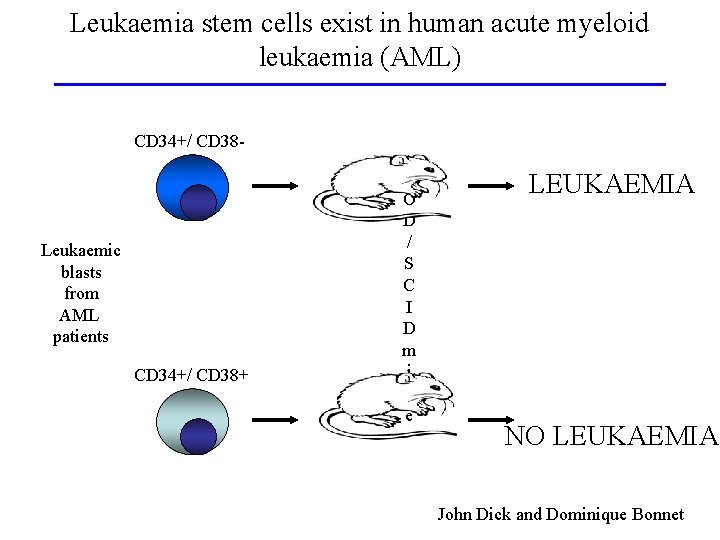
Leukaemia stem cells exist in human acute myeloid leukaemia (AML) CD 34+/ CD 38 - Leukaemic blasts from AML patients CD 34+/ CD 38+ N O D / S C I D m i c e LEUKAEMIA NO LEUKAEMIA John Dick and Dominique Bonnet

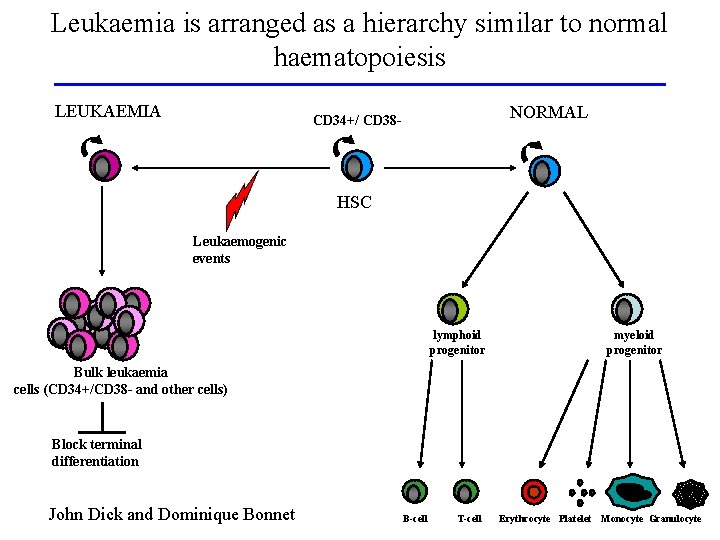
Leukaemia is arranged as a hierarchy similar to normal haematopoiesis LEUKAEMIA NORMAL CD 34+/ CD 38 - HSC Leukaemogenic events lymphoid progenitor myeloid progenitor Bulk leukaemia cells (CD 34+/CD 38 - and other cells) Block terminal differentiation John Dick and Dominique Bonnet B-cell T-cell Erythrocyte Platelet Monocyte Granulocyte

Le cellule staminali tumorali come meccanismo di mantenimento del tumore 1. 2. 3. Isolamento di sub-popolazioni cellulari con marcatori di superficie caratteristici delle SC normali (CD 34+CD 38 -), o di cellule piú differenziate, da blasti leucemici di pazienti affetti da varie forme di leucemia mieloide acuta Reinoculo di queste cellule in topi NOD/SCID ed analisi della loro capacitá leuchemogenica Mentre le cellule CD 34+38 - sono leuchemogeniche, quelle CD 34+CD 38+ non possono trasferire la leucemia nell’animale immunocompromesso 4. Le cellule tumorali non sono tutte uguali, e le CSC sono responsabili del mantenimento della massa tumorale

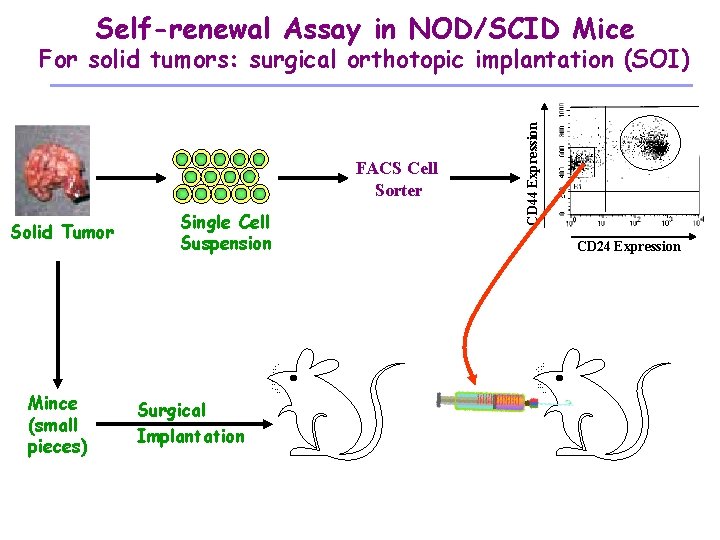
Evidenze da altri tumori Nei tumori solidi si può osservare sperimentalmente una simile struttura gerarchica (i marker sono definiti in maniera meno precisa)

Self-renewal Assay in NOD/SCID Mice FACS Cell Sorter Solid Tumor Mince (small pieces) Single Cell Suspension Surgical Implantation CD 44 Expression For solid tumors: surgical orthotopic implantation (SOI) CD 24 Expression

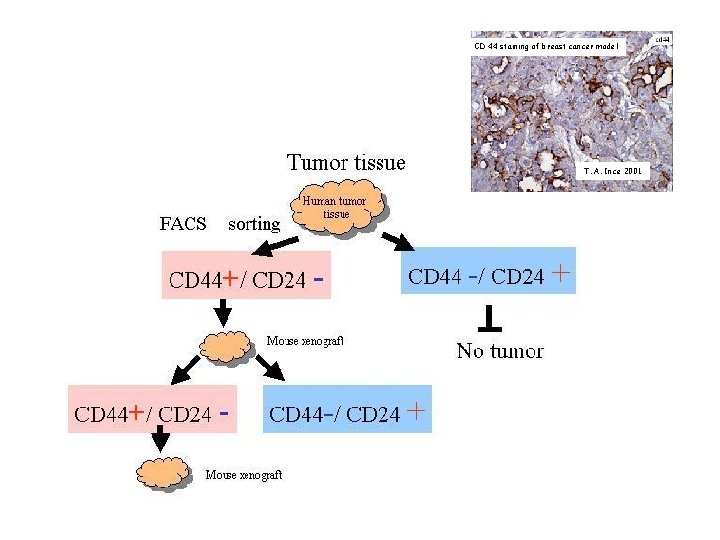
CD 44 staining of breast cancer model T. A. Ince 2001

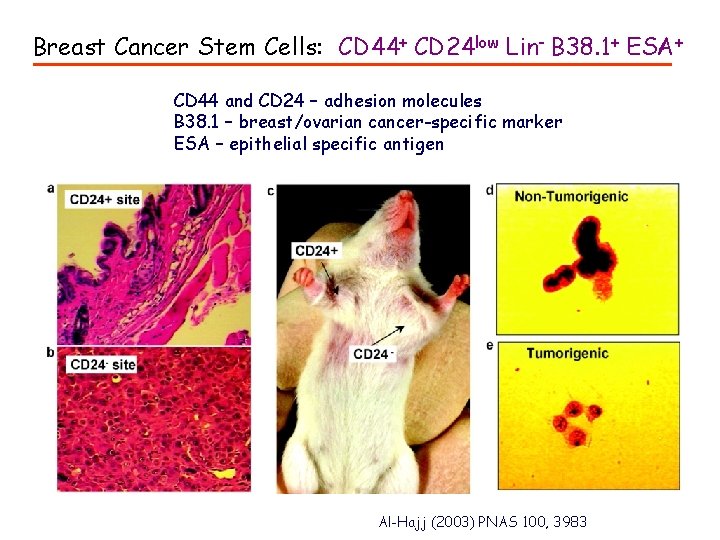
Breast Cancer Stem Cells: CD 44+ CD 24 low Lin- B 38. 1+ ESA+ CD 44 and CD 24 – adhesion molecules B 38. 1 – breast/ovarian cancer-specific marker ESA – epithelial specific antigen Al-Hajj (2003) PNAS 100, 3983

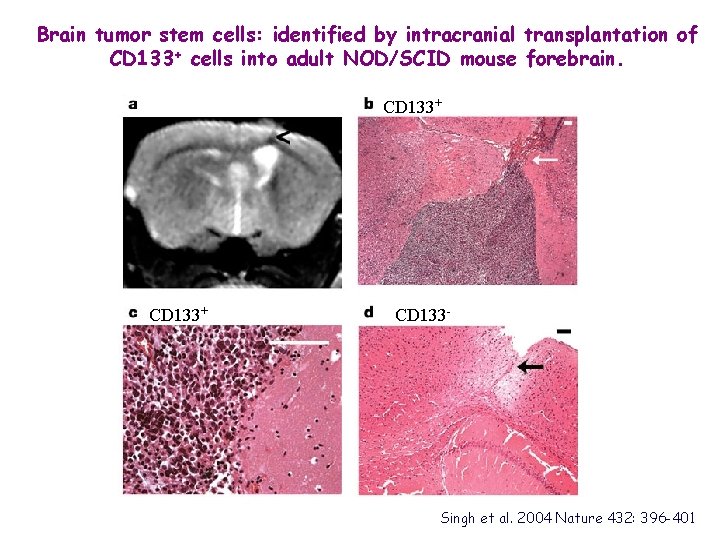
Brain tumor stem cells: identified by intracranial transplantation of CD 133+ cells into adult NOD/SCID mouse forebrain. CD 133+ CD 133 - Singh et al. 2004 Nature 432: 396 -401

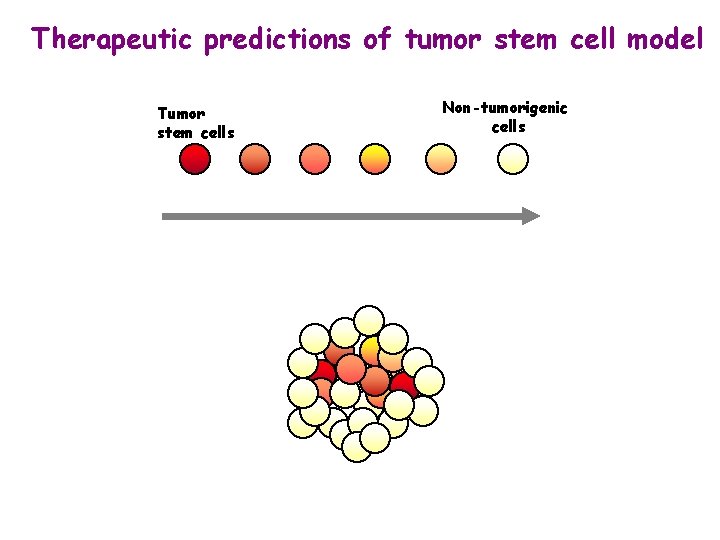
Therapeutic predictions of tumor stem cell model Tumor stem cells Non-tumorigenic cells

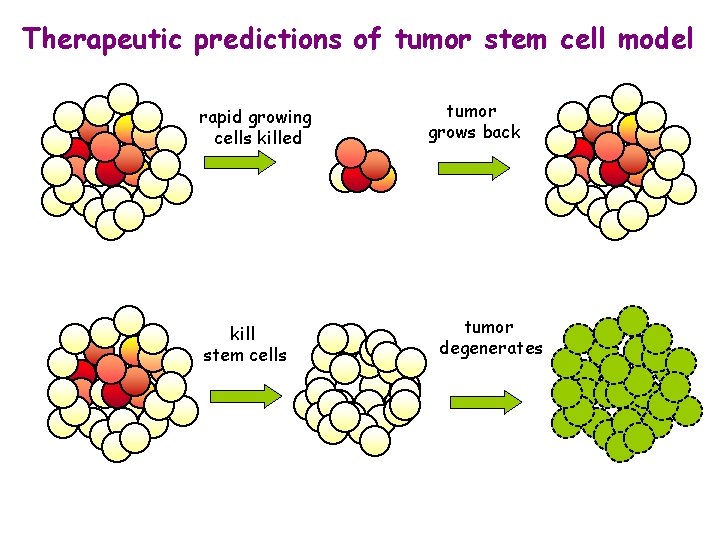
Therapeutic predictions of tumor stem cell model rapid growing cells killed kill stem cells tumor grows back tumor degenerates

Therapeutic implications of Cancer Stem Cells Hypothesis: -Most therapies (chemotherapy and radiation) target rapidly proliferating, non-tumorigenic cells and spare the relatively quiescent cancer stem cells -Cell surface pumps -Cancer stem cells have greater invasive and migratory properties and can home to specific tissue niches

Cancer stem cells sono più resistenti alle terapie antitumorali

Experimental models in vitro models (ex vivo ) • Cultured cell from human gliomas: D 456 MG D 54 MG • Patient glioblastoma samples in vivo models • Human xenograft models in immunocompromised mice

Resistance to radiation: → given by CD 133+

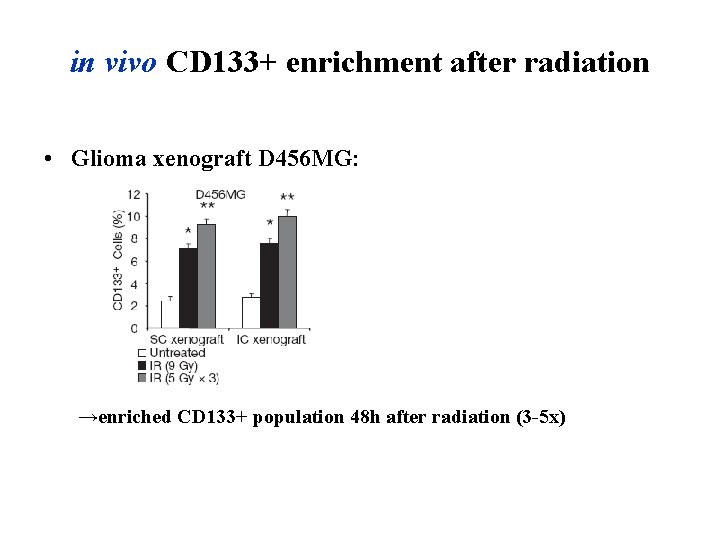
in vivo CD 133+ enrichment after radiation • Glioma xenograft D 456 MG: →enriched CD 133+ population 48 h after radiation (3 -5 x)

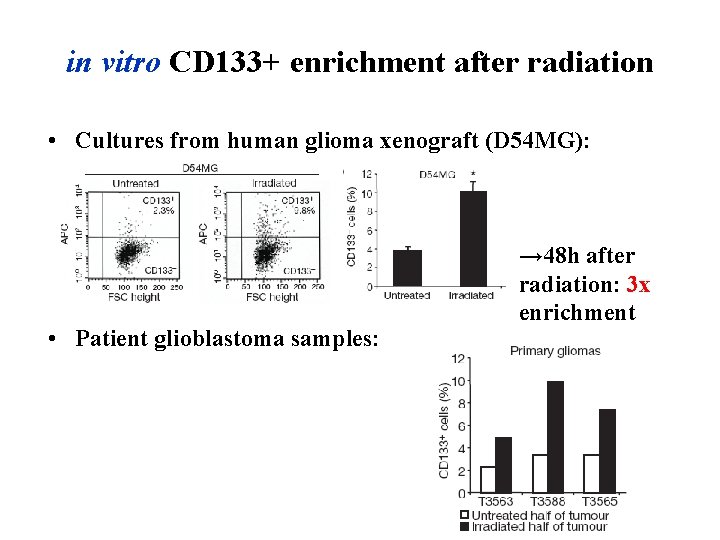
in vitro CD 133+ enrichment after radiation • Cultures from human glioma xenograft (D 54 MG): • Patient glioblastoma samples: → 48 h after radiation: 3 x enrichment

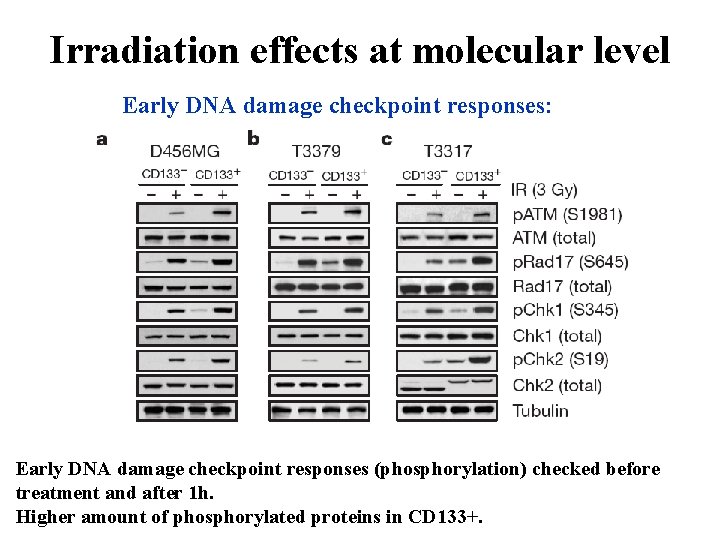
Irradiation effects at molecular level Early DNA damage checkpoint responses: Early DNA damage checkpoint responses (phosphorylation) checked before treatment and after 1 h. Higher amount of phosphorylated proteins in CD 133+.

In cosa differiscono le cancer stem cells dalle cellule staminali normali?




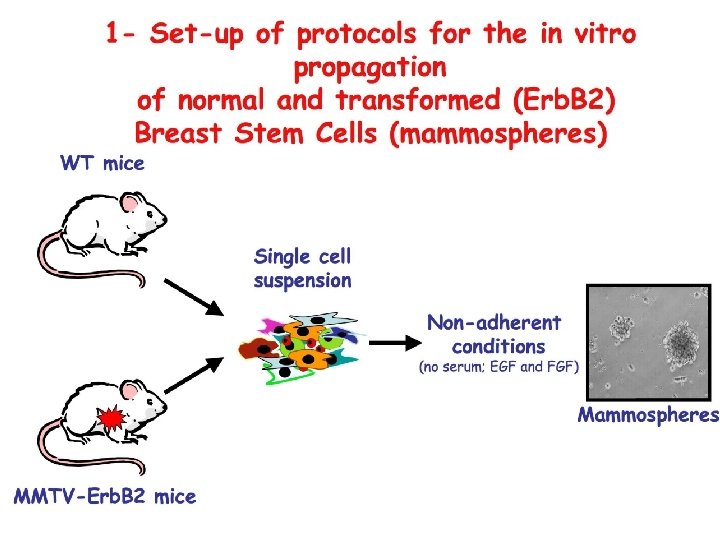
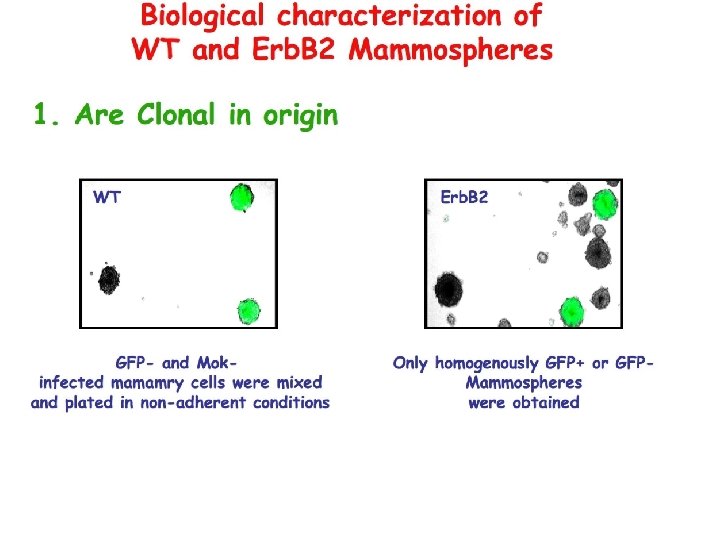
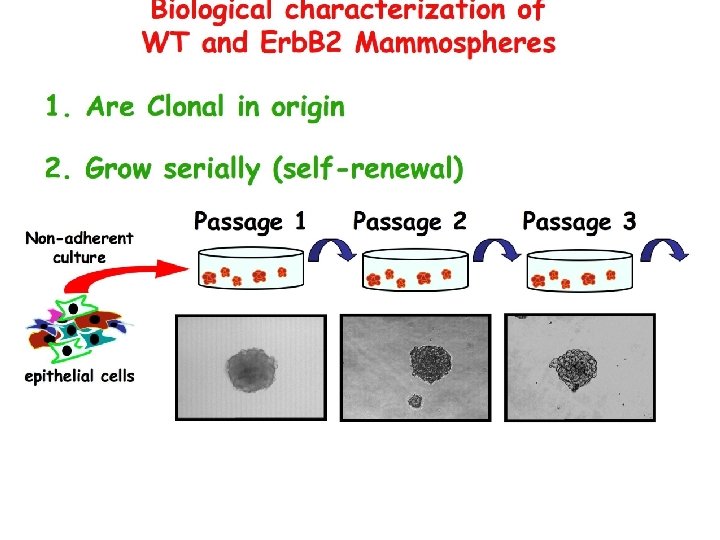
Biological characterization of WT and Erb. B 2 Mammospheres 1. Are Clonal in origin 2. Grow serially (self-renewal) 3. Contain SCs Transplantation into the cleared fat pad of syngenic mice: • WT mammospheres form a normal breast tissue • Erb. B 2 mammospheres form tumors

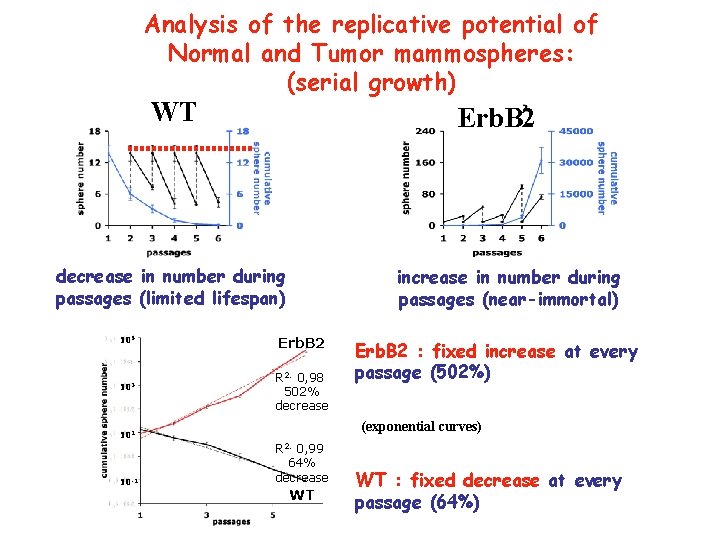
Analysis of the replicative potential of Normal and Tumor mammospheres: (serial growth) WT Erb. B 2 decrease in number during passages (limited lifespan) 105 103 increase in number during passages (near-immortal) Erb. B 2 R 2: 0, 98 502% decrease (exponential curves) 101 10 -1 Erb. B 2 : fixed increase at every passage (502%) R 2: 0, 99 64% decrease WT WT : fixed decrease at every passage (64%)

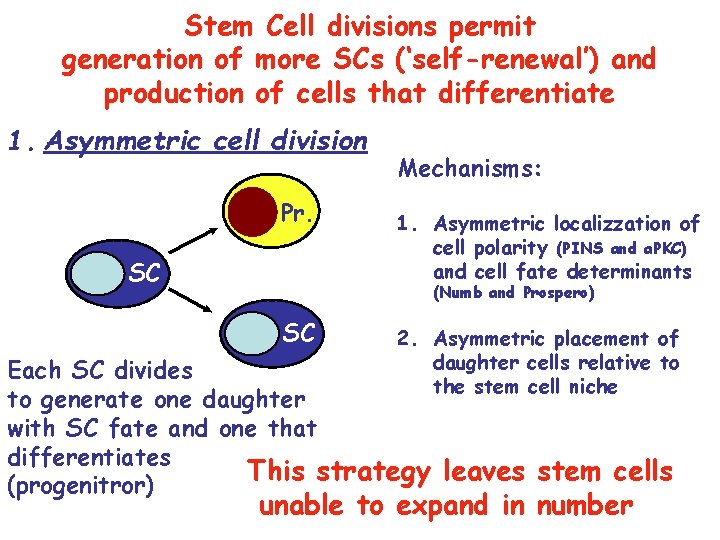
Stem Cell divisions permit generation of more SCs (‘self-renewal’) and production of cells that differentiate 1. Asymmetric cell division Pr. SC Mechanisms: 1. Asymmetric localizzation of cell polarity (PINS and a. PKC) and cell fate determinants (Numb and Prospero) SC 2. Asymmetric placement of daughter cells relative to the stem cell niche Each SC divides to generate one daughter with SC fate and one that differentiates This strategy leaves stem cells (progenitror) unable to expand in number

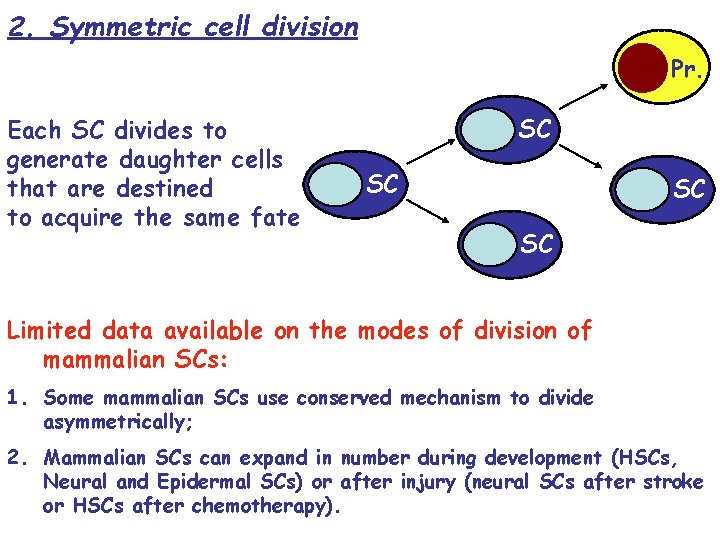
2. Symmetric cell division Pr. Each SC divides to generate daughter cells that are destined to acquire the same fate SC SC Limited data available on the modes of division of mammalian SCs: 1. Some mammalian SCs use conserved mechanism to divide asymmetrically; 2. Mammalian SCs can expand in number during development (HSCs, Neural and Epidermal SCs) or after injury (neural SCs after stroke or HSCs after chemotherapy).

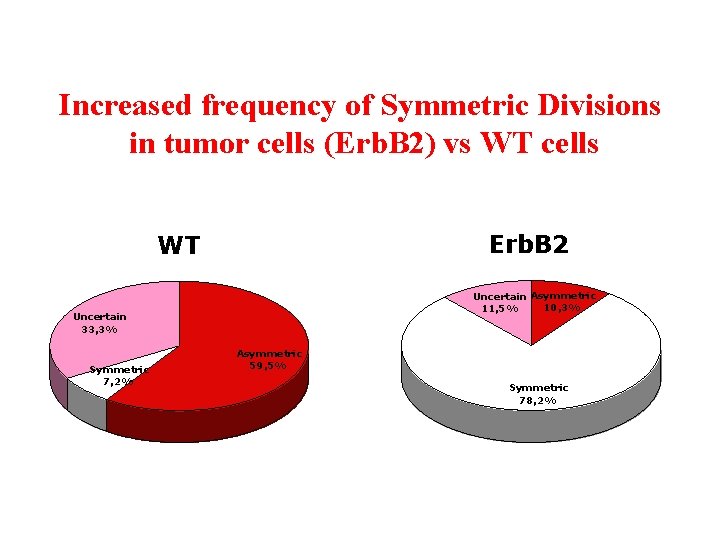
Increased frequency of Symmetric Divisions in tumor cells (Erb. B 2) vs WT cells Erb. B 2 WT Uncertain Asymmetric 10, 3% 11, 5% Uncertain 33, 3% Symmetric 7, 2% Asymmetric 59, 5% Symmetric 78, 2%

Aggiornamento dei risultati di Dick e Bonnet nelle leucemie • Utilizzando topi immunocompromessi con alterazioni genetiche addizionali (> grado di immunocompromissione) il dato originale viene confermato (la frazione CD 34+CD 38 - contiene le cellule staminali della leucemia), ma in una certa percentuale di leucemie anche la frazione CD 34+CD 38+ contiene cellule staminali in minore proporzione rispetto alle CD 34+CD 38– In questi casi I livelli di espressione di alcuni mi. RNA sono più precisi dei marker di superficie nel definire le cellule staminali leucemiche • Maggiore eterogeneità nel definire I marcatori di superficie delle cellule staminali tumorali

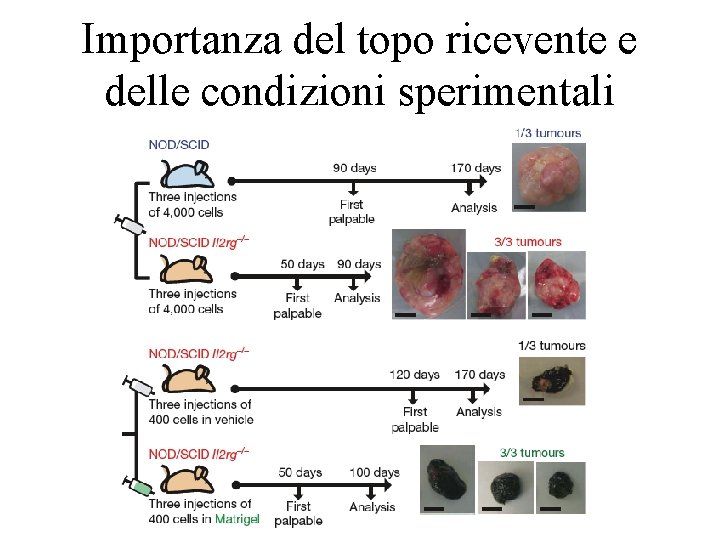
Nuovi risultati e incertezze anche nei tumori solidi • I dati di maggiore rilevanza a supporto della teoria delle CSC derivano da xenotrapianti di cellule tumorali umane in topi immunocompromessi • Recentemente è apparso un lavoro molto importante sulla caratterizzazione delle CSC nel melanoma, dove emerge che: – almeno in questo tumore, il numero di cellule con caratteristiche di CSC è altissimo (se si accettano alcune assunzioni, si arriva quasi al 100% delle cellule): se tutte le cellule sono CSC, le CSC non esistono – i protocolli sperimentali per gli xenotrapianti possono influenzare l’attecchimento di determinate sottopopolazioni

Importanza del topo ricevente e delle condizioni sperimentali

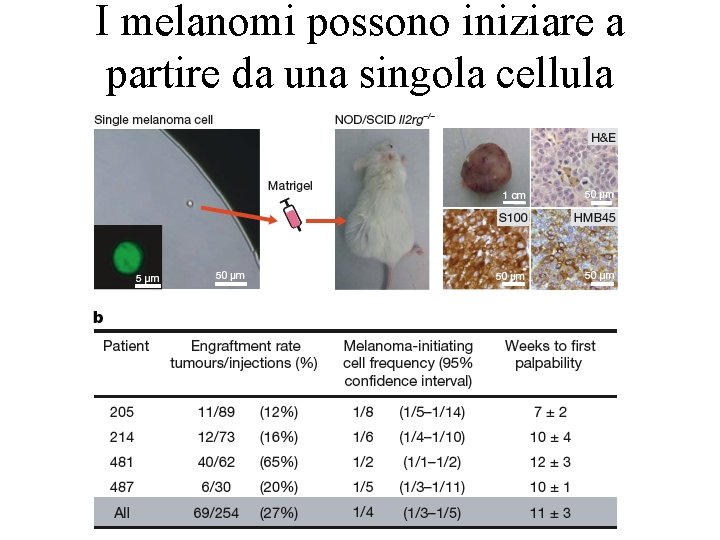
I melanomi possono iniziare a partire da una singola cellula

Ci sono modelli complementari/alternativi? • Plasticità fenotipica: non c’è una vera e propria gerarchia (staminale->non-staminale), ma diversi stati cellulari determinati dalle condizioni “ambientali” (microambiente e segnali) – La stessa cellula può assumere reversibilmente morfologia diversa, espressione di diversi pattern trascrizionali e non di mutazioni irreversibili, manifestando nei suoi diversi fenotipi una maggiore o minore propensione alla “staminalità”