Catalyse enzymatique Dr BENSAAD S Maitre Assistante en

Catalyse enzymatique Dr BENSAAD. S Maitre Assistante en Biochimie 2ème année Pharmacie: 2019/2020 catalyse enzymatique

Objectifs du cours • Définir le principe de la catalyse enzymatique • Expliquer le rôle du site actif et des coenzymes dans la réaction enzymatique • Expliquer le mode d’action des enzymes catalyse enzymatique
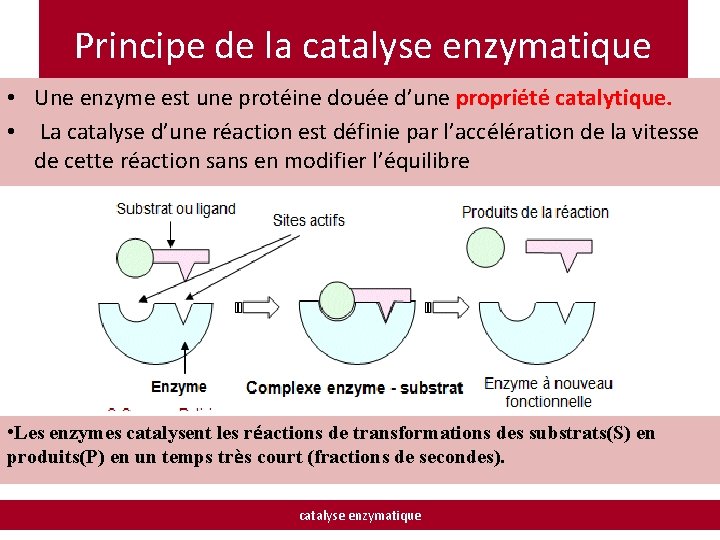
Principe de la catalyse enzymatique • Une enzyme est une protéine douée d’une propriété catalytique. • La catalyse d’une réaction est définie par l’accélération de la vitesse de cette réaction sans en modifier l’équilibre • Les enzymes catalysent les réactions de transformations des substrats(S) en produits(P) en un temps très court (fractions de secondes). catalyse enzymatique
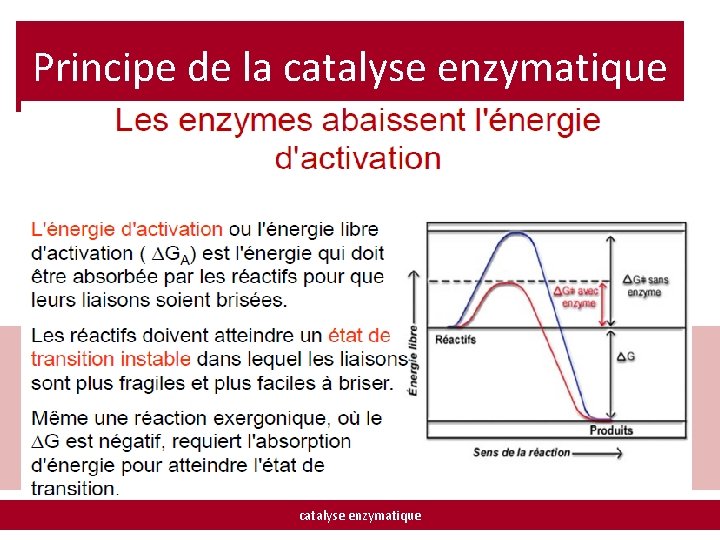
Principe de la catalyse enzymatique
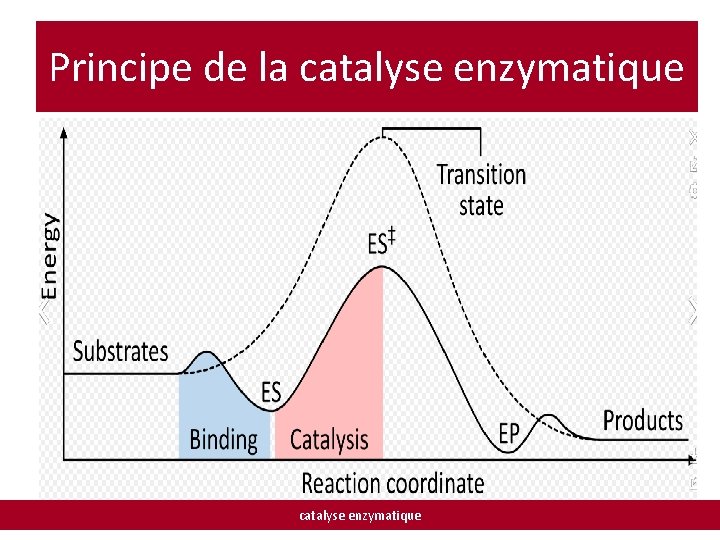
Principe de la catalyse enzymatique
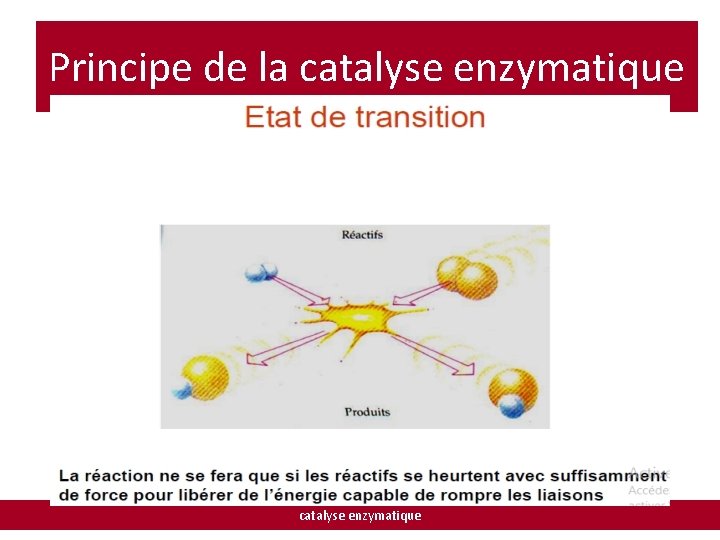
Principe de la catalyse enzymatique
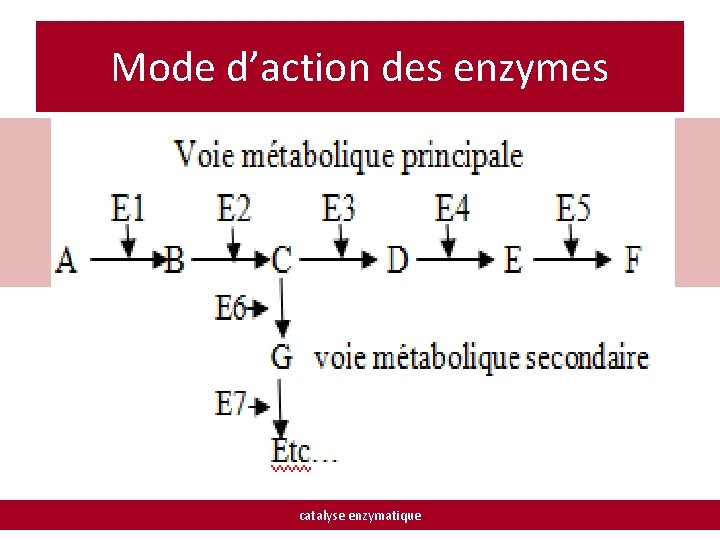
Mode d’action des enzymes catalyse enzymatique

Mode d’action des enzymes La spécificité Les enzymes présentent une double spécificité Spécificité d’action: Spécificité de substrat: une enzyme ne catalyse, pour un substrat donné, qu’un seul type de réaction. Ex: pour un AA on pourra avoir soit une transamination, une décarboxylation, une oxydation… une enzyme n’agit que sur un substrat ou une classe de substrat. *l’amylase salivaire n’hydrolyse que l’amidon en maltose (spécificité étroite) Les phosphodiestérases hydrolysent les esters de l’acide phosphorique (spécificité de groupe). la Stéréospécificité : l’enzyme distingue des isomères optiques (L-D) ou des isomères Z et E (cis-trans) catalyse enzymatique
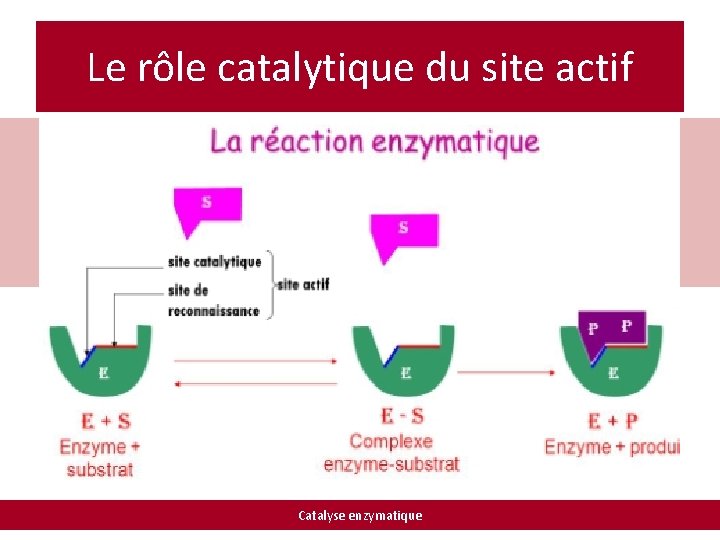
Le rôle catalytique du site actif Catalyse enzymatique
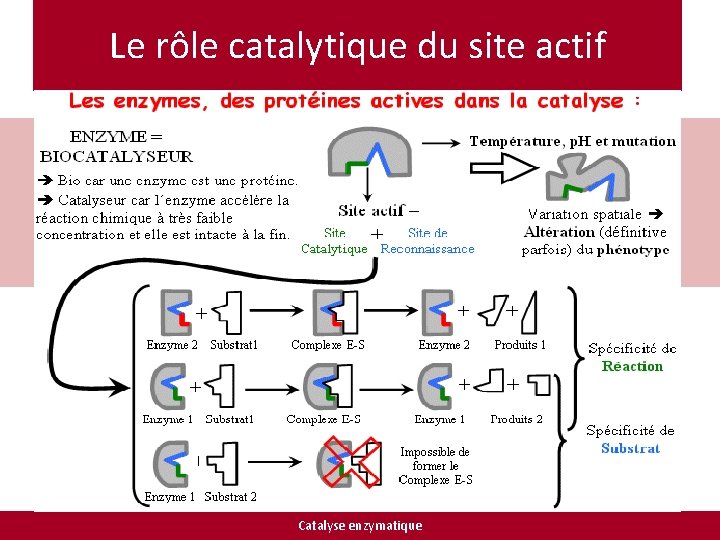
Le rôle catalytique du site actif Catalyse enzymatique

Le rôle des cofacteurs De nature organique: les coenzymes De nature inorganique: les ions métalliques Catalyse enzymatique

Les ions métalliques Mg 2+, Mn 2+, Cu 2+, Zn 2+, Fe 2+… Exemples: Fer: cytochrome oxydase, catalase et peoxydase… Zn 2+ dans l’alcool deshydogénase forme un pont entre l’enzyme et son substrat Mg 2+: indispensable aux kinases Catalyse enzymatique

les coenzymes Catalyse enzymatique
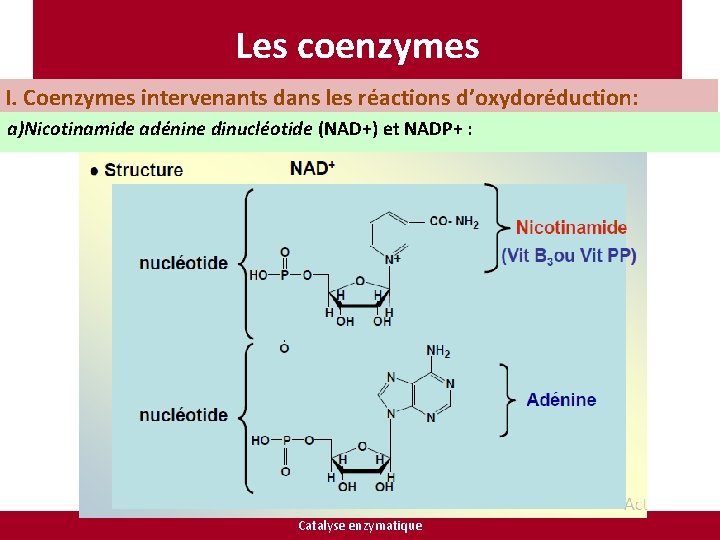
Les coenzymes I. Coenzymes intervenants dans les réactions d’oxydoréduction: a)Nicotinamide adénine dinucléotide (NAD+) et NADP+ : Catalyse enzymatique
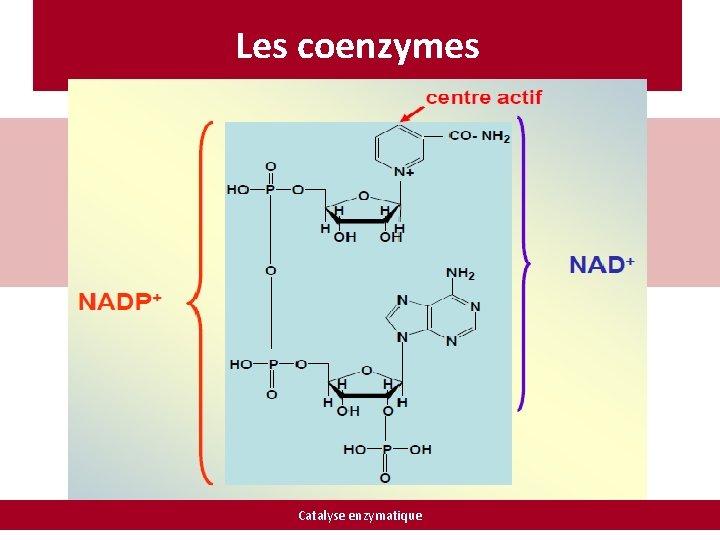
Les coenzymes Catalyse enzymatique
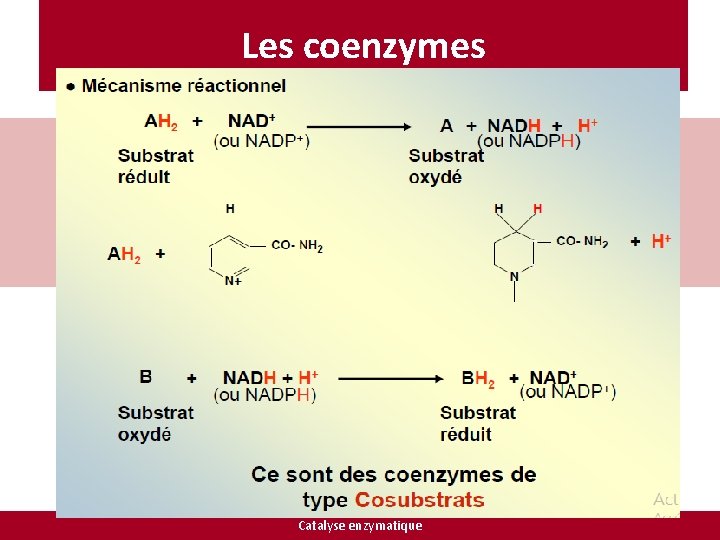
Les coenzymes Catalyse enzymatique
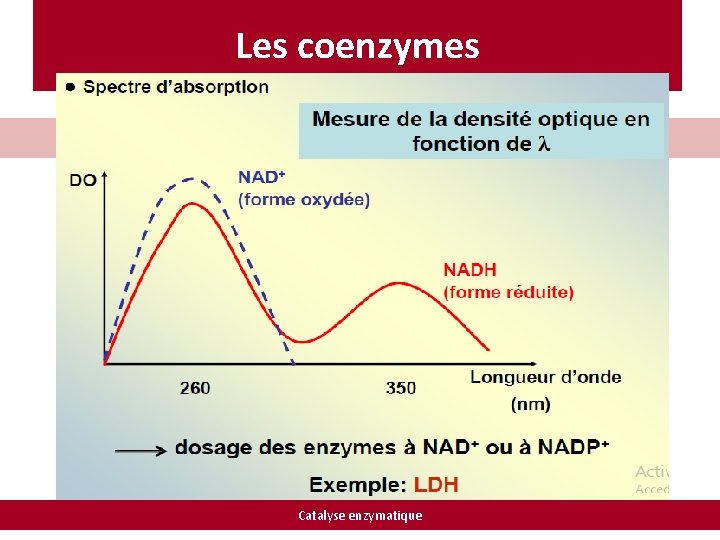
Les coenzymes Catalyse enzymatique
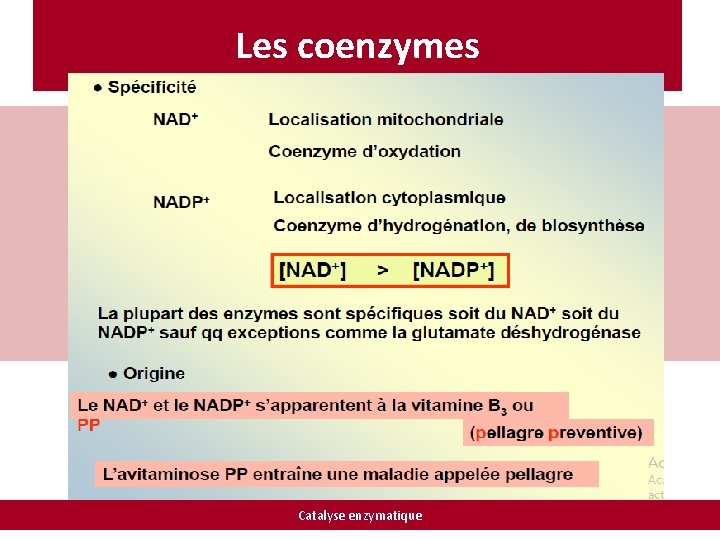
Les coenzymes Catalyse enzymatique
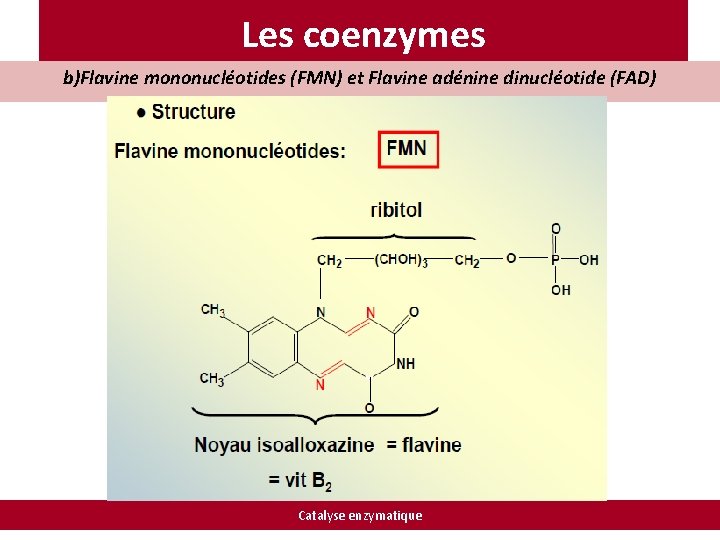
Les coenzymes b)Flavine mononucléotides (FMN) et Flavine adénine dinucléotide (FAD) Catalyse enzymatique
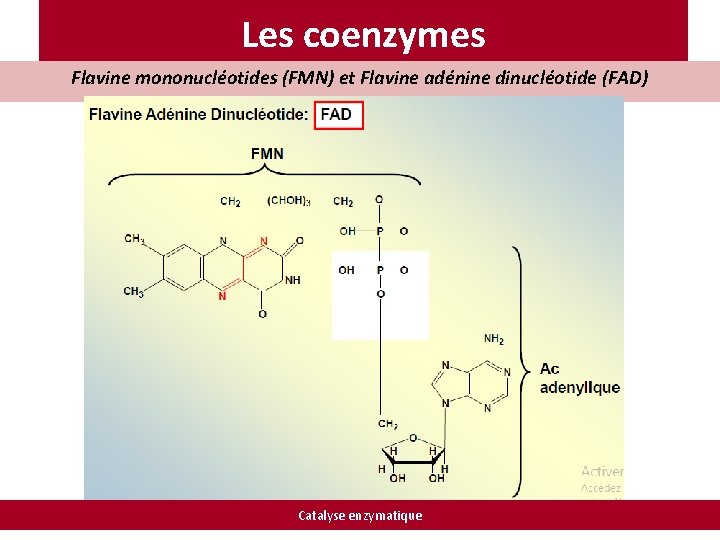
Les coenzymes Flavine mononucléotides (FMN) et Flavine adénine dinucléotide (FAD) Catalyse enzymatique

Les coenzymes Catalyse enzymatique
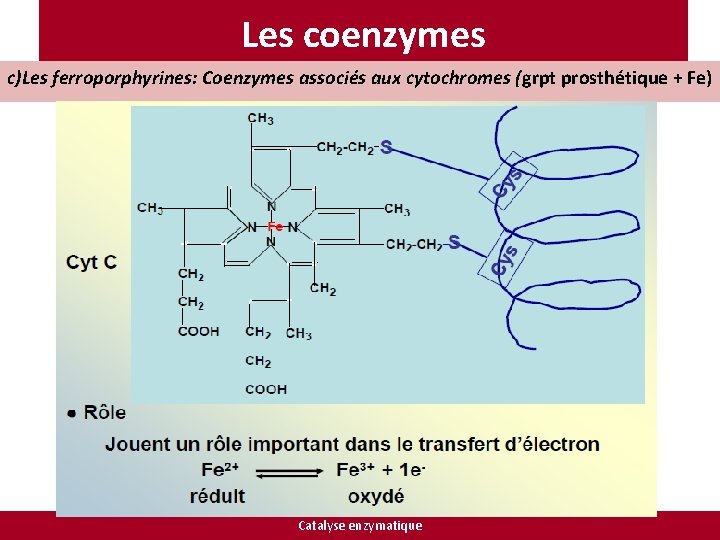
Les coenzymes c)Les ferroporphyrines: Coenzymes associés aux cytochromes (grpt prosthétique + Fe) Catalyse enzymatique
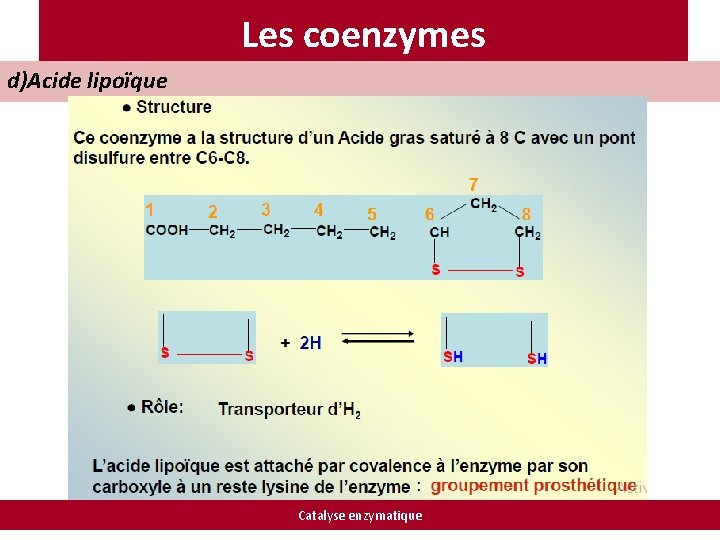
Les coenzymes d)Acide lipoïque Catalyse enzymatique
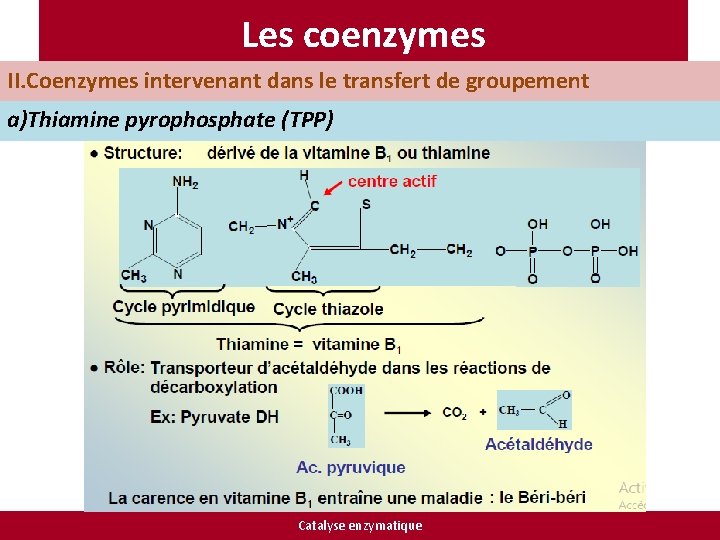
Les coenzymes II. Coenzymes intervenant dans le transfert de groupement a)Thiamine pyrophosphate (TPP) Catalyse enzymatique
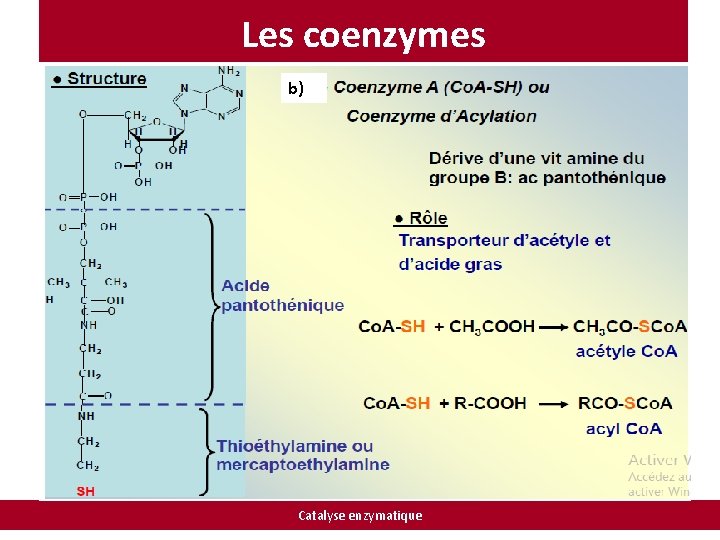
Les coenzymes b) Catalyse enzymatique
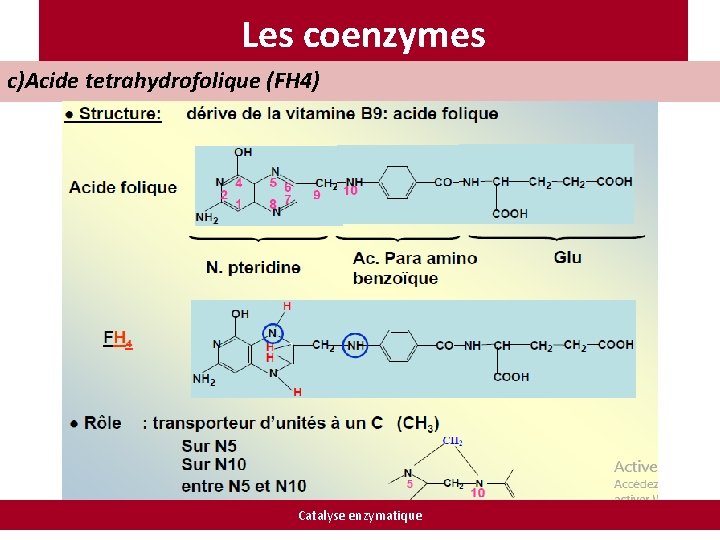
Les coenzymes c)Acide tetrahydrofolique (FH 4) Catalyse enzymatique
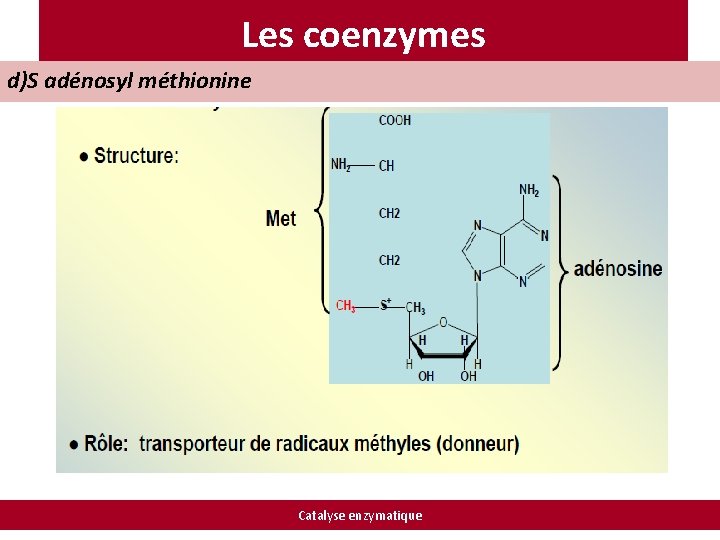
Les coenzymes d)S adénosyl méthionine Catalyse enzymatique
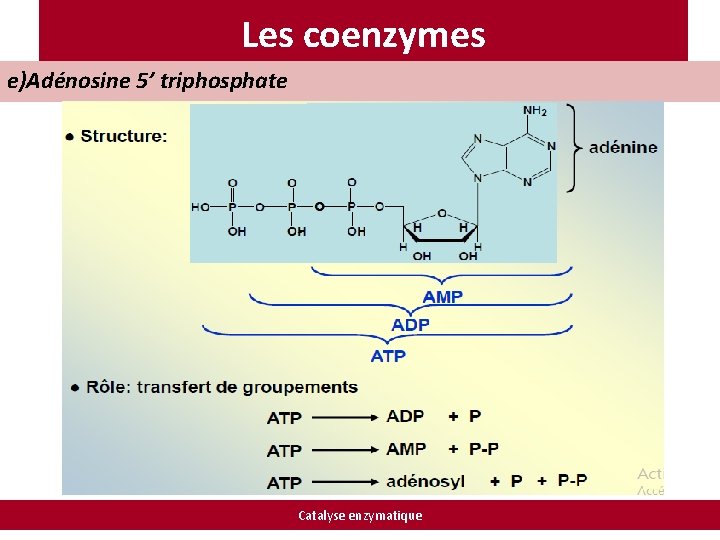
Les coenzymes e)Adénosine 5’ triphosphate Catalyse enzymatique
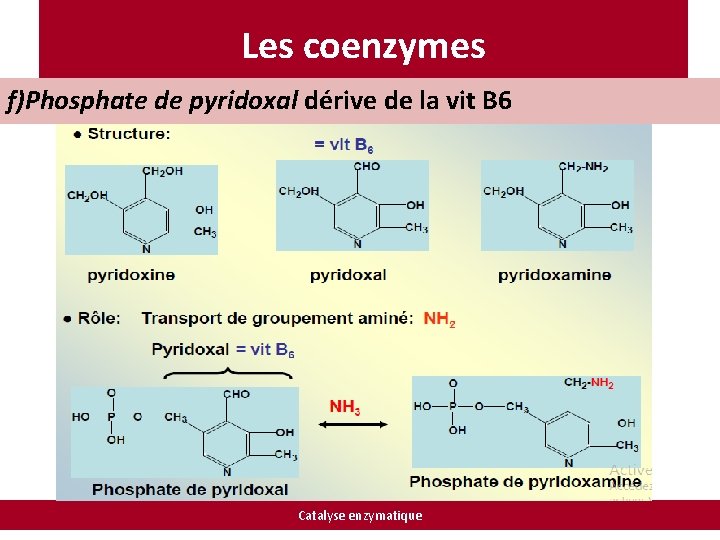
Les coenzymes f)Phosphate de pyridoxal dérive de la vit B 6 Catalyse enzymatique
Mécanismes catalytiques Catalyse acide/base Catalyse covalente Catalyse métallodépendante Catalyse par effets de proximité et facteurs d’orientation Catalyse par liaison et stabilisation de l’état de transition Catalyse enzymatique
Mécanismes catalytiques Catalyse acide/base Catalyse covalente Catalyse métallodépendante Catalyse par effets de proximité et facteurs d’orientation Catalyse par liaison et stabilisation de l’état de transition Catalyse enzymatique

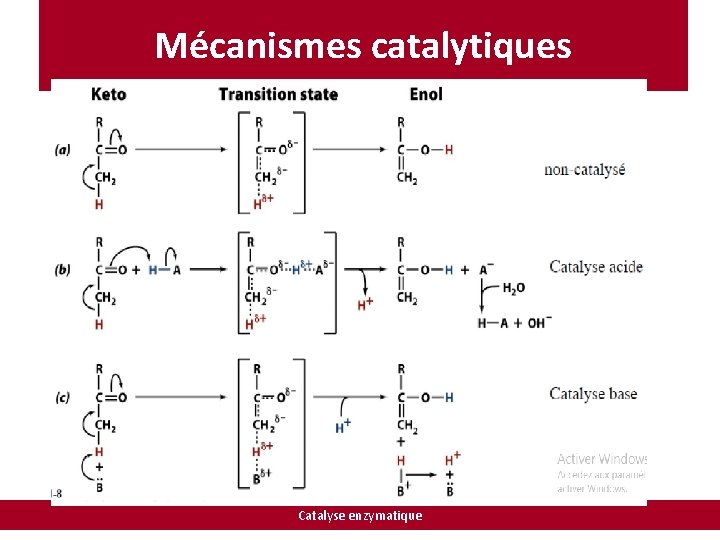
Mécanismes catalytiques La catalyse acide générale est un procédé dans lequel le transfert partiel d'un proton à partir d'un groupe acide abaisse l'énergie libre de l'état de transition. Une réaction peut aussi être stimulée par la catalyse basique générale, si la vitesse de la réaction est augmentée par l'abstraction partielle d'un proton par une base. Catalyse enzymatique
Mécanismes catalytiques Catalyse enzymatique

Mécanismes catalytiques (a) la réaction non catalysée est lente. (b) catalyse acide générale : l’acide AH accélère la réaction en donnant son proton H+. (c) catalyse basique générale : la base B accélère la réaction en captant un proton H+. Exemples d’enzymes: • Ribonucléase A • Chymotrypsine (protéase à sérine) • Protéase du VIH (protéase à acide aspartique) Catalyse enzymatique
Mécanismes catalytiques Catalyse acide/base Catalyse covalente Catalyse métallodépendante Catalyse par effets de proximité et facteurs d’orientation Catalyse par liaison et stabilisation de l’état de transition Catalyse enzymatique

Mécanismes catalytiques La catalyse covalente appelée aussi catalyse nucléophile: implique l'accélération de la vitesse par la formation transitoire d'une liaison covalente entre l’enzyme et un ou plusieurs substrats. L’enzyme modifiée devient alors un réactif mais elle revient à son état d’origine à la fin de la réaction. Ce mécanisme concerne surtout les transférases et les résidus le plus souvent impliquée sont: ü la portion imidazole de l'His, üle groupement thiol de la Cys, üle groupement hydroxyle de la Ser. Catalyse enzymatique

Mécanismes catalytiques Cette catalyse obéit souvent à un mécanisme « ping pong » dans lequel il y a fixation du premier substrat puis libération du produit correspondant avant la fixation du deuxième substrat. Ex : transaminases et PLP. Le site actif contient un groupe réactif, habituellement un puissant nucléophile qui est temporairement modifié par covalence au cours de la catalyse. Catalyse enzymatique

Mécanismes catalytiques La catalyse covalente se divise en deux étapes : 1) la réaction nucléophile entre le catalyseur et le substrat afin de former une liaison covalente. 2) le retrait d'électron du centre réactionnel par le catalyseur qui est devenu électrophile. Exemple d’enzymes: ØSérines protéases Ø fructose-2, 6 -diphosphatase Catalyse enzymatique
Mécanismes catalytiques Catalyse acide/base Catalyse covalente Catalyse métallodépendante Catalyse par effets de proximité et facteurs d’orientation Catalyse par liaison et stabilisation de l’état de transition Catalyse enzymatique

Mécanismes catalytiques Métalloenzymes possédant des ions métalliques fortement liés comme Fe 2+, Fe 3+, Cu 2+, Zn 2+, Mn 2+ , Mo 2+ ou Co 2+. Des enzymes activés par des ions métalliques faiblement liés en solution comme Na+, K+, Mg 2+, ou Ca 2+. Catalyse enzymatique

Mécanismes catalytiques Les ions métalliques participent à la catalyse de quatre façons majeures : a) Dans la liaison des substrats afin de les orienter. b) Facilitent les réactions d’oxydation-réduction par les changements réversibles de leur état d'oxydation. c) Servir de catalyseur électrophile en stabilisant une charge négative sur un intermédiaire de la réaction. « kinases » d) Créer un nucléophile en augmentant l’acidité d’une molécule voisine ex : la coordination par le métal rend les molécules d’eau plus acides et donc une source OH- à des p. H neutres. « anhydrase carbonique » Catalyse enzymatique
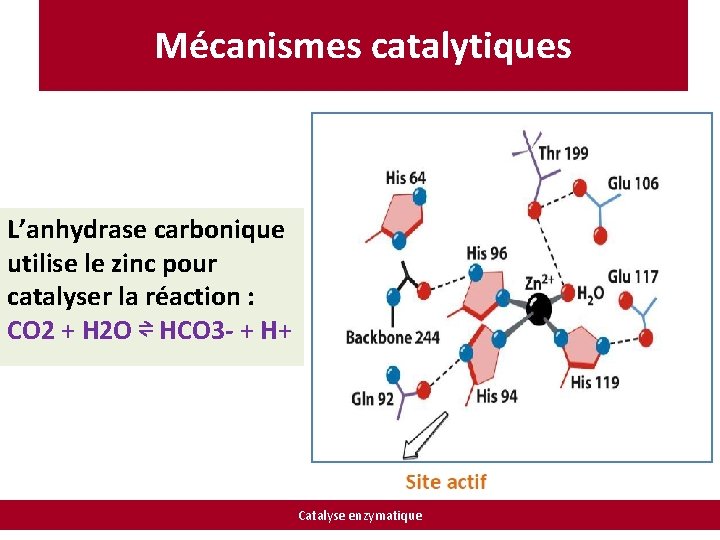
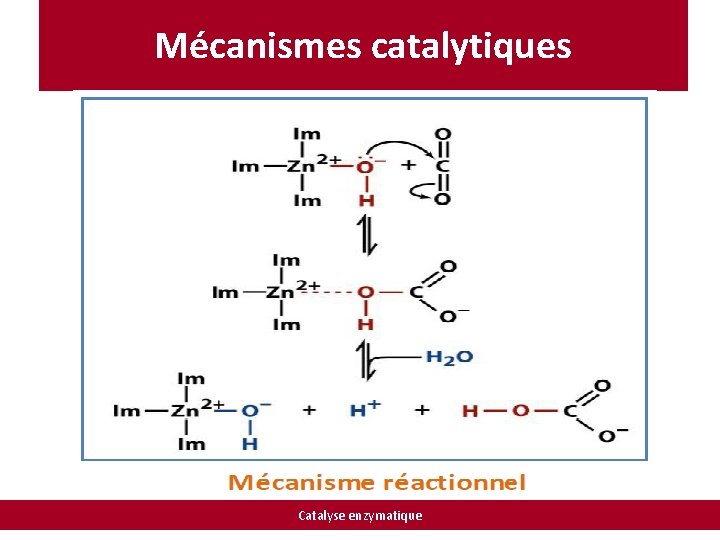
Mécanismes catalytiques L’anhydrase carbonique utilise le zinc pour catalyser la réaction : CO 2 + H 2 O ⇌ HCO 3 - + H+ Catalyse enzymatique
Mécanismes catalytiques Catalyse enzymatique

Mécanismes catalytiques Mécanisme réactionnel: 1) coordination d’une molécule de zinc par trois histidines et une molécule d'eau. Il est postulé que l'ionisation de la molécule d'eau est facilitée par catalyse base générale impliquent le résidu histidine-64 voisin. 2) attaque nucléophile par le OH- du CO 2 et la conversion en HCO 3 -. 3) régénération du site catalytique par la liaison d'une autre molécule de H 2 O avant le départ de HCO 3 - pour former un intermédiaire : complexe de zinc penta coordonné puis libération du HCO 3 -. Catalyse enzymatique
Mécanismes catalytiques Catalyse acide/base Catalyse covalente Catalyse métallodépendante Catalyse par effets de proximité et facteurs d’orientation Catalyse par liaison et stabilisation de l’état de transition Catalyse enzymatique

Mécanismes catalytiques De nombreuses réactions mettent en jeu 2 substrats distincts, la vitesse de réaction peut être considérablement augmentée en rapprochant les deux substrats au niveau d’une unique surface de liaison sur une enzyme et en les orientant de façon adéquate. Catalyse enzymatique

Mécanismes catalytiques Effet de proximité Pour que les molécules puissent réagir, elles doivent s’approcher l’une de l’autre à une distance permettant de former une liaison. L'alignement spatial des réactifs sur une surface enzymatique permet leur réaction de façon optimale dans le site actif. Les réactions catalysées sont accélérées par la réduction relative en translation et rotation des réactifs. Catalyse enzymatique
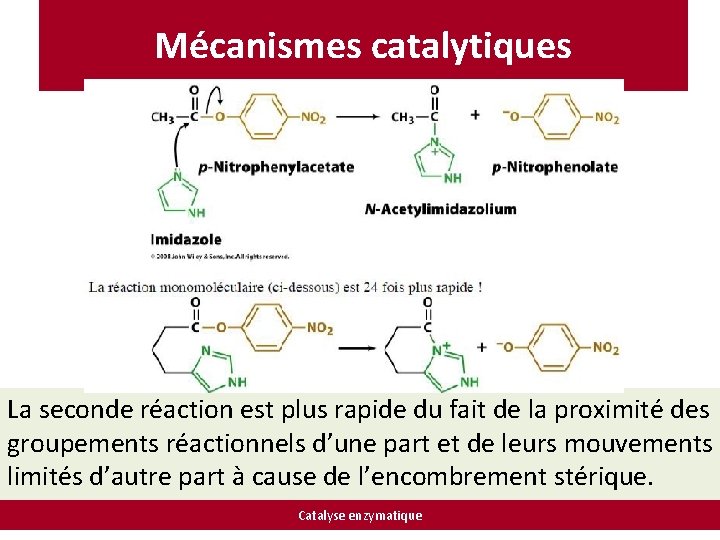
Mécanismes catalytiques La seconde réaction est plus rapide du fait de la proximité des groupements réactionnels d’une part et de leurs mouvements limités d’autre part à cause de l’encombrement stérique. Catalyse enzymatique
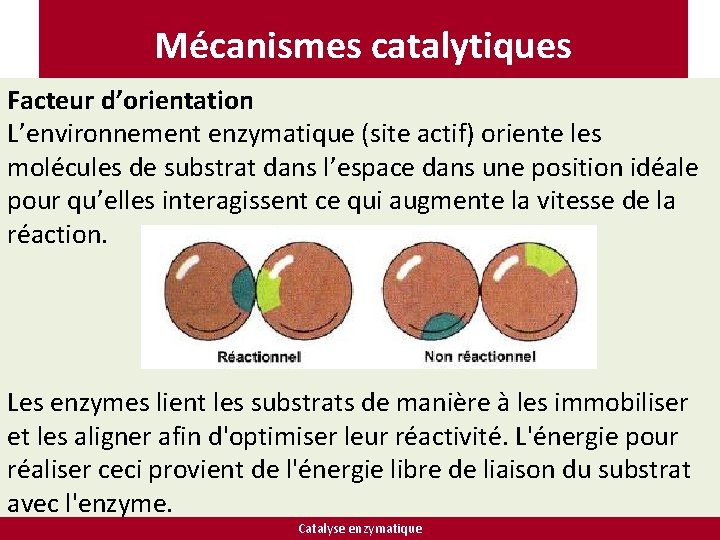
Mécanismes catalytiques Facteur d’orientation L’environnement enzymatique (site actif) oriente les molécules de substrat dans l’espace dans une position idéale pour qu’elles interagissent ce qui augmente la vitesse de la réaction. Les enzymes lient les substrats de manière à les immobiliser et les aligner afin d'optimiser leur réactivité. L'énergie pour réaliser ceci provient de l'énergie libre de liaison du substrat avec l'enzyme. Catalyse enzymatique

Mécanismes catalytiques L’enzyme doit: ØLier les substrats dans une orientation favorable ØBloquer l’agitation moléculaire des substrats et groupes catalytiques ØAmener les partenaires en contact ØFavoriser les chances de collision ØStabiliser l’état de transition de la réaction (=catalyse électrostatique) Exemple d’enzyme: NMP kinases Catalyse enzymatique
Mécanismes catalytiques Catalyse acide/base Catalyse covalente Catalyse métallodépendante Catalyse par effets de proximité et facteurs d’orientation Catalyse par liaison et stabilisation de l’état de transition Catalyse enzymatique

Mécanismes catalytiques Ou catalyse par effet de contrainte: Les enzymes catalysant des réactions lytiques qui impliquent la rupture d’une liaison covalente se fixent généralement à leur substrat dans une conformation légèrement défavorable pour la liaison destinée à être coupée. Cette conformation mime celle de l’intermédiaire de l’état de transition. La contrainte résultante étire ou tord la liaison cible la rendant plus faible et plus vulnérable à la coupure. « lysozyme » Catalyse enzymatique
Facteurs influençant la catalyse enzymatique Facteurs physicochimiques: T° et le p. H Effecteurs chimiques (inhibiteurs et activateurs) Catalyse enzymatique
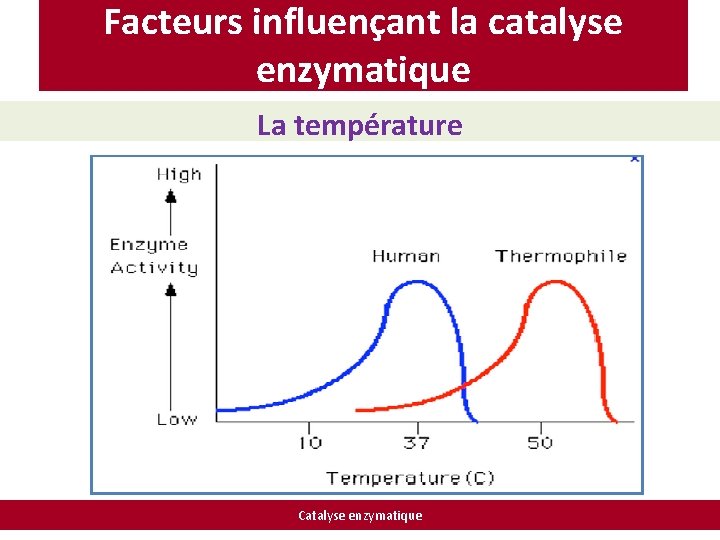
Facteurs influençant la catalyse enzymatique La température Catalyse enzymatique
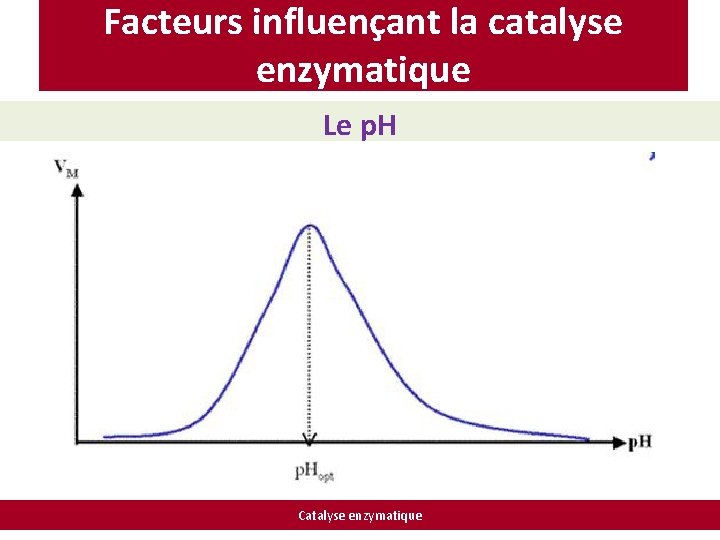
Facteurs influençant la catalyse enzymatique Le p. H Catalyse enzymatique
- Slides: 55