CASO CLNICO 24 Javier Gonzlvez Aracil MIR4 CASO









- Slides: 12

CASO CLÍNICO 24 Javier Gonzálvez Aracil MIR-4

CASO CLÍNICO l EXPOSICIÓN DEL CASO ¡ Niña de 6 meses que acude a urgencias por presentar un episodio de crisis convulsiva, somnolencia y palidez. Refieren pico febril de 38ºC en las últimas 24 horas y episodios intermitentes de vómitos. l HISTORIA CLÍNICA ¡ Gestación controlada sin incidencias. ¡ Desde el nacimiento se detecta hepatomegalia y distensión abdominal. ¡ Cribado metabólico neonatal: no realizado. ¡ AF: consanguinidad paterna en grado lejano y hermano varón fallecido a los 5 días de vida (refieren por ictericia).

CASO CLÍNICO l Exploración física: ¡ Peso: 6, 400 Kg (Percentil 25). ¡ Talla: 60 cm (Percentil 10). ¡ T: 38ºC. ¡ Sat. O 2: 97% ¡ BEG. Buena respuesta a estímulos. Aspecto de muñeca (mejillas hinchadas, extremidades y tórax delgado con vientre prominente). No exantemas ni petequias. Revascularización normal. ¡ Abdomen: Globuloso y depresible. Hepatomegalia. Bazo normal.

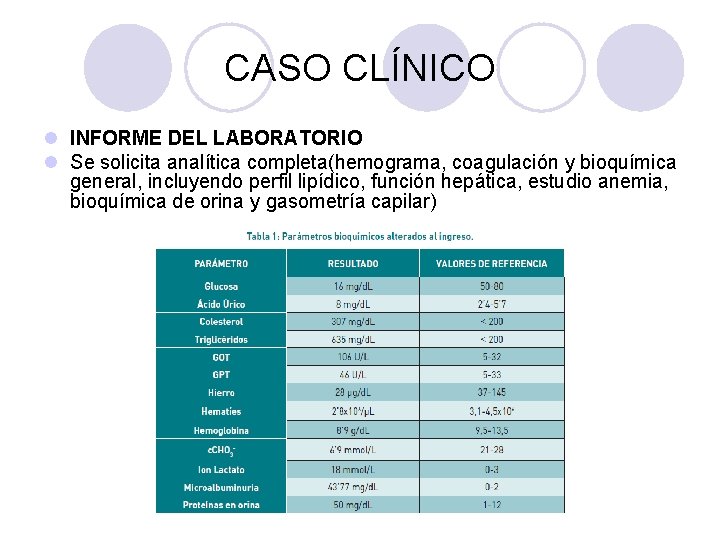
CASO CLÍNICO l INFORME DEL LABORATORIO l Se solicita analítica completa(hemograma, coagulación y bioquímica general, incluyendo perfil lipídico, función hepática, estudio anemia, bioquímica de orina y gasometría capilar)

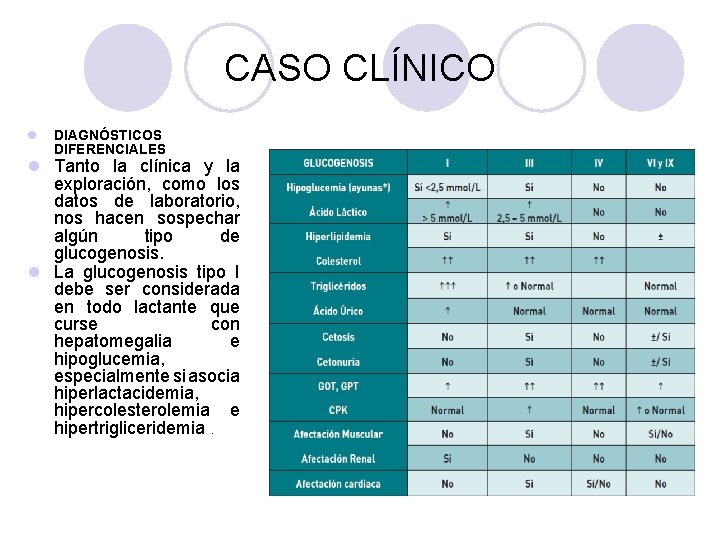
CASO CLÍNICO l DIAGNÓSTICOS DIFERENCIALES l Tanto la clínica y la exploración, como los datos de laboratorio, nos hacen sospechar algún tipo de glucogenosis. l La glucogenosis tipo I debe ser considerada en todo lactante que curse con hepatomegalia e hipoglucemia, especialmente si asocia hiperlactacidemia, hipercolesterolemia e hipertrigliceridemia.

CASO CLÍNICO l PRUEBAS COMPLEMENTARIAS l Ecocardiografía: MCH secundaria, sin afectación del septo IV. l Ecografía abdominal: alteración de la ecoestructura hepática, lo que sugiere una enfermedad de depósito y permite valorar la presencia de adenomas hepáticos, bazo SHP, riñones grandes con aumento de la ecogenicidad pero con buena diferenciación corticomedular. l Test del glucagón: no se produce aumento de la glucemia, lo que sugiere patología(glucogenosis tipo I), pero no permite un diagnóstico definitivo.

CASO CLÍNICO l PRUEBAS COMPLEMENTARIAS l Detección de la actividad enzimática de Glucosa-6 -fosfatasa en una biopsia de hígado: Esta prueba evidenció una disminución de la actividad enzimática en la paciente. l Estudio genético, mediante la secuenciación del gen, estudiando las mutaciones genéticas más frecuentes en pacientes de origen caucásico como son la R 83 C (32. 81%) y la Q 347 X (20. 7%): mutación en homocigosis (p. R 83 C) causada por la sustitución de una arginina por una cistina en el exón 2 del gen localizado en 17 q 21. . l Estos dos últimos estudios son necesarios para poder distinguir entre los dos subtipos actualmente establecidos de esta glucogenosis: Ia, Ib, puesto que el fenotipo clínico es similar en ambas.

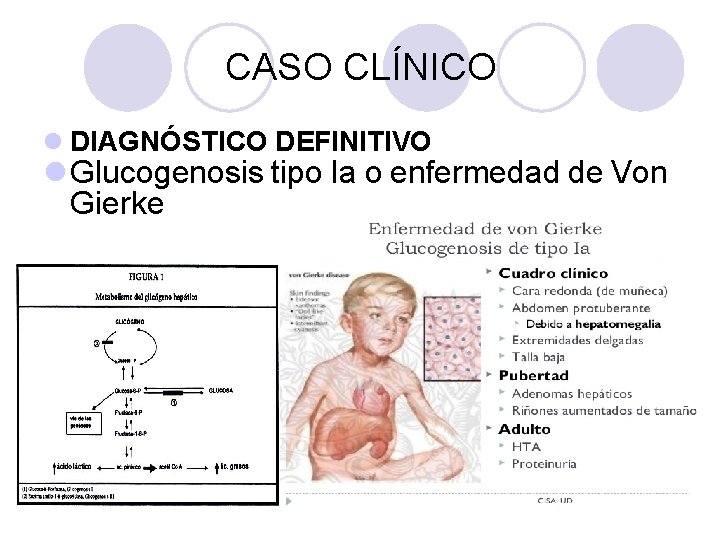
CASO CLÍNICO l DIAGNÓSTICO DEFINITIVO l Glucogenosis tipo Ia o enfermedad de Von Gierke

CASO CLÍNICO l EVOLUCIÓN l La paciente es ingresada para control de la hipoglucemia y desnutrición severa, por lo que se inicia alimentación enteral a través de sonda nasogástrica. l Se obtiene una discreta mejoría de la proteinuria con estabilización gasométrica y moderada recuperación de los niveles de lactato y c. CHO 3 - tras los ajustes de hidratos de carbono y de bicarbonato. l El objetivo del tratamiento consiste prevenir la hipoglucemia y sus consecuencias. Para ello, se utilizan dos estrategias: la realización de comidas frecuentes (cada 2 a 4 horas) ricas en hidratos de carbono durante el día, junto a una infusión nocturna de glucosa a través de una sonda nasogástrica o bien la administración de almidón crudo de maíz. En este caso, gastroenterología infantil le pauta un régimen de comidas cada 2 horas. l Se incluye a la paciente en un protocolo de pretransplante de hepatocitos. La paciente recibe el alta con seguimiento por los servicios de Genética Médica, Gastroenterología infantil, Nefrología infantil y Cardiología pediátrica

CASO CLÍNICO l ACTUALIZACIÓN l Se desconoce la prevalencia. La incidencia anual es de aproximadamente 1/100. 000 (80% tipo a). l La enfermedad puede manifestarse al nacimiento por una hepatomegalia o, más frecuentemente, entre los 3 y 4 meses, por síntomas de hipoglucemia de ayuno (temblores, convulsiones, cianosis y apnea). l Los pacientes presentan trastornos en la homeostasis de la glucosa caracterizados por una baja tolerancia al ayuno, hepatomegalia significativa (alcanzando en ocasiones entre ocho y diez cm por debajo del reborde costal derecho), retraso en el crecimiento (estatura baja y retraso de la pubertad) que generalmente mejora con una dieta apropiada, osteopenia y, en algunos casos, osteoporosis, cara redondeada “de muñeca”, hipotonía leve, nefromegalia, y un trastorno funcional de las plaquetas que puede provocar una epistaxis frecuente. Puede darse diarrea.

CASO CLÍNICO l Las complicaciones tardías son hepáticas (adenomas que raramente se transforman en carcinomas hepatocelulares) y renales (hiperfiltración glomerular que conduce a una proteinuria y en ocasiones a una insuficiencia renal), pero pueden comportar también una anemia, a veces grave, y un riesgo de daño cerebral ligado a la hipoglucemia. En unos pocos casos se ha descrito hipertensión pulmonar. l La enfermedad se debe a una disfunción del sistema G 6 P, un paso clave en la regulación de la glucemia. El tipo a se debe a mutaciones en el gen G 6 PC (17 q 21), que causa un déficit de la subunidad catalítica G 6 P-alfa expresada en hígado, riñón e intestino. l Las numerosas mutaciones identificadas subrayan la heterogeneidad alélica de la enfermedad. Su transmisión es autosómica recesiva. El manejo es similar en los dos tipos, a y b. l El tratamiento se lleva exclusivamente mediante terapias paliativas que, principalmente a través del seguimiento de unas pautas nutricionales adecuadas, suelen permitir un control aceptable de la sintomatología de la enfermedad.
