CARICA ELETTRICA strofinato con seta Cariche di due




- Slides: 31

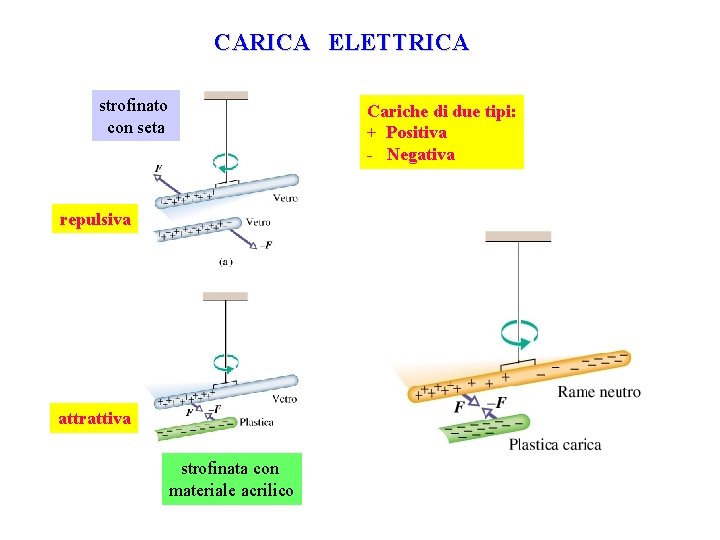
CARICA ELETTRICA strofinato con seta Cariche di due tipi: + Positiva - Negativa repulsiva attrattiva strofinata con materiale acrilico

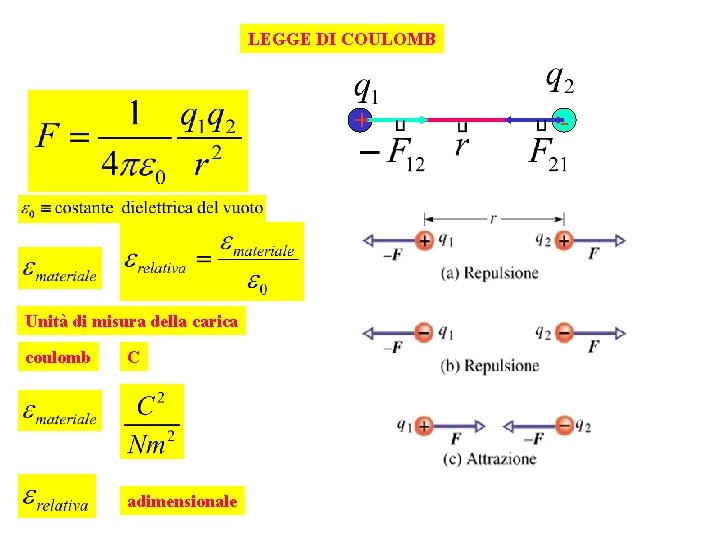
LEGGE DI COULOMB + Unità di misura della carica coulomb C adimensionale -

Ordini di grandezza repulsiva 18/5/06 Forza nucleare per legare il nucleo

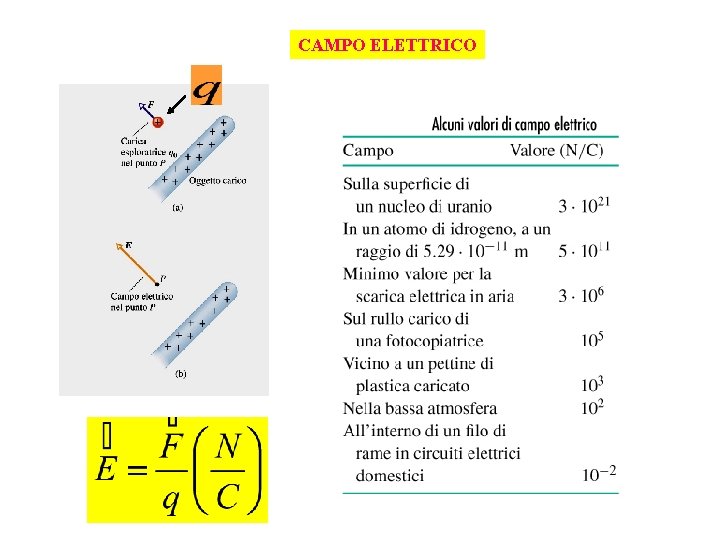
CAMPO ELETTRICO

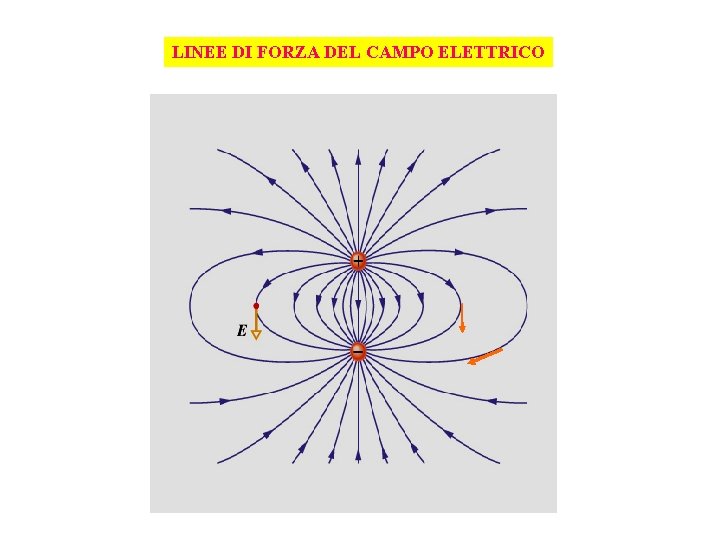
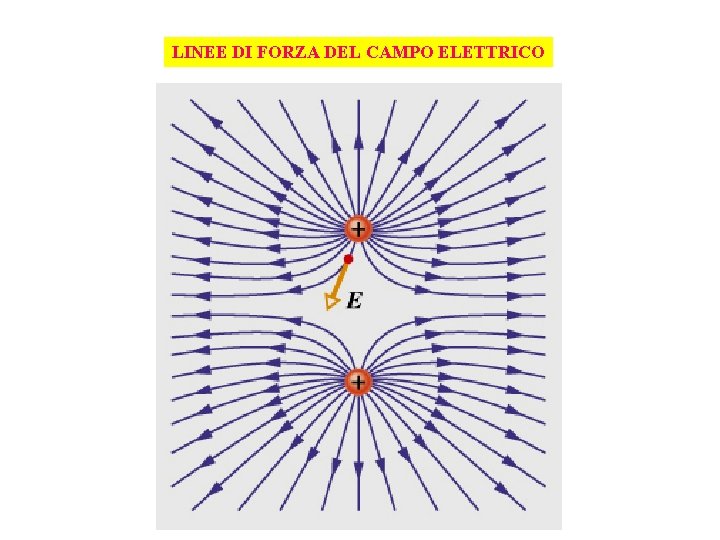
LINEE DI FORZA DEL CAMPO ELETTRICO Il campo elettrico è tangente punto per punto alla linea di forza

LINEE DI FORZA DEL CAMPO ELETTRICO

LINEE DI FORZA DEL CAMPO ELETTRICO

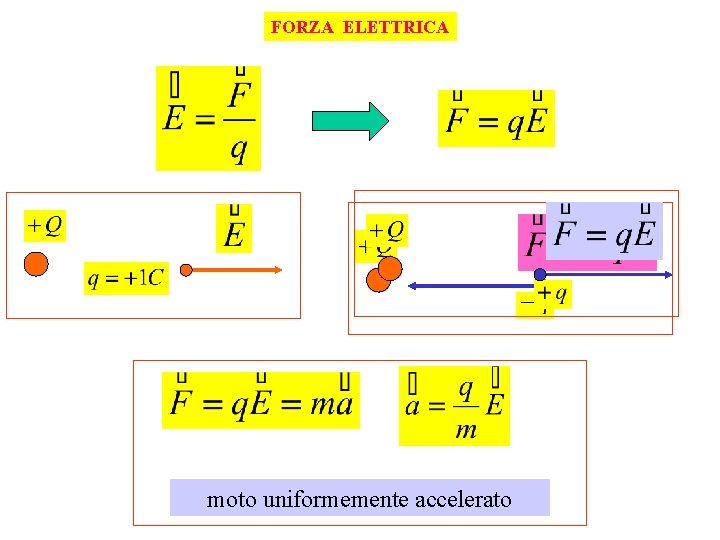
FORZA ELETTRICA moto uniformemente accelerato

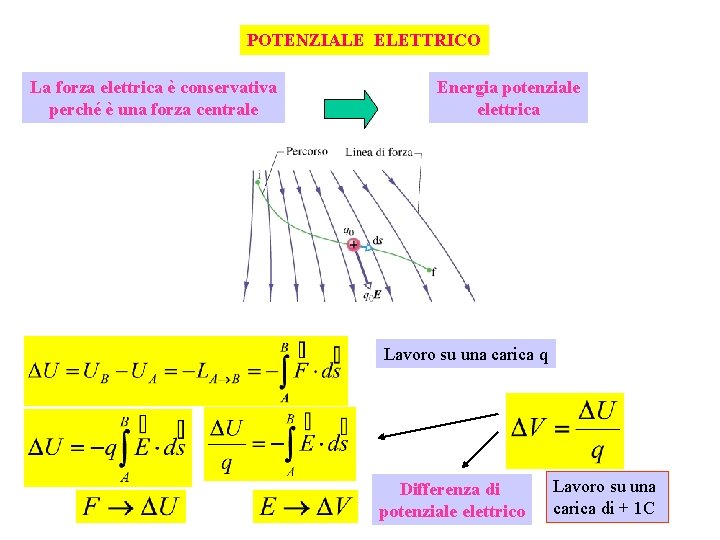
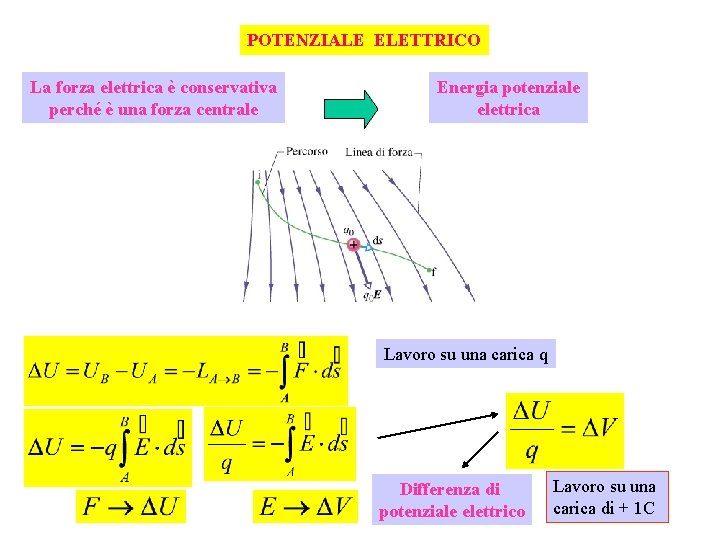
POTENZIALE ELETTRICO La forza elettrica è conservativa perché è una forza centrale Energia potenziale elettrica Lavoro su una carica q Differenza di potenziale elettrico Lavoro su una carica di + 1 C

POTENZIALE ELETTRICO La forza elettrica è conservativa perché è una forza centrale Energia potenziale elettrica Lavoro su una carica q Differenza di potenziale elettrico Lavoro su una carica di + 1 C

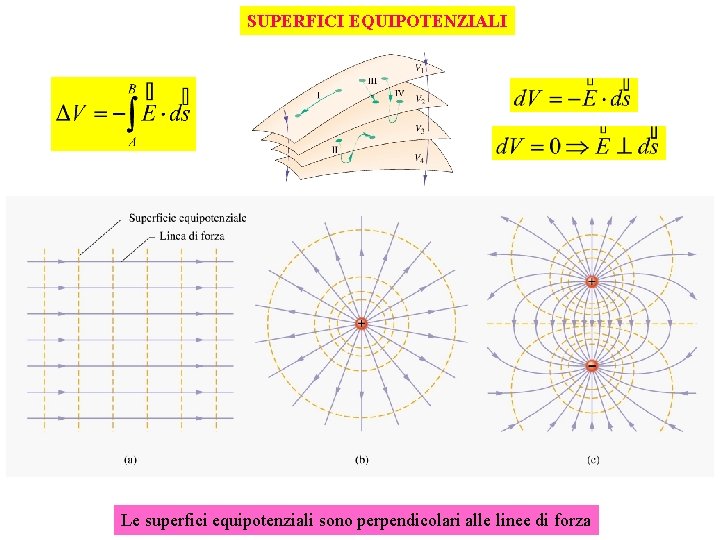
SUPERFICI EQUIPOTENZIALI Le superfici equipotenziali sono perpendicolari alle linee di forza

SUPERFICI EQUIPOTENZIALI

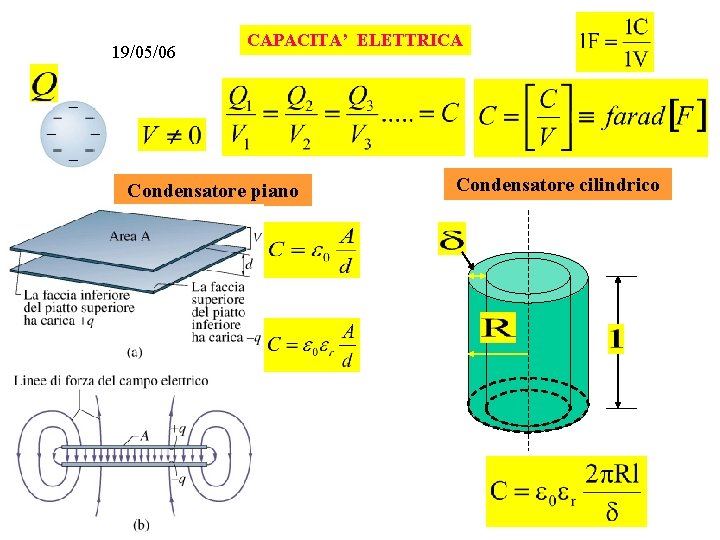
19/05/06 CAPACITA’ ELETTRICA Condensatore piano Condensatore cilindrico

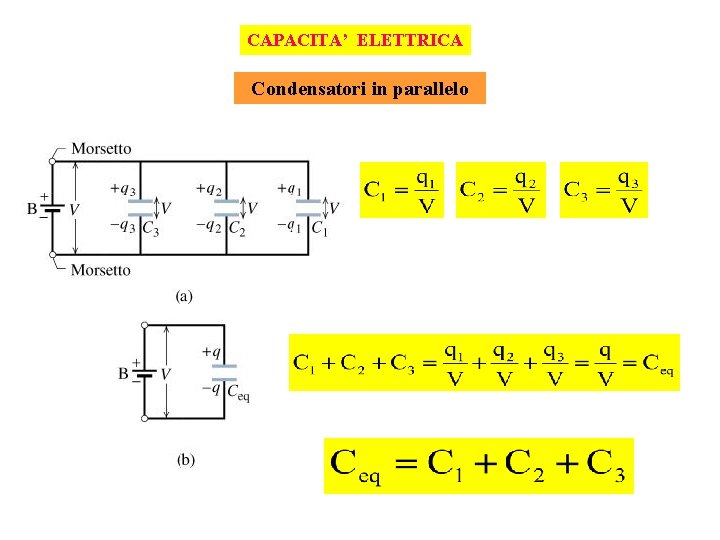
CAPACITA’ ELETTRICA Condensatori in parallelo

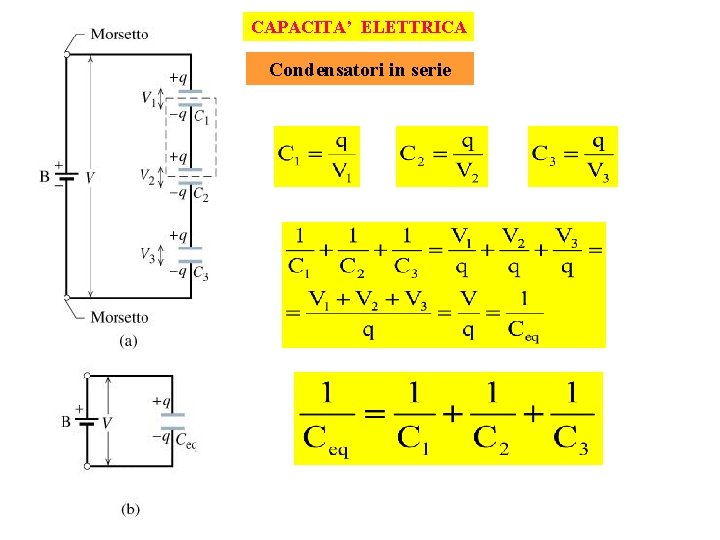
CAPACITA’ ELETTRICA Condensatori in serie

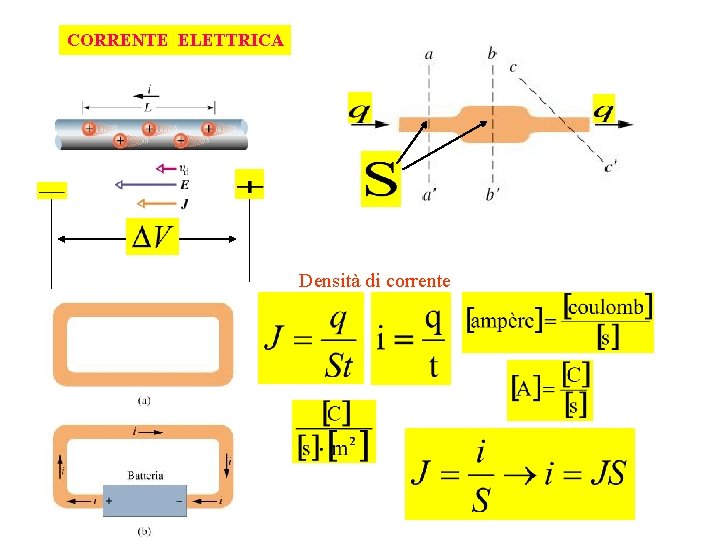
CORRENTE ELETTRICA Densità di corrente

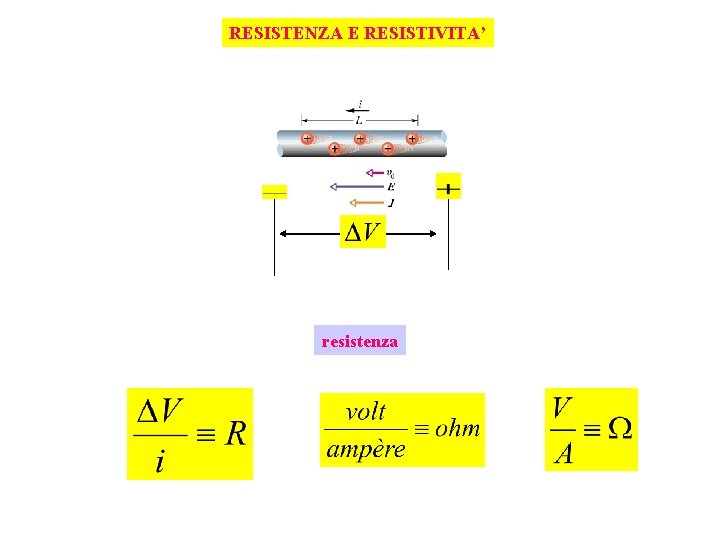
RESISTENZA E RESISTIVITA’ resistenza

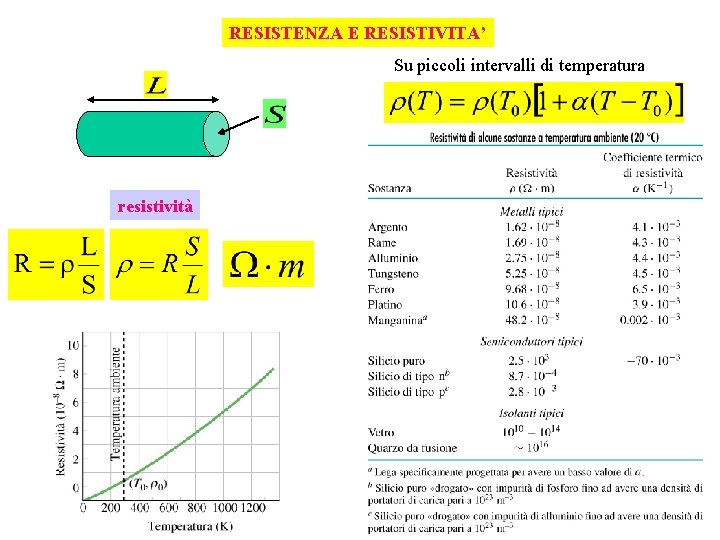
RESISTENZA E RESISTIVITA’ Su piccoli intervalli di temperatura resistività

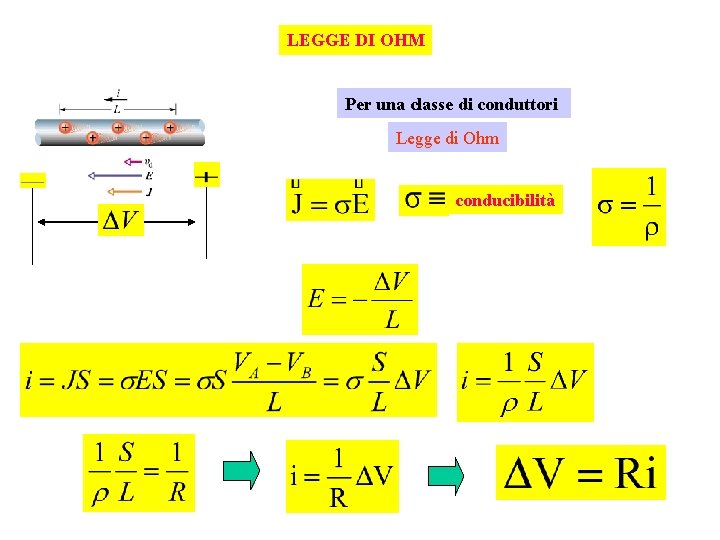
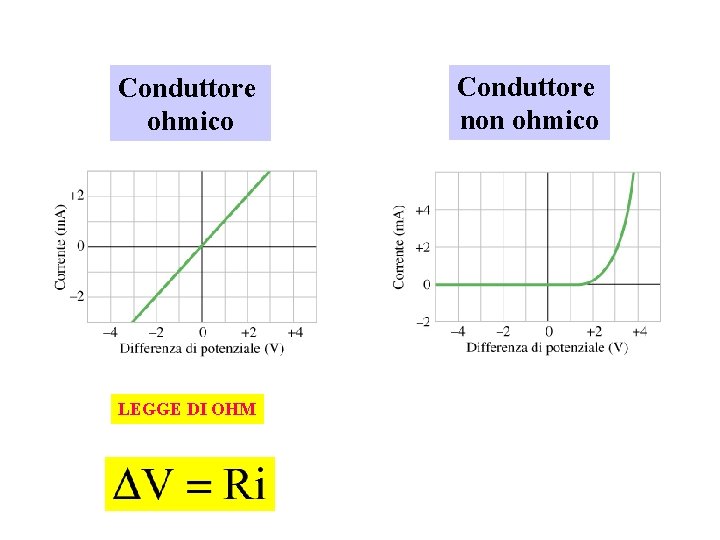
LEGGE DI OHM Per una classe di conduttori Legge di Ohm conducibilità

Conduttore ohmico LEGGE DI OHM Conduttore non ohmico

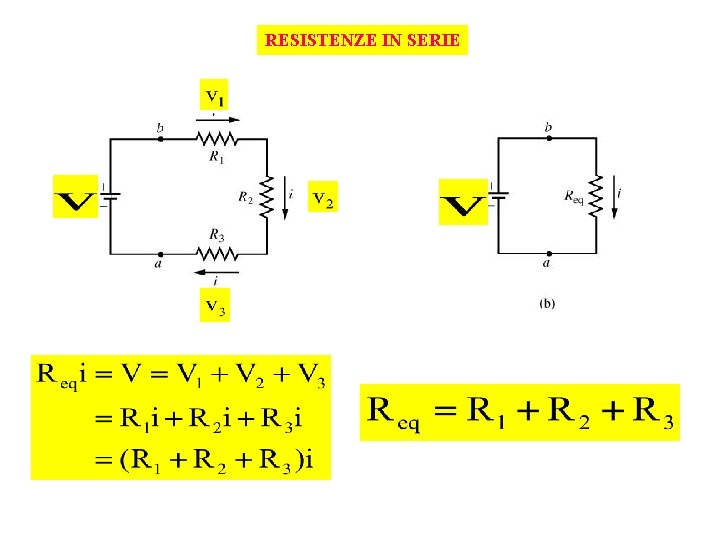
RESISTENZE IN SERIE

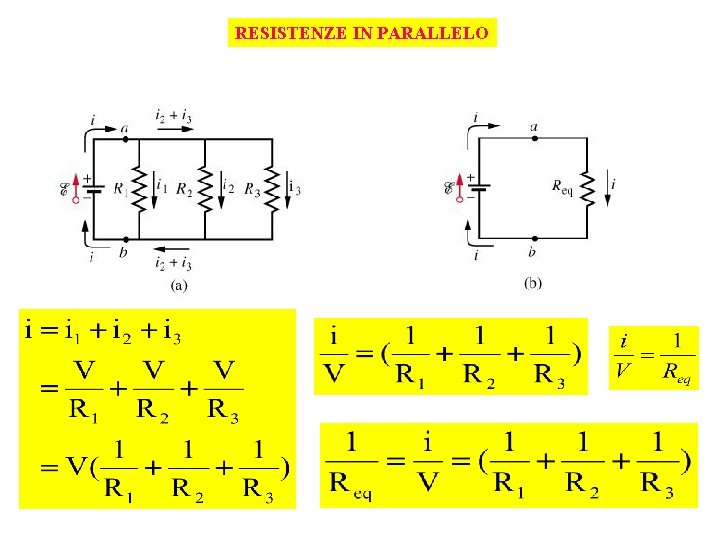
RESISTENZE IN PARALLELO

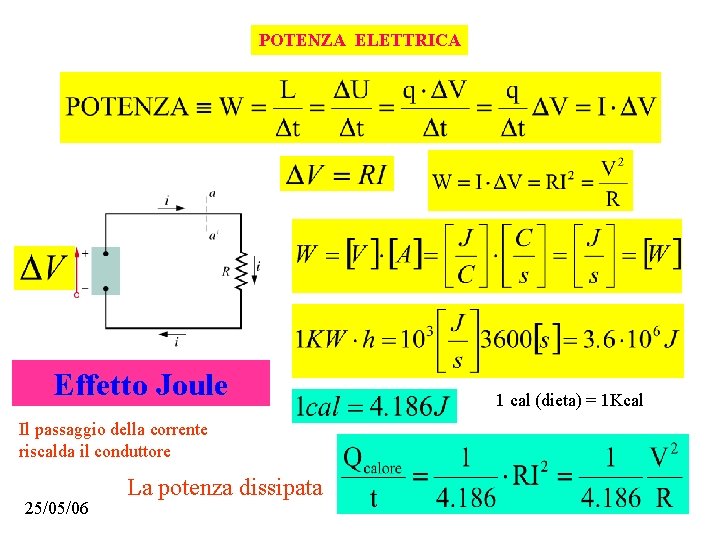
POTENZA ELETTRICA Effetto Joule Il passaggio della corrente riscalda il conduttore 25/05/06 La potenza dissipata 1 cal (dieta) = 1 Kcal

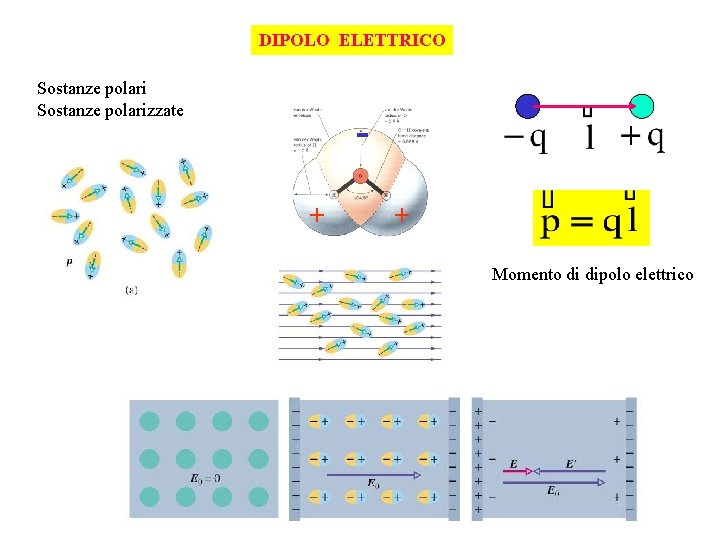
DIPOLO ELETTRICO Sostanze polarizzate + + Momento di dipolo elettrico

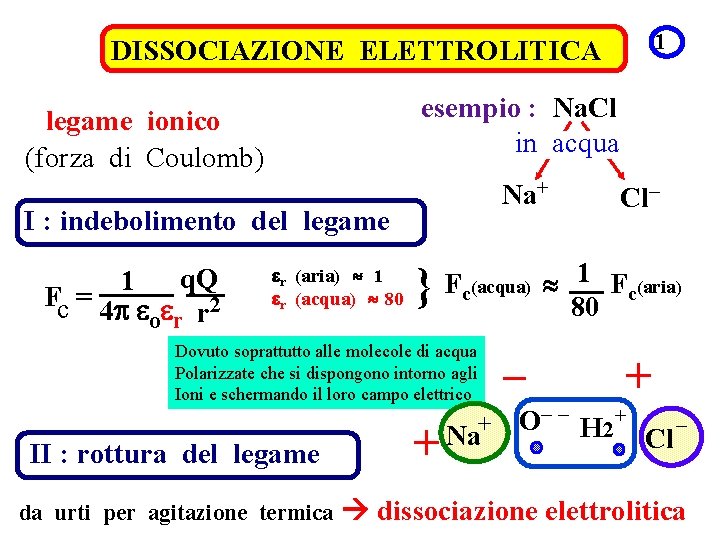
1 DISSOCIAZIONE ELETTROLITICA esempio : Na. Cl in acqua legame ionico (forza di Coulomb) Na+ I : indebolimento del legame q. Q 1 Fc = 4 p e e 2 o r r er (aria) » 1 er (acqua) » 80 } Fc(acqua) » 1 Fc(aria) 80 Dovuto soprattutto alle molecole di acqua Polarizzate che si dispongono intorno agli Ioni e schermando il loro campo elettrico + II : rottura del legame da urti per agitazione termica Cl– + Na – + O– – H 2+ – Cl dissociazione elettrolitica

DISSOCIAZIONE ELETTROLITICA

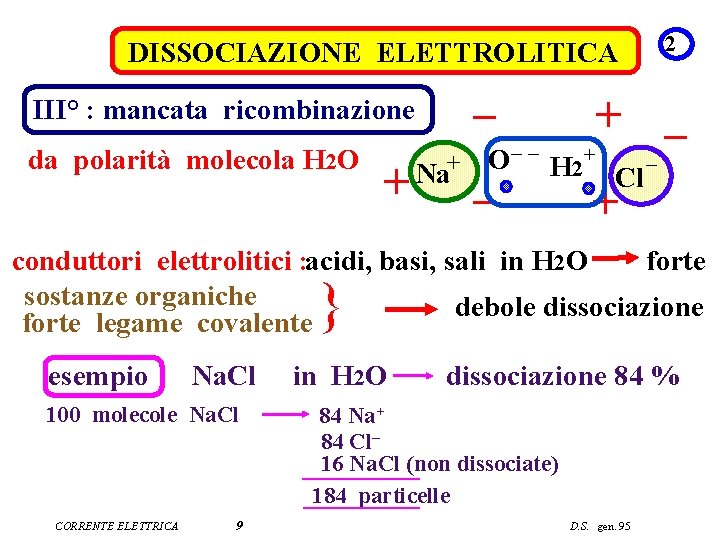
DISSOCIAZIONE ELETTROLITICA – III° : mancata ricombinazione da polarità molecola H 2 O 2 + Na + + – O– – H 2+ – Cl – + conduttori elettrolitici : acidi, basi, sali in H 2 O forte sostanze organiche debole dissociazione forte legame covalente } esempio Na. Cl 100 molecole Na. Cl CORRENTE ELETTRICA 9 in H 2 O dissociazione 84 % 84 Na+ 84 Cl– 16 Na. Cl (non dissociate) 184 particelle D. S. gen. 95

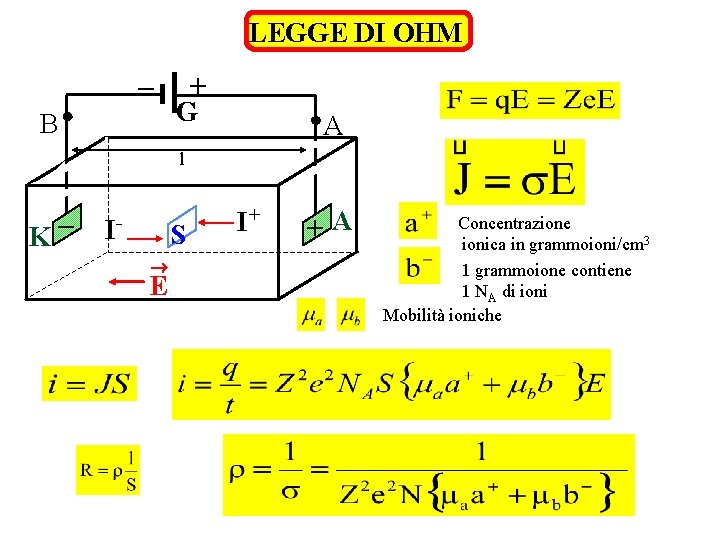
LEGGE DI OHM – B + G A l K– I- S ® E I+ +A Concentrazione ionica in grammoioni/cm 3 1 grammoione contiene 1 NA di ioni Mobilità ioniche

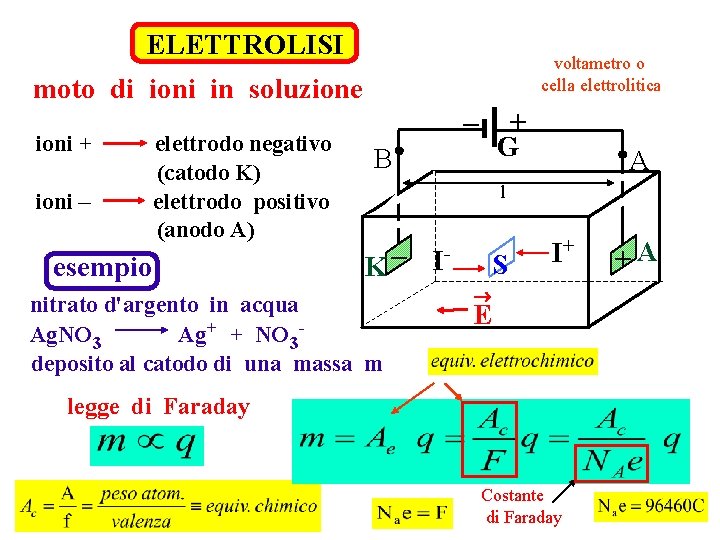
ELETTROLISI voltametro o cella elettrolitica moto di ioni in soluzione ioni + ioni – elettrodo negativo (catodo K) elettrodo positivo (anodo A) esempio – + G B A l – I K nitrato d'argento in acqua Ag. NO 3 Ag+ + NO 3 deposito al catodo di una massa m S I+ ® E legge di Faraday Costante di Faraday +A

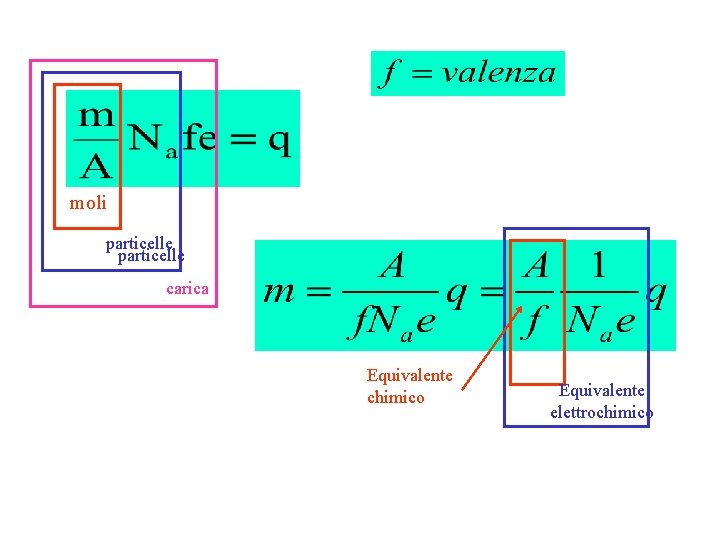
moli particelle carica Equivalente chimico Equivalente elettrochimico

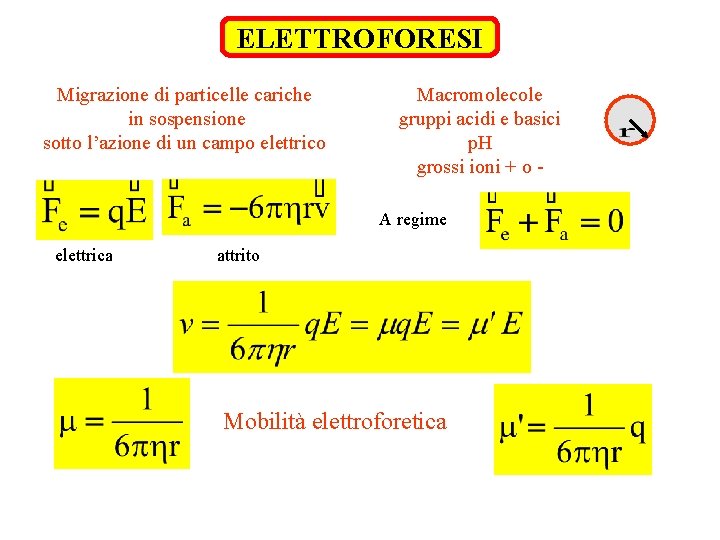
ELETTROFORESI Migrazione di particelle cariche in sospensione sotto l’azione di un campo elettrico Macromolecole gruppi acidi e basici p. H grossi ioni + o A regime elettrica attrito Mobilità elettroforetica