Carbonsuren und ihre Derivate Allgemeine Erkennungsmerkmale n org

Carbonsäuren und ihre Derivate
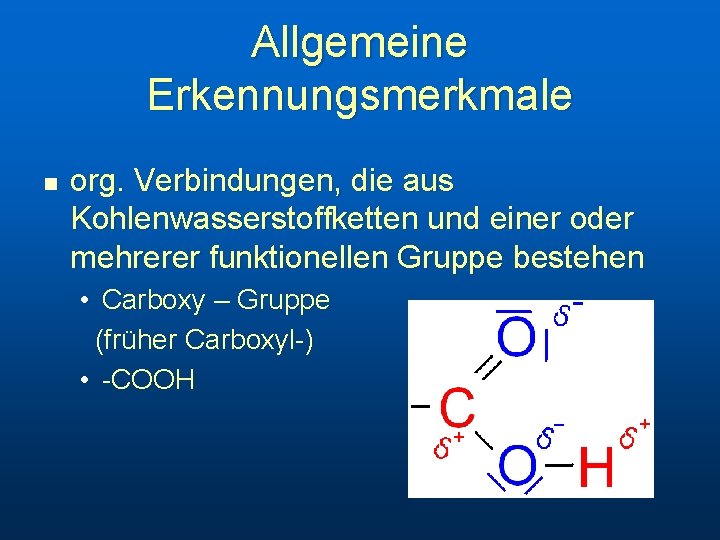
Allgemeine Erkennungsmerkmale n org. Verbindungen, die aus Kohlenwasserstoffketten und einer oder mehrerer funktionellen Gruppe bestehen • Carboxy – Gruppe (früher Carboxyl-) • -COOH

Gruppeneinteilung n Großgruppen • aliphatisch • aromatisch n Anzahl der Carboxy – Gruppen • Mono-, Di-, … Polycarbonsäuren n Kohlenstoffreste • gesättigte und ungesättigte Carbonsäuren
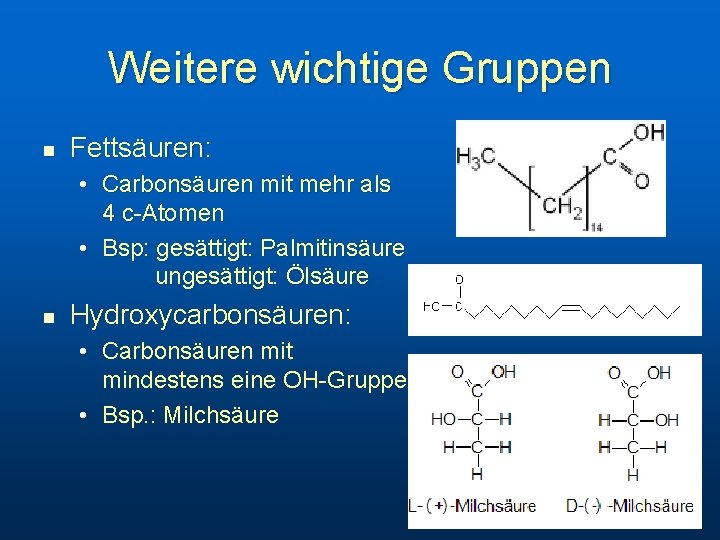
Weitere wichtige Gruppen n Fettsäuren: • Carbonsäuren mit mehr als 4 c-Atomen • Bsp: gesättigt: Palmitinsäure ungesättigt: Ölsäure n Hydroxycarbonsäuren: • Carbonsäuren mit mindestens eine OH-Gruppe • Bsp. : Milchsäure

Einblick in die Nomenklatur n n veraltet: Stammalkan mit Anhang „…-carbonsäure“ aktuell: Stammalkan + 1 mit Anhang „…-säure“ Trivialnamen sind möglich und weit verbreitet, sie leiten sich meist von der Erstentdeckung ab. Bsp. : CH 3(CH 2)4 COOH • Pentancarbonsäure • Hexansäure • Capronsäure
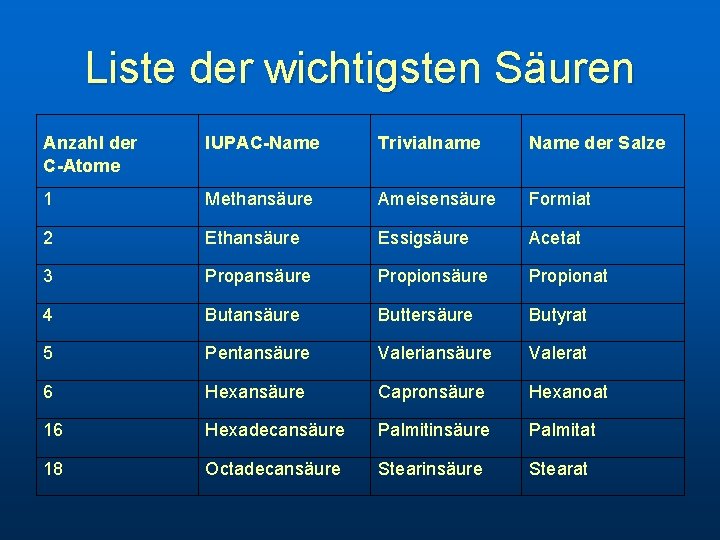
Liste der wichtigsten Säuren Anzahl der C-Atome IUPAC-Name Trivialname Name der Salze 1 Methansäure Ameisensäure Formiat 2 Ethansäure Essigsäure Acetat 3 Propansäure Propionat 4 Butansäure Buttersäure Butyrat 5 Pentansäure Valeriansäure Valerat 6 Hexansäure Capronsäure Hexanoat 16 Hexadecansäure Palmitinsäure Palmitat 18 Octadecansäure Stearinsäure Stearat
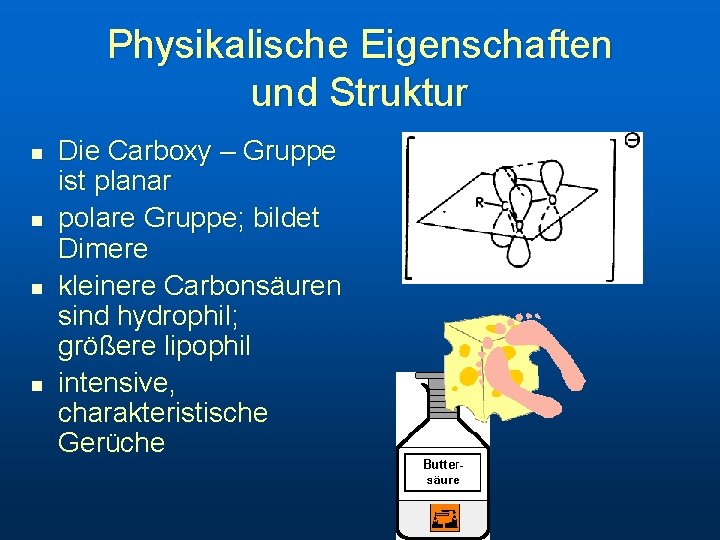
Physikalische Eigenschaften und Struktur n n Die Carboxy – Gruppe ist planar polare Gruppe; bildet Dimere kleinere Carbonsäuren sind hydrophil; größere lipophil intensive, charakteristische Gerüche

Demonstration 1 Wasser- bzw. Etherlöslichkeit verschiedener Carbonsäuren ♦ Ameisensäure ♦ Propionsäure ♦ Ölsäure ♦ Benzoesäure in Wasser und Diethylether

Auswertung ♦ Ameisensäure mischt sich gut mit Wasser, nicht mit Ether ♦ Propionsäure mischt sich mit Wasser, besser aber mit Ether ♦ Ölsäure mischt sich nur mit Ether ♦ Benzoesäure löst sich nicht in Wasser aber in Ether
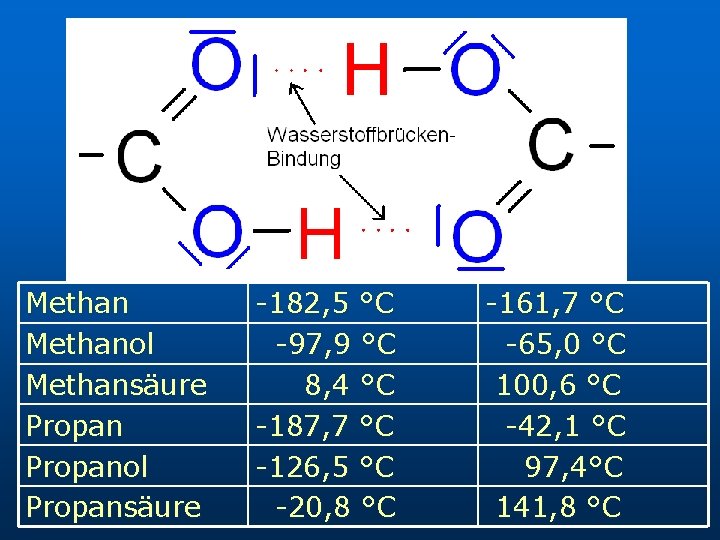
Methanol Methansäure Propanol Propansäure -182, 5 °C -97, 9 °C 8, 4 °C -187, 7 °C -126, 5 °C -20, 8 °C -161, 7 °C -65, 0 °C 100, 6 °C -42, 1 °C 97, 4°C 141, 8 °C

Die Ameisensäure n n die einfachste und kleinste Carbonsäure nat. Vorkommen in Tieren und Pflanzen starke bakterizide Wirkung wirkt wie ein Aldehyd

Demonstration 2 n Ameisensäure brennt John Ray isolierte als erster die Ameisensäure
![„Gewinnung“ n Die Ameisensäure erhält man durch Destillation aus den Ameisen (Formica rufa). […] „Gewinnung“ n Die Ameisensäure erhält man durch Destillation aus den Ameisen (Formica rufa). […]](http://slidetodoc.com/presentation_image/14a3e7b3ca41eed32b276d970db4e8a2/image-13.jpg)
„Gewinnung“ n Die Ameisensäure erhält man durch Destillation aus den Ameisen (Formica rufa). […] man sammelt Ameisen, preßt sie aus, ohne Wasser, und destilliert die Säure davon. (um 1795) Heute: aus Na. OH und CO durch ansäuern mit H 2 SO 4 n

Versuch 1 Säurecharakter der Ameisensäure

Auswertung n Kalkstein: 2 HCOOH(l) + Ca. CO 3(s) CO 2(g) + H 2 O + Ca(HCOO)2(s) n Magnesium:
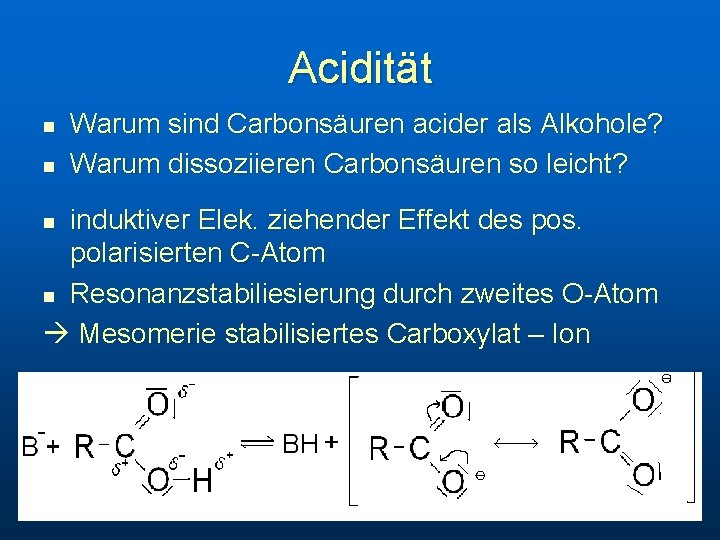
Acidität n n Warum sind Carbonsäuren acider als Alkohole? Warum dissoziieren Carbonsäuren so leicht? induktiver Elek. ziehender Effekt des pos. polarisierten C-Atom n Resonanzstabiliesierung durch zweites O-Atom Mesomerie stabilisiertes Carboxylat – Ion n
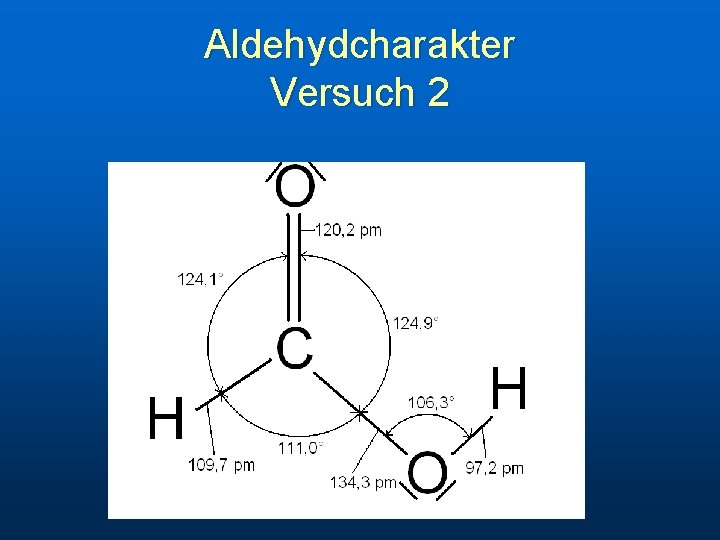
Aldehydcharakter Versuch 2

Durchführung n jeweils Ameisen- und Essigsäure in einem RG auf • • • n Kaliumpermanganatlösung Silbernitratlösung Kaliumchromatlösung evt. erwärmen um Reaktion abzuschließen

Auswertung n n Essigsäure hat keinen Aldehydcharakter und wirkt nicht auf die Oxidationsmittel Ameisensäure: • Kaliumpermanganat Braunstein Mg(II)-Ionen violett braun farblos • Silbernitrat Silber farblos grau • Kaliumchromat Kaliumdichromat Cr(III)-Ionen gelb orange grün

Im Detail am Bsp. Chromat Allgemeine Reaktion mit Säure: gelb Redoxreaktion: orange

Carbonsäuren im Alltag n n Natürliche Vorkommen Lebensmittelindustrie • • • n n E – (Zusatz-)Stoffe Gewürze Säuerungsmittel Reinigungsmittel Kosmetikindustrie

Alles Essig ? ! Versuch 3 (a, b, c) Von Reinigungsmitteln, Zusatzstoffen und natürlichen Vorkommen
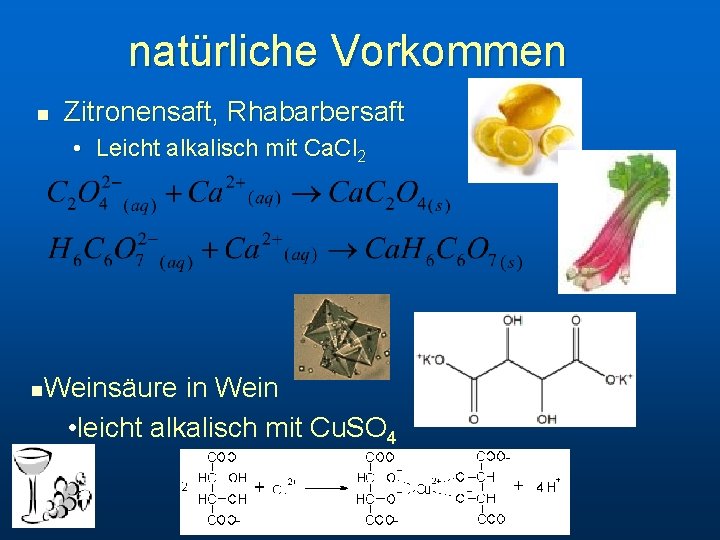
natürliche Vorkommen n Zitronensaft, Rhabarbersaft • Leicht alkalisch mit Ca. Cl 2 Weinsäure in Wein • leicht alkalisch mit Cu. SO 4 n

Zusatzstoffe n Carbonsäure in Süßigkeiten • p. H Messung bei Süßigkeiten n Essig im Gurkensaft • leicht alkalisch mit Fe(Cl)3 n Herstellung von Brausepulver und Auflösen • aus Weinsäure und Na. HCO 3

Reinigungsmittel n n Nachweise wie zuvor lösen von • • • „Urinstein“ Eierschalen (Schutz durch Zahnpaste!) versch. Gesteinen Ca. CO 3(s) + 2 CH 3 COOH(l) —> Ca(CH 3 COO)2(l) + H 2 O + CO 2(g) Die Zahnpaste tauscht das Hydroxidion im Apatit des Zahnschmelzes gegen ein Fluoridiuon was ihn säureresistenter macht.
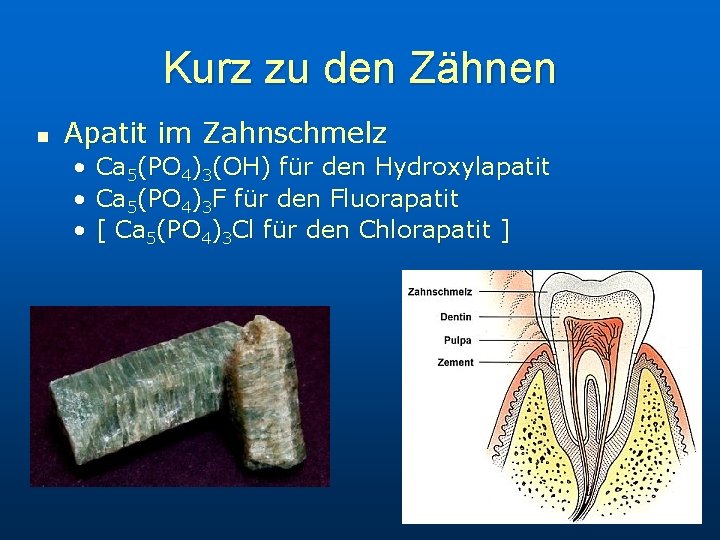
Kurz zu den Zähnen n Apatit im Zahnschmelz • • • Ca 5(PO 4)3(OH) für den Hydroxylapatit Ca 5(PO 4)3 F für den Fluorapatit [ Ca 5(PO 4)3 Cl für den Chlorapatit ]
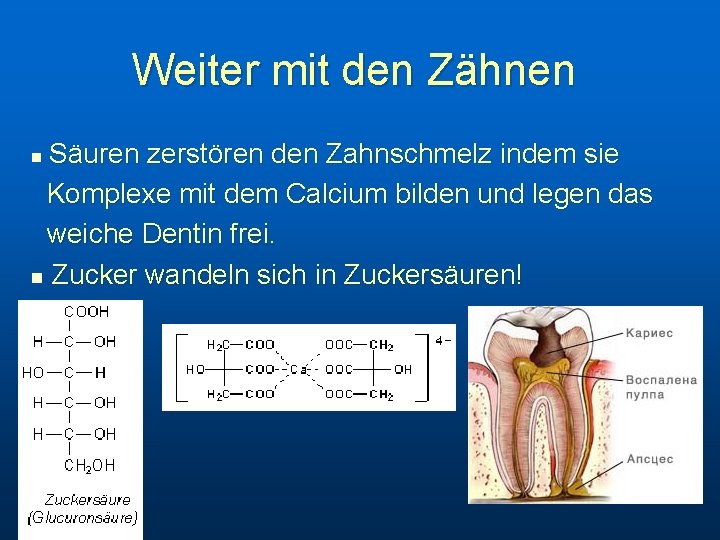
Weiter mit den Zähnen Säuren zerstören den Zahnschmelz indem sie n Komplexe mit dem Calcium bilden und legen das weiche Dentin frei. n Zucker wandeln sich in Zuckersäuren!

Weitere Anwendungen Versuch 4 Aspirin und Paracetamol

Durchführung n n je eine halbe Tablette aufschlemmen und filtrieren messen des p. H-Wertes Eisen(III)-chlorid Nachweis den Rest sauer hydrolisieren und den Nachweis nochmals durchführen
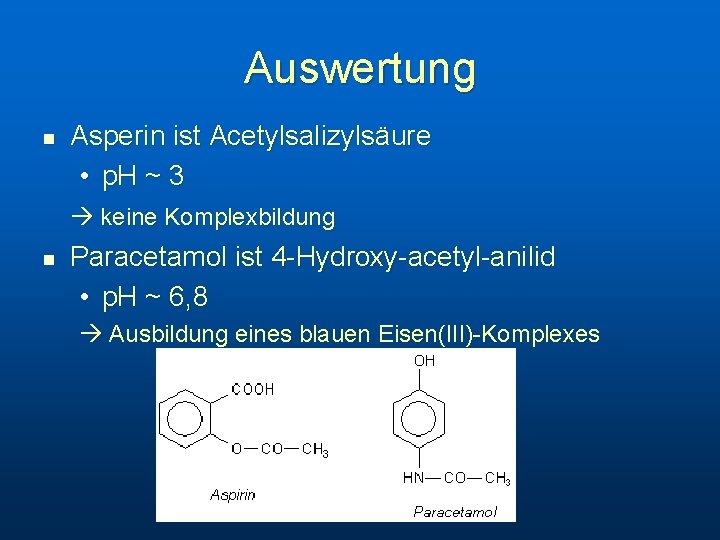
Auswertung n Asperin ist Acetylsalizylsäure • p. H ~ 3 keine Komplexbildung n Paracetamol ist 4 -Hydroxy-acetyl-anilid • p. H ~ 6, 8 Ausbildung eines blauen Eisen(III)-Komplexes
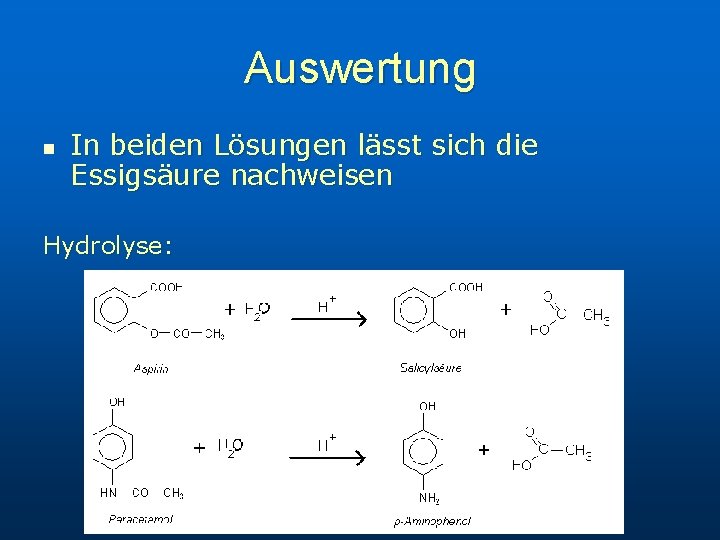
Auswertung n In beiden Lösungen lässt sich die Essigsäure nachweisen Hydrolyse:
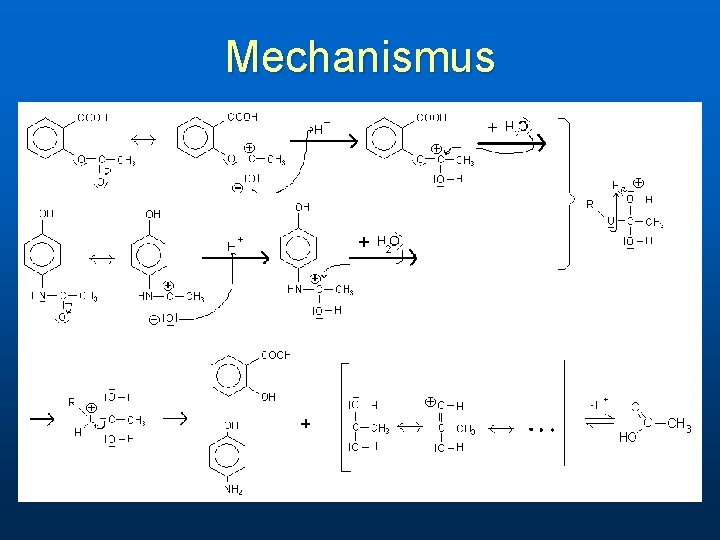
Mechanismus

Versuch 5 Herstellung von Kernseife

Durchführung n n 10 g Kokosfett werden mit 5 m. L H 2 O erwärmt 10 m. L Na. OH (w=0, 25) dazu und 10 min aufkochen H 2 O ergänzen wenn nötig Nach 10 min in Kochsalzlösung geben

Schulrelevanz 1 n n 12. 1 Kohlenstoffchemie Alkansäuren und ihre Derivate GK • Homologe Reihe und ausgewählte Eigenschaften von Monocarbonsäuren • Salze Ester und ihre Bedeutung (Fruchtessenzen und Lösungsmittel) • Reaktionstyp und Mechanismus der Esterbildung und Verseifung • Derivate der Monocarbonsäuren (Hydroxy- und Aminosäuren)

Schulrelevanz 2 n zusätzlich LK • • Halogenalkansäuren Beispiele für Di- / Trisäuren Spiegelbildisomerie Milchsäure, Weinsäure, asymmetrisches Kohlenstoffatom, Fischer-Projektion

Schulrelevanz 3 n fakultativ GK • Alkansäuren und Derivate im Alltag • Milchsäuregärung; Konservierungsstoffe; Kalkreiniger; Alkensäuren; technische Herstellung von Essigsäur n fakultativ LK • Reaktionen von Alkansäuren und ihren Salzen • Kolbe-Elektrolyse • Deutung der Bindungsverhältnisse mit Hilfe des Orbitalmodells; • Reaktivität und Eigenschaften von Nitroverbindungen und anorganischer Säuren • Sprengstoffe • Recycling von Explosivstoffen
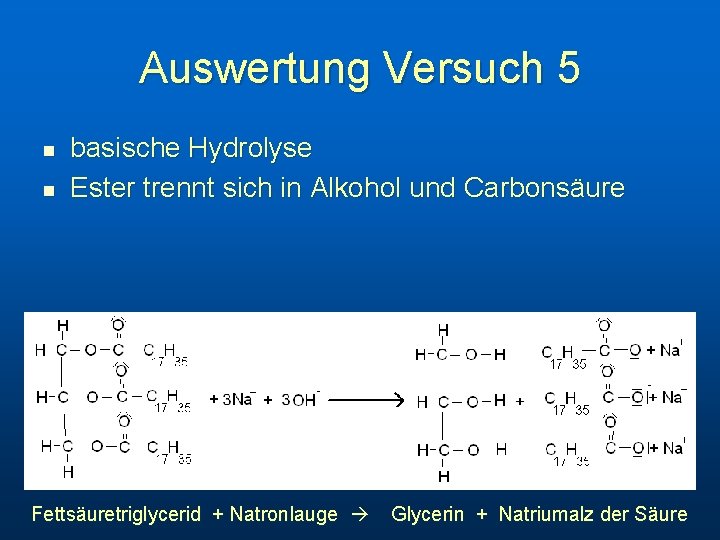
Auswertung Versuch 5 n n basische Hydrolyse Ester trennt sich in Alkohol und Carbonsäure Fettsäuretriglycerid + Natronlauge Glycerin + Natriumalz der Säure
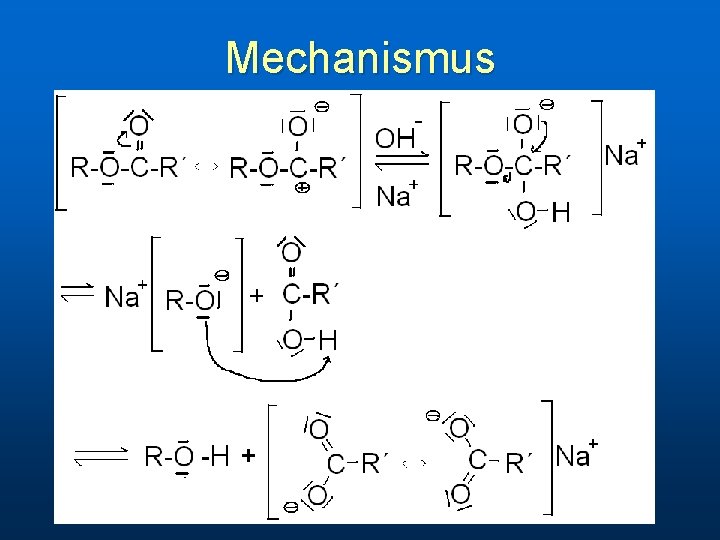
Mechanismus
- Slides: 39