CAPITOLO Lequilibrio chimico e gli acidi e le

CAPITOLO L’equilibrio chimico e gli acidi e le basi 11 Indice 1. Reazioni complete e reazioni reversibili 2. Costante di equilibrio 3. Il principio di Le Châtelier Mappa concettuale: L’equilibrio chimico 4. Acidi e basi 5. Le teorie sugli acidi e sulle basi 6. La ionizzazione dell’acqua 7. Il p. H 8. Gli indicatori e il piaccametro 9. Gli ioni che intervengono nelle neutralizzazioni 10. Il p. H di soluzione saline (idrolisi salina) 11. Soluzioni tampone 12. La titolazione acido-base Mappa concettuale: Le reazioni tra acidi e basi © Paolo Pistarà © Istituto Italiano Edizioni Atlas 1
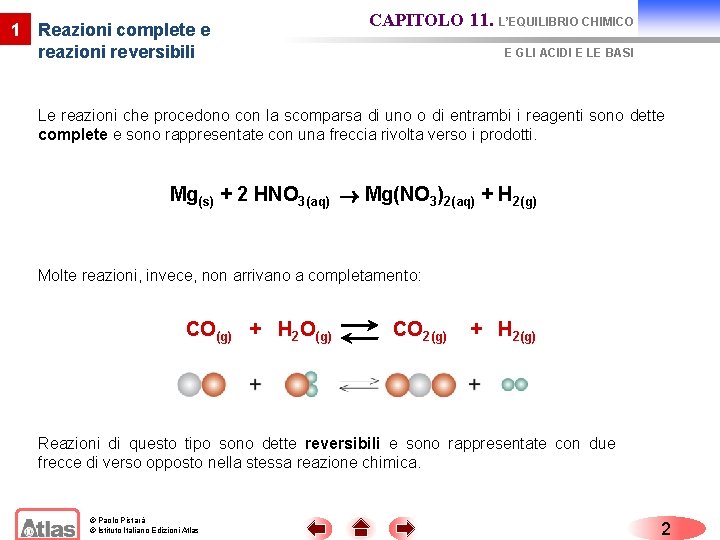
1 Reazioni complete e reazioni reversibili CAPITOLO 11. L’EQUILIBRIO CHIMICO E GLI ACIDI E LE BASI Le reazioni che procedono con la scomparsa di uno o di entrambi i reagenti sono dette complete e sono rappresentate con una freccia rivolta verso i prodotti. Mg(s) + 2 HNO 3(aq) Mg(NO 3)2(aq) + H 2(g) Molte reazioni, invece, non arrivano a completamento: CO(g) + H 2 O(g) CO 2(g) + H 2(g) Reazioni di questo tipo sono dette reversibili e sono rappresentate con due frecce di verso opposto nella stessa reazione chimica. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 2
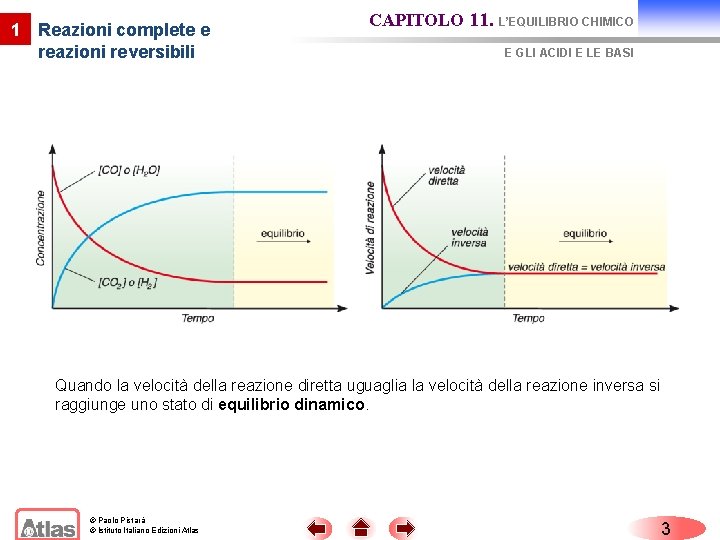
1 Reazioni complete e reazioni reversibili CAPITOLO 11. L’EQUILIBRIO CHIMICO E GLI ACIDI E LE BASI Quando la velocità della reazione diretta uguaglia la velocità della reazione inversa si raggiunge uno stato di equilibrio dinamico. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 3
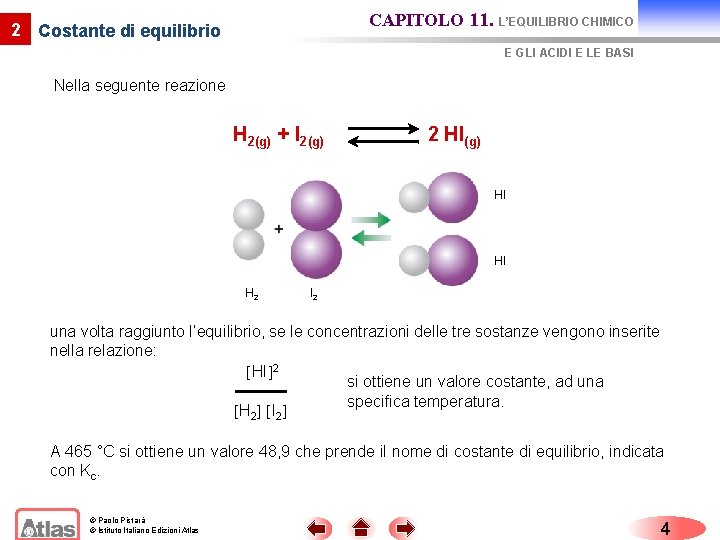
CAPITOLO 11. L’EQUILIBRIO CHIMICO 2 Costante di equilibrio E GLI ACIDI E LE BASI Nella seguente reazione H 2(g) + I 2(g) 2 HI(g) Hl Hl H 2 I 2 una volta raggiunto l’equilibrio, se le concentrazioni delle tre sostanze vengono inserite nella relazione: HI 2 si ottiene un valore costante, ad una specifica temperatura. H 2 I 2 A 465 °C si ottiene un valore 48, 9 che prende il nome di costante di equilibrio, indicata con Kc. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 4

CAPITOLO 11. L’EQUILIBRIO CHIMICO 2 Costante di equilibrio E GLI ACIDI E LE BASI In una generica reazione: a. A + b. B c. C + d. D la costante di equilibrio, Kc, è data dalla relazione: C c D d costante di equilibrio = Kc = A a B b prodotti reagenti Questa equazione prende il nome di legge dell’equilibrio chimico o legge di azione di massa. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 5

2 Costante di equilibrio CAPITOLO 11. L’EQUILIBRIO CHIMICO E GLI ACIDI E LE BASI u Significato del valore di Kc Il valore numerico della costante di equilibrio, Kc, rileva se in una reazione l’equilibrio è più spostato verso i prodotti o verso i reagenti. Kc 1 l’equilibrio è più spostato verso i prodotti Kc 1 l’equilibrio è più spostato verso i reagenti Kc ≈ 1 non vengono favoriti né i reagenti né i prodotti © Paolo Pistarà © Istituto Italiano Edizioni Atlas 6

3 Il principio di Le Châtelier CAPITOLO 11. L’EQUILIBRIO CHIMICO E GLI ACIDI E LE BASI Il principio di Le Châtelier afferma che: “un sistema all’equilibrio reagisce ad ogni variazione delle condizioni sperimentali spostandosi nel verso che contrasta l’effetto di tale variazione instaurando un nuovo equilibrio”. Variazione della concentrazione “Quando un reagente o un prodotto viene aggiunto ad un sistema all’equilibrio, questo si sposta nella direzione opposta a quella dove è stato aggiunto il componente”. 2 SO 2(g) + O 2(g) 2 SO 3(g) Un aumento di concentrazione di O 2 sposta l’equilibrio della reazione verso destra, cioè verso il prodotto SO 3. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 7
![Mappa concettuale: L’equilibrio chimico ESPRESSIONE DELLA COSTANTE DI EQUILIBRIO [Prodotti] KC = [Reagenti] Kc Mappa concettuale: L’equilibrio chimico ESPRESSIONE DELLA COSTANTE DI EQUILIBRIO [Prodotti] KC = [Reagenti] Kc](http://slidetodoc.com/presentation_image_h/db8ca98c7e1b95536e76275be32b51fa/image-8.jpg)
Mappa concettuale: L’equilibrio chimico ESPRESSIONE DELLA COSTANTE DI EQUILIBRIO [Prodotti] KC = [Reagenti] Kc determina la posizione di equilibrio VARIAZIONE DI CONCENTRAZIONE CAPITOLO 11. L’EQUILIBRIO CHIMICO E GLI ACIDI E LE BASI EQUILIBRIO CHIMICO Una reazione chimica in cui sono presenti sia i reagenti che i prodotti CATALIZZATORE Non influenza l’equilibrio, ma solo il tempo per raggiungerlo Fattori che influenzano l’equilibrio chimico VARIAZIONE DI PRESSIONE VARIAZIONE DELLA TEMPERATURA Influenza Kc Teoria dell’equilibrio mobile: principio di Le Châtelier © Paolo Pistarà © Istituto Italiano Edizioni Atlas 8

CAPITOLO 11. L’EQUILIBRIO CHIMICO 4 Acidi e basi E GLI ACIDI E LE BASI Sono definiti acidi le sostanze che hanno in comune un sapore aspro e pungente. Alcuni dei piÙ comuni acidi e loro applicazioni nella vita quotidiana. Sostanza Uso ACIDI Acido acetico (aceto) CH 3 COOH Condimento dei cibi, conservante, disincrostante di calcare nelle pentole, nelle vasche ecc. Acido citrico (succo di limone e di agrumi) H 3 C 6 H 5 O 7 Condimento dei cibi, disincrostante di calcare Acido fosforico H 3 PO 4 Rimuove la ruggine dai materiali ferrosi Acido borico H 3 BO 3 Mite antisettico Acido cloridrico (acido muriatico) HCl Elimina le incrostazioni più resistenti di calcare Acido ossalico H 2 C 2 O 4 Rimuove la ruggine dai tessuti © Paolo Pistarà © Istituto Italiano Edizioni Atlas 9

CAPITOLO 11. L’EQUILIBRIO CHIMICO 4 Acidi e basi E GLI ACIDI E LE BASI Sono classificate basi le sostanze che hanno in comune un sapore amaro e sono scivolose al tatto. Alcune delle piÙ comuni basi e loro applicazioni nella vita quotidiana. Sostanza Uso BASI Idrossido di sodio Na. OH Pulisce i forni, decompone tutte le sostanze (capelli, grasso, sapone) che ostruiscono gli impianti idraulici Ammoniaca NH 3 Pulizia della casa (sgrassante) Carbonato di sodio Na 2 CO 3 Addolcisce l’acqua, rimuove il grasso Bicarbonato di sodio Na. HCO 3 Mite antiacido, facilita la lievitazione delle torte, elimina impurità e antiparassitari da frutta e verdura © Paolo Pistarà © Istituto Italiano Edizioni Atlas 10
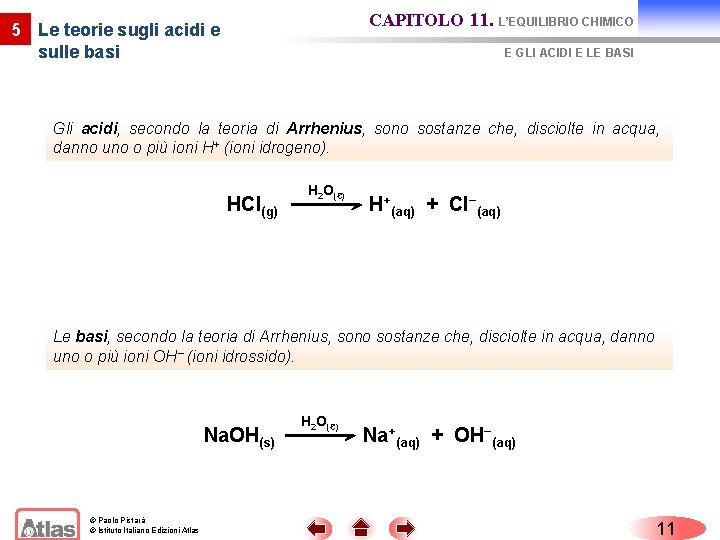
CAPITOLO 11. L’EQUILIBRIO CHIMICO 5 Le teorie sugli acidi e sulle basi E GLI ACIDI E LE BASI Gli acidi, secondo la teoria di Arrhenius, sono sostanze che, disciolte in acqua, danno uno o più ioni H+ (ioni idrogeno). HCl(g) H 2 O(ℓ) H+(aq) + Cl−(aq) Le basi, secondo la teoria di Arrhenius, sono sostanze che, disciolte in acqua, danno uno o più ioni OH (ioni idrossido). Na. OH(s) © Paolo Pistarà © Istituto Italiano Edizioni Atlas H 2 O(ℓ) Na+(aq) + OH−(aq) 11
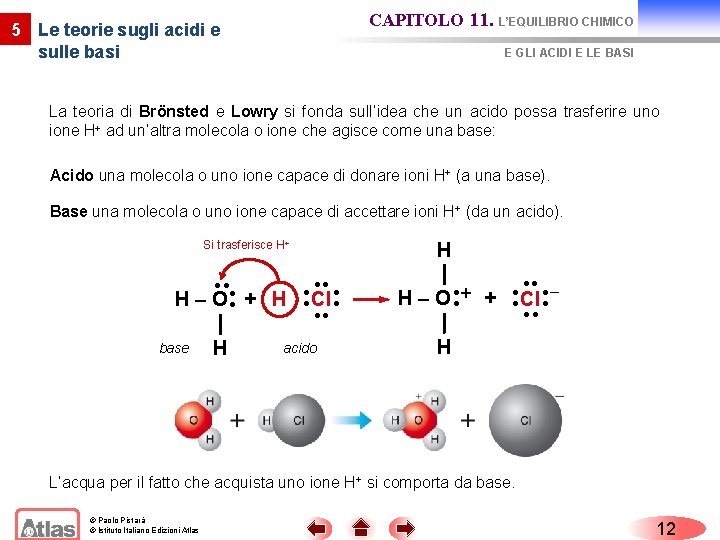
CAPITOLO 11. L’EQUILIBRIO CHIMICO 5 Le teorie sugli acidi e sulle basi E GLI ACIDI E LE BASI La teoria di Brönsted e Lowry si fonda sull’idea che un acido possa trasferire uno ione H+ ad un’altra molecola o ione che agisce come una base: Acido una molecola o uno ione capace di donare ioni H+ (a una base). Base una molecola o uno ione capace di accettare ioni H+ (da un acido). Si trasferisce H+ H – O + H Cl base H acido H − + H – O + Cl H L’acqua per il fatto che acquista uno ione H+ si comporta da base. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 12
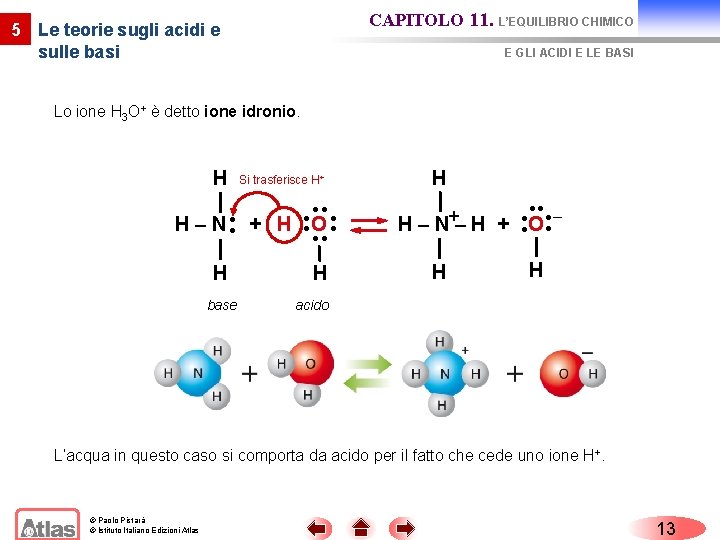
CAPITOLO 11. L’EQUILIBRIO CHIMICO 5 Le teorie sugli acidi e sulle basi E GLI ACIDI E LE BASI Lo ione H 3 O+ è detto ione idronio. H Si trasferisce H+ H – N + H O H base H H − + H – N – H + O H H acido L’acqua in questo caso si comporta da acido per il fatto che cede uno ione H+. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 13

6 La ionizzazione dell’acqua CAPITOLO 11. L’EQUILIBRIO CHIMICO E GLI ACIDI E LE BASI L’acqua distillata presenta una debole conducibilità elettrica. Poiché questo fenomeno è dovuto alla presenza di ioni, nell’acqua distillata vi deve essere un numero ridotto di ioni che si formano in seguito al seguente equilibrio: H 2 O(ℓ) molte molecole rimangono intatte H+(aq) + OH–(aq) solo un numero molto ridotto di molecole dà ioni La costante di questo equilibrio prende il nome di prodotto ionico dell’acqua. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 14

CAPITOLO 11. L’EQUILIBRIO CHIMICO 6 La ionizzazione dell’acqua E GLI ACIDI E LE BASI La costante è rappresentata con il simbolo Kw ed è scritta nella forma: Kw = H+ OH− H+ = 1, 0 10 7 mol/L e OH− = 1, 0 10 7 mol/L Pertanto Kw = 1, 0 10 14 a 25 °C L’equazione del prodotto ionico si applica a tutte le soluzioni acquose non solo all’acqua pura. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 15
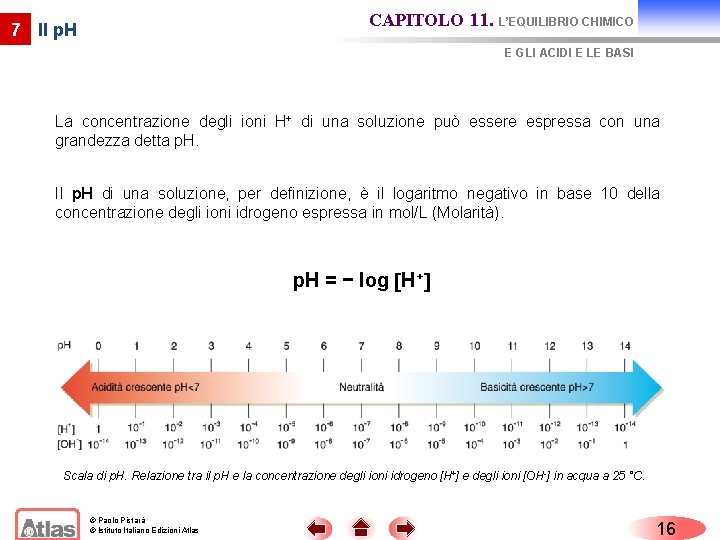
CAPITOLO 11. L’EQUILIBRIO CHIMICO 7 Il p. H E GLI ACIDI E LE BASI La concentrazione degli ioni H+ di una soluzione può essere espressa con una grandezza detta p. H. Il p. H di una soluzione, per definizione, è il logaritmo negativo in base 10 della concentrazione degli ioni idrogeno espressa in mol/L (Molarità). p. H = − log H+ Scala di p. H. Relazione tra il p. H e la concentrazione degli ioni idrogeno [H+] e degli ioni [OH-] in acqua a 25 °C. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 16

CAPITOLO 11. L’EQUILIBRIO CHIMICO 7 Il p. H E GLI ACIDI E LE BASI In base al p. H, una soluzione acquosa, a 25 °C, è definita: neutra se p. H = 7 acida se p. H 7 basica se p. H 7 © Paolo Pistarà © Istituto Italiano Edizioni Atlas 17

CAPITOLO 11. L’EQUILIBRIO CHIMICO 7 Il p. H E GLI ACIDI E LE BASI In analogia con il p. H si può definire la grandezza p. OH = − log OH− Il valore negativo del logaritmo di Kw a 25 °C viene indicato con p. Kw = − log Kw = 14 Pertanto p. H + p. OH = 14 © Paolo Pistarà © Istituto Italiano Edizioni Atlas 18
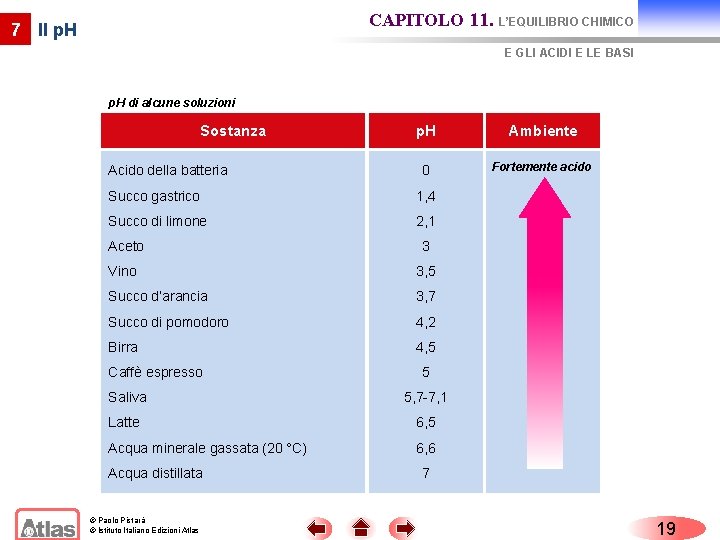
CAPITOLO 11. L’EQUILIBRIO CHIMICO 7 Il p. H E GLI ACIDI E LE BASI p. H di alcune soluzioni Sostanza Acido della batteria p. H Ambiente 0 Fortemente acido Succo gastrico 1, 4 Succo di limone 2, 1 Aceto 3 Vino 3, 5 Succo d’arancia 3, 7 Succo di pomodoro 4, 2 Birra 4, 5 Caffè espresso 5 Saliva 5, 7 -7, 1 Latte 6, 5 Acqua minerale gassata (20 °C) 6, 6 Acqua distillata © Paolo Pistarà © Istituto Italiano Edizioni Atlas 7 19
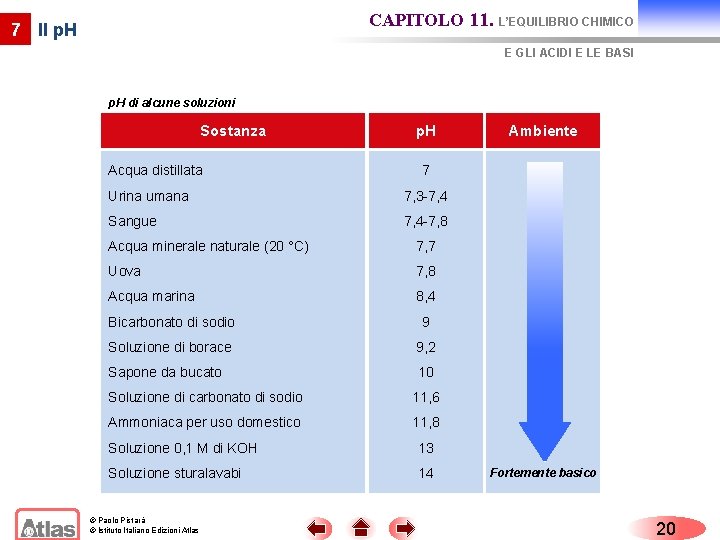
CAPITOLO 11. L’EQUILIBRIO CHIMICO 7 Il p. H E GLI ACIDI E LE BASI p. H di alcune soluzioni Sostanza Acqua distillata p. H 7 Urina umana 7, 3 -7, 4 Sangue 7, 4 -7, 8 Acqua minerale naturale (20 °C) 7, 7 Uova 7, 8 Acqua marina 8, 4 Bicarbonato di sodio 9 Soluzione di borace 9, 2 Sapone da bucato 10 Soluzione di carbonato di sodio 11, 6 Ammoniaca per uso domestico 11, 8 Soluzione 0, 1 M di KOH 13 Soluzione sturalavabi 14 © Paolo Pistarà © Istituto Italiano Edizioni Atlas Ambiente Fortemente basico 20

CAPITOLO 11. L’EQUILIBRIO CHIMICO 8 Gli indicatori e il piaccametro E GLI ACIDI E LE BASI Gli indicatori sono sostanze che assumono colori differenti se vengono a contatto con una soluzione acida o basica. Blu di bromotimolo in ambiente acido (giallo). Blu di bromotimolo in ambiente basico (blu). L’indicatore assume il colore verde in acqua distillata. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 21

8 Gli indicatori e il piaccametro CAPITOLO 11. L’EQUILIBRIO CHIMICO E GLI ACIDI E LE BASI Per determinare in modo semplice e rapido il p. H di una soluzione incolore si usa la carta indicatrice di p. H. La carta indicatrice di p. H è una carta impregnata di una miscela di coloranti opportunamente scelti. Carta indicatrice con scala di p. H fino a 14. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 22

8 Gli indicatori e il piaccametro CAPITOLO 11. L’EQUILIBRIO CHIMICO E GLI ACIDI E LE BASI La misura accurata del p. H di una soluzione è fatta con il piaccametro (o p. H-metro). Misura del p. H del succo di arancia. Misura del p. H di una soluzione basica con p. H-metro a stilo opportunamente calibrato. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 23

9 Gli ioni che intervengono nelle neutralizzazioni CAPITOLO 11. L’EQUILIBRIO CHIMICO E GLI ACIDI E LE BASI Le proprietà di un acido vengono annullate da una sostanza di natura opposta, una base. a. Le reazioni di acidi con idrossidi acido + idrossido sale + acqua Un acido può essere neutralizzato da un idrossido per dare un sale e acqua. L’equazione ionica netta si presenta nella forma: H+(aq) + OH−(aq) H 2 O(ℓ) © Paolo Pistarà © Istituto Italiano Edizioni Atlas 24
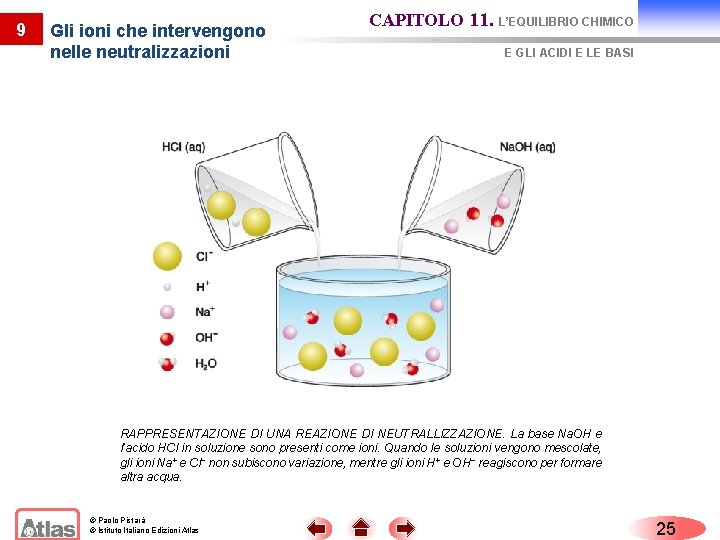
9 Gli ioni che intervengono nelle neutralizzazioni CAPITOLO 11. L’EQUILIBRIO CHIMICO E GLI ACIDI E LE BASI RAPPRESENTAZIONE DI UNA REAZIONE DI NEUTRALLIZZAZIONE. La base Na. OH e l’acido HCl in soluzione sono presenti come ioni. Quando le soluzioni vengono mescolate, gli ioni Na+ e Cl− non subiscono variazione, mentre gli ioni H+ e OH− reagiscono per formare altra acqua. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 25

9 Gli ioni che intervengono nelle neutralizzazioni CAPITOLO 11. L’EQUILIBRIO CHIMICO E GLI ACIDI E LE BASI b. Le reazioni di acidi con ossidi metallici insolubili acido + ossido metallico sale + acqua Un acido neutralizzato da un ossido metallico insolubile dà un sale più acqua. c. La reazione di un antiacido con un acido + carbonato sale + acqua + diossido di carbonio Oltre alla formazione di un sale e acqua, si ha anche sviluppo di diossido di carbonio. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 26

10 CAPITOLO 11. L’EQUILIBRIO CHIMICO Il p. H di soluzioni saline (idrolisi salina) E GLI ACIDI E LE BASI La reazione che si verifica tra gli ioni in soluzione e le molecole di acqua prende il nome di idrolisi. ACIDA NEUTRA BASICA NH 4 Cl Na. Cl CH 3 COONa Le soluzioni dei sali nell’acqua danno reazione acida, basica o neutra come evidenzia la colorazione assunta da poche gocce di indicatore universale. Questo comportamento è dovuto al fatto che uno degli ioni che deriva dal sale può scambiare un protone con l’acqua secondo la teoria di Brönsted e Lowry. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 27

10 Il p. H di soluzioni saline (idrolisi salina) CAPITOLO 11. L’EQUILIBRIO CHIMICO E GLI ACIDI E LE BASI u Sali che danno soluzioni neutre (assenza di idrolisi): il p. H della soluzione è 7 Na+ + H 2 O nessuna reazione Cl− + H 2 O nessuna reazione Tutti gli ioni che derivano da un acido forte o da una base forte non reagiscono con H 2 O per cui il p. H della soluzione è 7. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 28
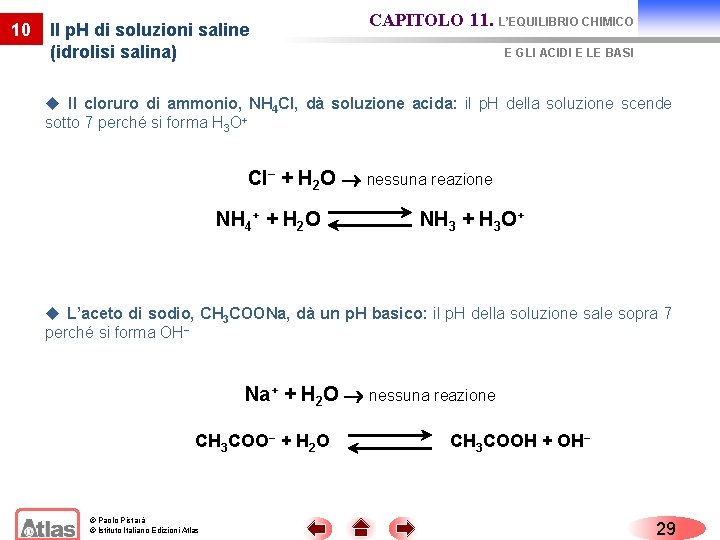
10 Il p. H di soluzioni saline (idrolisi salina) CAPITOLO 11. L’EQUILIBRIO CHIMICO E GLI ACIDI E LE BASI u Il cloruro di ammonio, NH 4 Cl, dà soluzione acida: il p. H della soluzione scende sotto 7 perché si forma H 3 O+ Cl− + H 2 O nessuna reazione NH 4+ + H 2 O NH 3 + H 3 O+ u L’aceto di sodio, CH 3 COONa, dà un p. H basico: il p. H della soluzione sale sopra 7 perché si forma OH− Na+ + H 2 O nessuna reazione CH 3 COO− + H 2 O © Paolo Pistarà © Istituto Italiano Edizioni Atlas CH 3 COOH + OH− 29

CAPITOLO 11. L’EQUILIBRIO CHIMICO 11 Soluzioni tampone E GLI ACIDI E LE BASI Una soluzione che limita le variazioni di p. H in un campo molto ristretto, quando ad essa si aggiungono quantità limitate di acidi o di basi, è detta soluzione tampone. A B Poche gocce di HCl (A) e di Na. OH (B) in acqua distillata determinano forti variazioni di p. H e l’indicatore blu di bromotimolo assume due colorazioni differenti. © Paolo Pistarà © Istituto Italiano Edizioni Atlas A’ B’ Nelle soluzioni tamponate il p. H non subisce variazioni, per cui il colore dell’indicatore non varia. 30

12 La titolazione acido-base CAPITOLO 11. L’EQUILIBRIO CHIMICO E GLI ACIDI E LE BASI La titolazione acido-base consente di conoscere la concentrazione di una sostanza acida o basica in soluzione mediante aggiunta di un reattivo di natura opposta di concentrazione nota. La titolazione acido-base è una reazione di neutralizzazione. La condizione in cui un acido ha reagito completamente con una base è detta punto di equivalenza. Soluzione di HCl in presenza di BBT. Soluzione con una goccia in eccesso di Na. OH. L’indicatore svolge l’importante funzione di segnalare quando il punto di equivalenza è stato raggiunto. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 31
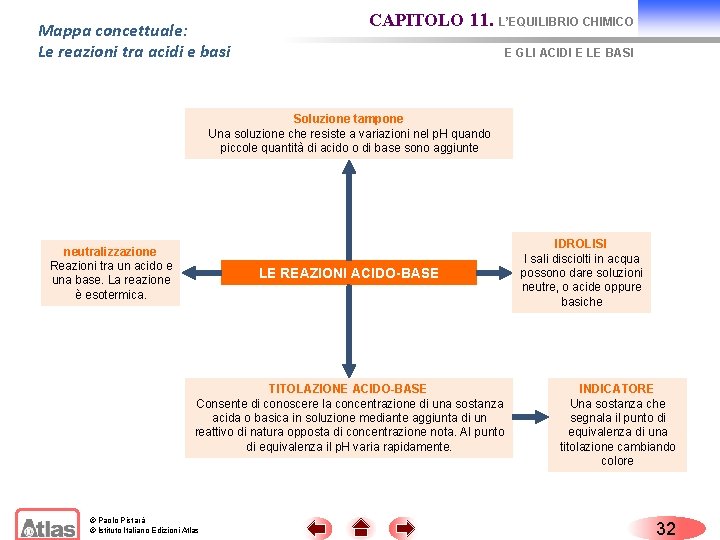
Mappa concettuale: Le reazioni tra acidi e basi CAPITOLO 11. L’EQUILIBRIO CHIMICO E GLI ACIDI E LE BASI Soluzione tampone Una soluzione che resiste a variazioni nel p. H quando piccole quantità di acido o di base sono aggiunte neutralizzazione Reazioni tra un acido e una base. La reazione è esotermica. LE REAZIONI ACIDO-BASE TITOLAZIONE ACIDO-BASE Consente di conoscere la concentrazione di una sostanza acida o basica in soluzione mediante aggiunta di un reattivo di natura opposta di concentrazione nota. Al punto di equivalenza il p. H varia rapidamente. © Paolo Pistarà © Istituto Italiano Edizioni Atlas IDROLISI I sali disciolti in acqua possono dare soluzioni neutre, o acide oppure basiche INDICATORE Una sostanza che segnala il punto di equivalenza di una titolazione cambiando colore 32
- Slides: 32